阴囊来源软组织在Snodgrass尿道成形术中的应用研究*
2018-03-19张敬悌
白 明,张敬悌
西安市儿童医院泌尿外科(西安 710003)
尿道下裂是小儿泌尿生殖系统的常见先天畸形,发病率约为1/250~1/300,且仍呈逐年上升趋势。尿道下裂的修复是极其复杂精细的过程,随着现代医学的发展,其手术方式也在不断的进行着改良和创新。Snodgrass尿道成形术因其操作简单、阴茎外形美观等特点而广泛应用于临床,但尿道瘘仍是该术式最常见并发症[1]。为预防尿道下裂手术后尿道瘘的发生,可以在新成形尿道和皮肤之间填入各种来源的软组织以加固尿道[2]。阴囊做为阴茎的邻近器官,因其所含有的睾丸鞘膜和肉膜等能够方便的成为手术填充物的组织来源,所以在尿道下裂手术中具有一定的使用价值。我院于2012年1月至2016年4月采用阴囊来源软组织作为尿道覆盖材料Snodgrass手术完成尿道成形术102例,并对不同覆盖材料的疗效进行对比,现报告如下。
资料与方法
1 一般资料 选择Snodgrass尿道成形术患儿102例,术中均使用阴囊来源软组织对新尿道腹侧进行覆盖。其中带蒂睾丸鞘膜组40例,年龄1.5~15岁,平均(5.34±3.16)岁。阴囊肉膜组32例,年龄1.6~14岁,平均(5.21±3.24)岁。带蒂睾丸鞘膜联合阴囊肉膜组30例,年龄1.3~15岁,平均(5.08±3.46)岁。手术由同一名医师完成,所有患儿均为初次手术,均无阴囊以及腹股沟区域手术史。三组患儿年龄、尿道下裂分型,尿道板及龟头发育,重建尿道长度等方面比较,差异无统计学意义(P>0.05),具有可比性。
2 手术方法 麻醉成功后,分离包皮粘连,龟头缝牵引线,阴茎尿道板两外侧缘平行切开,远端至龟头顶部,两切口至尿道口近端呈“U”形汇合,保留尿道板宽度约0.6~0.8cm。环形切开包皮内板,沿阴茎Back筋膜脱套阴茎包皮,切除阴茎腹侧以及两侧的发育不良条索。游离龟头海绵体,形成两个对称的龟头翼瓣。尿道板正中纵行切开至阴茎白膜,置入6~10F导尿管,以尿管为支架用6-0单桥线连续缝合尿道板形成新尿道。最后自阴茎根部与阴囊的切口间隙采集不同的阴囊软组织,对新尿道腹侧进行覆盖。① 带蒂睾丸鞘膜组:游离出一侧睾丸,裁取带蒂睾丸鞘膜组织转移并至阴茎创面覆盖于新尿道腹侧,鞘膜两侧缘与阴茎白膜缝合固定。② 阴囊肉膜组:仔细解剖出一侧阴囊肉膜,裁取相应大小肉膜瓣,转移并覆盖于整个新尿道腹侧并缝合固定。③ 睾丸鞘膜联合阴囊肉膜组:相同方法两侧阴囊分别取相应的睾丸鞘膜和肉膜组织,将鞘膜覆盖在新尿道上后再将肉膜加盖于鞘膜之上并固定。最后合拢缝合龟头翼,纵劈背侧包皮转经两侧转至腹侧覆盖阴茎创面。包扎阴茎固定导尿管。
3 观察指标 比较三种尿道覆盖材料在手术时间,出血量,尿道瘘、尿道狭窄以及阴囊并发症(阴囊血肿或感染)等方面的差异。
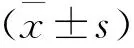
结 果
术后使用抗生素5~7 d,第10~14 d拔尿管出院。所有患儿均顺利完成手术。随诊3个月至5年。三组手术时间、出血量、尿道狭窄以及阴囊并发症方面差异无统计学意义(P>0.05);睾丸鞘膜组发生尿道瘘5例(12.5%),阴囊肉膜组发生尿道瘘8例(25.0%),睾丸鞘膜联合阴囊肉膜组发生尿道瘘3例(10.0%),阴囊肉膜组与睾丸鞘膜、睾丸鞘膜联合阴囊肉膜两组相比较,差异有统计学意义(P<0.05),但睾丸鞘膜与睾丸鞘膜联合阴囊肉膜两组间比较,差异无统计学意义(P>0.05)。
讨 论
尿道下裂是仅次于包茎的泌尿生殖系统先天畸形,手术是其唯一的治疗方法。尿道下裂可以分为阴茎冠状沟型、阴茎体型、阴囊型以及会阴型等不同的临床类型。不同类型的尿道下裂临床特征各不相同,所以手术方法不能一概而论,虽然各种改良术式已达300余种之多,但实际上并不存在适用于所有类型的所谓万能术式。成功的尿道修复手术应达到以下几点:阴茎完全伸直且外观正常无臃肿、尿道口正位、能站立排尿且尿线正常、性生活正常。
尿道下裂手术治疗难度大、并发症高始终是一个突出的难题,主要并发症包括尿道瘘、尿道狭窄、尿道憩室,龟头开裂,皮瓣坏死感染等。尿道瘘做为最常见的术后并发症,总的发生率为5%~20%[3]。尿道板由富含血管平滑肌和神经纤维的结缔组织组成,具有较强的延展性,被认为是重建尿道的重要材料[4-5]。Only、Mateieu、Snodgrass均为保留尿道板尿道下裂手术中的主流术式[6]。既往部分具备保留条件的尿道板因为发育较窄无法独立完成卷管,必须通过加盖带蒂皮瓣或镶嵌游离皮瓣的方式来实现尿道的重建,如 Onlay、Mateieu、Inlay等术式。Snodgrass术式不仅大大的提升了尿道板的临床价值,并且还因其操作简单,术后阴茎美观、尿道口呈裂隙状以及适用于部分再次手术病人等特点,受到了越来越多医生的青睐。尽管具备上述众多优势,但是尿道瘘在Snodgrass术式中的发生率仍然为5.7%~15.5%[7]。尿道下裂手术方法本身的改进对于减少并发症和提高手术成功率具有重要意义,在新成形的尿道与皮肤之间填入软组织可以可以起到加固尿道,增加尿道壁抗尿流冲击的作用,从而达到减少尿道瘘的目的。阴茎包皮由于组织量充足且血供丰富,往往成为尿道覆盖组织的首选来源。标准的Snodgrass手术通常将肉膜从背侧包皮分离下来,形成带蒂肉膜瓣后转移至阴茎腹侧并覆盖于尿道缝合缘以预防尿道瘘,这种源自包皮的带蒂组织尽管血供丰富而易于成活,但是仍有不足之处:① 背侧带蒂肉膜瓣绕过阴茎一侧转向腹侧时,可能会因为肉膜瓣的牵拉导致阴茎扭转或者阴茎下弯[8]。有学者认为将背侧肉膜纵切形成两个肉膜瓣后,再分别自阴茎两侧转移覆盖到尿道腹侧可以有效减少因张力不均所致阴茎扭转和下弯[9]。② 如果背侧包皮肉膜组织本身发育欠佳或有过包皮环切手术史,其覆盖往往不能达到满意效果,适用范围受到限制。③ 背侧包皮尤其是其远端部分做为手术的最外层覆盖组织,在缺少肉膜血供支撑的情况下容易发生皮肤愈合不良甚至坏死,尿道瘘可能性随之增大,这在阴茎近端类型的病例中显得尤为突出。为尽可能减少因包皮血供减少出现的尿道瘘,学者们曾尝试采用非包皮背侧肉膜瓣来源的组织来对尿道进行覆盖。临床上阴茎腹侧筋膜,分叉的尿道海绵体、精索组织、带蒂睾丸鞘膜和阴囊肉膜等也可以用来做为尿道覆盖材料以减少尿道瘘的发生睾丸鞘膜具有较强的延展性且血供丰富,经充分游离后可以容易地转移至阴茎腹侧。阴囊肉膜是富有弹性纤维的肉膜肌,位于阴囊皮肤下层,暴露方便。两种组织都具有取材方便,容易操作的特点,均可以用来覆盖尿道预防尿道瘘。除了阴囊,其他部位来源的肉膜组织也可以用来做为尿道覆盖物,如包皮背侧肉膜等。Ramesh B等[10]研究认为:在首次TIP手术的病例中的阴茎中段尿道下裂修复中,睾丸鞘膜的作用明显优于包皮背侧肉膜,而对于远端病例两者则无明显差异。Chatterjee等[11]的一项研究显示:使用带蒂睾丸鞘膜和阴茎腹侧筋膜做为覆盖材料,尿道瘘的发生率分别为10%和20%。此外有学者推荐在尿道下裂手术中,尤其是在TIP手术中使用带蒂睾丸鞘膜来预防尿道瘘的发生[11]。在同时合并有鞘膜积液、腹股沟斜疝等的尿道下裂中,TVF被认为是最佳的覆盖材料[12]。自阴囊获取软组织,主要的并发症包括阴囊血肿和感染,甚至有脓肿形成的报告。在获取软组织时可采用小功率电刀,注意精准止血,避免不必要的以及大范围的电凝,这样不仅能够使所获鞘膜及肉膜保持最佳组织活性,增强覆盖效果减少尿道瘘,而且可以减少渗出,尽可能降低阴囊并发症。Sharma等[12]通过精准解剖和密切止血,用阴囊软组织治疗39例复杂尿道瘘无一例出现阴囊血肿或感染的并发症。Kamyar等[1]在29例TIP手术中使用睾丸鞘膜结果显示尿道瘘发生率为10.3%(3/29),无阴囊并发症发生。我们三组病人组织均取自阴囊,三组阴囊并发症比较无统计学意义,此外三种覆盖技术在手术时间,出血量,尿道狭窄等方面差异也无统计学意义。睾丸鞘膜具有较好的延展性,组织致密且相对较薄,其浆膜层可以紧密贴附于整个尿道腹侧,能够最大程度的完成对重建尿道的整体覆盖且表面血供丰富容易成活。既往研究多通过睾丸鞘膜和阴囊肉膜的两两比较显示鞘膜更具优势,我们的研究通过将睾丸鞘膜联合肉膜的技术分别与鞘膜和肉膜进行比较,显示这种联合技术优于单独使用肉膜,但是和单独使用睾丸鞘膜相比较并不能明显降低尿道瘘的发生率,从而进一步证实了睾丸鞘膜在预防尿道瘘中的作用。所以我们认为对于预防Snodgrass手术尿道瘘的发生可首选睾丸鞘膜进行覆盖,尤其对于同时合并有鞘膜积液,鞘膜组织量丰富的的病人更为适用。睾丸鞘膜不仅可用于TIP 手术,而且在多次手术史的尿道瘘的修复中也明显优于其他组织[13]。
虽然多种软组织的应用能够减少Snodgrass术后尿道瘘的发生,但是需要注意的是尿道板宽度应在纵切后宽度能够扩展至两倍以上,从而保证其能无张力卷管形成新尿道。如果Snodgrass手术的适应证把握不准确,即使应用了合理的覆盖材料,也会导致并发症的增加。
[1] Kamyar TT,Shabnam M.Tunica vaginalis flap as a second layer for tubularized incised plate urethroplasty[J]. Urology Journal ,2010,7(4):254-257.
[2] El-Kassaby AW, Al-Kandari AM, Elzayat T,etal. Modified tubularized incised plate urethroplasty for hypospadias repair: a long-term results of 764 patients[J]. Urology, 2008,71(4):611-615.
[3] Rushton HG, Belman AB. The split prepuce in situ onlay hypospadias repair[J].J Urol,1998,160(3 Pt 2):1134-1136.
[4] Oswald J, Korner I, Riccabona M. Comparison of the perimeatal-based flap (Mathieu) and the tubularized incised-plate urethroplasty (Snodgrass) in primary distal hypospadias[J]. BJU Int,2000,85(6):725-727.
[5] Erol A, Baskin LS, Li YW,etal. Anatomical studies of the urethral plate: why preservation of the urethral plate is important in hypospadias repair[J]. BJU Int,2000 ,85(6):728-734.
[6] 陈嘉波,杨体泉,王双全,等.加盖包皮岛状皮瓣尿道成形术的临床应用和单因素分析[J].中华实用临床儿科杂志,2014,29(2):151-153.
[7] Baskin LS. Hypospadias and urethral development[J]. J Urol,2000,163(3):951-956.
[8] Babu R, Hariharasudhan S. Tunica vaginalis flap is superior to inner preputial dartos flap as a waterproofing layer for primary TIP repair in midshaft hypospadias[J].J Pediatr Urol,2013,9(6 Pt A):804-807.
[9] Abolyosr A. Snodgrass hypospadias repair with onlay overlapping double-layered dorsal dartos flap without urethrocutaneous fistula: experience of 156 cases[J]. J Pediatr Urol ,2010,6:403-407.
[10] Ramesh B, Sekar H.Tunica vaginalis flap is superior to inner preputial dartos flap as a waterproofing layer for primary TIP repair in midshaft hypospadias[J]. Journal of Pediatric Urology,2013,9:804-807.
[11] Chatterjee US, Mandal MK, Basu S,etal. Comparative study of dartos fascia and tunica vaginalis pedicle wrap for the tubularized incised plate in primary hypospadias repair[J].BJU Int,2004,94(7):1102-1104.
[12] Sharma N, Bajpai M, Panda SS,etal. Tunica vaginalis flap cover in repair of recurrent proximal urethrocutaneous fistula: a final solution[J].Afr J Paediatr Surg, 2013,10(4):311-314.
[13] Nerli R, Amarkhed SS, Hiremath MB. Vascularized tunica vaginalis interposition flap for the treatment of recto-urethral fstulas[J]. Indian J Urol,2009,25:467-469.
