肥胖2型糖尿病患者血皮质醇水平与血糖、血脂的关系
2018-03-05刘长丽金秀平王晓迪
刘长丽,金秀平,王 颖,王晓迪
(华北理工大学附属医院,河北 唐山 063000)
糖尿病是一种以糖代谢紊乱为特征的慢性代谢性疾病,患病率逐年上升,严重影响了患者的生活质量[1]。血糖控制不良可导致多种严重并发症的发生,肥胖作为糖尿病的常见合并症,被称为“万病之源”,对于糖尿病患者来说,合并肥胖更是雪上加霜,于是有了“糖尿病+肥胖=糖胖病”一说。近30年来,中国人群的血脂水平逐步升高,血脂异常患病率明显增加[2]。我国儿童青少年高胆固醇血症患病率也明显升高[3],预示我国未来血脂异常病患及相关疾病负担将继续加重。高血脂症也是糖尿病患者常见的合并疾病[4]。肥胖是糖尿病及高血脂症的共同危险因素,肥胖者患糖尿病的危险性增加,是正常体质量患者的2.5倍[5],糖尿病合并肥胖患者的血脂、血糖更是难以控制。因此进一步寻找导致糖尿病患者血糖、血脂难于控制的因素对糖尿病患者的治疗至关重要;皮质醇作为一种激素,既可以通过脂肪重新分布导致肥胖,也可以从多种途径升高血糖[6-7]。已有大量研究证明糖尿病患者存在垂体下丘脑肾上腺轴的功能紊乱[8-10],皮质醇水平升高。本研究观察了肥胖2型糖尿病(T2DM)患者血皮质醇及血糖、血脂水平,旨在进一步明确皮质醇与糖尿病患者血糖、血脂水平的关系。 现报道如下。
1 临床资料
1.1一般资料 选择2015年6月—2016年6月在我院内分泌科住院的T2DM患者146例,均符合1999年WHO制定的T2DM标准诊断[11],排除标准:其他类型糖尿病、糖尿病酮症酸中毒、孕妇及哺乳期妇女、原发性皮质醇增多症、垂体瘤、接受外源性糖皮质激素治疗者、严重的精神心理疾病、弥漫性毒性甲状腺肿、各种感染、妊娠、口服避孕药、手术、外伤或其他应激情况等。同时除外肾衰竭、甲状腺功能减退、肝胆疾病、应用降压药物、胰腺炎、乙醇中毒、特发性高血钙、多发性骨髓瘤、系统性红斑狼疮、口服避孕药、口服精神类药物、有长期吸烟及引用咖啡嗜好者等。其中男75例,女71例;年龄33~79岁。按腰臀比(WHR)将其分为非肥胖组(男WHR<0.9或女WHR<0.85)36例和肥胖组(男WHR≥0.9或女WHR≥0.85)110例,2组性别、年龄、病程、身高比较差异均无统计学意义(P均>0.05),具有可比性。见表1。
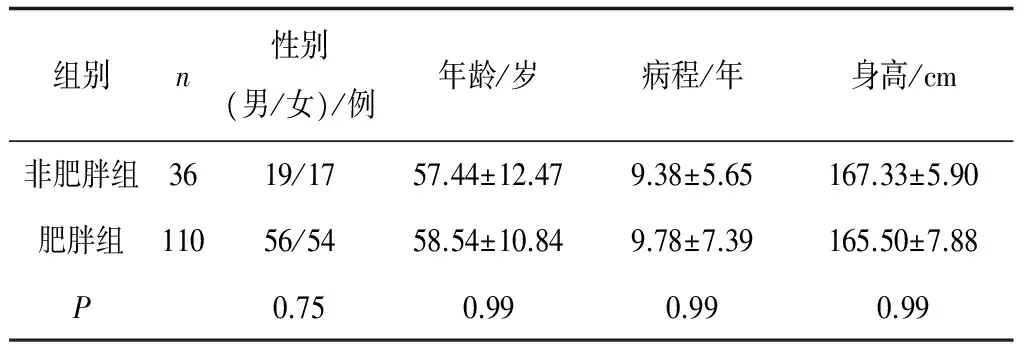
表1 2组一般资料比较
1.2方法 测量身高、体质量、腰围、臀围,计算体质量指数(BMI),BMI=体质量(kg)/身高(m)2;计算腰臀比(WHR)=腰围(cm)/臀围(cm)。肘静脉采血,检测各组患者8点皮质醇(8:00 F)、16点皮质醇(16:00 F)及夜间0点皮质醇(0:00 F)水平;同时测定空腹血糖(FPG)、空腹胰岛素(FINS)、三酰甘油(TG)、总胆固醇(TC)、低密度脂蛋白(LDL-C)、高密度脂蛋白(HDL-C)、载脂蛋白A(ApoA)、载脂蛋白B(ApoB)、Lp(a)及糖化血红蛋白水平;计算胰岛素敏感指数(ISI)、胰岛素抵抗指数(HOMA-IR),ISI=1/(FPG×FINS)、HOMA-IR=FPG×FINS/22.5。
2 结 果
2.12组体质量、BMI、腰围、臀围、WHR比较 肥胖组体质量、BMI、腰围、臀围、WHR均高于非肥胖组(P均<0.05)。见表2。

表2 2组体质量、BMI、腰围、臀围、WHR比较
2.22组FPG、各时点皮质醇、HbA1c、TG、TC等血生化指标比较 肥胖组FPG、0:00F、HbA1 c、TG、TC、LDL-C、ApoB、Lp(a)、HOMA-IR均显著高于非肥胖组(P均<0.05),而HDL-C、ApoA、ISI均显著低于非肥胖组(P均<0.05)。见表3。
2.3各临床指标的相关性分析结果 Pearson相关分析结果显示FPG、00:00F、HbA1c、TG、LDL-C与WHR呈显著正相关(r=0.317,0.226,0.316,0.232,0.186,P均<0.05),ISI、HDL-C与WHR呈显著负相关(r=-0.447,-0178,P均<0.05);00:00F与FPG呈显著正相关(r=0.242,P<0.05),与HDL-C呈显著负相关(r=-0.186,P<0.05);TG与ISI呈显著负相关(r=0.216,P<0.05),与HbA1c呈显著正相关(r=0.225,P<0.05)。

表3 2组FPG、各时点皮质醇、HbA1c、TG、TC血生化指标比较

组别nApoA/(g/L)ApoB/(g/L)HbA1c/%FPG/(mmol/L)ISIHOMA-IRLp(a)/(mg/L)非肥胖组361.44±0.340.86±0.256.7±1.427.85±2.730.026±0.014.73±1.0581.96±37.4肥胖组1101.30±0.231.04±0.298.7±1.6610.71±3.510.013±0.0086.06±5.9173.76±69.6P0.0420.0030.0000.0000.0000.5170.000
3 讨 论
糖尿病是一种慢性代谢性疾病,中国2型糖尿病防治指南(2013年版)指出,超重或肥胖及血脂异常均是糖尿病高危人群的危险因素[1]。研究表明,糖尿病患者存在一定的下丘脑-垂体-肾上腺(HPA)轴的紊乱,尤以皮质醇水平的升高明显[8]。目前也有研究提示下丘脑-垂体-肾上腺轴调节功能异常和唾液或血皮质醇水平与肥胖及血脂、血糖关系密切, 如殷立万等[12]研究表明,清晨唾液皮质醇水平与WC、BMI、SBP、TG、FPG、HOMA-IR呈正相关,与HDL-C有负相关。皮质醇的升高不但与肥胖息息相关,而且导致血糖及血脂代谢紊乱,血糖、血脂及血皮质醇之间相互影响最终加重病情。皮质醇作为糖皮质激素,可从多种途径升高血糖,其机制[9]主要体现在:①糖皮质激素促进糖原分解,抑制肝糖原输出,刺激糖异生;②糖皮质激素直接作用于胰岛β细胞抑制胰岛素分泌,加重胰岛素抵抗,从而使血糖升高;③糖尿病患者长期血糖控制差可导致糖皮质激素代谢异常,糖皮质激素增加进一步加重病情,形成恶性循环。张炜等[10]研究显示,高血糖患者8:00,16:00及日均血皮质醇、尿游离皮质醇水平均高于血糖正常者,高血糖患者空腹FPG、2 hPG与血尿皮质醇水平相关,得出高血糖患者高皮质醇分泌的发生率升高,血糖升高与高皮质醇分泌相关的结论。11β羟化固醇脱氢酶2(11βHSD2)可使皮质醇迅速灭活,而葡萄糖是11βHSD2的抑制剂[13],倘若11βHSD2缺陷,致使皮质醇不能及时灭活,血中皮质醇水平升高;血糖、皮质醇也会相互影响。张永生等[13]研究结果显示,随着血糖水平的增高,血浆皮质醇水平也相应增高;血糖水平与血浆皮质醇水平呈明显正相关(r=0.46,P<0.01),葡萄糖可能通过抑制11β羟化固醇脱氢酶2的催化活性,致使血浆皮质醇水平升高。另外,刘颖[14]通过回顾性分析得出,糖尿病患者全天血皮质醇水平增高,而24:00血皮质醇水平明显升高,24:00血皮质醇水平与空腹血糖呈正相关。皮质醇可导致肥胖,主要体现在:①皮质醇可抑制葡萄糖的利用和增强肝糖原异生使血糖升高,刺激胰岛β细胞分泌胰岛素增加,促进脂肪合成,导致肥胖。②皮质醇可增加糖尿病患者食欲,导致肥胖。皮质醇可升高血脂,一方面皮质醇可以促进脂肪动员,另一方面可以促进脂肪合成,但合成代谢相对较强,而致脂肪总量增多,脂肪代谢可以出现血脂代谢紊乱。糖尿病患者的血脂紊乱主要表现为TG的升高和HDL的降低[1],HDL是血液中密度最高、颗粒最小的一种脂蛋白,是血脂代谢的基础物质,专门在体内结合多余血脂,清除血液垃圾,转运体外。正常的血脂代谢HDL的数量与LDL或TG的数量是呈比例的,即一个HDL分子可以运输5~6个LDL或TG分子到肝脏进行分解处理,最终排出体外。当上述比例失调时,就会使血液中的TG、TC等指标超出正常范围,打破了原正常的血脂代谢平衡,发生异常。研究结果中皮质醇与HDL呈负相关,说明皮质醇参与了HDL降低的过程,升高了TG和TC水平,导致血脂代谢紊乱。
皮质醇可以通过不同途径升高血糖、血脂,也可以通过脂肪重新分布导致肥胖,皮质醇在糖尿病患者的血糖、血脂及肥胖的调节中起到了纽带的作用,使之相互连通,相互促进,最终使病情难以控制,因高血糖及高血脂导致的各种并发症随即产生,严重降低糖尿病患者的生存质量。因此,研究肥胖、血糖、血脂及皮质醇水平之间的关系,为更好地治疗糖尿病及其合并症,提高糖尿病患者的生存质量尤为重要。
本研究以WHR分组,将2型糖尿病患者分为肥胖组和非肥胖组,分别监测其血糖、血脂及血皮质醇水平,结果显示:①肥胖组FPG、HbA1c、HOMA-IR、TG及TC、00:00F水平均显著高于非肥胖组,说明肥胖影响了T2DM患者的血糖、血脂及血皮质醇水平,是血糖、血脂及血皮质醇水平升高的危险因素,增加了胰岛素抵抗;FPG、00:00F、HbA1c、TG、LDL-C与WHR呈显著正相关,进一步证实了FPG、00:00F、HbA1c、TG、LDL-C可随肥胖而升高。②肥胖组HDL-C、ApoA均显著低于非肥胖组;ISI、HDL-C与WHR呈负相关,说明肥胖可以降低HDL-C水平及胰岛素敏感性,从而影响了血糖血脂代谢;③00:00F水平与FPG呈显著正相关,与HDL-C呈显著负相关,说明00:00F水平可以升高空腹血糖,参与了糖尿病患者血糖“黎明现象”的发生,降低了高密度脂蛋白水平,打破了HDL与TG或LDL的平衡,导致了脂代谢紊乱的产生。④TG与ISI呈显著负相关,与HbA1c呈显著正相关,说明TG升高降低了胰岛素敏感性,参与了HbA1c的升高。
综上所述,血糖、血脂、肥胖、皮质醇之间相互促进和影响,因此,对糖尿病患者,尤其是合并肥胖及高脂血症患者的治疗,不应从单纯应用胰岛素及口服降糖药物降糖入手,还应配合以下治疗:①嘱患者减肥,使其了解减轻体重对控制血糖血脂水平的重要性,并取得患者的积极配合;②尽最大可能地减少促进皮质醇分泌的危险因素,如适当减轻生活及工作压力,保持充足睡眠,尤其是改善夜间睡眠质量,从而减少夜间及清晨皮质醇水平的分泌,以减轻糖尿病患者的“黎明现象”,达到更好地控制空腹血糖的目的。控制皮质醇水平,还可以减轻其对高密度脂蛋白的降低,使血中三酰甘油及胆固醇更好地转化,使高密度脂蛋白“清道夫”作用充分发挥,为更好地控制糖尿病患者的血糖、血脂提供帮助,减轻糖尿病患者并发症的发生。
[1] 中华医学会糖尿病学分会.中国2型糖尿病防治指南(2013年版)[M].中国糖尿病杂志,2014,22(8):2-42
[2] 顾景范.《中国居民营养与慢性病状况报告(2015年)》解读[J].营养学报,2016,38(6):525-529
[3] 丁文清,董虹孛,米杰.中国儿童青少年血脂异常流行现状meta分析[J].中华流行病学杂志,2015,36(1):71-77
[4] 中国成人血脂异常防治指南修订联合委员会.中国成人血脂异常防治指南(2016年修订版)[J].中国循环杂志,2016,31(10):937-953
[5] 高血压联盟(中国),国家心血管病中心,中华医学会心血管病学分会,中国医师协会高血压专业委员会,吴兆苏,霍勇,王文,赵连友,朱鼎良代表《中国高血压患者教育指南》编撰委员会.中国高血压患者教育指南[J].中华高血压杂志,2013,21(12),1123-1149
[6] Rebecca MR,Mark WJ,Javier L,et al.Morning cortisol levels and cognitive abilities in people with type 2 diabetes.Diabetes care,2010,33(4):714-720
[7] Chan O,Inouye K,Akirav EM,et al.Hyperactivation of the hypothalamo-pituitary-adrenal(HPA) in diabetes is not mediated by glucose perse[J].Diabetes,2002,51(6):49
[8] 张炜,张征,徐尔理,等.2型糖尿病患者下丘脑-垂体-肾上腺轴功能变化的临床意义[J].中国全科医学,2011,14(25):2881-2883
[9] Chan O,Inouye K,Akirav EM,et al.Hyperactivation of the hypothalamo-pituitary-adrenal(HPA) in diabetes is not mediated by glucose perse[J].Diabetes,2002,51(6):49
[10] 张炜,张征,徐尔理.高血糖患者皮质醇分泌情况的临床观察[J].中国糖尿病杂志,2014,22(11):1015-1020
[11] WHO.1999糖尿病诊断标准[S].北京:人民卫生出版社,2001
[12] 殷立万,赵茜,李红.代谢综合征患者唾液皮质醇水平与心血管危险因素的关系[J].当代医学,2011,17(1):44-45
[13] 张永生,楚立云,辛苏宁,等.306例男性血糖水平和动脉血压及血浆皮质醇水平的关系及其可能机制[J].中国现代医学杂志.2007,17(7):837-838
[14] 刘颖.探讨2型糖尿病患者空腹血糖与24:00血皮质醇相关性[J].糖尿病天地·临床,2016,10(5):224-227
