不同方法治疗重型再生障碍性贫血儿童临床不良反应分析
2018-03-04孔令军何海龙
孔令军 何海龙

摘 要:目的 探讨HSCT和IST治疗儿童重型再生障碍性贫血的不良反应。方法 回顾性分析2011年10月~2017年11月我院收治的113例SAA及vSAA患儿的临床资料,其中接受HSCT治疗的30例设为HSCT组,接受IST治疗的83例设为IST组,比较两组不良反应发生率,HSCT组内不同供体状态不良反应发生率、IST组内应用p-ALG与r-ATG不良反应发生率。结果 治疗后HSCT组感染发生率(60.00%)总体较IST组(35.92%)高(P<0.05);其中HSCT组疱疹病毒感染发生率(23.33%)较IST组(3.61%)高(P<0.05);两组脓毒血症、肺部感染及真菌感染发生率比较差异无统计学意义(P>0.05);HSCT组中,非MSD治疗与MSD治疗其Ⅰ度aGVHD发生率比较,差异无统计学意义(P>0.05); 非MSD治疗较MSD治疗发生Ⅱ度及以上aGVHD、cGVHD的发生率高(P<0.05);药物应用时主要不良反应为类过敏反应,r-ATG发生率高于p-ALG(P<0.05);药物应用后主要不良反应为血清病样反应,两种药物发生率比较,差异无统计学意义(P>0.05)。结论 感染是SAA治疗中最常见不良反应,HSCT组更易发生,尤其是疱疹病毒感染比例高;HSCT治疗应注意供体选择,减少GVHD发生率;IST组应用r-ATG更易出现类过敏反应,需引起重视。
关键词:造血干细胞移植;免疫抑制治疗;移植物抗宿主病;血清病样反应;再生障碍性贫血
中图分类号:R556 文獻标识码:A DOI:10.3969/j.issn.1006-1959.2018.24.015
文章编号:1006-1959(2018)24-0059-04
Abstract:Objective To investigate the adverse reactions of HSCT and IST in the treatment of severe aplastic anemia in children. Methods The clinical data of 113 children with SAA and vSAA admitted to our hospital from October 2011 to November 2017 were retrospectively analyzed. Among them, 30 patients receiving HSCT were assigned to HSCT group, and 83 patients receiving IST treatment were set as IST group. The incidence of adverse reactions in the two groups was compared, the incidence of adverse reactions in different donor states in the HSCT group, and the incidence of adverse reactions in the IST group using p-ALG and r-ATG. Results The incidence of infection in HSCT group after treatment (60.00%) was higher than that in IST group (35.92%) (P<0.05). The incidence of herpesvirus infection in HSCT group (23.33%) was higher than that in IST group (3.61%) (P<0.05). There was no significant difference in the incidence of sepsis, pulmonary infection and fungal infection between the two groups (P>0.05).There was no significant difference in the incidence of grade I aGVHD between the non-MSD group and the MSD group in the HSCT group (P>0.05). The incidence of aGVHD and cGVHD was higher in the non-MSD treatment than in the MSD treatment (P<0.05); the main adverse reactions in drug application were allergic reactions, the incidence of r-ATG was higher than that of p-ALG (P<0.05); the main adverse reaction after drug application was serum-like reaction, the incidence of the two drugs was compared, the difference was not statistically significant (P>0.05). Conclusion Infection is the most common adverse reaction in SAA treatment, HSCT group is more likely to occur, especially herpes virus infection rate; HSCT treatment should pay attention to donor selection, reduce the incidence of GVHD; IST group is more prone to allergic reactions using r-ATG, need to cause pay attention to it.
Key words:Hematopoiet·ic stem cell transplantation;Immunosuppressive therapy;Graft versus host disease;Serum-like reaction;Aplastic anemia
再生障碍性贫血(aplastic allemia,AA)为多种发病机制引起的一种骨髓造血功能衰竭症,其中重型生障碍性贫血(severe aplastic anemia,SAA)预后较差,儿童SAA比例高于成人[1]。造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)尤其是MSD-HSCT为首选治疗方案[2]。近年来随着免疫抑制治疗(immunosuppressive therapy,IST)治疗技术的提高,也成为主要治疗手段应用于临床[3]。两者是当前治疗儿童SAA及极重型再生障碍性贫血(very severe aplastic anemia,vSAA)的主要方法[4],然而不同的治疗方法近期及远期不良反应又各有不同,本研究观察SAA患儿治疗的不良反应,以期为临床对SAA患儿治疗方法、用药选择、移植方案的改善提供参考。
1资料与方法
1.1一般资料 回顾性分析2011年10月~2017年11月苏州大学附属儿童医院收治的诊断为SAA 或vSAA,且正規应用IST或HSCT治疗的113例患儿临床资料。诊断标准参照国际再障诊疗指南,分型标准参照国际通用Camitta再障分型标准和国内标准[4,5]。本研究经医院伦理委员会备案批准,其中接受HSCT治疗的30例设为HSCT组,接受IST治疗的83例设为IST组。IST组男46例,女37例,年龄1~15岁,应用抗人淋巴细胞免疫球蛋白(r-ATG)治疗32例,应用抗人胸腺细胞免疫球蛋白(p-ALG)51例;HSCT组男15例,女15例,年龄2~11岁,其中供体为全相合同胞供者(matched sibling donor,MSD) 12例为MSD治疗,非全相合同胞供者18例为非MSD治疗。
1.2治疗方法
1.2.1 IST组 p-ALG (武汉生物制品研究所,批准文号:S20040023,250 mg/支)25 mg/(kg·d)×5 d,r-ATG(法国赛达药厂,批准文号:S20090067,25 mg/瓶)2.5 mg或3.75 mg/(kg·d)×5 d。皮试阴性后静脉滴注。p-ALG 或r-ATG 治疗后联合环孢素(CsA) 5 mg/(kg·d),口服,1次/12 h,并根据血药浓度调整剂量,使之维持在 150~250 ng/dl。
1.2.2 HSCT组 首先给予预处理,具体方案如下:①MSD-HSCT患儿选用r-ATG+氟达拉滨(fludarabine,FLU)+ 环磷酰胺(CTX)方案;②单倍体相合移植应用利妥昔单克隆抗体+r-ATG+马利兰(Busulfan,BU)+CTX。③脐血移植应用利妥昔单克隆抗体+阿糖胞苷(cytarabine,Ara-c)+FLU+CTX方案;三种方案具体剂量如下:r-ATG: 2.5 mg/(kg·d),共4 d;CTX:50 mg/(kg·d),共4 d;利妥昔单克隆抗体375 mg/(m2·次),使用1~2次;FLU:40 mg/(m2·d)2~5 d;Ara-c:2 g/(m2·d),共2 d,BU:0.8 mg/(kg·d),共4 d。采用联合应用钙调蛋白拮抗剂+霉酚酸酯+短程甲氨蝶呤方案预防及治疗移植物抗宿主病(graft versus host disease ,GVHD)。
1.2.3辅助治疗 患儿治疗在层流病房或净化帐进行,并给予红细胞、血小板、粒细胞刺激因子等支持。
1.3随访 随访截止2018 年 2月 11日,共随访4~69个月,内容包括:患儿生存状态、治疗时及治疗后发生感染、GVHD、类过敏反应、血清病样反应的发生率。
1.4评价指标及标准 比较患儿治疗期间及治疗后不良反应指标:①感染类型、部位及诊断依据;②HSCT后GVHD发生情况及严重程度;③r-ATG/p-ALG使用时类过敏反应及使用后血清病样反应。评价标准:①患儿治疗中及治疗后血培养、痰培养等实验室阳性指标,影像学表现阳性及临床体格检查显示存在感染;②HSCT后100 d以内发生皮疹、肝脏、肠道、肺脏等排异反应为aGVHD,100 d以上为cGVHD,并根据受累器官严重程度分为Ⅰ~Ⅳ度;r-ATG/p-ALG用药时排除感染的发热、皮疹、呛咳、关节肿痛等为类过敏反应,用药7~10 d后出现发热、皮疹、关节肿痛、关节积液、骨质损害等为血清病样反应。
1.5统计学处理 数据使用SPSS 24.0 进行数据分析。计数资料使用[n(%)]进行描述,采用?字2检验,P<0.05 认为差异有统计学意义。
2结果
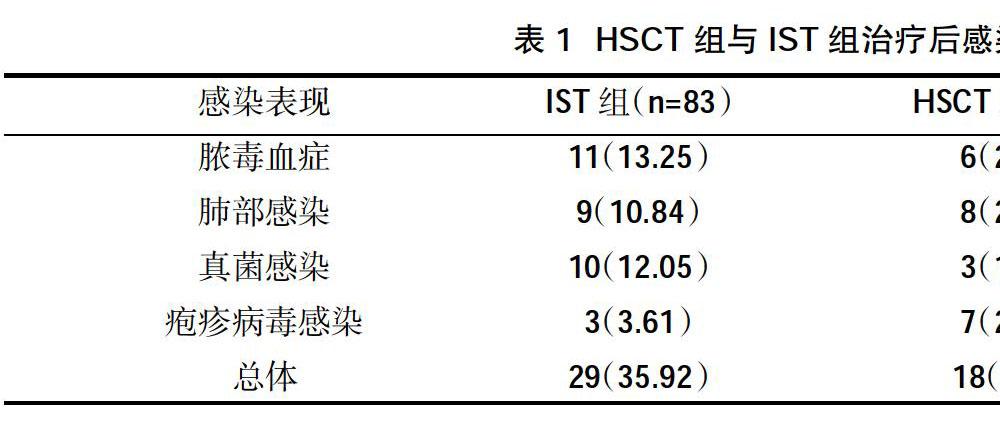
2.1两组患者感染情况表现比较 治疗后HSCT组感染发生率总体较IST组高,差异有统计学意义(P<0.05);其中HSCT组疱疹病毒感染发生率较IST组高,差异有统计学意义(P<0.05),两组脓毒血症、肺部感染及真菌感染发生率比较,差异无统计学意义(P>0.05),见表1。
2.2 HSCT组不同供体状态GVHD发生率的比较 HSCT组中,非MSD治疗与MSD治疗其Ⅰ度aGVHD发生率比较,差异无统计学意义(P>0.05); 非MSD治疗较MSD治疗发生Ⅱ度及以上aGVHD、cGVHD的发生率高,差异有统计学意义,见表2。
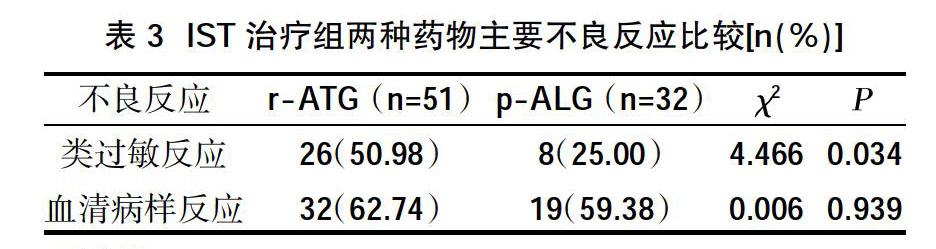
2.3 IST治疗组两种药物主要不良反应比较 83例IST患儿中,51例使用r-ATG,32例使用p-ALG。药物应用时主要不良反应为类过敏反应,使用r-ATG类过敏反应发生率高于p-ALG,差异有统计学意义(P<0.05);药物应用后主要不良反应为血清病样反应,两种药物血清病样反应发生率比较,差异无统计学意义(P>0.05),见表3。
3讨论
再生障碍性贫血是一种自身免疫功能异常导致的骨髓造血功能衰竭性疾病,其发病原因可能与各种未知病因所致的T细胞功能异常和骨髓造血组织免疫损伤有关。无论使用哪种治疗方法,最终治疗的目的是恢复骨髓造血功能[5]。
感染是SAA治疗期间主要并发症,也是导致严重不良后果的主要因素之一。采用IST治疗可显著清除人外周血淋巴细胞起治疗作用,但此刻治疗破坏白细胞导致粒细胞进一步下降,国内陶晓虹等有报道[6]显示其感染发生率为50%左右,其中主要为血液及呼吸道感染,但因各中心治疗环境及预防措施不同,感染情况存在差异,本研究中IST患儿感染发生率为35.92%,这可能与我们净化帐及层流病房的应用、严格地消毒隔离措施有关。HSCT治疗前需给予预处理清髓,其后期免疫重建需要的时间长达1年甚至数年,在此期间也容易产生严重的机会性感染;本研究HSCT治疗感染发生率高于IST治疗组,且主要为血液感染,其中疱疹病毒感染率高于IST组。感染是导致植入失败、免疫功能重建失败的主要因素之一,尽管SAA治疗指南[2]建议HSCT为首选方案,但治疗期间感染的发生也应该给予重点关注, 适当给予合理的防治措施尤为重要。目前针对AA患儿预防性应用抗生素的安全性和有效性的对照研究报道较少,但国内SAA儿童诊疗建议对积极控制感染的必要性是肯定的[3]。结合中国中性粒细胞缺乏伴发热患者抗菌药物临床应用指南[7],当AA治疗后中性粒细胞绝对值<0.5×109/L时,需预防性口服抗真菌药物;当出现粒细胞缺乏时,发热超过1 h或血象恢复后感染超过48 h应该应用抗菌药物,在感染超过96 h并具有影像学和临床表现者,应进行抗真菌治疗。
GVHD也是接受HSCT治疗患儿主要的并发症,是导致移植治疗失败的一个重要原因。GVHD的防治是目前研究的热点,为显著降低GVHD发生率,欧洲骨髓移植协作组重型再生障碍性贫血工作组[8]及我国中华医学会儿科学分会血液组[3]均将MSD-HSCT为首选治疗方案,本研究中采用非MSD治疗的患儿发生Ⅱ度及以上aGVHD、cGVHD比例与采用MSD治疗的患儿比较有差异显著,故HSCT治疗选择合适的供体尤为重要。IST治疗需重视类过敏反应,国内有报道r-ATG治疗儿童AA类过敏反应为34.4%[9],本研究中r-ATG发生率(50.98%)高于p-ALG发生率(25.00%),两者比较差异有统计学意义;国内也有报道显示使用r-ATG或p-ALG治疗SAA发生血清病反应比例无显著差异,一般为52.0%~68.0%[10];本研究发生血清病样反应r-ATG組比例为62.74%,p-ALG组比例59.38%,两者比较,差异无统计学意义。
综上所述,随诊治疗技术的提高治疗技术已相对成熟,但为提高SAA患儿长期生存质量,治疗过程中需重视不良反应,尤其高度重视防治感染,在治疗方案的选择时建议考虑; 选择HSCT治疗时应注意尽量选择MSD作为供体,减少GVHD发生率;IST组治疗时r-ATG、p-ALG导致的类过敏反应、血清病样反应需注意防治。
参考文献:
[1]Boddu PC,Kadia TM.Updates on the pathophysiology and treatment of aplastic anemia:a comprehensive review[J].Expert Review of Hematology,2017,10(5):433-438.
[2]Barone A,Lucarelli A,Onofrillo D,et a1.Diagnosis and management of acquired aplastic anemia in childhood.Guidelines from the Marrow Failure Study Group of the Pediateic Haemato Oncology Italian Association(AIEOP)[J].Blood Cells Mol Dis,2015,55(1):40-47.
[3]中华医学会儿科学分会血液学组,《中华儿科杂志》编辑委员会.儿童获得性再生障碍性贫血诊疗建议[J].中华儿科杂志,2014,52(2):103-106.
[4]Killick SB,Bown N,Cavenagh J,et a1.Guidelines for the diagnosis and management of adult aplastic anaemia[J].Br J Haemat,2016,172(2):187-207.
[5]中华医学会血液学分会红细胞疾病(贫血)学组.再生障碍性贫血诊断与治疗中国专家共识(2017年版)[J].中华血液学杂志,2017,38(1):1-5.
[6]陶晓虹,董红华.再生障碍性贫血患者医院感染相关因素分析与预防[J].中华医院感染学杂志,2016,26 (5):1020-1030.
[7]中华医学会血液学分会.中国中性粒细胞缺乏伴发热患者抗菌药物临床应用指南(2016年版)[J].中华血液学杂志,2016, 37(5):353-359.
[8]Dufour C,Pillon M,Passweg J,et al.Outcome of aplastic anemia in adolescence:a survey of the Severe Aplastic Anemia Working Party of the European Group for Blood and Marrow Transplantation[J].Haematologica,2015,169(4):565-573.
[9]苏雁,吴润晖,马洁,等.兔抗胸腺细胞球蛋白联合环孢素免疫抑制治疗儿童重型再生障碍性贫血的疗[J].中华实用儿科临床杂志,2015,30(3):189-193.
[10]杨楠,马肖容,张卉,等.猪抗人淋巴细胞球蛋白与兔抗人胸腺细胞球蛋白治疗重型再生障碍性贫血的疗效比较[J].南方医科大学学报,2016,36(3):303-308.
收稿日期:2018-12-12;修回日期:2018-12-20
编辑/肖婷婷
