用P204从不锈钢酸洗污泥浸出液中萃取重金属试验研究
2018-03-02刘平阳谈定生丁伟中
刘平阳,谈定生,2,丁伟中,2
(1.上海大学 材料科学与工程学院,上海 200072;2.上海大学 省部共建高品质特殊钢冶金与制备国家重点实验室,上海 200072)
不锈钢酸洗污泥是不锈钢生产加工过程中用酸进行表面处理时产生的废水经石灰乳中和后产生的固体废弃物,其中含有铬、镍、铁等重金属,不可随意处置。采用浸出法处理酸洗污泥,将其中的有价金属转入溶液,再进行分离回收,可使酸洗污泥得到无害化处理,进而实现资源综合利用[1-2]。
酸洗污泥浸出液中的金属综合回收法有沉淀除铁—离子交换法分离回收铬镍、膜电解法回收有价金属等[3-4],这些方法在工业应用过程中都存在一些尚待进一步解决的问题,经济性也有待提高。试验研究了以二(2-乙基己基)磷酸(P204)为萃取剂,采用溶剂萃取法从不锈钢酸洗污泥硫酸浸出液中分离金属,探讨萃取条件对铬、镍、铁分离效果的影响,以期为酸洗污泥的综合治理提供参考方法。
1 试验部分
1.1 试验料液与试剂
不锈钢酸洗污泥硫酸浸出液中含有硫酸铬、硫酸镍和硫酸亚铁,其中铬、镍、铁质量浓度分别为4.1、1.6和28.0 g/L。
萃取剂P204,购自上海彭浦化工厂;其他试剂均购自国药集团化学试剂有限公司。
1.2 分析方法与仪器
铬的测定采用高锰酸钾氧化-二苯碳酰二肼分光光度法,镍的测定采用丁二酮肟分光光度法,铁的测定采用邻菲啰啉分光光度法[5-6]。
主要仪器:pHs-3C型pH计(上海精密科学仪器有限公司),722型可见分光光度计(上海精密科学仪器有限公司),傅立叶变换红外光谱仪(德国Bruker Optik Gmbh 公司)。
1.3 试验方法
萃取和反萃取均在分液漏斗中进行。将有机相和水相按一定比例加入到分液漏斗中,振荡一定时间后,静置至两相分层,然后分离出水相,测定水相中Cr3+、Ni2+、Fe2+质量浓度,据此计算Cr3+、Ni2+、Fe2+萃取率、萃取分配比和元素间的分离系数。
1.4 试验原理
P204(HA)为酸性磷类萃取剂,在非极性溶剂中以二聚分子(HA)2形式存在,并以二聚分子形式与金属离子发生反应。在硫酸盐体系中,P204萃取Cr3+、Ni2+、Fe2+的反应式如下:
(1)
(2)
(3)
萃取后,金属离子以配合物形式进入有机相。在同一体系中,不同金属离子与P204发生反应的平衡常数存在差异,平衡常数较大者易被萃入到有机相中,因而与平衡常数较小者分离。
2 试验结果与讨论
2.1 金属离子的萃取平衡等温线
有机相组成50%P204+40%260#溶剂油+10%正辛醇,P204皂化率为75%,室温条件下,金属离子水溶液pH=3.0,混合振荡5 min,采用等相比法测定Cr3+、Ni2+、Fe2+萃取平衡等温线,试验结果如图1所示。

图1 金属离子的萃取平衡等温线
由图1看出:水相中金属离子质量浓度较低时,等温线几乎为直线;随水相中金属离子质量浓度增大,有机相中金属离子质量浓度提高幅度逐渐降低,直至不再升高,有机相达到饱和。试验条件下,P204对Cr3+、Ni2+、Fe2+的饱和萃取容量分别为32.45、18.89和24.27 g/L,表明P204对Cr3+的萃取能力最强,对Fe2+的萃取能力次之,对Ni2+的萃取能力最弱。
2.2 萃取剂皂化率对金属离子萃取的影响
酸性萃取剂萃取金属离子的萃取能力与平衡时的pH密切相关。根据萃取原理,P204萃取金属离子时,氢离子与金属离子交换,会使水相pH降低[7-8]。为使萃取过程中水相pH变化幅度较小,通常将P204进行皂化预处理,即将P204部分转化为钠型。
在有机相组成50%P204+40%260#溶剂油+10%正辛醇、相比1/1、料液初始pH=3.14、室温条件下,P204皂化率对金属离子萃取率的影响试验结果如图2所示。
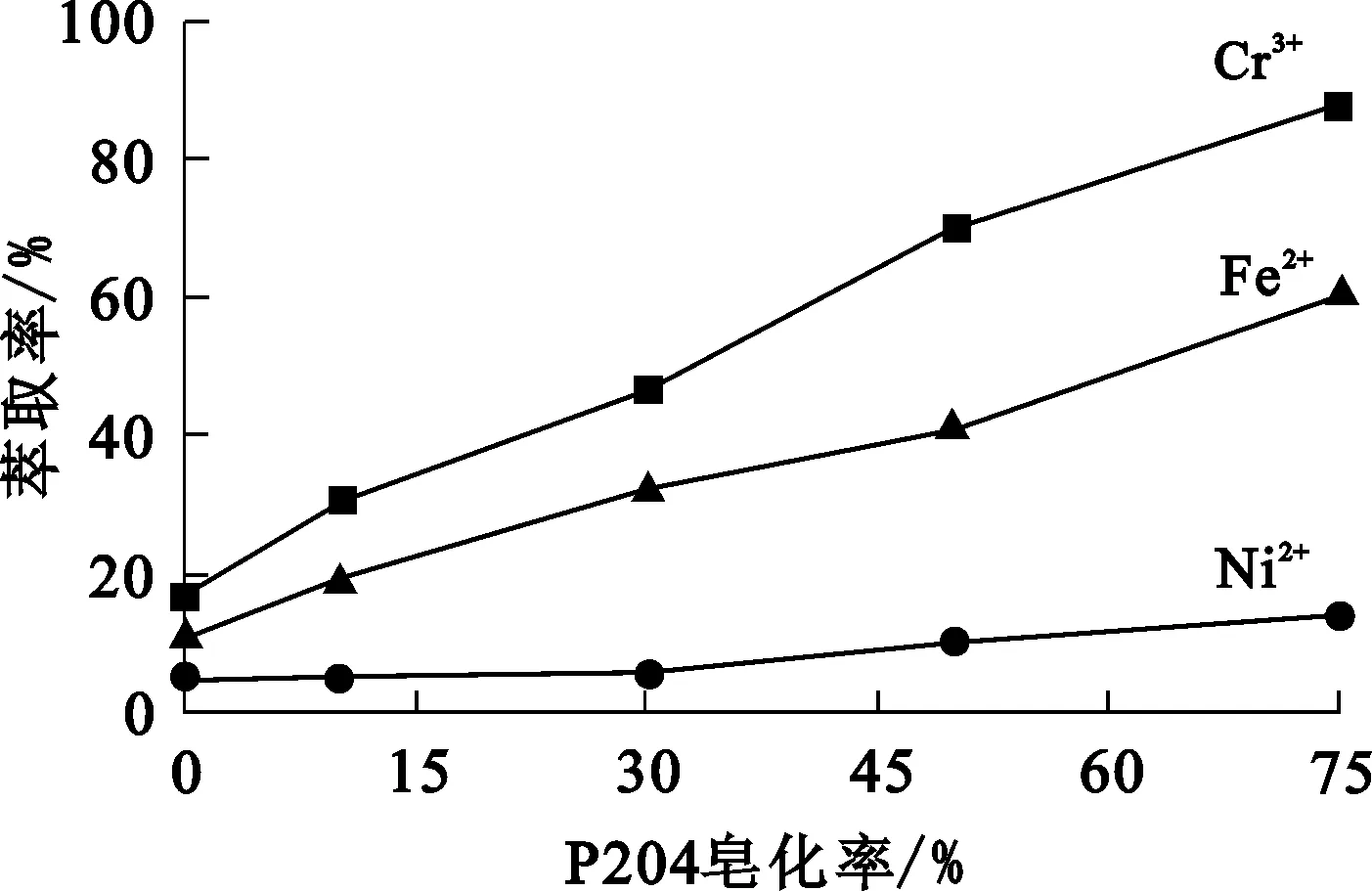
图2 P204皂化率对金属离子萃取率的影响
由图2看出:随P204皂化率升高,3种金属离子萃取率均呈上升趋势,但对3种金属离子萃取的影响程度不同;价态高的Cr3+较价态低的Ni2+和Fe2+的萃取受萃取剂皂化率变化影响更大,根据这一特点,提高萃取剂皂化率,不仅能提高有机相萃取能力,还可提高金属离子间的萃取分离系数,有利于金属的分离;萃取剂皂化率为75%时,Cr3+、Ni2+、Fe2+的萃取率分别为87.93%、14.19%和59.83%,分离系数β(Cr/Ni)、β(Cr/Fe)和β(Fe /Ni)分别为44.12、4.90和9.02。
试验中还发现,随萃取剂皂化率升高,萃取后两相分相时间延长,因此,确定适宜的皂化率,还需综合考虑实际操作中对分相时间的要求。
2.3 振荡时间对金属离子萃取的影响
在有机相组成50%P204+40%260#溶剂油+10%正辛醇、萃取剂皂化率75%、相比1/1、料液初始pH=2.98、室温条件下,振荡时间对金属离子萃取率的影响试验结果如图3所示。
萃取达到平衡的时间与萃取速率有关;剧烈振荡时,萃取速率取决于金属离子与萃取剂反应生成萃合物的反应速率;对同一萃取剂而言,反应速率与萃取剂浓度、金属离子浓度、温度和体系pH有关。由图3看出:试验条件下,随振荡时间延长,Cr3+、Ni2+、Fe2+萃取率缓慢提高;萃取5 min时,3种金属离子的萃取反应均达到平衡。
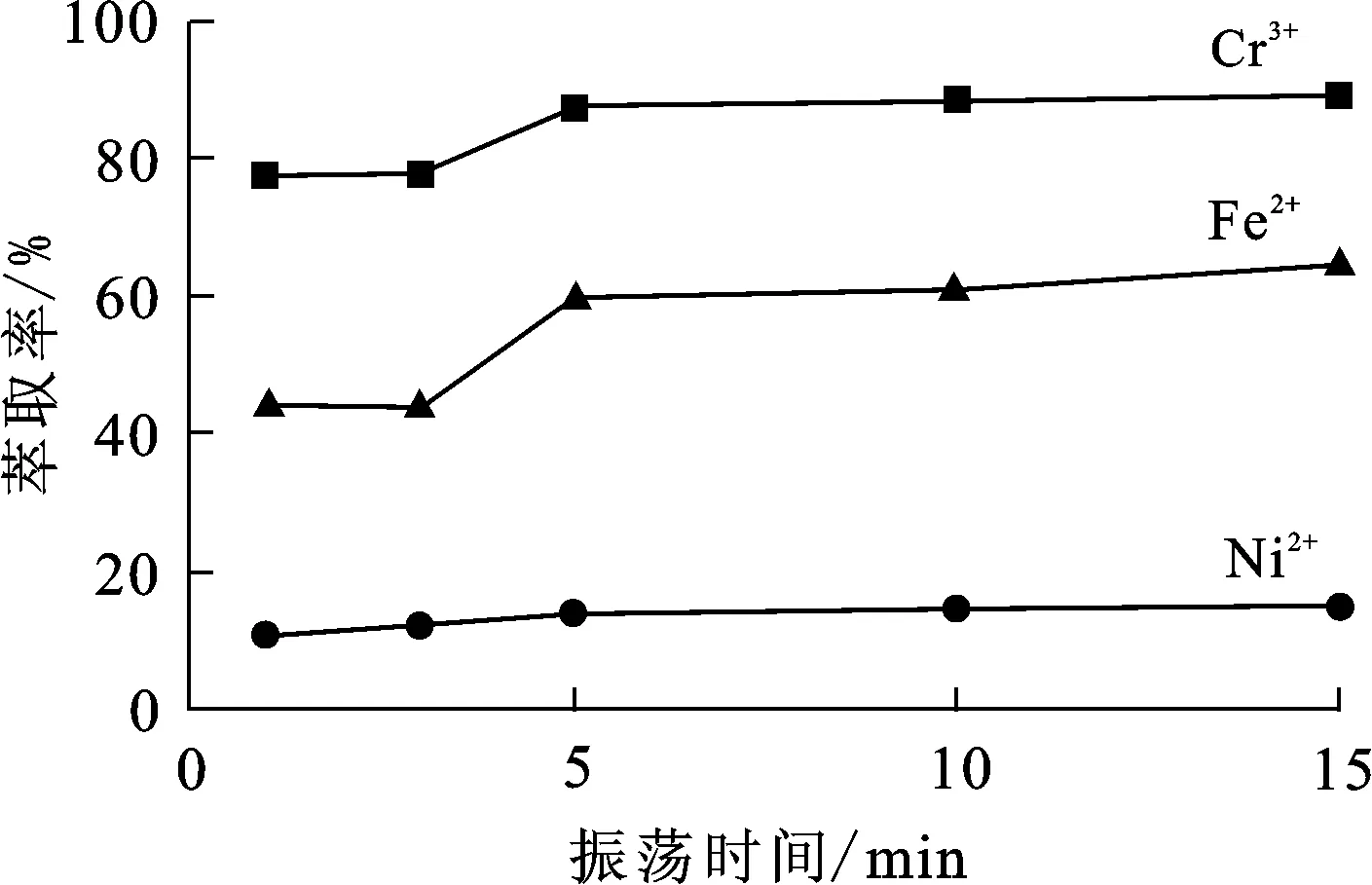
图3 振荡时间对金属离子萃取率的影响
2.4 稀释剂对金属离子萃取的影响
稀释剂是有机相的重要组成部分,不仅能改善两相的分相性能,还会影响萃取剂与萃合物在两相中的分配。其他条件不变,稀释剂对金属离子萃取率的影响试验结果如图4所示。
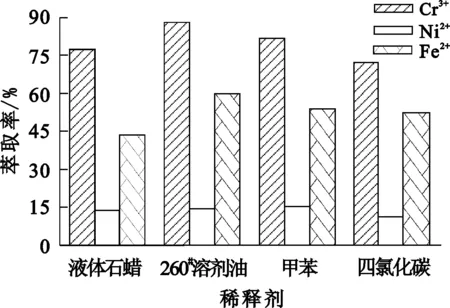
图4 稀释剂对金属离子萃取率的影响
由图4看出,采用260#溶剂油作稀释剂,金属萃取率最高。尽管用四氯化碳作稀释剂,两相分相时间最短,但考虑到价格、毒性等因素,确定选择260#溶剂油更合适。
2.5 相比对金属离子萃取的影响
有机相与水相体积比对金属的萃取和分离有较大影响。其他条件不变,相比对金属萃取率和金属离子间的分离系数的影响分别如图5、6所示。
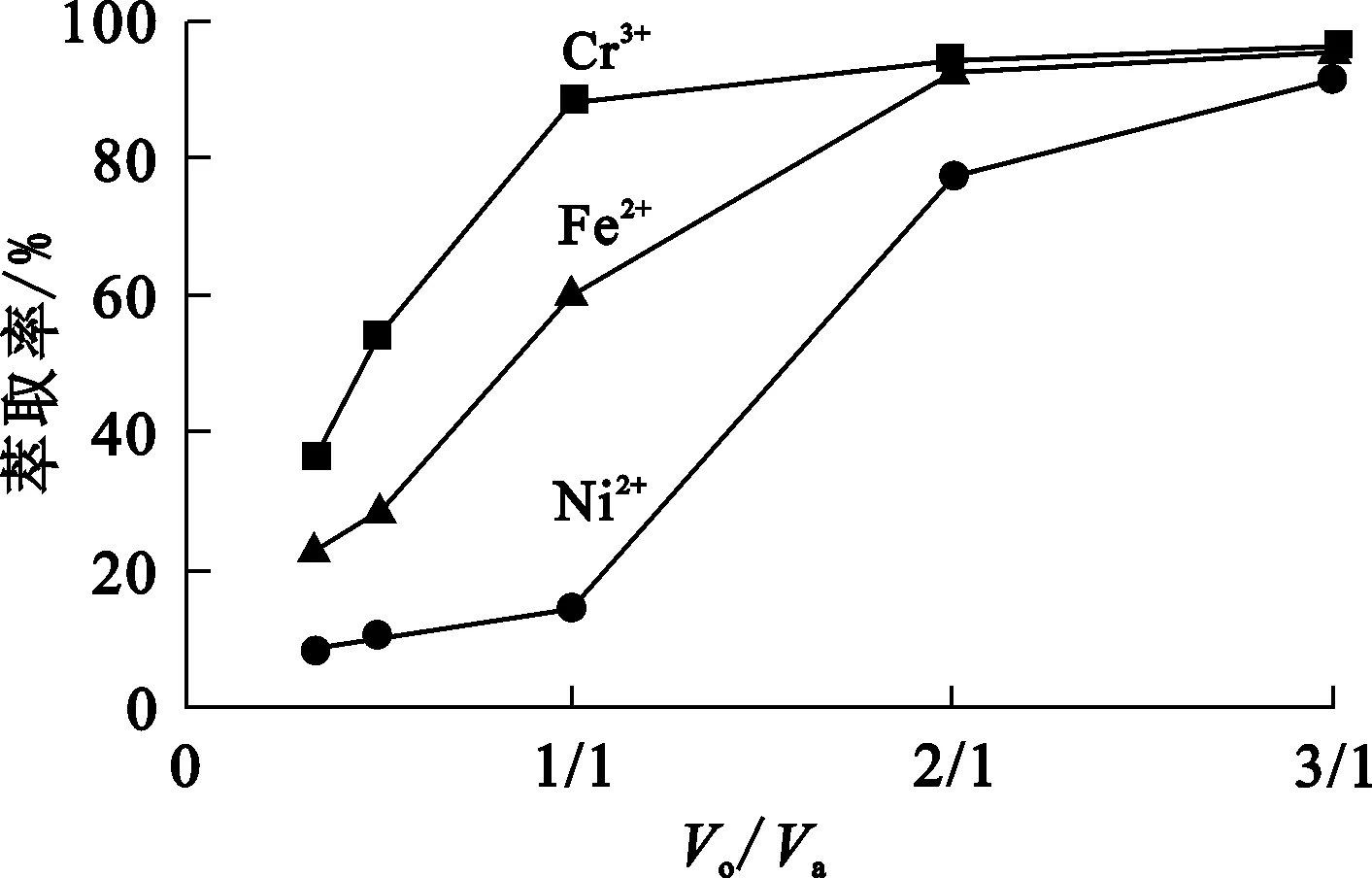
图5 相比对金属离子萃取率的影响

图6 相比对金属离子间分离系数的影响
由图5看出:随相比增大,3种金属离子萃取率均提高;相比大于2/1后,3种金属离子萃取率提高幅度均变小。由图6看出,相比对影响金属离子间的分离系数也有影响:相比为1/1时,不同离子间的萃取分离系数最大,即此条件下,3种金属离子之间的分离效果最好。综合考虑萃取剂的成本和分离效果,确定相比为1/1较为适宜。
2.6 料液pH对金属离子萃取的影响
P204萃取金属离子时,料液酸度对萃取有较大影响。在有机相组成50%P204+40%260#溶剂油+10%正辛醇、相比1/1、振荡时间5 min、室温条件下,料液pH对金属离子萃取率的影响试验结果如图7所示。

图7 料液pH对金属离子萃取率的影响
由萃取反应可知,随溶液pH增大,反应有利于正向进行。从反应平衡角度考虑,若要得到较高萃取率,料液pH越高越好;但金属离子的水解效应决定了料液pH不能太高,否则会出现氢氧化物沉淀使萃取无法正常进行:综合考虑,试验确定料液初始pH以3.0为宜。
2.7 温度对金属离子萃取的影响
温度影响萃取反应的平衡常数和萃合物在两相中的分配,进而影响金属萃取率。在有机相组成为50%P204+40%260#溶剂油+10%正辛醇、P204皂化率75%、相比1/1、料液初始pH=3.0、萃取时间5 min条件下,温度对金属离子萃取率的影响试验结果如图8所示。
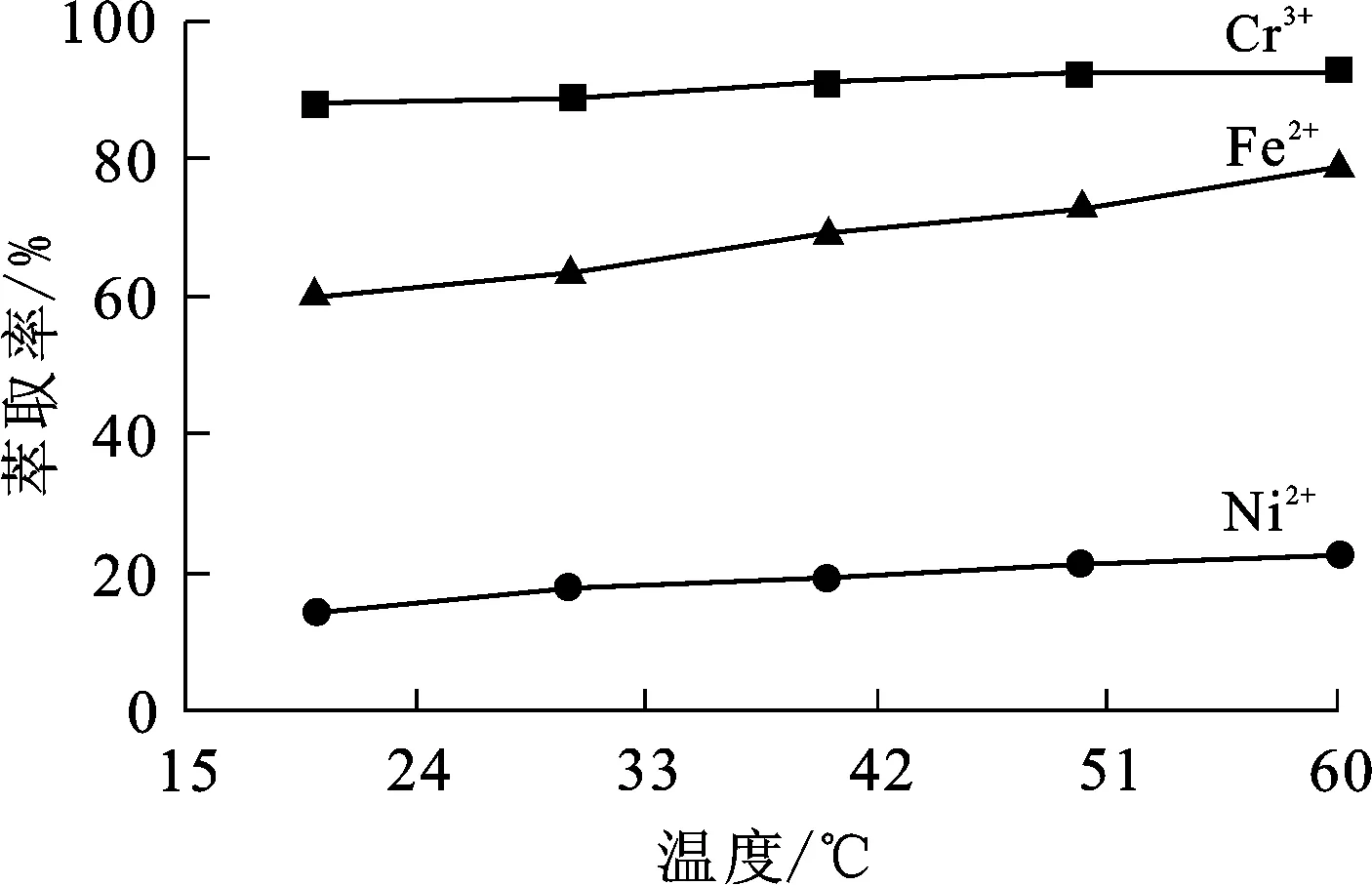
图8 温度对金属离子萃取率的影响
由图8看出,随温度升高,金属离子萃取率有一定幅度提高,但幅度不大。
根据萃取过程热力学,当金属离子与萃取剂只生成一种萃合物时,萃取分配比(D)和温度(T)之间的关系式为[9]
(4)
以lgD为纵坐标、1/T为横坐标作图得分配比与温度之间的关系曲线,如图9所示。
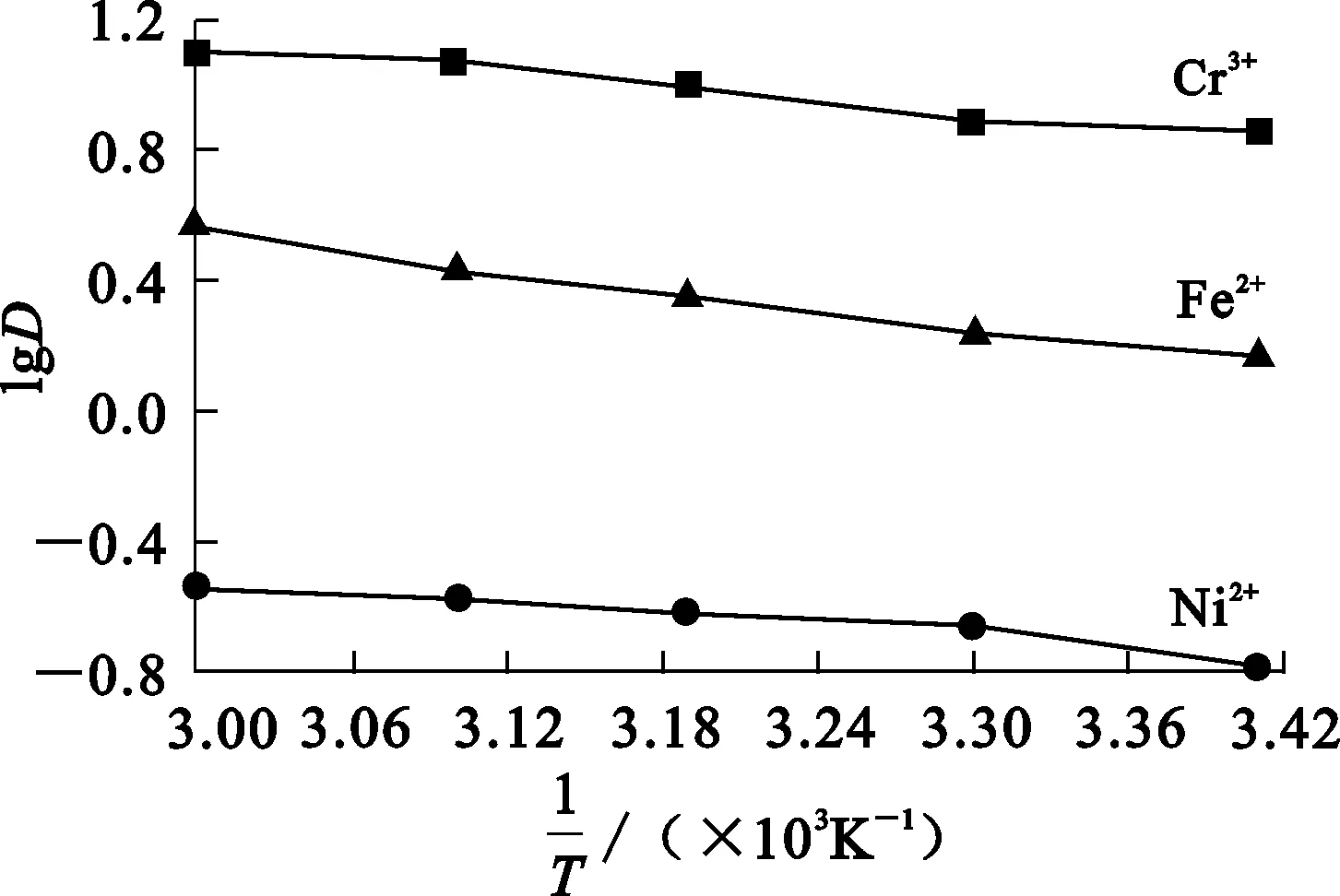
图9 lgD与1/T之间的关系曲线
对图9数据进行线性拟合,得到P204萃取Cr3+、Ni2+、Fe2+的萃取热焓分别为13.76、11.98、20.32 kJ/mol。数据表明,3种金属离子的萃取反应均为吸热反应,升高温度有利于萃取反应的进行。相比而言,温度对Fe2+萃取的影响更大。
2.8 负载有机相的反萃取
对适宜条件下获得的负载有机相用硫酸反萃取,控制相比为1/1,振荡时间5 min,室温下进行反萃取试验,结果如图10所示。
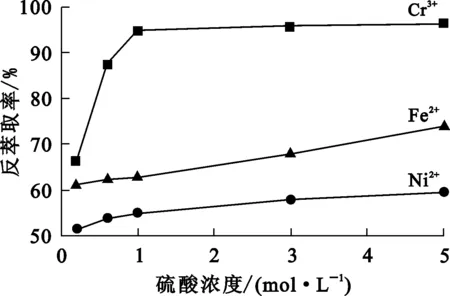
图10 硫酸浓度对金属离子反萃取率的影响
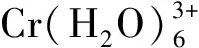
2.9 萃合物的红外光谱分析
图11为萃取前后有机相的红外光谱分析结果。

a—萃取前有机相;b—负载Cr3+有机相; c—负载Ni2+有机相;d—负载Fe2+有机相。
3 结论
以P204为萃取剂,260﹟溶剂油为稀释剂,采取溶剂萃取工艺可以处理不锈钢酸洗污泥的硫酸浸出液去除Cr3+、Fe2+、Ni2+等重金属离子。在P204皂化率75%条件下,Cr3+的一级萃取率达87.93%,Cr3+与Fe2+、Ni2+的分离系数可达44.12和4.90。用稀硫酸反萃取,Cr3+反萃取率最高。采用本方法可以实现铬与镍、铁的有效分离并有效处理含重金属Cr3+、Ni2+的酸性废水。
[1] 黄文平.江苏省酸洗污泥现状调查及管理对策研究[J].中国资源综合利用,2011,29(9):58-60.
[2] 石磊,陈荣欢,王如意.不锈钢冷轧重金属污泥的处理与利用对策[J].再生资源与循环经济,2011,4(6):33-36.
[3] 戴伟华.镍铬酸洗污泥处理工艺的探讨[J].有色冶金设计与研究,2010,31(6):48-51.
[4] ROGENER F,SARTOR M,BAN A,et al.Metal recovery from spent stainless steel pickling solutions[J].Resources,Conservation and Recycling,2012,60(3):72-77.
[5] 国家环境保护总局.水和废水监测分析方法[M].4版.北京:中国环境科学出版社,2002.
[6] 北京矿冶研究总院测试研究所.有色冶金分析手册[M].北京:冶金工业出版社,2008.
[7] 朱屯.萃取与离子交换[M].北京:冶金工业出版社,2005.
[8] 唐双华,覃文庆.从硫酸锌溶液中萃取锌的试验研究[J].湿法冶金,2008,27(2):96-100.
[9] 徐光宪.萃取化学原理[M].上海:上海科学技术出版社,1984.
[10] SZE Yu Keung Peter,XUE Lizhen.Extraction of zinc and chromium(Ⅲ) and its application to treatment of alloy electroplating wastewater[J].Separation Science and Technology,2003,38(2):405-425.
[11] 宁永成.有机化合物结构鉴定与有机波谱学[M].3版.北京:科学出版社,2014.
[12] 薛松.有机结构分析[M].合肥:中国科学技术大学出版社,2005.
