SO2对Pd掺杂La0.9Sr0.1MnO3催化剂去除NOx和碳烟的影响
2018-03-02朱淑维舒新前王苏健邓增社中国矿业大学北京化学与环境工程学院北京00083陕西煤业化工技术研究院有限责任公司陕西西安70065
杨 丽,朱淑维,舒新前*,王苏健,邓增社 (.中国矿业大学(北京)化学与环境工程学院,北京 00083;.陕西煤业化工技术研究院有限责任公司,陕西 西安 70065)
国民经济的快速发展,导致了严重的环境污染.其中一个重要原因,就是交通运输业的迅猛发展以及机动车保有量的持续增加.环境监测表明,随着机动车保有量的快速增加,我国城市空气开始呈现出煤烟和机动车尾气复合污染的特点,直接影响群众健康.而我国至今没有成熟的针对柴油机主要污染组分NOx控制的机外后处理技术,且国内也尚未对柴油车尾气碳烟排放进行有效的机外净化治理.
柴油机排放的尾气中主要污染物有:一氧化碳(CO)、碳氢化合物(CH)、氮氧化物(NOx)和碳烟颗粒(PM).其中,NOx是形成酸雨的重要原因,同时还会在大气中与CH发生光化学反应,生成臭氧等多种氧化性很强的物质,造成光化学烟雾[1-2];NOx还是主要的刺激性气味来源,对人类健康产生严重影响.所排放的碳烟颗粒,能够引发许多呼吸系统疾病,严重危害人类健康[3-6].柴油车排放已引起世界各国的高度重视,相继制定出越来越严格的排放法规.目前,美国、欧洲和日本都制定了日趋严格的汽车排放标准体系[7].中国的重型柴油车国五排放标准将于2017年7月1日起全面实施,轻型柴油车国五排放标准将于2018年1月1日起全面实施.并且,近日环境保护部发布“关于征求国家环境保护标准《车用压燃式、气体燃料点燃式发动机与汽车排气污染物排放限值及测量方法(中国第六阶段)(征求意见稿)》意见的函”,环境保护部正式对柴油车国六排放法规向企业单位征求意见,也就是说柴油车国六排放标准,将于2020年1月1日起全面实施[8].因此,世界各国正在努力开发尾气处理新技术,以解决柴油机碳烟颗粒与氮氧化物等排放所引发的环境污染问题.目前针对柴油发动机空燃比高的特点提出的在稀燃条件下去除NOx技术主要有四种,分别是NO直接分解技术,选择性催化还原(SCR)技术[9],NOx和碳烟同时催化脱除技术和NOx储存还原(NSR)技术[10].特别是,随着柴油车越来越广泛的使用,高效处理柴油车排放的尾气是目前的重要课题,也是将来的方针趋势.实施柴油车尾气中四种污染物的同时处理技术(即四效催化技术)已经显得越来越迫切.
钙钛矿型化合物具有稳定的结构,较多的氧空位和优异的导热性,且其B位离子具有多种可变价态和异常价态等优点,在富氧条件下钙钛矿型化合物对NO有一定的转化能力,因此,钙钛矿型材料有望成为新一代的汽车尾气净化催化剂[11].
孙志强[12]课题组采用低温燃烧法制备了Sr部分取代La1-xSrxCo0.5Mn0.5O3钙钛矿型复合氧化物催化剂,实验结果表明,Sr部分取代La可以增加催化剂表面的氧空位数,同时形成 Mn3+—Mn4+共存体系,催化剂对碳颗粒和NO去除显示出很好的催化活性.赵震等[13-15]研究了LaMnO3钙钛矿型复合氧化物催化剂, La0.8K0.2MnO3催化剂有较好的催化性能, CO和碳烟颗粒的起燃温度降低,生成CO2的选择性高于99%,烃类在较低温度下的转化率为90%.但对NOx还原为N2的效率则有待提高.
目前四效组合催化存在着运行成本较高、结构复杂、占用空间大等问题,例如,用于碳烟-NOx氧化还原的催化剂普遍存在NOx转化率较低、低温选择性较差且易发生硫中毒等问题[16-18].
由于Mn具有可变的d电子结构,有多种价态,因而表现出较好的氧化还原性能,La原子半径大,同时具有较高的热稳定性,因此LaMnO3是一种高温稳定的氧化还原催化剂.它在很多领域都已得到应用.例如,燃料电池,气体传感器,磁性结构、碳氢化合物氧化燃烧等[19-24].在LaMnO3的A位掺杂Sr2+离子后,La1-xSrxMnO3体系中出现了Mn4+和氧空位,使得该钙钛矿型复合金属氧化物催化剂具有优异的催化活性.经研究表明在钙钛矿催化剂中添加少量的贵金属可以提高催化剂的活性,负载少量贵金属Pd的钙钛矿型氧化物催化剂具有更高的催化活性,即使在高温含有水蒸气和硫化物的汽车尾气中也可长时间具有很高的催化性能[25-26].一个具有高催化活性的氮氧化物储存还原催化剂要求其在富氧条件下能够完全储存NOx,在贫氧气氛中通过还原剂将NOx还原为N2.因此,本文中制备的(La1-xSrxMn1-yPdyO3)催化剂是同时含有能将NOx以硝酸盐的形式储存的碱性储存中心Sr和催化活性中心Pd的锰基钙钛矿,具有优秀的氧化还原性能,且能在高硫浓度下依旧保持较好的催化活性,使其成为一个有前景的应用于柴油机尾气治理的NOx-PM同脱催化剂.
1 材料与方法
1.1 催化剂制备
按摩尔比9:1:9.7:0.3分别称取硝酸镧、硝酸锶、硝酸锰和氯化钯溶解于适量的去离子水中,按照柠檬酸:金属离子总和为1:1.2的摩尔比例加入柠檬酸,先将称量的柠檬酸溶解于适量的去离子水中,再与上述金属硝酸盐溶液混合均匀,制得湿凝胶.再将湿凝胶转移至真空干燥箱中120℃恒温干燥12h,得到疏松多孔的干凝胶.干凝胶经破碎、研磨再转移至坩埚中,随后放置于马弗炉中,在空气气氛下缓慢升温至200~800℃并保持2h,然后升温至煅烧400~800℃,煅烧4h.煅烧后得到黑色粉末状的催化剂,研磨后储存备用.
1.2 催化剂表征和活性测试
1.2.1 表面形态及结构表征 吸附剂表面分析采用扫描电子显微镜(SEM,该仪器由日本HITACHI公司生产,仪器加速电压为15kv,实验所用的放大倍数为2000~10000倍).吸附剂形态采用X射线衍射(XRD,型号Utima Ⅲ,日本,Cu Kα靶,功率40kV×40mA).比表面积测试采用氮气吸附-解吸等温线法(BET,型号NOVA4000,美国康塔公司).催化剂表面官能团,采用傅里叶红外光谱仪进行分析(FT-IR,该仪器由美国Nicolet公司生产,型号Magna-IR750).
1.2.2 性能评价系统 催化剂的装填:在催化反应器的恒温区,将0.45g催化剂与0.05g碳烟紧密接触后装入反应器内,然后将高压钢瓶中的相应反应气体(NO(0.1%)、C3H6(0.05%)、CO(0.5%)和O2(10%)),经过气体混合器后通入催化反应器内,进行程序升温反应,空速为16000h-1.
开始升温反应之前,系统用高纯Ar气在200℃下吹扫2h,以清扫掉催化剂和残留的气体和水分.之后再将纯的Ar气切换成按一定配比组成的原料气进入反应器,按一定的升温速率进行升温反应.反应后气体产物用色谱仪检测分析.反应过程中,反应气体的转化率分别采用以下的公式计算:

表1 试验烟气参数Table 1 Flue gas parameters of the experiment
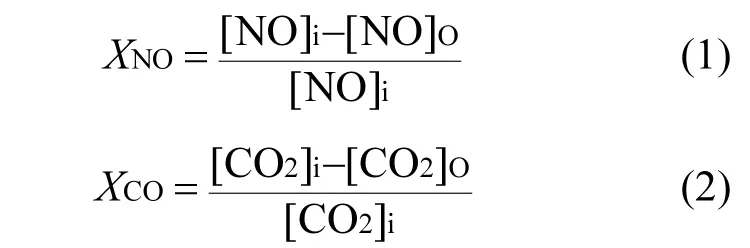
式中: X代表反应过程中某组分的转化率;i代表反应过程中某组分的进口浓度;O代表反应过程中某组分的出口浓度(由色谱分析得到).
2 结果与讨论
2.1 形貌及晶体结构表征
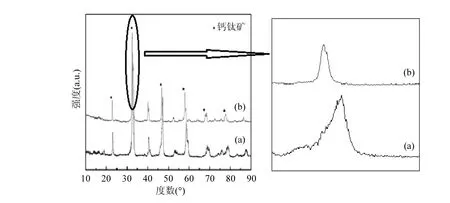
图1 催化剂的XRD及特征峰32.8°处的放大(右)图谱Fig.1 the XRD of catalyst and its amplification (right) map in 32.8°
图1对比了所制的La0.9Sr0.1MnO3以及La0.9Sr0.1Mn0.97Pd0.03O3催化剂反应前的XRD图谱,从图1可以看出,催化剂(a)和(b)都在23.4°、32.8°、40.2°、47.5°、58.9°附近出现明显的钙钛矿晶型特征峰(与标准JCPDS卡片中NO.01-084-0848R-3C(167)构型比对)[27].掺杂Pd后,虽然峰强度略有下降,但依旧能够保持较好的钙钛矿结构.La0.9Sr0.1MnO3号催化剂的晶粒尺寸为13.7nm,掺杂Pd后的La0.9Sr0.1Mn0.97Pd0.03O3号催化剂晶粒尺寸增大到21.6nm,且掺杂Pb后钙钛矿衍射峰向小角度偏移.因为Pd2+的离子半径比Mn4+的大,当Pd2+取代Mn4+进入钙钛矿晶格后,会导致钙钛矿晶胞尺寸的增大,引起衍射峰位置向小角度偏移,晶面间距变大.进一步证实了Pd掺杂入了LaSrMnO3钙钛矿的晶格中.

图2 La0.9Sr0.1MnO3和La0.9Sr0.1Mn0.97Pd0.03O3的SEM照片Fig.2 SEM photos of La0.9Sr0.1MnO3 and La0.9Sr0.1Mn0.97Pd0.03O3 catalysts
图2A,B分别是La0.9Sr0.1MnO3和La0.9Sr0.1Mn0.97Pd0.03O3催化剂放大×5000倍的扫描电镜照片,从图中可以看出未掺杂Pd催化剂颗粒堆积在一起呈现絮状,可能是由于分散不够均匀造成.而掺杂了Pd的La0.9Sr0.1Mn0.97Pd0.03O3催化剂明显的颗粒尺度变小,团聚程度较催化剂La0.9Sr0.1MnO3少,且颗粒分布较为均匀,分散度好,且形成的孔隙更为丰富,有利于增大催化剂的比表面积,促进与污染物的接触和吸附效果.
由测得的孔结构及比表面积数据知La0.9Sr0.1Mn0.97Pd0.03O3催化剂的比表面积为11.045m2/g,而未掺杂贵金属Pd的比表面积为8.718m2/g.说明掺杂Pd后增大了催化剂的比表面积,其中的孔可能为颗粒的堆积孔.
2.2 La0.9Sr0.1MnO3掺杂Pd前后催化活性比较
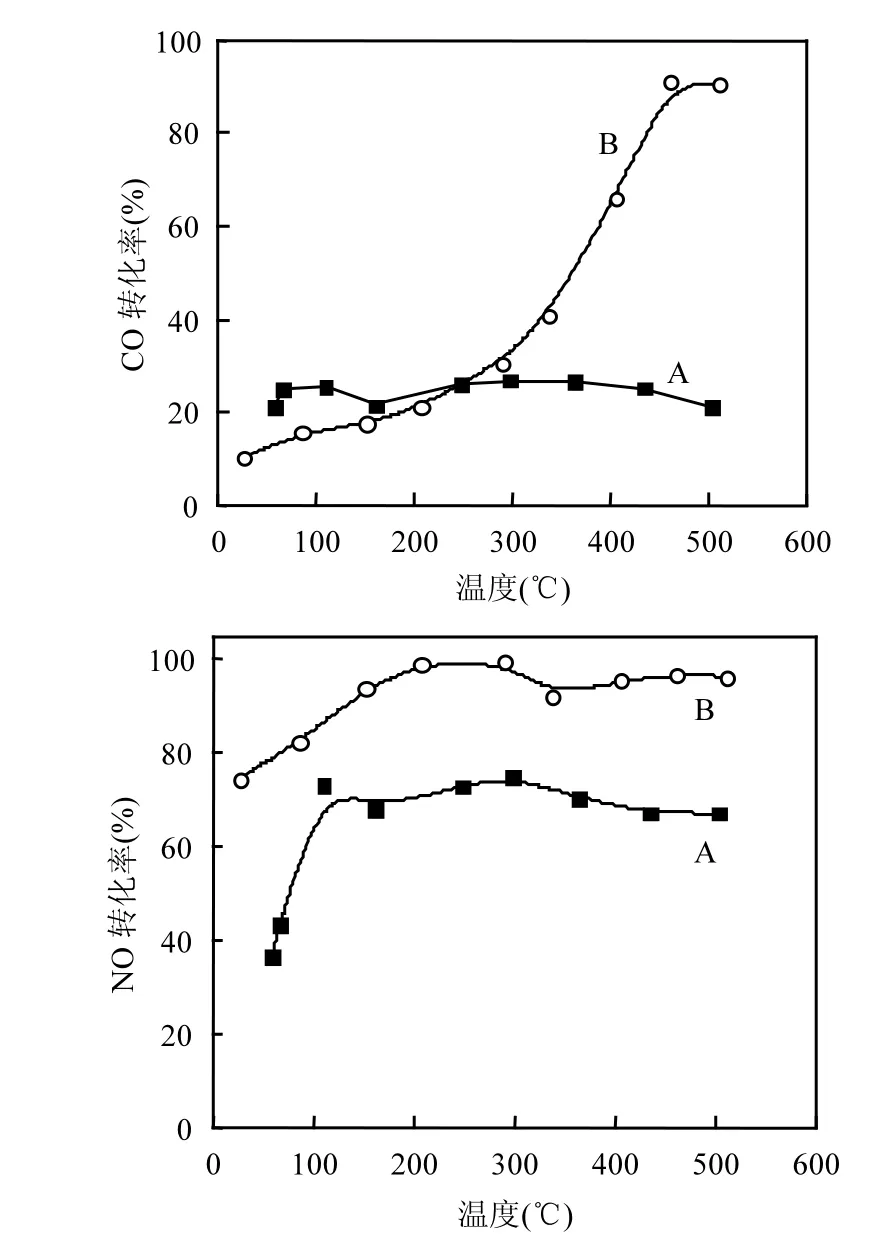
图3 催化剂掺杂前后CO和NO转化率对比Fig.3 Comparison of CO and NO conversion before and after Pd doping
图3表示的是催化剂La0.9Sr0.1MnO3(A)与催化剂La0.9Sr0.1Mn0.97Pd0.03O3(B)分别对CO和NO的转化率对比图,从图3中可以看出掺杂Pd后的催化剂B对CO和NO的去除效果明显都高于未掺杂的A,催化剂A对CO的平均转化率只达到23.69%,而掺杂后的B催化剂随着温度的升高CO转化率逐渐升高,在360℃时已达到50%.催化剂A对NO的平均转化率为63.81%,而掺杂后的催化剂B达到92.25%.因为掺杂Pd后,由于Pd2+价态低于Mn3+,为维持电荷平衡,必然导致大量氧空位产生或高价态的Mn4+离子出现,因而增加了氧空位[28]和氧的流动性有利于使NO氧化为NO2以硝酸盐的形式储存在SrO和SrCO3上,在适当的温度点NOx脱附与还原性气体CO发生反应进而也相应提高了CO转化率.综上贵金属Pd的掺杂有效提高了催化剂的活化性能.
2.3 SO2对La0.9Sr0.1Mn0.97Pd0.03O3去除效果的影响
图4给出了La0.9Sr0.1Mn0.97Pd0.03O3催化剂在较高浓度SO2条件下耐久性试验前后的XRD图谱.可以看出,在较高SO2浓度下长时间反应后催化剂中的钙钛矿衍射峰的强度有所减弱但钙钛矿结构基本保持不变,说明较高SO2浓度对样品中钙钛矿结构的影响不是很大,其结构仍然保持很好而且相对很稳定.并且反应后,谱图中未发现任何的硫酸盐衍射峰,说明样品经高浓度SO2条件下耐久实验后未形成较明显的硫酸盐颗粒.但是,不能排除可能在样品中形成少量高度分散在表面的硫酸盐物种.在XRD谱图中观察到了微弱的硝酸盐Sr(NO3)2衍射峰,也进一步说明该催化剂具有一定的抗硫或耐硫性能.此外,该催化剂经含有SO2混合气实验是在750℃的高温下进行,钙钛矿型结构保持良好,意味着该催化剂具有较强的耐热性能,可以在一定的程度上避免催化剂高温失活.
2.3.1 透射红外(FT-IR)表征 图5是La0.9Sr0.1Mn0.97Pd0.03O3催化剂在混合气实验前后的红外吸收光谱图,从图5可以看出,1620cm-1和3437cm-1分别为吸附水O-H的弯曲振动峰和伸缩振动峰.1468cm-1和848cm-1对应于碳酸盐的特征峰.1396cm-1处是自由硝酸根离子的振动峰,可能是由于吸附在碳酸盐表面的NOx形成硝酸盐,对应于碳酸锶向硝酸锶的转变,经混合气体实验后的样品碳酸盐的特征峰消失而相应出现自由硝酸根离子,也就是硝酸盐,说明该处NOx在催化剂表面的碳酸盐上进行了储存.1134cm-1是体相硫酸盐物种的特征峰,经含有SO2混合气体实验后的样品在该处出现了一个很弱的硫酸盐振动峰.在621cm-1和512cm-1处出现了明显的吸收峰,为钙钛矿结构的特征振动峰,且在混合气实验后钙钛矿结构也保持良好,说明SO2对催化剂结构影响较小,这也与前面的XRD未检测出硫酸盐特征峰的结果一致.
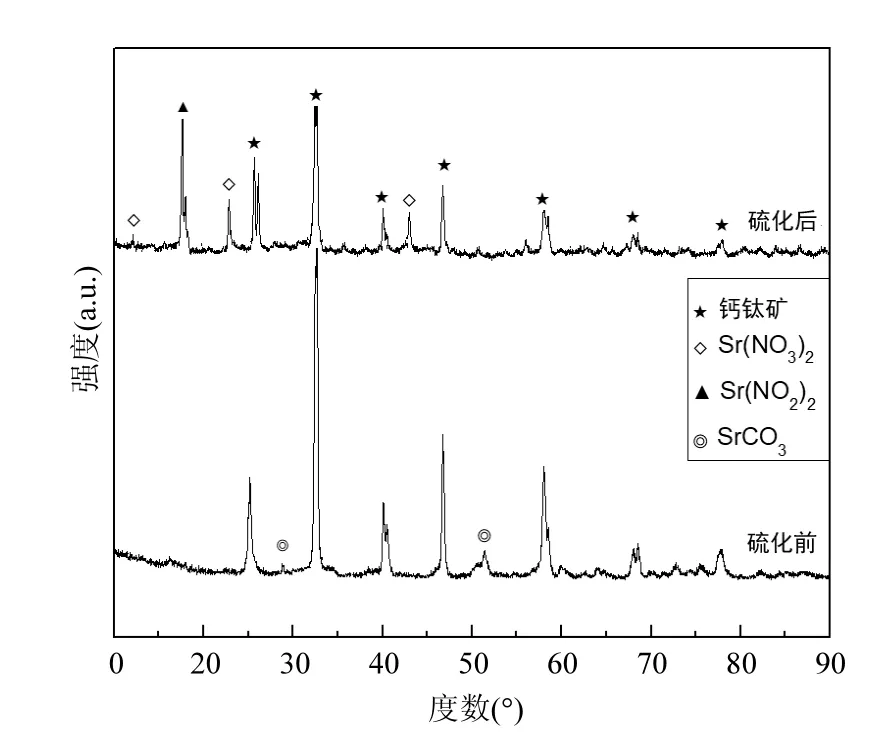
图4 催化剂耐硫实验前后的XRD图谱Fig.4 XRD pattern of the catalyst before and after sulfur test
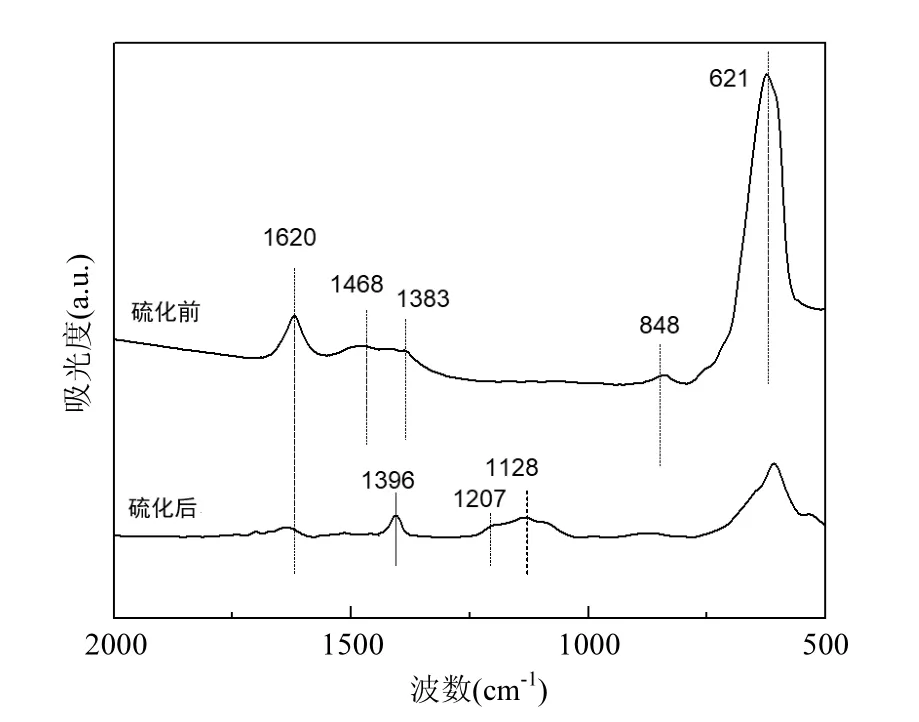
图5 催化剂耐硫实验前后的FT-IR图谱Fig.5 FTIR pattern of the catalyst before and after gas test
2.4 混合烟气实验
如图6所示,分别为不同SO2浓度对催化剂(La0.9Sr0.1Mn0.97Pd0.03O3)N2转化率和CO去除率的影响,从图中可以看出,在没有SO2存在时La0.9Sr0.1Mn0.97Pd0.03O3催化剂具有良好的催化活性,303℃时,CO的去除率已达到80%以上,N2的收率最高达到87%.当SO2浓度低于200ppm时,对催化剂的脱硝效率影响不大,当SO2浓度达到300ppm时催化剂的活性明显下降,303℃时CO的去除率只有27%,N2的收率最高也只有63%.并且碳烟的起燃温度为368℃比不含SO2时的353℃升高了15℃.说明,较高浓度的SO2使催化剂(La0.9Sr0.1Mn0.97Pd0.03O3)发生一定程度的钝化,这可能是因为SO2与NOx在催化剂表面存在竞争吸附,而由于硫酸盐结构中的(p-d)π键比硝酸盐中的离域大π键稳定性更好,因此硫酸盐比硝酸盐更加稳定,在含有SO2的气氛中使得一部分储存位被SO2占据形成SrSO4,造成催化剂硫中毒,导致催化剂对NOx的储存能力下降.
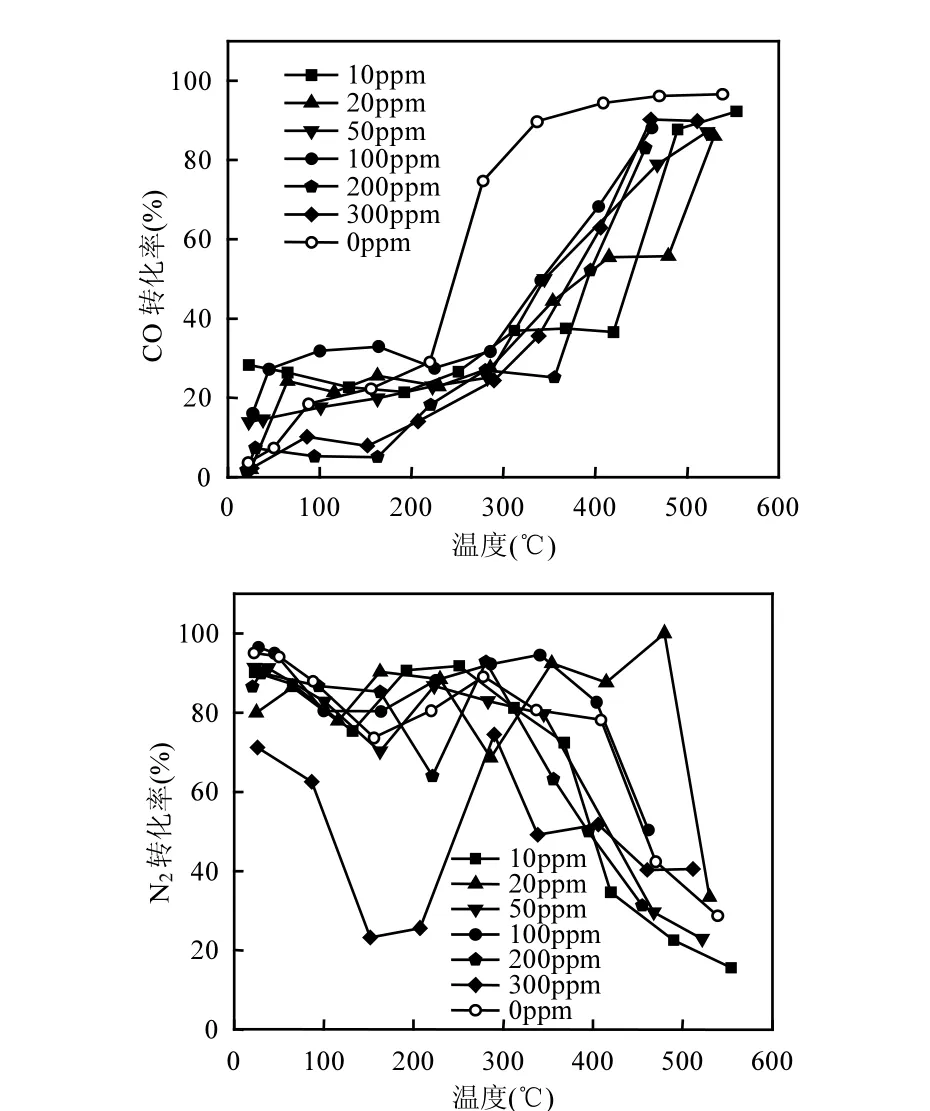
图6 不同SO2浓度对催化剂CO和N2转化率的影响Fig.6 Effect of different sulfur concentrations on the CO conversion and N2 yield of the catalyst
3 结论
3.1 掺杂Pd后的La0.9Sr0.1Mn0.97Pd0.03O3催化剂保持了良好的钙钛矿结构,衍射峰向小角度偏移,说明La0.9Sr0.1MnO3成功掺杂入贵金属Pd,使晶格膨胀变大.且催化剂比表面积增大能够使催化活性位点更充分的与污染气体接触,有利于催化效率的提高.
3.2 掺杂贵金属Pd后对CO和NO的转化率明显提高,掺杂Pd前对CO的平均转化率只达到23.69%,对NO的平均转化率为63.81%而掺杂后的催化剂随着温度的升高CO转化率逐渐升高,在360℃时已达到50%,对NO的平均转化率达到92.25%. La0.9Sr0.1Mn0.97Pd0.03O3催化剂混合气实验后碳酸盐峰消失,出现了硝酸盐峰说明催化剂对NOx进行了储存,而硫酸盐峰很弱说明制得的La0.9Sr0.1Mn0.97Pd0.03O3催化剂对SO2有一定的耐受性.
3.3 当浓度较高的SO2存在时会对La0.9Sr0.1Mn0.97Pd0.03O3的催化活性有明显的抑制作用,这可能是因为SO2与NOx在催化剂表面存在竞争吸附,而由于硫酸盐结构中的(p-d)π键比硝酸盐中的离域大π键稳定性更好,因此硫酸盐比硝酸盐更加稳定,从而使得催化剂对NOx的储存能力下降,且当硫浓度越高时NOx的储存能力越低,造成催化剂失活.
[1] 贺 泓,翁 端,资新运.柴油车尾气排放污染控制技术综述 [J].环境科学, 2007,28(6):1169-1176.
[2] 陆凯波,刘双喜,李振国,等.国Ⅳ柴油机颗粒物与颗粒态多环芳烃排放特征 [J]. 中国环境科学, 2016,36(2):376-381.
[3] 朱清霞.柴油机的尾气处理技术 [J]. 科技资讯, 2014,13(9):63-68.
[4] Zhao Zhen, Zhang Guizhen, Liu Jian, et al. Latest research progresses in catalysts for the purification of exhaust gases from diesel engines [J]. Chinese Journal of Catalysis, 2008,29(3):303-312.
[5] Isabella Nova, Lidia Castoldi, Luca Lietti, et al. NOx adsorption study over Pt-Ba/alumina catalysts: FT-IR and pulse experiments,Journal of Catalysis, 2004,222:377—388.
[6] 江 同.柴油/LPG双燃料发动机工作状态的控制及性能研究[D]. 浙江大学, 2004.
[7] Brisley, Robert James, Twigg, et al. Catalytic wall-flow filter: US,B01J 35/00 (20060101) 6753294 [P]. 2004:6-22.
[8] 环境保护部.关于征求国家环境保护标准《车用压燃式、气体燃料点燃式发动机与汽车排气污染物排放限值及测量方法(中国第六阶段)(征求意见稿)》意见的函[EB/OL]. http://www.mep.gov.cn/gkml/hbb/bgth/201610/t20161017_365634.ht m/2016-10-11.
[9] Cao Chunmei, Xing Lingli, Yang Yuexi, et al. The monolithic transition metal oxide crossed nanosheets used for diesel soot combustion under gravitational contact mode [J]. Applied Surface Science, 2017,406:245-253.
[10] Li Lei, Shen Xiangqian, Wang Pan, et al. Soot capture and combustion for perovskite La-Mn-O based catalysts coated on honeycomb ceramic in practical diesel exhaust [J]. Applied Surface Science, 2011,257:9519-9524.
[11] Zhang Xiaojing, Li Yong, Li Huaju, et al. Preparation of LaFe0.95Pd0.05O3perovskites and their catalytic performances in methane combustion [J]. Journal of Natural Gas Chemistry,2012,21:113-118.
[12] 孙志强,王 虹.La1-xSrxCo0.5Mn0.5O3催化剂同时去除柴油机碳颗粒和NOx的性能 [J]. 石油化工高等学校学报, 2007,20(1):35-38.
[13] Liu J, Zhao Z, Xu C M, et al. Simultaneous removal of NOxand diesel soot particulates over nanometric La2-xKxCuO4complex oxide catalysts [J]. Catalysis Today, 2007,119(1-4):267-272.
[14] Wang H, Zhao Z, Xu C M, et al., Nanometric La1-xKxMnO3perovskite-type oxides & highly active catalysts for the combustion of diesel soot particle under loose contact conditions[J]. Catalysis. Lett. 2005,102:251-256.
[15] Liu J, Zhao Z, Xu C M, et al., Study of the catalytic combustion of diesel soot over nanometric lanthanum-cobalt mixed oxide catalysts [J]. Reaction Kinetics and Catalysis Lett, 2005,87:107-114.
[16] Denton P, Giroir-Fendler A, Praliaud H, et al. Role of the nature of the support (alumina or silica), of the support porosity, and of the Pt dispersion in the selective reduction of NO by C3H6under lean-bum condition [J]. Journal of Catalysis, 2000,189(2):410-420.
[17] 俞守耕.柴油车尾气后处理技术的进展 [J]. 贵金属, 2003,24(1):62-66.
[18] 王林江,郭子峰,吴群英.柴油车尾气净化四效催化技术进展 [J].工业催化, 2009,17(5):3-6.
[19] Yang F, Kim S, Takamura Y, et al. Strain effect on the electrical conductivity of epitaxial La0.67Sr0.33MnO3thin films [J]. Scripta Materialia, 2011,65(1):29-32.
[20] Cimino S, Lisi L, Pirone R, et al. Methane combustion on perovskites-based structured catalysts [J]. Catalysis Today,2000,59(1/2):19-31.
[21] Armstrong E N, Striker T, Ramaswamy V, et al. NOxadsorption behavior of LaFeO3and LaMnO3and its influence on potentiometric sensor response [J]. Sensors and Actuators B,2011,158(1):159-170.
[22] Hirohisa Tanaka, Noritaka Mizuno, Makoto Misono, Catalytic activity and structural stability of La0.9Ce0.1Co1- xFexO3perovskite catalysts for automotive emissions control [J]. Applied Catalysis-A, 2003,244(2):371-382.
[23] Femina Patel, Sanjay Patel, La1-xSrxCoO3(x=0, 0.2) perovskites type catalyst for carbon monoxide emission control from autoexhaust [J]. Procedia Engineering, 2013,51:324-329.
[24] E. A. Parvaneh, K. Abbasali, Z. A. Hessam et al. Effects of excess manganese in lanthanum manganite perovskite on lowering oxidation light-off temperature for automotive exhaust gas pollutants [J]. Chemical Engineering Journal, 2011,169:282-289.
[25] Tanaka H, Takahashi I, Advances in designing perovskite catalysts [J]. J-SAE, 1993,47(10):51-58.
[26] Tanaka H, Fujikawa H, Takahashi I., Excellent oxygen storage capacity of perovskite-PD three-way catalysts [C]. SAE paper 950256, 1995.
[27] 姚文生,镧钴钙钛矿催化剂制备及去除氮氧化物和碳烟性能研究 [D]. 天津:天津大学化工学院, 2009.
[28] Zhang Zhaoshun, Mark Crocker, Chen Bingbing, Bai Zhifeng,Wang Xinkui, Shi Chuan, Pt-free, non-thermal plasma-assisted NOxstorage and reduction overM/Ba/Al2O3(M = Mn, Fe, Co, Ni,Cu) catalyst [J]. Catalysis Today, 2015,256:115—123.
