硫磷混酸浸出黑钨矿动力学
2018-03-01杨凯华张文娟何利华李永立郭福亮陈星宇李江涛刘旭恒赵中伟
杨凯华,张文娟,何利华,李永立,郭福亮,陈星宇,李江涛,刘旭恒,赵中伟
硫磷混酸浸出黑钨矿动力学
杨凯华,张文娟,何利华,李永立,郭福亮,陈星宇,李江涛,刘旭恒,赵中伟
(中南大学 冶金与环境学院,长沙 410083)
采用单因素实验法研究了硫磷混酸分解黑钨矿浸出过程中的动力学过程,考察搅拌速度、矿物粒度、反应温度、硫酸浓度和磷酸浓度对黑钨矿浸出速率的影响。结果表明:黑钨矿在该体系中的浸出过程可用Avrami方程描述,其模型特征参数为0.83,反应的表观活化能为67.54 kJ/mol,属化学反应控制,建立硫磷混酸浸出黑钨矿的反应动力学方程。
黑钨矿;硫酸;磷酸;Avrami方程;浸出动力学
当前工业上分解钨矿物原料的主要方法是NaOH分解法和苏打压煮法,这两种工艺都能稳定的分解钨矿,但需要在高温、高压及高碱用量的条件下处理钨矿。相比之下,传统的盐酸分解法热力学驱动力大,可在较低温度下分解白钨矿,具有流程短、成本低等特点。但由于过程中产生的胶状黄钨酸包裹在未反应的白钨矿颗粒表面,阻碍了传质过程,导致分解不完全,因此,不得不通过提高分解温度,增加盐酸用量,减小精矿粒度等措施来减弱钨酸膜的影响,促进反应的进行。但这些措施的增强在工业生产中都是有限度的,而且会加剧HCl的挥发和生产设备的腐蚀,恶化生产环境[1−3]。
为了消除固体钨酸的阻碍,有研究者采用机械活化、超声波等方式来破坏钨酸固膜的阻碍作用。如瑞典的可乐满公司通过采用机械活化的方法来破坏钨酸膜的阻碍作用,在较低的酸用量依靠盐酸与白钨矿的放热反应来维持分解温度,不需要外界补充热量的情况下,实现了白钨矿的高效分解,但该技术的应用最大障碍是要求热球磨反应器的内衬材料及球的材质在工作温度下应耐腐蚀耐磨[4]。彭少芳等[5]利用超声振动的去膜和活化作用,进而降低盐酸浓度和反应温度,改善浸出环境,但超声波设备的产业化仍需一段进程。另外有研究者通过控制溶液pH值生成可溶性的偏钨酸[6],或配合加入易与钨形成可溶性钨酸盐的络合剂(如磷酸[7]、草酸[8]和双氧水[9]),从而在本质上避免了固体膜的产生,但上述方法多在实验室分解人造白钨矿的研究阶段,对实际矿物的分解效果还未被验证。中南大学开发出硫酸−磷酸协同浸出白钨矿的新工艺,实现了白钨矿的高效常压浸出,并且采用的浸出剂对环境无污染可循环利用,浸出渣为石膏可用作建材[10−11]。事实上,该分解工艺的开发目前主要针对的是白钨矿。然而,我国钨资源储量中仍有相当部分为黑钨矿[12−13]。如我国储量较大的钨矿湖南柿竹园矿,其钨探明储量为74.7万t,黑、白钨的质量比为3:7[14]。再如福建行洛坑黑、白钨共生的超大型矿床,其保有钨储量在30万t左右,黑、白钨储量含量各占一半[15]。
12FeWO4+12H2SO4+H3PO4=12FeSO4+H3PW12O40+12H2O (1)
12MnWO4+12H2SO4+H3PO4=12MnSO4+H3PW12O40+12H2O (2)
对于黑钨矿在硫酸磷酸混酸体系中的反应(反应(1)和(2)),本文作者根据文献[16−18]提供的热力学数据对上述反应的标准吉布斯自由能变化进行了估算,25 ℃时反应式(1)和(2)的标准吉布斯自由能分别为−1450.48 kJ/mol和−1578.07 kJ/mol。可见,硫磷混酸分解黑钨矿的热力学驱动力非常大,但实际在低温下黑钨矿的分解效果往往不太理想,造成黑钨矿分解困难的原因应该是动力学因素。在此,本文作者对黑钨矿分解过程的动力学进行了研究,以期探明该过程的动力学因素对浸出的影响,为强化其过程提供依据。
1 实验
1.1 实验原料
实验所用黑钨精矿经干燥和磨细后筛分成不同的粒径。所用黑钨精矿的主要化学成分如表1所示,其XRD谱如图1所示。

表1 黑钨精矿的主要化学成分

图1 黑钨精矿的XRD谱
1.2 实验方法
每次实验量取300 mL一定浓度的硫酸−磷酸混合溶液加入到500 mL的三颈烧瓶中。将其置于恒温水浴锅中进行加热,开动电动搅拌装置,待溶液温度达到设定值并保持稳定后,将称量好的3 g黑钨矿原料加入到搅拌中的混酸溶液中并开始计时。定时用移液管从反应体系中取1 mL浸出液,迅速移入到容量瓶中稀释至50 mL,并向浸出体系中补充1 mL等浓度的硫酸−磷酸混酸溶液。采用ICP−AES分析溶液中钨的浓度,根据检测结果,可计算出不同时间黑钨矿的浸出率。由于实验在100:1的液固比下进行,浸出剂大大过量,可认为浸出过程浸出剂浓度基本不变。
2 实验结果与动力学模型建立
2.1 搅拌速度对钨浸出率的影响
选用粒径大小为32~38.5 μm的黑钨精矿,在硫酸浓度为2.5 mol/L、磷酸浓度为3.5 mol/L、温度为90 ℃的条件下考察了搅拌速度为400~600 r/min对黑钨矿浸出的影响,实验结果如图2所示。结果表明不同的搅拌速度对黑钨矿浸出的动力学曲线没有影响,亦即在该转速范围内反应不受外扩散控制,后续实验均在500 r/min的搅拌速度下进行。
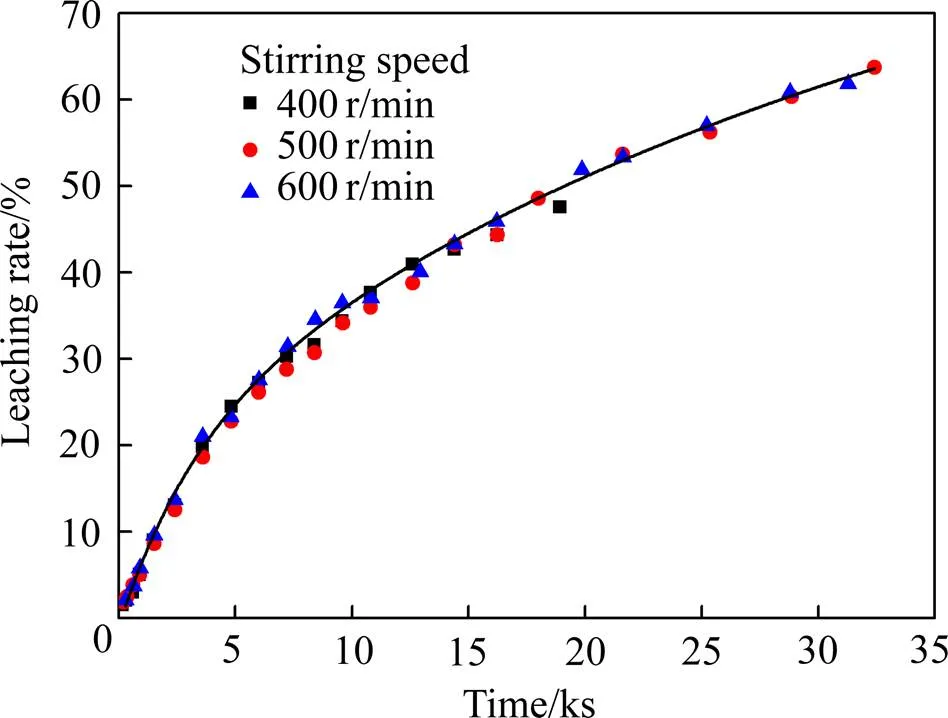
图2 搅拌速度对钨浸出率的影响
2.2 矿物粒度对钨浸出率的影响
在反应温度90 ℃,硫酸浓度2.5 mol/L,磷酸浓度3.5 mol/L的条件下,考察不同矿物粒度32~38.5 μm、38.5~43 μm、43~50 μm、50~61 μm、61~74 μm对浸出率的影响,其结果如图3所示。由图3可以看出,矿物粒度对浸出过程有一定的影响,矿物粒度越小,反应速率越快,相同反应时间内黑钨精矿的分解率越高。即粒径越小,比表面积大,反应速率越快。
黑钨矿在硫磷混酸体系下的浸出反应属于无固相产物层生成的液固多相反应,反应发生在液固两相的界面。对于多数液固化学反应,常用经典的收缩未反应核模型处理,硫磷混酸浸出黑钨矿的动力学过程分为以下3步:1) 反应剂硫酸、磷酸从主体溶液通过边界层液膜向黑钨矿表面的扩散;2) 硫酸、磷酸与黑钨矿的化学反应;3) 生成的磷钨杂多酸通过边界层液膜向主体溶液中扩散。浸出过程的浸出速度取决于上述3个环节中最慢的环节,即浸出反应的控制步骤。
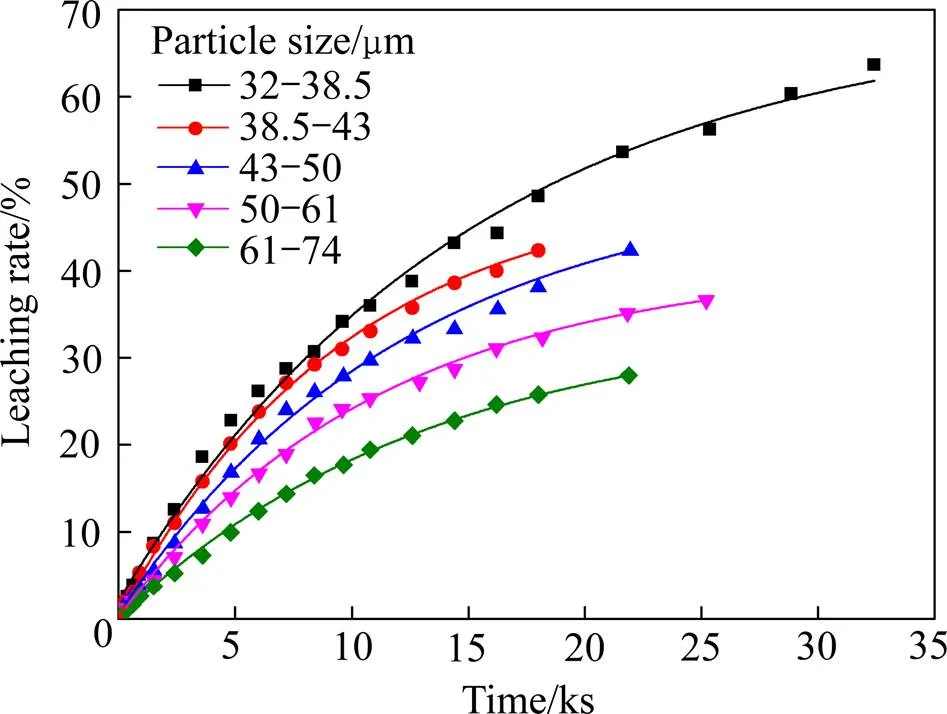
图3 黑钨矿粒度对钨浸出率的影响
当浸出过程为液膜扩散控制时,其动力学方程为

当浸出反应为界面化学反应控制时,其动力学方程为
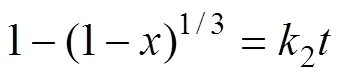
式中:为浸出率;为反应时间;1、2分别为反应表观速率常数。
根据图3中黑钨矿浸出的实验数据,按收缩未反应核模型动力学方程式(3)和(4)进行处理,处理后数据如图4和5所示,可以看出,利用收缩未反应核模型处理该实验数据,不管是利用收缩未反应核模型的化学反应控制模型还是扩散控制模型,处理后的实验数据均不具备线性相关性。
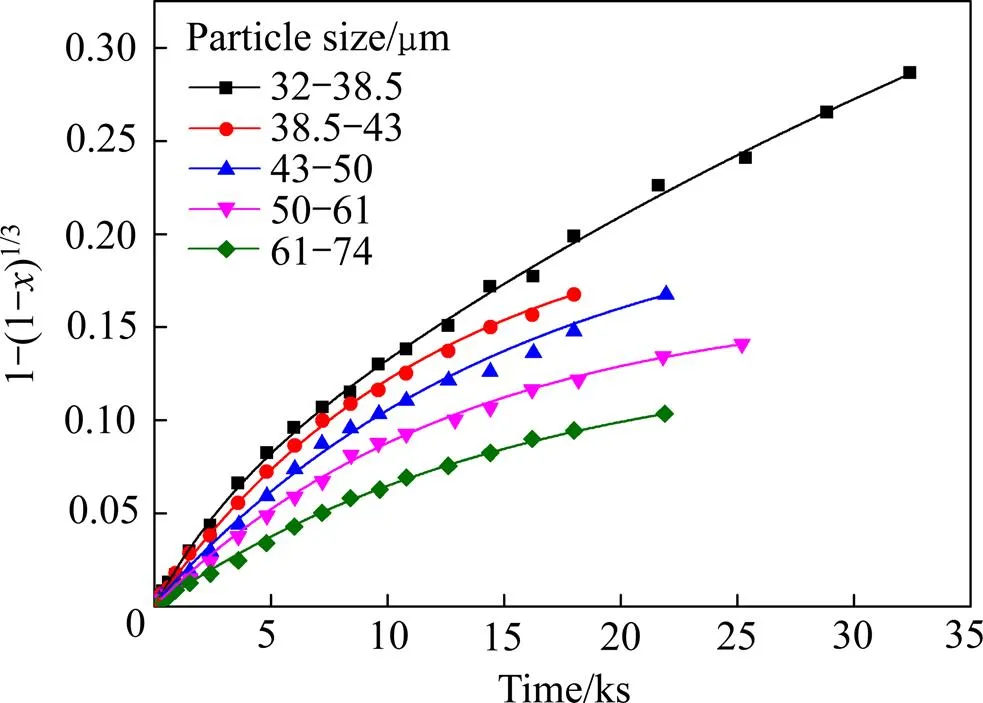
图4 不同粒径黑钨矿浸出过程中的1−(1−x)1/3−t关系图
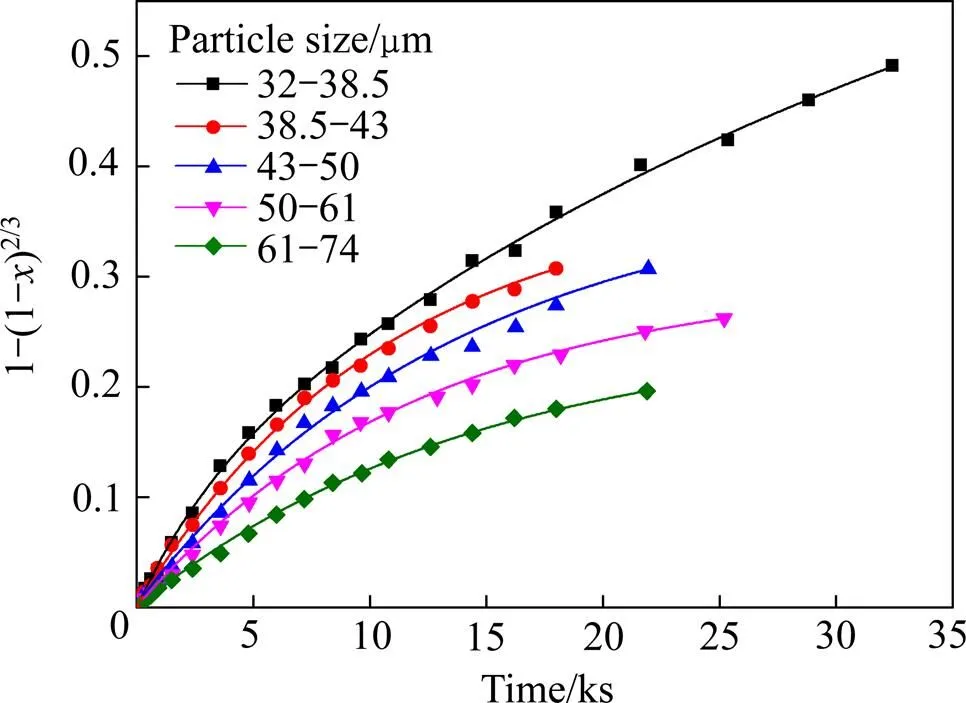
图5 不同粒径黑钨矿浸出过程中的1−(1−x)2/3−t关系图
图6所示为黑钨矿以及浸出率约60%的黑钨矿浸出渣的SEM像。从图6中可以看出,黑钨矿的形貌是一种板状结构,比较图6(a)和(b)可以看出,黑钨矿浸出渣相比于原矿来说有一定的体积缩小,但单颗粒的放大图显示黑钨矿浸出渣呈现千疮百孔的形貌,并不似收缩未反应核模型所述的层层推进的缩核反应过程。因此,需要寻求另外的模型来描述该动力学过程。

图6 黑钨矿原矿和浸出渣的SEM像
Avrami方程最早多用于结晶与固相转变动力学方程,之后被应用于描述多种矿物的浸出反应动力学过程[19−24],其动力学方程如下:
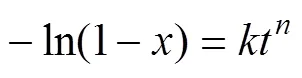
式中:为表观反应速率常数;为浸出率;为反应时间;为反应特征参数。
KABAI[25]运用Avrami方程研究了50余种金属以及金属氧化物在酸性溶液中的反应动力学过程,取决于反应温度,浸出剂浓度等因素。其中反应特征参数可以反映浸出过程的反应机理,只与固体晶粒的性质和几何形状相关,不会随反应条件发生变化,并且总结出当<1时,初始反应速率极大,随反应进行反应速率不断降低;当=1时,初始反应速率有限;当>1时,初始反应速率接近0。
对式(5)两边取对数得到式(6):

将图3实验数据代入式(6),得到− 图,结果如图7所示。由图7可见,−具有很好的线性相关性。
表观反应速率常数是溶液浓度、矿物粒度、搅拌速度和温度等的函数,结合阿仑尼乌斯变方程可用式(7)表示[14, 20]:
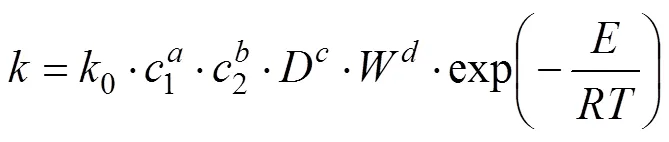
式中:0为频率因子;1为硫酸浓度,mol/L;2为磷酸浓度,mol/L;为粒径,mm;为搅拌速度,r/min;为活化能,J/mol;为热力学温度,K;为普适气体常数(8.314 J/(K∙mol));为硫酸浓度反应级数;为磷酸浓度反应级数;为粒径影响指数;为搅拌速度影响指数。
对式(7)两边取对数,得到
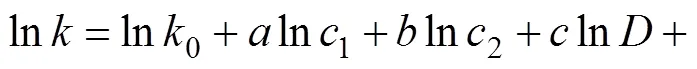
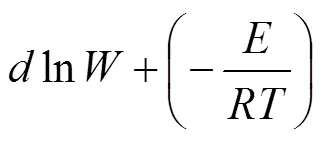

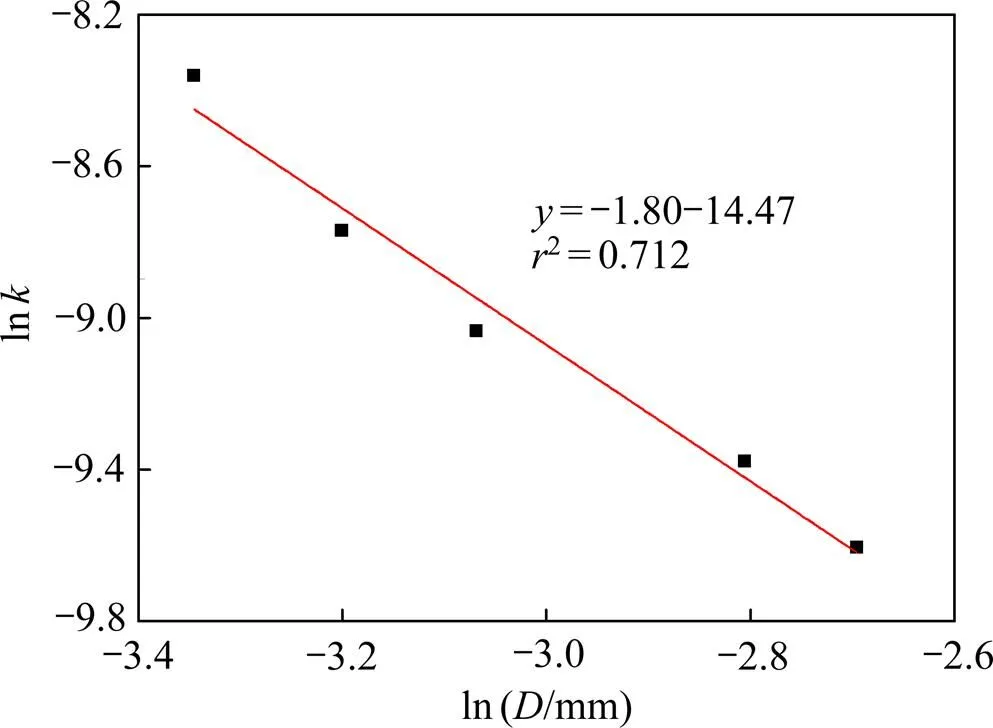
图8 黑钨矿浸出过程中−关系图
2.3 温度对钨浸出率的影响
选用粒径大小为38.5~43 μm的黑钨精矿,在硫酸浓度2.5 mol/L,磷酸浓度3.5 mol/L,搅拌速度500 r/min实验条件下,研究了70~100 ℃温度范围内反应温度对黑钨矿浸出动力学曲线的影响,实验结果如图9所示。由图9可以看出,反应温度对黑钨矿浸出率影响显著,在低温和高温条件下,相同时间钨的浸出率差别很大,在373 K温度下反应5 h黑钨矿的浸出率可以达到60.83%,而当温度降至343 K时,反应 5 h,浸出率仅有15.09%。温度对浸出率的影响说明黑钨矿在硫磷混酸体系中的浸出反应可能受化学反应控制。根据式(6)拟合的数据如图10所示,拟合数据具有很好的线性相关性。

图9 温度对钨浸出率的影响

图10 不同温度下黑钨矿浸出过程中−关系图

图11 黑钨矿浸出过程中−T−1关系图
2.4 硫酸浓度对钨浸出率的影响
在反应温度90 ℃,粒径大小为38.5~43 μm,磷酸浓度3.5 mol/L,搅拌速度500 r/min实验条件下,研究了0.5~3.0 mol/L范围内硫酸浓度对黑钨矿浸出率的影响,实验结果如图12所示。由图12可以看出,随着硫酸浓度的增加,黑钨矿的浸出速率有一定增加,但其影响并不显著,在硫酸浓度为0.5 mol/L时分解反应3 h,浸出率为32.02%,而当硫酸浓度提高至3 mol/L时,浸出率达到44.70%。根据式(6)拟合的数据如图13所示,可以看出:拟合数据依然具有很好的线性相关性。
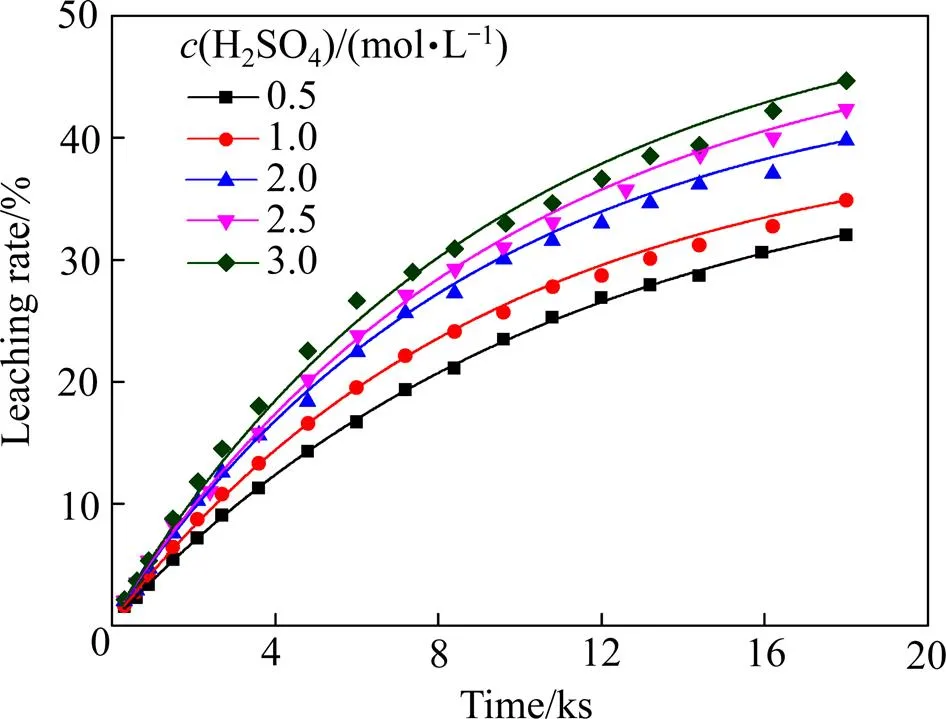
图12 硫酸浓度对钨浸出率的影响
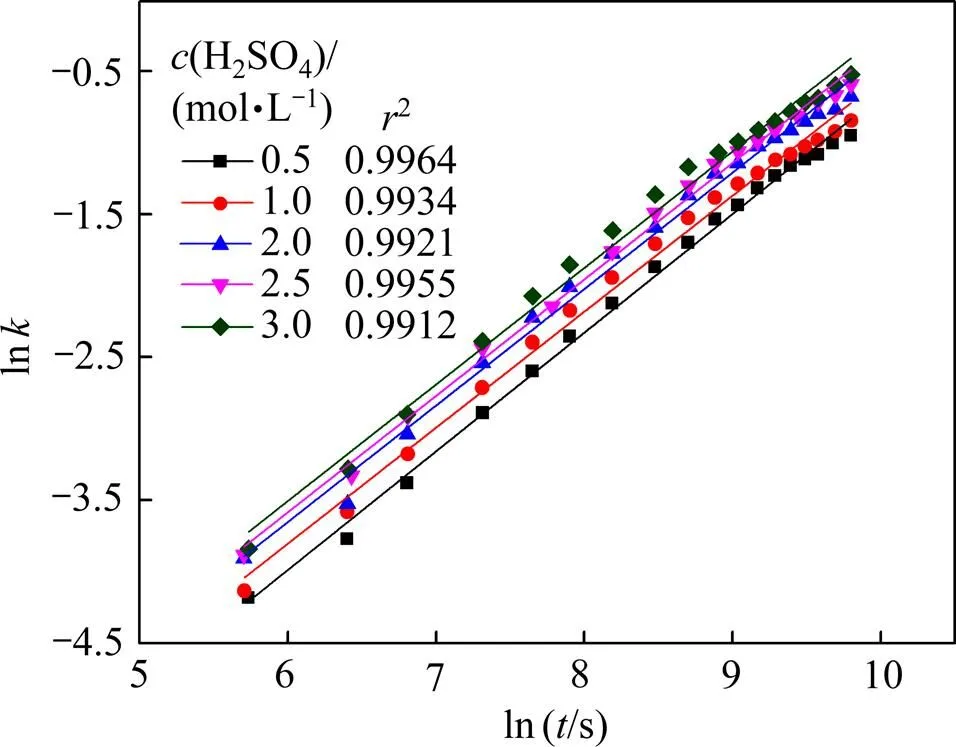
图13 不同硫酸浓度下黑钨矿浸出过程中− 关系图

图14 黑钨矿浸出过程中−关系图
2.5 磷酸浓度对钨浸出率的影响
在反应温度90 ℃、粒径为38.5~43 μm、硫酸浓度3.5 mol/L、搅拌速度500 r/min实验条件下,研究了1.0~3.5 mol/L范围内磷酸浓度对黑钨矿浸出率的影响,实验结果如图15所示。由图15可以看出,随着磷酸浓度的增加,黑钨矿的浸出速率增加,但相同时间内浸出率的提高并不显著。根据式(6)拟合的数据如图16所示,可以看出,拟合数据仍具有很好的线性相关性。
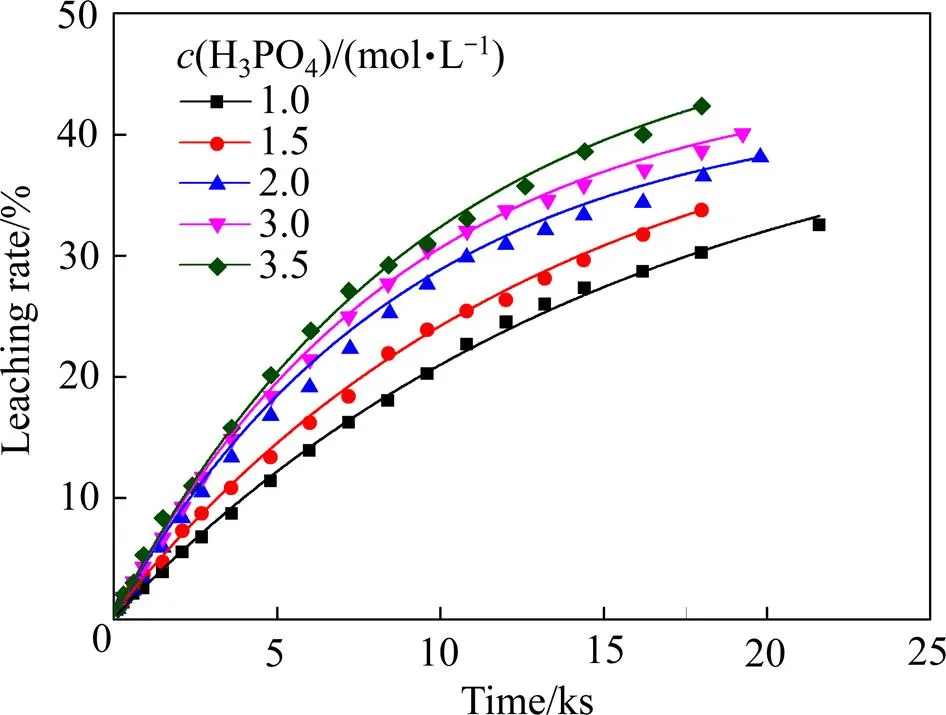
图15 磷酸浓度对钨浸出率的影响

图16 不同磷酸浓度下黑钨矿浸出过程中− 关系图
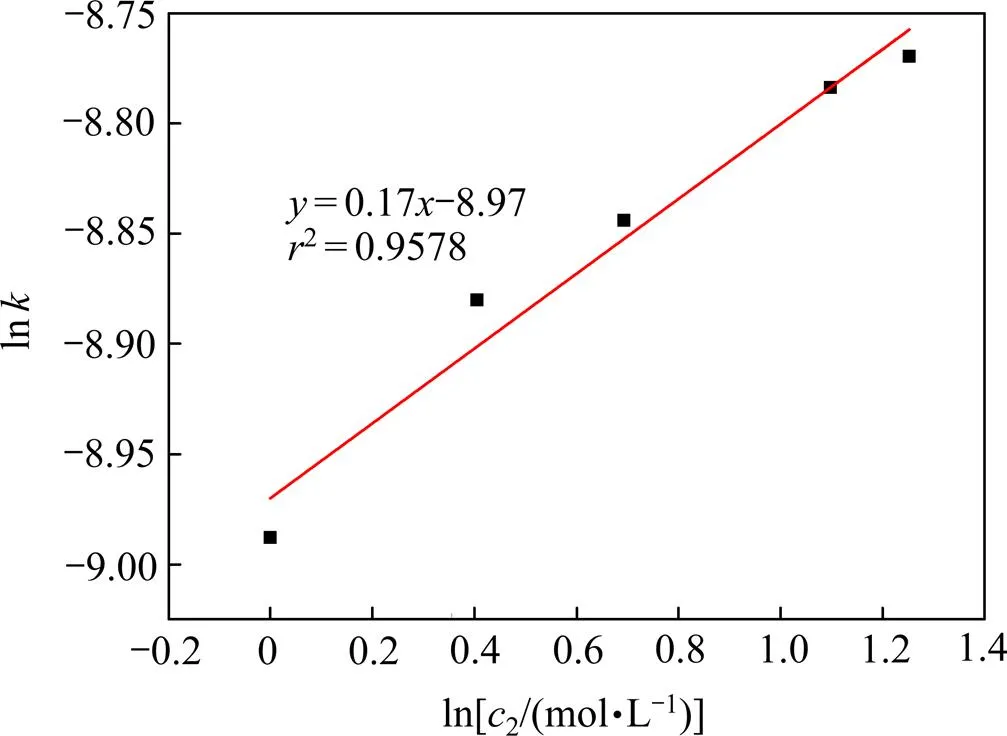
图17 黑钨矿浸出过程中−曲线
2.6 动力学方程的确立

图18与的关系图
至此,可得到黑钨矿在硫磷混酸体系中的浸出的动力学方程如下:
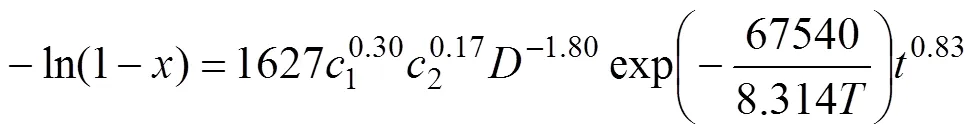
3 结论
1) 研究硫磷混酸体系浸出黑钨矿的动力学过程,浸出渣呈现千疮百孔的形貌,反应并非层层推进的缩核反应过程,不符合收缩未反应核动力学模型,结果表明其浸出过程可用Avrami方程描述。
2) 通过Avrami方程求得该浸出过程的反应特征参数为0.83,反应表观活化能为67.54 kJ/mol,属于化学反应控制,温度对黑钨矿的浸出过程影响显著。矿物粒径影响指数为−1.80,粒径对浸出过程有较大影响。硫酸浓度反应级数为0.30,磷酸浓度反应级数为0.17,硫酸浓度和磷酸浓度对黑钨矿在该体系下的浸出影响较小。所建立的动力学方程为
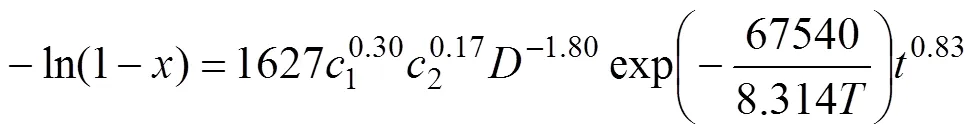
[1] 李洪桂, 羊建高, 李 昆. 钨冶金学[M]. 长沙: 中南大学出版社, 2010: 53−112. LI Hong-gui, YANG Jian-gao, LI Kun. Tungsten metallurgy[M]. Changsha: Central South University Press, 2010: 53−112.
[2] 莫似浩. 钨冶炼的原理与工艺[M]. 北京: 轻工业出版社, 1984: 43−82. MO Si-hao. The principle and technology of tungsten metallurgy[M]. Beijing: Light Industry Press, 1984: 43−82.
[3] 赵中伟. 钨冶炼的理论与应用[M]. 北京: 清华大学出版社, 2013: 21−28. ZHAO Zhong-wei. Tungsten metallurgy: Fundamentals and applications[M]. Beijing: Tsinghua University Press, 2013: 21−28.
[4] 张启修, 赵秦生. 钨钼冶金[M]. 北京: 冶金工业出版社, 2007: 104. ZHANG Qi-xiu, ZHAO Qin-sheng. Metallurgy of molybdenum and tungsten[M]. Beijing: Metallurgical Industry Press, 2007: 104.
[5] 彭少方, 向 兰, 张 昭. 超声振动下盐酸浸出白钨矿的研究[J]. 中国钨业, 1989(2): 7−13.PENG Shao-fang, XIANG Lan, ZHANG Zhao. Study of scheelite leaching with HCl assisted by ultrasonic wave[J]. China Tungsten Industry, 1989(2): 7−13.
[6] MARTINS J I. Leaching of synthetic scheelite by nitric acid without the formation of tungstic acid[J]. Industrial & Engineering Chemistry Research, 2003, 42(21): 5031−5036.
[7] KAHRUMAN C, YUSUFOGLU I. Leaching kinetics of synthetic CaWO4 in HCl solutions containing H3PO4as chelating agent[J]. Hydrometallurgy, 2006, 81(3/4): 182−189.
[8] KALPAKLI A O, ILHAN S, KAHRUMAN C, YUSUFOGLU I. Dissolution behavior of calcium tungstate in oxalic acid solutions[J]. Hydrometallurgy, 2012, 121/124: 7−15.
[9] 王小波, 李江涛, 张文娟, 何贵香, 何利华. 双氧水协同盐酸分解人造白钨[J]. 中国有色金属学报, 2014, 24(12): 3142−3146. WANG Xiao-bo, LI Jiang-tao, ZHANG Wen-juan, HE Gui-xiang, HE Li-hua. Decomposition of synthetic scheelite in HCl solution with hydrogen peroxide as complexing agent[J].The Chinese Journal of Nonferrous Metals, 2014, 24(12): 3142−3146.
[10] ZHAO Zhong-wei, LI Jiang-tao. Method for extracting tungsten from scheelite. 2014, U.S. Patent 8771617[P]. 2014−07−08.
[11] LI Jiang-tao, ZHAO Zhong-wei. Kinetics of scheelite concentrate digestion with sulfuric acid in the presence of phosphoric acid[J]. Hydrometallurgy, 2016, 163: 55−60.
[12] 王明燕, 贾木欣, 肖仪武, 孙传尧, 李艳峰, 金健文. 中国钨矿资源现状及可持续发展对策[J]. 有色金属工程, 2014, 4(2): 76−80. WANG Ming-yan, JIA Mu-xin, XIAO Yi-wu, SUN Chuan-yao, LI Yan-feng, JIN Jian-wen. The Current situation and sustainable development countermeasures for China's tungsten resources[J]. Nonferrous Metallurgical Engineering, 2014, 4(2): 76−80.
[13] 刘良先. 中国钨矿资源及开采现状——国际钨业协会第25届年会报告[J]. 中国钨业, 2012, 27(5): 4−8. LI Liang-xian. China’s tungsten resources and mining status—Report of the 25th annual conference of the international tungsten industry association[J].China Tungsten Industry, 2012, 27(5): 4−8.
[14] 曹登国, 石志中, 李晓东, 崔小凯, 王文明. 黑白钨强磁分选在柿竹园钨浮选回收中的应用[J]. 中国钨业, 2014, 29(3): 17−20. CAO Guo-deng, SHI Zhi-zhong, LI Xiao-dong, CUI Xiao-kai, WANG Wen-ming. Application of wolframite and scheelite magnetic separation in Shizhuyuan[J]. China Tungsten Industry, 2014, 29(3): 17−20.
[15] 贾木欣, 王明燕, 李艳峰, 孙传尧. 我国钨资源矿石性质特点及资源利用存在的问题[J]. 矿冶, 2013, 22(1): 90−94. JIA Mu-xin, WANG Ming-yan, LI Yan-feng, SUN Chuan-yao. Characteristics of Chinese tungsten ore and the problems in the tungsten resource utilization[J]. Ming & Metallurgy, 2013, 22(1): 90−94.
[16] 郎中玲, 关 威, 颜力凯,苏忠民.-Keggin型[PW12O40]3−形成机理的热力学研究[EB/OL]. 北京: 中国科技论文在线. [2011−09−02]. http://www.paper.edu.cn/html/releasepaper/2011/ 09/42/.LANG Zhong-ling, GUANG Wei, YAN Li-kai, SU Zhong-min. Theoretical study on formation thermodynamic of-Keggin-type [PW12O40]3−anion. [EB/OL]. Beijing: Sciencepaper Online. [2011−09−02]. http://www.paper.edu.cn/html/releasepaper/ 2011/09/42/.
[17] JAMES G. Lange’s handbook of chemistry[M]. New York: McGraw-Hill Press, 2005: 1350, 1355.
[18] 伊赫桑·巴伦. 纯物质热化学手册[M]. 程乃良, 牛四通, 徐桂英, 译. 北京: 科学出版社, 2003. BARIN I. Thermochemical data of pure substances[M]. CHENG Nai-liang, NIU Si-tong, XU Gui-ying, transl. Beijing: Science Press, 2003.
[19] AVRAMI M. Kinetics of phase change. I General theory[J]. Journal of Chemical Physics, 1939, 7(12): 1103−1112.
[20] NIZAMETTIN D, ASIM K. Dissolution kinetics of ulexite in perchloric acid solutions[J]. International Journal of Mineral Processing, 2007, 83: 76−80.
[21] OKUR H, TEKIN T, KADIR OZER A, BAYRAMOGLU M. Effect of ultrasound on the dissolution of colemanite in H2SO4[J]. Hydrometallurgy, 2002, 67: 79−86.
[22] HE Gui-xiang, ZHAO Zhong-wei, WANG Xiao-bo, LI Jiang-tao, CHEN Xingyu, HE Li-hua, LIU Xu-heng. Leaching kinetics of scheelite in hydrochloric acid solution containing hydrogen peroxide as complexing agent[J]. Hydrometallurgy, 2014. 144/145: 140−147.
[23] ZHENG Ya-jie, CHEN Kun-kun. Leaching kinetics of selenium from selenium-tellurium-rich materials in sodium sulfite solutions[J].Transactions of Nonferrous Metals Society of China, 2016, 24(2): 536−543.
[24] 畅永锋, 秀 静, 符 岩, 李斌川, 张廷安. 还原焙烧红土矿的硫酸浸出动力学[J]. 分子科学学报, 2008, 24(4): 241−245. CHANG Yong-feng, ZHAI Xiu-jing, FU Yan, LI Bin-chuan, ZHANG Ting-an. Sulphuric acid leaching kinetics of pre-reduced laterite ores[J]. Journal of Molecular Science, 2008, 24(4): 241−245.
[25] KABAI J. Determination of specific activation energies of metal oxides and metal oxides hydrates by measurement of the rate of dissolution[J]. Acta Chim Acad Scientiarium Hungaricae, 1973, 78: 57−73.
[26] 李洪桂. 冶金原理[M]. 北京: 科学出版社, 2005: 291−311. LI Hong-gui. Metallurgical principle[M]. Beijing: Science Press, 2005: 291−311.
Leaching kinetics of wolframite with sulfuric-phosphoric acid
YANG Kai-hua, ZHANG Wen-juan, HE Li-hua, LI Yong-li, GUO Fu-liang, CHEN Xing-yu, LI Jiang-tao, LIU Xu-heng, ZHAO Zhong-wei
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
The leaching kinetics of wolframite with sulfuric-phosphoric acid were studied by single factor method. The effects of process parameters, such as stirring speed, particle size, temperature, as well as the concentrations of sulfuric acid and phosphoric acid were investigated in order to simulate the kinetics of wolframite dissolution. The results show that the leaching process can be described by Avrami model, with the chemical reaction as the controlling step, the model parameter is determined to be 0.83, the apparent activation energy is calculated as 67.54 kJ/mol, and the kinetics equation for wolframite leaching with sulfuric-phosphoric acid is established.
wolframite; sulfuric acid; phosphoric acid; Avrami equation; leaching kinetics
(编辑 李艳红)
Project (51334008) supported by the National Natural Science Foundation of China
2016-11-29;
2017-04-24
ZHAO Zhong-wei; Tel: +86-731-88830476; E-mail: zhaozw@csu.edu.cn
国家自然科学基金重点项目(51334008)
2016-11-29;
2017-04-24
赵中伟,教授,博士;电话:0731-88830476;E-mail: zhaozw@csu.edu.cn
10.19476/j.ysxb.1004.0609.2018.01.21
1004-0609(2018)-01-0175-08
TF111.31
A
