CaO与K2HPO4·3H2O协同作用下纤维素的热解研究
2018-02-20林郁郁汪沪军顾明言朱良涛
林郁郁,汪沪军,李 尚,顾明言,朱良涛
(1.安徽工业大学能源与环境学院,安徽马鞍山243002;2.上海理工大学能源与动力工程学院,上海200093)
热解是从煤、生物质等固体燃料中直接获得液体燃料和化工产品的一个重要途径[1-3]。生物质催化热解可在催化剂作用下将生物质选择性热解转变为高附加值化学品或高品质生物油,是一种极具竞争力的生物质转化方法[4-5]。磷酸和磷酸盐作为催化剂,被广泛运用于生物质催化热解过程中[6-7],如Wang等[8]研究发现活性氧化铝负载KH2PO4可催化玉米秸秆生成烷基苯酚;Zhang等[9-10]发现,K3PO4、K2HPO4、KH2PO4均可促进杨木热解中酚类产物的生成,K2HPO4、KH2PO4加入后小分子酸产率增大。
CaO同样作为催化剂在生物质催化热解领域得到了广泛研究[11-12],研究者们发现[13-16]:生物质-CaO共热解后生物油氧含量下降,热值增加,热解油中酸类、呋喃类、愈创木酚等高含氧量酚类相对下降;1-羟基-2-丙酮、苯酚等升高。杨林等[17-18]在催化微拟球藻热解研究中发现,水合CaO催化热解得到的生物油有机相由无催化时的富含N-棕榈酸等成分转变为富含C12~C17直链烷烃。现有文献研究表明,在生物质催化热解过程中,CaO可降低酸类物质产率,K2HPO4在提高酚类产物的同时可增加酸类产量,但目前较少学者研究磷酸盐和CaO共同作用下生物质的热解产品生成行为。为此,笔者利用热重-质谱联用(TG-MS)技术,探究CaO与K2HPO4共同作用下纤维素热解过程中的小分子生成行为,为CaO与磷酸盐协同催化生物质热解研究提供基础。
1 实验
1.1 实验原料
为国药集团化学试剂有限公司(SCRC)提供的CaO、K2HPO4·3H2O、微晶纤维素,实验前将纤维素样品在N2气氛下80℃干燥至恒重,各样品配置见表1。实验过程中保证每组样品纤维素的质量一致。

表1 实验样品Tab.1 Experimental samples
1.2 实验方法
实验用TG-MS系统为Netzsch STA 449C型热重分析仪(TGA)和Netzsch QMS 403型质谱仪(MS)。TGA和MS之间的连接管路采用梯度升温,即沿TGA炉膛出口到MS仪器入口分别加热至220,240,260℃,以防止气相产物冷凝。样品均置于热重分析仪的三氧化二铝坩埚内,且通入纯度为99.999%(体积分数)的高纯氩气置换体系内的空气,重复置换3次,待质谱仪信号稳定,开始程序升温,同时开始进行在线记录。氩气流量50 mL/min,温度设置为在50℃停留30 min稳定,然后以20℃/min的升温速率升高至900℃。对实验结果均进行归一化修正处理。
2 实验结果与讨论
2.1 热解TG/DTG曲线分析
图1为实验样品的热失重(TG)和热失重速率(DTG)曲线。由图1可知,纤维素单独热解过程大致分为3个阶段:第一阶段为室温到293℃,是纤维素中水分的析出阶段,由于所用纤维素经干燥预处理,故该阶段TG曲线相对平缓,没有明显的质量变化;第二阶段为293~411℃[19],是纤维素热解的主要失重阶段,此阶段挥发分大量析出,TG曲线陡然下降,DTG曲线呈现出一个单一且尖锐的失重峰,并在357℃左右出现峰值,说明纤维素热解挥发分生成过程的能垒较为集中,且集中在较窄的温度范围区间;第三阶段为411~900℃,这一阶段残余产物缓慢分解、缩聚炭化带来微量失重,TG曲线平缓变化,失重速率近似为0[20]。

图1 样品热解热失重和热失重速率曲线Fig.1 Thermal gravimetric and derivative thermogravimetric curves of the samples
由图1还可知:纤维素中加入CaO,即样品2热解过程中在560~721℃区间出现二次失重,这是因为纤维素热解过程会产生“类CO2活性中间体”等酸类产物及其前驱物等,而CaO与之反应生成羧酸钙盐或有机钙盐,并分解生成无定型CaCO3,无定型CaCO3继续在560~721℃区间分解释放出CO2[11-12];纤维素中加入K2HPO4·3H2O,即样品3的TG曲线起始值并不在100%,有一定的降低,这是仪器初始保温过程中K2HPO4·3H2O干燥失水所致,另外样品3的热解过程明显提前,纤维素的热解反应过程明显改变;纤维素中混合加入CaO与K2HPO4·3H2O,即样品4的热解起始值并未降低,这是因为CaO在混合过程中吸收K2HPO4·3H2O中的水生成Ca(OH)2。比较图1可知,相对于纤维素中单独添加K2HPO4·3H2O,热解起始的失重过程较为缓和,同时热解最终失重率低于单独添加催化剂过程,这是因为CaO和K2HPO4·3H2O部分反应生成Ca(OH)2和磷酸氢钙等物质,改变了催化剂的反应性;另外,此两种物质和其反应产物会协同耦合影响纤维素的热解过程,改变热解反应的最终产物分布。
2.2 热解过程析出气体的质谱分析
离子流强度可定性说明气体组分含量变化,M/Z表示H2、CH4等气体的核质比。图2为样品热解过程中H2、CH4等气体的质谱离子流强度曲线。
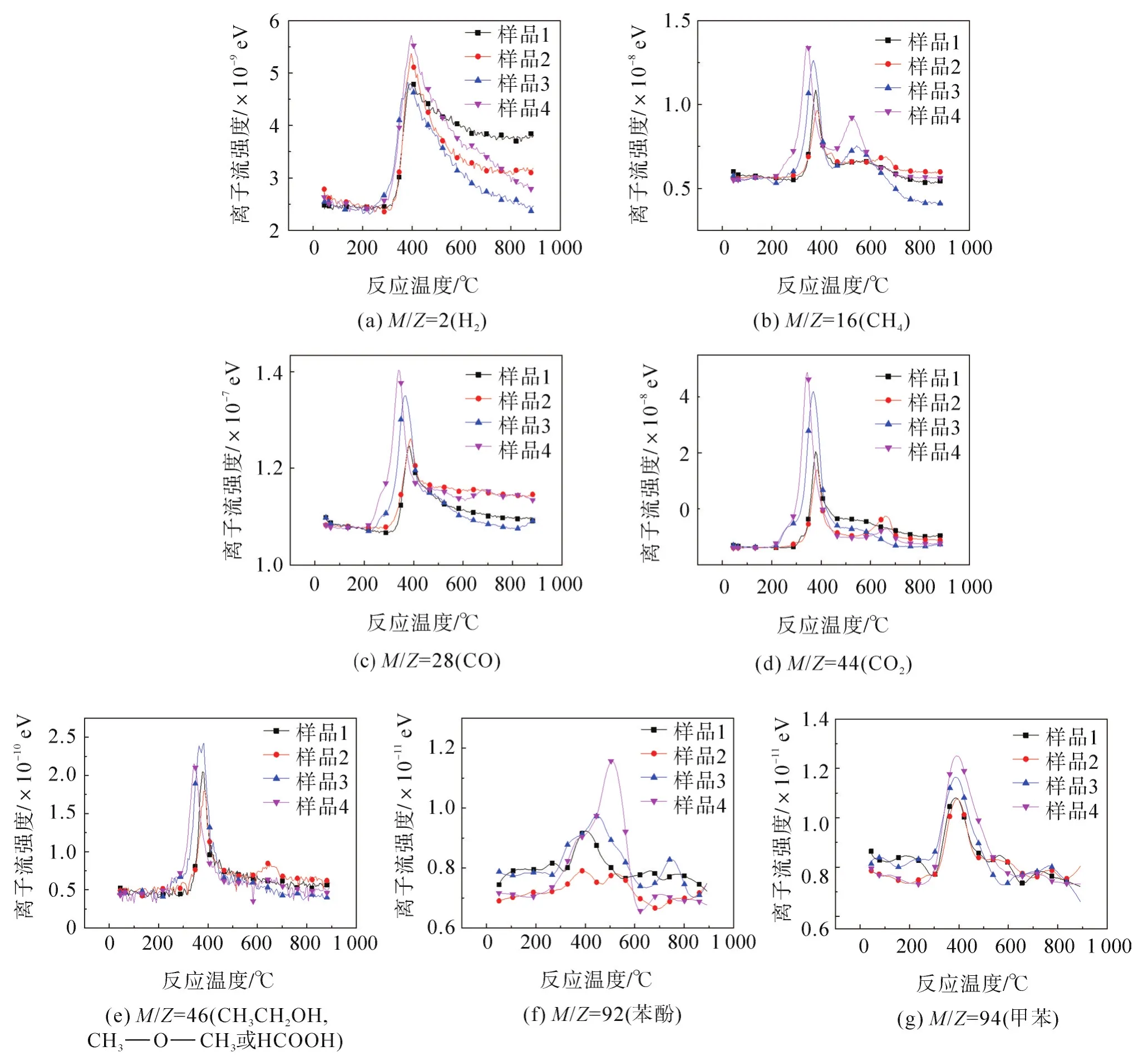
图2 热解过程中不同小分子产物离子流强度曲线Fig.2 Ion intensity curves of different small molecular products during pyrolysis
由图2(a)可看出:纯纤维素的H2析出起始温度为293℃左右,峰值温度为402℃,加入CaO后,H2析出起始温度稍提前,主要热解温度区间200~410℃内H2析出量增大。这是因为CaO可催化促进C H键断裂从而加强热解过程中的析氢反应,或通过降低主要热解阶段CO2的产率促使主要热解阶段水煤气转换反应向H2生成反应方向进行(如式(1));加入K2HPO4·3H2O后,H2析出起始温度提前,析出量降低,析出温度提前是因为热解过程的部分产氢路径发生改变所致;K2HPO4·3H2O与CaO混合加入后,H2析出总量增加,CaO与K2HPO4·3H2O相互反应可固定水分,并使主反应区的水分析出增多,增加主反应区氢自由基的浓度,同时2种催化剂及相互反应生成的化合物产生协同作用,可降低主反应区CH键断裂活化能或促使部分反应向析氢的方向进行,从而降低催化剂单独加入后的析氢难度或改变其析氢途径。

由图2(b)可看出:纯纤维素的CH4析出主要区间起始温度为293℃左右,峰值温度为378℃,纤维素热解过程中加入CaO,CH4析出起始温度与峰值温度没有显著变化,此阶段CH4析出量降低,表明CaO可阻碍热解主要阶段脱甲基反应的生成,降低主要热解区间CH4含量;K2HPO4·3H2O加入后,CH4析出起始温度提前至224℃左右,析出量增加,同时在450~760℃区间析出峰明显增大,表明K2HPO4可改变CH4初始产出部分反应路径,同时催化纤维素热解一次及二次反应中甲基的断裂,并催化二次反应过程中挥发份重整甲烷化反应,从而提高CH4的生成量;CaO与K2HPO4·3H2O混合加入后,CH4析出量进一步增长,表明2种催化剂产生协同作用可进一步降低一次及二次热解过程中脱甲基反应的活化能,或进一步增强挥发份重整甲烷化反应。
纤维素中CO主要来自于含氧杂环、羰基和醚键的裂解[20-22]。由图2(c)可看出:纯纤维素的CO析出起始温度为293℃左右,峰值温度为383℃,加入CaO后,CO析出起始和峰值温度没有显著变化,析出微量升高;K2HPO4·3H2O加入后,起始析出温度为224℃,峰值温度为368℃,CO析出量显著增加,表明K2HPO4·3H2O可改变CO初始产出部分反应路径,并同时显著催化热解过程中脱羰基反应键的断裂反应以及二芳基醚的分解反应[19-21];CaO与K2HPO4·3H2O混合加入后,CO析出量进一步增加,说明CaO与K2HPO4·3H2O产生一定的协同作用,进一步催化脱羰基等反应的发生。
CO2的释放主要来自纤维素末端羧基、乙酰基等的分解[11-13]。由图2(d)可看出:纯纤维素的CO2在271~465℃区间存在单一的析出区间,峰值温度为378℃;加入CaO,这一区间析出起始温度没有明显变化,峰值温度为382℃,CO2析出量降低,这是CaO与纤维素热解所生成的“类CO2活性中间体”等酸类产物或其前驱物等反应所致[11-12],另外560~721℃区间出现第二个CO2析出峰,峰值温度为657℃,由于CaO会与“类CO2活性中间体”反应生成羧酸钙盐或有机钙盐,这些产物继续分解生成无定型CaCO3,进而继续分解释放出CO2;加入K2HPO4·3H2O,CO2在200~523℃区间大量析出,峰值温度为368℃,表明K2HPO4·3H2O可显著降低纤维素热解过程的脱羧反应活化能,改变脱羧反应路径,提高CO2产率;CaO与K2HPO4·3H2O混合加入,第一阶段的CO2产率进一步升高,峰值温度进一步提前为344℃,说明CaO与K2HPO4·3H2O混合产生协同作用,可进一步降低主要热解阶段脱羧反应活化能,从而进一步提高主要反应过程的脱羧效应。
由图2(e)可看出:纯纤维素热解时,M/Z=46在300~470℃区间存在单一的析出峰,峰值温度为377℃;加入CaO,这一区间析出起始及峰值温度没有明显变化,析出量降低,这是CaO可固定甲酸基等基团或者抑制这些基团分解,或促使醇类中的羟基被脱除而生成小分子烃类物质所致,另外582~716℃区间出现第二个析出峰,峰值温度为642℃,这是CaO与热解反应挥发份反应产物二次分解所致;加入K2HPO4·3H2O,M/Z=46在224~484℃大量析出,峰值温度为382℃,析出总量增大,同样是因为K2HPO4·3H2O改变M/Z=46初始产出部分反应路径,并显著降低纤维素热解整个过程的脱甲酸基团、醇羟基脱除等反应活化能所致;混合加入CaO与K2HPO4·3H2O,M/Z=46生成量显著高于纯纤维素热解,但低于单独添加K2HPO4·3H2O所得M/Z=46产物生成量。
纤维素热解过程中首先发生开环和解聚反应,继而随着温度的升高经缩聚反应或苯环生成反应可产生苯自由基,苯自由基与甲基可结合为甲苯[22-23]。由图2(f)可看出:纯纤维素热解时,甲苯在313~520℃区间有极其微量的析出,峰值温度为402℃;添加CaO热解时,析出量降低,这是因为CaO抑制苯环生成反应或促使甲苯产生脱甲基反应;加入K2HPO4·3H2O,甲苯在266~627℃区间析出量明显增大,峰值温度为455℃,但析出量远低于其他产物。由此表明K2HPO4·3H2O可改变甲苯初始产出部分反应路径,并降低纤维素热解过程苯环形成反应的活化能,催化苯环形成反应,或促使热解过程中长链多烷基苯分解生成甲苯,因纤维素本身热解特性,甲苯析出量依然很少。混合加入CaO与K2HPO4·3H2O,甲苯产量大幅增长,峰值温度为509℃,表明CaO与K2HPO4·3H2O共同作用时,在纤维素热解过程中产生较强的协同催化作用,从而产生更多的甲苯。
由图2(g)可看出:纯纤维素热解时,苯酚在293~651℃区间析出,峰值温度为387℃,加入CaO,这一区间析出起始及峰值温度没有明显变化,析出量出现微量降低;加入K2HPO4·3H2O,苯酚的主要析出区间为277~573℃,峰值温度为387℃,析出量增长,同样表明K2HPO4·3H2O可改变苯酚初始产出部分反应路径,并催化纤维素热解过程苯环形成反应或促使烷基苯酚断裂分解生成苯酚;混合加入CaO与K2HPO4·3H2O,苯酚析出起始温度进一步降低,产率继续增长,表明CaO与K2HPO4·3H2O共同作用时,在纤维素热解过程中产生较强的协同催化作用,从而进一步降低反应起始温度并产生更多的苯酚。
3 结 论
1)纤维素热解过程中加入CaO,H2析出增多,CO、CH4等气体析出量降低,CaO会固定纤维素热解过程中产生的酸类产物及其前驱物等,从而降低271~465℃区间CO2的析出量,并使CO2继续在560~721℃区间析出。
2)纤维素热解过程中加入K2HPO4·3H2O,热解显著提前,H2、CO析出量降低,CH4、CO2等气体析出量增加,K2HPO4·3H2O可显著改变热解反应历——如提高苯环形成反应的发生。
3)纤维素热解过程中混合加入CaO与K2HPO4·3H2O,热解起始的失重过程相对于单独添加K2HPO4·3H2O较为缓和,且主要热解阶段H2、CH4、CO等气体生成量相对增加,CaO与K2HPO4·3H2O在热解过程中产生较强的协同作用。
