银配位聚醋酸乙烯酯的制备与表征
2018-02-08吴之传谭康惠
周 凯,吴之传,谭康惠
(滁州职业技术学院食品与环境系,安徽滁州239000)
作为一种新兴的功能材料,金属配位聚合物既保持了有机高分子的特性,又具有无机金属的特性,是一类结构新颖、性能奇特的高分子材料,可以应用于光学材料、催化剂材料、抗菌材料、生物传感器材料、涂料、电池电极材料、防静电材料、低温超导材料等,因此,受到了人们越来越多的关注[1-5]。
本文以聚醋酸乙烯酯(PVAc)为高分子配体,与金属Ag(Ⅰ)反应,选用水合肼(N2H4·H2O)作为还原剂,PVP为高分子保护剂,通过“配位-还原”法,最终在四氢呋喃体系中还原制得银配位聚醋酸乙烯酯(Ag/PVAc)溶胶。由于通过“配位-还原”法,可以使制得的材料中银粒达到纳米级。聚醋酸乙烯酯是粘合剂、水性涂料漆、纤维等材料的重要原料,成功制备混合均匀Ag/PVAc,可以使材料具备气调、保湿和缓释防霉等多种功效,对于拓展复合材料有着重要的意义。
1 实验部分
1.1 实验原理
本研究采用液相化学还原法,以硝酸银、PVAc为原料,水合肼为还原剂,PVP为高分子助剂,制备纳米Ag/PVAc溶胶。水合肼还原银的反应方程式为
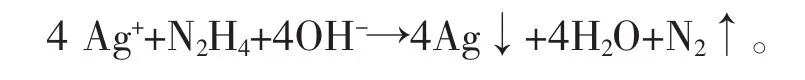
1.2 实验仪器
JJ-1大功率电动搅拌器,HH-2型数显恒温水浴锅,日立公司H600型透射电子显微镜,X射线衍射仪,激光粒度分析仪,紫外可见分光光谱仪。
1.3 方法及步骤
先将 PVP 用四氢呋喃溶解,移取一定量 0.1 mol·L-1的 AgNO3溶液,一起加入 40 ml PVAc(1mol·L-1)溶液中,避光,50℃下水浴,高速搅拌,制得PVAc-Ag(Ⅰ)溶液。
将PVAc-Ag(Ⅰ)溶液移入分液漏斗,以每分钟20~30滴的速度滴入含有还原剂N2H4·H2O的溶液中,继续高速搅拌20~40 min,即得红棕色银配位聚醋酸乙烯酯(Ag/PVAc)。
2 结果与讨论
2.1 温度的影响
取按上述1.3所述方法制备的PVAc-Ag(Ⅰ)溶液6份,分别于30℃、40℃、50℃、60℃、70℃、80℃下进行还原反应,反应0.5 h后,取出溶液稀释后用激光粒度分析仪进行测试,结果如图1所示。
由图1可以看出,还原温度对颗粒尺寸的影响较为明显,银粉粒度总趋势是先降后升,在50℃时Ag/PVAc的数均粒径达到最小值15.5 nm。根据实验中Ag/PVAc微粒的粒径大小等方面的观察,得出体系的最适宜反应温度为50℃。
2.2 PVP用量的影响
取 0.1 mol·L-1的 AgNO3溶液 0.6 ml,加入含有 1 mol·L-1PVAc(THF 溶液)链节的溶液 20 ml,避光反应2 h。反应完全后,以30滴/min的速度滴加入含有0.12 mol N2H4·H2O溶液中,反应温度50℃,反应时间0.5 h。选择PVP(单体):AgNO3(摩尔比)分别为:3∶1、6∶1、9∶1、15∶1和30∶1进行实验,结果如图2所示。由图2可知,在保持其他条件不变的情况下,Ag/PVAc的粒度随着保护剂PVP用量的增加而逐渐减小,当PVP(单体):AgNO3(摩尔比)增大到9∶1时,Ag/PVAc的粒度达到最小值。当PVP(单体)/AgNO3(摩尔比)的值继续增大时,Ag/PVAc的粒度反而呈增大的趋势。可见,助剂PVP的用量存在一个最佳值。
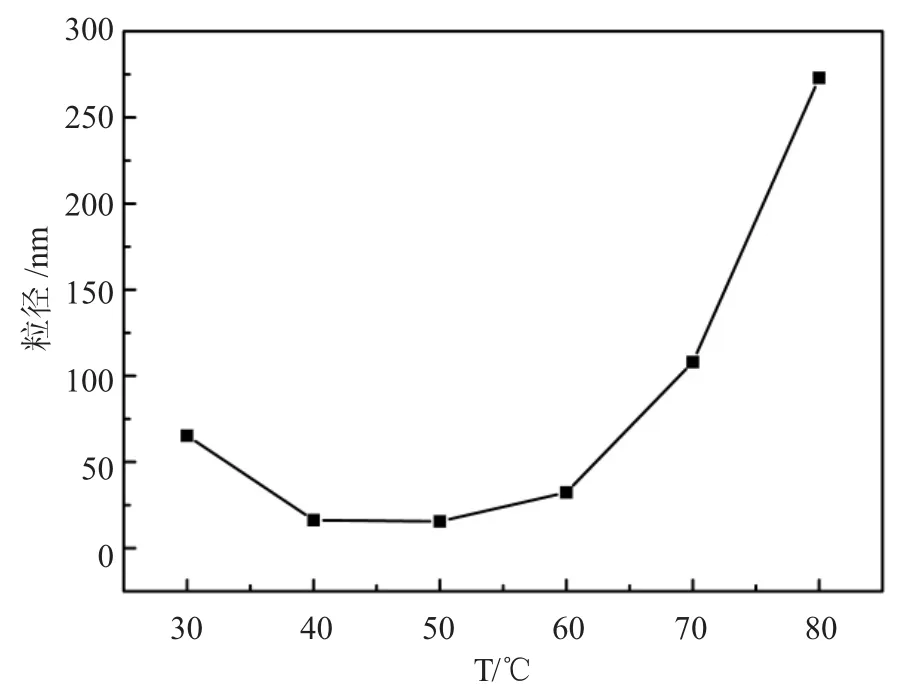
图1 粒径随温度变化关系
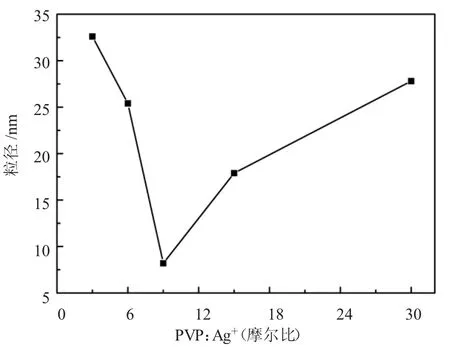
图2 粒径与PVP:Ag+(摩尔比)的关系
2.3 反应时间的影响
选择PVP(单体):AgNO3(摩尔比)为6∶1的溶液,进行考察时间与粒径关系的实验。用5 min的时间将PVP-Ag(Ⅰ)滴加入N2H4·H2O溶液中,回流搅拌,反应温度50℃,每隔一定的时间测试粒径的大小,结果如图3所示。
由于采用被还原液滴加入还原剂中的还原方法,初始反应物PVAc-Ag(Ⅰ)浓度小,反应速率慢,生成的Ag及时被PVAc束缚,加之助剂PVP的协同作用,阻止Ag微粒粒径的增长,从而得到粒径大小均匀的Ag/PVAc。反应最初阶段所得粒子粒径很小,数均仅为13.4 nm。而随着搅拌的进行,溶液中粒子碰撞的次数增多,团聚的机会加大,而且,随着溶液中还原剂的减少,还原气氛的降低等因素,都会使得溶液中粒子二次团聚的机会增大,表现为溶液的粒径随时间不断地增大。所以综合还原程度等因素,本试验反应时间定为20 min。
2.4 产物Ag/PVAc的UV光谱分析
将不同浓度的Ag/PVAc稀释后,用紫外-可见吸收光谱仪检测,如图4所示。图4中Ag/PVAc溶胶的银粒子表现出两个主要的吸收峰,位于411 nm和510 nm(如曲线a所示),分别对应于银粒子的四极子和偶极子表面等离子体共振,也可能由于红移,而发生两峰重叠成单峰的现象[6](如曲线b所示)。
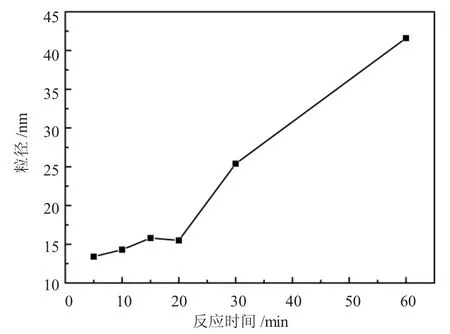
图3 粒径与反应时间的关系
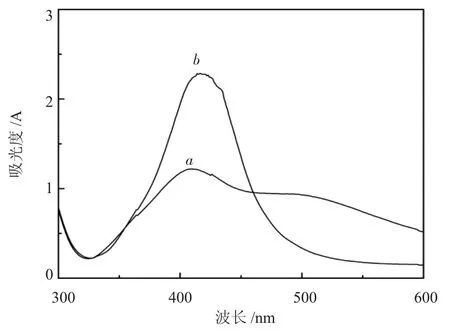
图4 Ag/PVAc的紫外-可见光谱
将不同反应时间内制得的Ag/PVAc粒子稀释后,在紫外-可见吸收光谱仪中试验,结果如图5曲线a~f所示。从图5可以看出,当反应刚开始时,由于Ag/PVAc粒子的粒径很小(如曲线a所示),在溶胶中的银粒子表现出两个主要的吸收峰,分别位于411 nm(图中1处)和510 nm(图中2处),而随着反应时间的延长,粒子粒径变大,510 nm处的吸收峰消失,只表现出位于411 nm处的一个单峰(如曲线f所示)。这可能是由于溶液中的PVAc、PVP分子与金属间存在强烈的化学键,分子与金属间发生电荷转移,从而改变金属内部的自由电子密度,致使金属的表面等离子体共振谱峰位移,位移的方向决定于分子与金属间电荷转移的方向,金属向PVAc、PVP分子的电荷转移,以致表面等离子体共振谱峰红移,而发生两峰重叠的现象[7]。
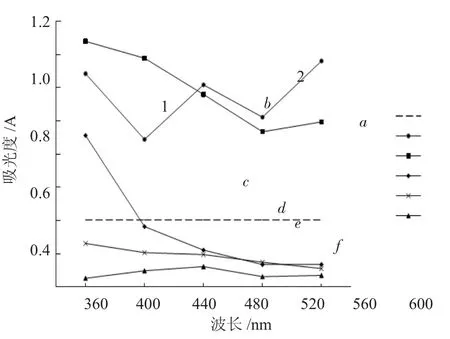
图5 不同反应时间Ag/PVAc的紫外-可见光谱
2.5 扫描电子显微镜(SEM)分析
将载玻片分别用乙醇和水进行超声波洗涤后晾干,然后将按上述1.3所述方法制得的2份不同Ag/PVAc溶液稀释100倍后滴至载玻片上,自然晾干,最后将载玻片用SEM分别进行观察。
另将按上述1.3所述方法制得的Ag/PVAc溶液取出用四氢呋喃(THF)和去离子水离心倾泻分离3次,将所得的粉末倒入培养皿中,一起放入真空干燥箱内,40℃下恒温干燥3 h,制得粉末。将上述粉末用SEM分别进行观察(放大倍数20 000倍)。从图6、7可以看出,由于在洗涤、干燥的过程中纳米级的颗粒容易发生堆积,发生小颗粒聚结到大颗粒上,也可能在粒子相互接触处局部溶合,形成一个大的多孔粒子聚合体,所以从图中可以看出两份试样都有不同程度的团聚现象,未加PVP的Ag/PVAc颗粒的团聚现象更严重,而加入PVP的粒子由于PVP的存在显得更加松散。
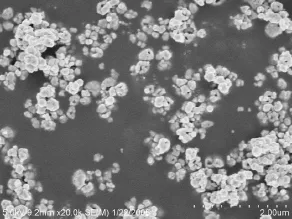
图6 Ag粉末(加入PVP)的SEM照片

图7 Ag粉末(未加PVP)的SEM照片
2.6 红外光谱(IR)分析
从Ag/PVAc的红外光谱(见图8)可以看到,形成Ag/PVAc后移至1 727 cm-1,而纯PVAc中Vc=o为1 735 cm-1,向低波数方向移动 8 cm-1。纯 PVAc中 Vc-o-c为 1 240 cm-1,而形成Ag/PVAc复合材料后移至1 222 cm-1,向低波数方向移动18 cm-1。这说明在PVAc链节单元O=C-O-C中的C=O因氧原子的共轭作用,使C=O上的电子云移向氧原子,C=O双键上的电子云密度降低,力常数减小,导致C=O键上的吸收峰向低波数方向移动。而在酯基C-O上氧原子的孤对电子向金属银转移,导致氧原子的电负性增大,C-O键上的电子云移向氧原子,C-O键的电子云密度降低,键的力常数减少,导致C-O键的吸收峰向低波数方向移动[8]。综合以上因素可以推论,在膜中金属Ag颗粒与PVAc分子间存在着化学相互作用,即Ag/PVAc以配位键的形式存在。
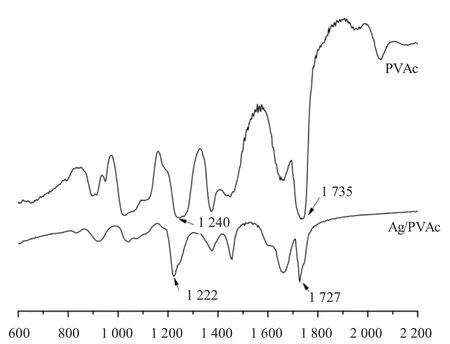
图8 Ag/PVAc的红外光谱图
2.7 X射线衍射(XRD)分析
取2份相同的PVAc-Ag(Ⅰ)溶液40 ml,其中 PVAc 浓度为 1 mol·L-1,AgNO3为0.005 mol,一份未加表面活性剂PVP,另一份加入0.75 gPVP。50℃条件下,以每分钟20~30滴的速度滴加入含有0.01 mol的N2H4·H2O溶液中,反应20 min后,分别倒入培养皿中,制得Ag/PVAc膜。用德国BrukerAXSD8X射线衍射仪做衍射分析,图谱如图9所示。
图9中,曲线a为加入PVP制得Ag/PVAc膜的衍射图,曲线b为未加PVP制得Ag/PVAc膜的衍射图,二者出峰位置基本相同。2θ角为37.94°,44.2°,64.44°处有明显的吸收峰,与JCPDS卡-040783上数据(2θ为 38.096°,44.257°,64.406°)基本吻合,分别对应于立方晶系银的(111),(200)和(220)晶面,说明膜中为立方系纯相单质银。该曲线衍射峰相当尖锐,表明产品结品性能良好。由Scherrer公式计算上例中加入PVP制备而成的Ag/PVAc膜晶粒尺寸,根据Scherrer公式计算的银粒粒径为13.4~23.5 nm,与粒度分析仪所测粒度的大小基本一致。
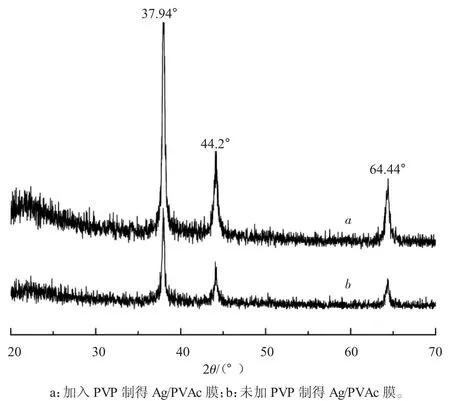
图9 Ag/PVAc膜的X射线衍射图谱
3 结论
产物的UV光谱显示:溶胶中的粒子表现出两个主要的吸收峰,证明是纳米银的特征峰。由于溶液中的PVAc、PVP分子与金属间存在强烈的化学键,分子与金属间发生电荷转移,从而改变金属内部的自由电子密度,致使金属的表面等离子体共振谱峰位移,金属向PVAc、PVP分子的电荷转移以致表面等离子体共振谱峰红移,而发生两峰重叠的现象。产物的IR光谱显示:Ag/PVAc膜中Ag与PVAc以配位键的形式存在。通过X射线衍射分析,证明膜中确有立方系纯相单质银。通过SEM电镜可以看出,Ag/PVAc颗粒成圆球状。与未加PVP的Ag/PVAc相比,加入PVP的粒子团聚现象不明显,粒子的粒径要小一些。
[1]QIN Yaqiong,JI Xiaohui,JING Jing,et al.Size control over spherical silver nanoparticles by ascorbic acid reduction[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2010,372(1-3):172-176.
[2]CHEN C N,CHEN C P,DONG T Y,et al.Using nanoparticles as direct-injection printing ink to fabricate conductive silver features on a transparent flexible PET substrate at room temperature[J].Acta Materialia,2012,60(16):5914-5924.
[3]廖立,熊继.液相还原法制备纳米银粉的研究[J].稀有金属材料与工程,2004,33(5):558-560
[4]江建军,谈定生,刘久苗,等.葡萄糖还原制取超细银粉[J].上海有色金属,2004,25(1):5-8.
[5]谭松庭,周建萍,姜忠民,等.微乳液法制备超细金属银粉的研究[J].湘潭大学学报(自然科学版),2001,23(4):60-62.
[6]MALYNYC S.Light-Induced Coherent Interactions between Silver Nanoparticles in Two-Dimensional Arrays[J].J Am Chem Soc,2003,125:2896-2898.
[7]KHOUIY J T,SCHAAF T G.Optical Absorption Spectra of Nanorystal Gold Molecules[J].Phsical Chemistry B,1997,101:3706-3712.
[8]张宇东.纳米铜/聚醋酸乙烯酯复合材料制备与表征[J].涂料工业,2006,36(2):46-48.
