分段碱调“无金属添加”水晶鸡皮蛋的控制技术
2018-01-22,,,,
, ,,,
(华中农业大学食品科学技术学院,湖北武汉 430070)
皮蛋是以禽蛋为原料,在碱性环境并搭配其他调味原料腌制加工而成的蛋制品。传统的皮蛋加工一般以鸭蛋作原料,鸡蛋因其壳薄、壳表气孔不一等,鸡皮蛋往往品质差异较大、稳定性差且蛋白透明度难控制;其次是鸡蛋白凝固的酸碱度范围窄,易水化[1],因此加工技术要求很高。从1985年以来,我国鸡蛋产量便稳居世界首位,2015年占全球产蛋量的比重更是接近50%,国内传统以鲜鸡蛋为主要消费的消费结构(占产蛋量的95%)亟需改变[2],鸡蛋加工业需要大力发展。所以研究以鸡蛋为原料腌制外观独特的皮蛋具有重要意义。
氧化铅在早期皮蛋的加工中有着重要的地位。近年来学者针对锌、铜等金属离子代替铅做了大量研究[3],目前“锌法”或“铜锌混合法”是鸭皮蛋生产的最普遍应用的工艺[4-5]。但随着消费者对食品安全和身体健康关注度的上升,以及对产品综合品质的要求不断提高,普通无铅皮蛋无论从外观还是风味上都已经不能满足消费者的需求,并且长期摄入金属盐难免会对人体造成伤害[6]。因此开发“无金属添加”的皮蛋加工工艺十分必要。
近来的研究表明腌制液碱浓度在皮蛋制作过程中起决定性的作用[7]。碱作用时间过长或料液碱浓度过大,易使凝胶的蛋清被稀化,反之则蛋清无法形成凝胶[8]。在传统腌制方法中金属离子的作用是形成难溶物将蛋壳的气孔堵塞,从而减少碱对蛋的渗入。所以本研究通过梯度降低料液碱浓度就可以充当金属离子的作用[9-10],取代金属盐腌制法,并可有效防止皮蛋出现烂头、节省碱用量等[4]。
本研究主要包括以下内容:以流变性等指标探究在化清期、凝结期五种NaOH浓度腌制料液下的鸡皮蛋性质变化,根据其流变性与碱度增减确定第一阶段最适料液碱浓度;以TPA质构、色差、感官等指标探究在更换料液后不同碱浓度下最佳腌制工艺条件,并研究鸡皮蛋透明度的良好控制技术。
1 材料与方法
1.1材料与仪器
鸡蛋 武汉市九峰山鸡养殖场同批次新鲜鸡蛋;氢氧化钠、乙醇(95%)、酚酞、氯化钠、无水氯化钙、HCl 国药集团化学试剂有限公司,AR级;精制碘盐 湖北盐业集团有限公司;红茶 临沧市龙凤茶业有限公司;蒸馏水 实验室制备。
FA2004B型电子天平 上海越平科学仪器有限公司;AR-2140型分析天平 梅特勒-托利多仪器(上海)有限公司;HH-8型数显恒温水浴锅 国华电器有限公司;MJ-BL25C5型搅拌机 广东美的生活电器制造有限公司;FJ-200型高速分散均质机 上海标本模型厂;101-2AB型电热鼓风干燥箱 天津市泰斯特仪器有限公司;食品盐度计(0~28%) 北京德明达光学仪器厂;AR-2000ex流变仪 美国 TA Instruments Lat1.2;UltraScan XEU3763型色度仪 柯尼卡美能达办公系统(中国)有限公司。
1.2实验方法
1.2.1 工艺流程 如下:

定期抽样:在腌制过程中,从腌制第二天开始,每个浓度组取样品蛋若干进行指标测定,要求每组所取样品蛋无人为因素损坏,切取相同部位测定。
1.2.2 皮蛋加工方法与分组 参考文献方法[11-13]。
第一阶段:取同一品种、同一饲养场、同一产蛋批次鸡蛋200枚,统一清洗干净,并将鸡蛋分为5组,每组40个鸡蛋。采用塘心皮蛋浸泡法[12]加工工艺腌制鸡蛋,保证腌制条件一致且每次取样顺序一致。固定腌制条件为:温度(25±2) ℃,蛋重∶料重=1∶1.5,以水重计,红茶浓度为3%,NaCl浓度为3.5%,设置5个NaOH浓度梯度(0、2%、3%、4%、5%);料液配制方法:首先量取茶叶熬制的水4 L,再依次加入碱、食盐混合并搅拌均匀,放凉后即可获得料液(如果有大量沉淀可适当的加热)。按照分组取0~14 d样品测定指标。
第二阶段:基于第一阶段结果,3%、4%、5% NaOH浓度的鸡蛋在腌制14 d后,分别将每组等分后(20个鸡蛋)放入1%、3%浓度NaOH溶液中,进入第二阶段腌制20 d。
1.2.3 料液碱浓度测定 参考文献方法[14-16]。料液NaOH质量分数即料液碱浓度。HCl-BaCl2滴定法:配制中性的氯化钡溶液备用,取1 mL的干净吸管准确吸取1 mL料液于250 mL容量瓶中,加入10 mL氯化钡溶液后用蒸馏水定容,摇匀过滤,取滤液25 mL于干净的三角瓶中,滴2~3滴酚酞作指示剂,并用0.l mol/L的盐酸滴定至溶液的粉红色消失为止。平行三次实验。
式(1)
式中:N为盐酸的浓度,单位:mol/L;V为消耗盐酸的体积,单位:mL;0.04为氢氧化钠的毫克相当量,单位:mg;G为0.1毫升各溶液的重量,单位:g。
1.2.4 蛋清游离碱度的测定 参考文献方法[17]。取蛋清待测样品与水以质量比2∶1比例混合,将样品用高速分散均质机上打匀;取15 g混合样品,加入蒸馏水至250 mL,搅匀,用双层纱布过滤,取滤液,待用。吸取50 mL滤液(皮蛋试样),在附酸度计的磁力搅拌器上用0.1 mol/L的盐酸溶液边滴边搅拌,直至溶液pH为7停止,平行两次实验。皮蛋的游离碱度(mg/l00 g)为:
式(2)
式中:X为试样中的游离碱度(以氢氧化钠含量计),单位:mg/100 g;V1为滴定试样时消耗盐酸标准滴定溶液的体积,单位:mL;V2为空白实验消耗盐酸标准滴定溶液的体积,单位:mol/L;C为盐酸标准滴定溶液的实际浓度,单位:mol/L;40为与1.0 mL盐酸标准滴定溶液[C(HCl)=1.00 mol/L]相当的NaOH的质量,单位:mg。
1.2.5 碱诱导蛋清凝胶形成中动态流变性质的测定 采用AR-2000ex流变仪,在样品的线性黏弹区内,进行小振幅振荡扫描实验,测试样品的弹性模量G′、损耗模量G″与相位角5。实验条件:温度为25 ℃;间距为1 mm;频率范围为0.1~10 rad/s;应变为2%[18]。

表1 感官评价标准Table 1 Standard of sensory evalution
1.2.6 色差测定 调整色度仪为RSIN模式,校正仪器,黑板和白板(black=0;white=0)。将准备好的待测样品用透明保鲜膜包好在室温下进行测定。测定时将蛋清的切割平面对准CCD摄像头,每个样品选择六个部位在小孔径光束下进行测定[19]。其中L*值为亮度,由小到大表示全黑至全白;a*值由小到大表示绿色至红色;b*值由小到大表示蓝色至黄色。
溶液白度测定:白度值(W)按式(3)计算,每组重复6次,取平均值。研究表明,白度值越大,感官可接受度越高。
式(3)
式中:L*为亮度,a*为正值表示偏红,负值表示偏绿;b*为正值表示偏黄,负值表示偏蓝。
1.2.7 质构分析 采用TPA质构分析模式,测试前速率1 mm/s,测试速率2 mm/s,测试后速率2 mm/s,压缩比70%,恢复时间5 s,探头型号为P/50,触发力分别为5 g。质构参数:硬度、弹性、咀嚼性和内聚性,数据采集由计算机软件完成。穿刺实验的测定条件为:测试前速率5 mm/s,测试速率2 mm/s,测试后速率5 mm/s,测试距离为15 mm,探头型号为P/0.5。考虑到两次压缩的破裂点无法确定,安排穿刺实验测量破坏力具体值,以具体反映蛋清的凝胶强度,每组重复6次取平均值。
1.2.8 皮蛋感官评价 腌制25 d后组织10名经过感官培训的人员对鸡皮蛋进行感官评定。将鸡皮蛋从腌制容器中取出,用清水洗净,在光线良好的条件下观察、触按和品尝,并分别从鸡蛋皮蛋蛋壳、蛋白、蛋黄和风味四个方面来评价,具体评分标准见表1[20]。
1.2.9 数据统计 本实验所有数据使用Microsoft Excel 2013和SPSS V17.0软件进行统计分析和绘图处理。
2 结果与分析
2.1加碱第一阶段料液碱浓度、蛋清碱浓度含量的变化
0~14 d的不同碱浓度料液腌制过程中料液碱浓度变化见图1。从图可看出浸渍期间不同碱浓度的料液的碱含量变化趋势相似,腌制初期由于碱液向皮蛋中的渗透,造成料液碱浓度的整体呈下降趋势并普遍在8~10 d碱浓度达到最低(从2%~5%分别是135.7、249.3、319、392.3 mg/10 g),然后缓慢上升。5%浓度与2%浓度组料液下降幅度最大,而2%浓度组料液碱浓度达最低点的时间最短在8 d(28.85%),而5%浓度组在10 d左右(11.57%)。但在最低点后所有组均出现料液碱度上升的情况,这可能是由于未添加金属离子,无法在蛋壳表面形成难溶物,因此未能在NaOH渗入过程中堵住气孔,造成NaOH部分渗出[9,21]。在皮蛋腌制过程中,NaOH通过蛋壳进入蛋内,再由蛋白渗入蛋黄,蛋白遇强碱后变性形成具有弹性的凝胶体,蛋黄因蛋白质变性和脂肪固化形成凝固体[22]。NaOH继续渗入会使蛋清局部出现再次化清[23-26],且在碱腐蚀的状态下气孔变大,所以出现料液碱度上升的情况。从整体来看料液碱浓度越高,变化趋势相对越平稳,变化幅度相对越小。
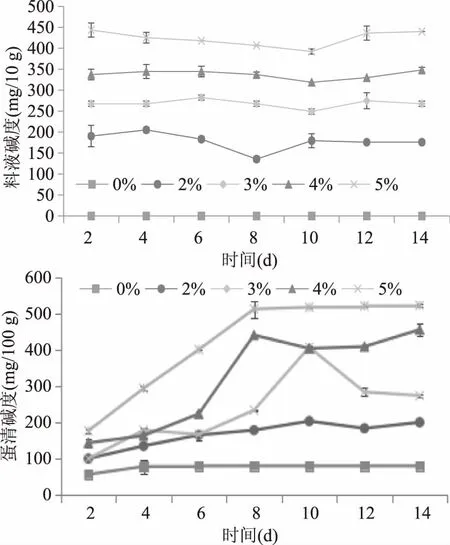
图1 皮蛋腌制14 d各组料液、蛋清碱浓度变化Fig.1 Alkalinity change of curing liquid and albumen during pickling period

图2 不同NaOH浓度腌制过程中鸡蛋清的动态流变图(G′、G″)Fig.2 Evolution of G′ and G″ values of egg white at different stages
观察图1可得,各组蛋清碱浓度的变化有相同趋势,但幅度不同。蛋清的碱浓度变化先呈现上升趋势,在8~10 d时达到最大值,后缓慢下降趋于平稳。出现上述变化趋势的原因可能是0~10 d料液中的NaOH通过蛋壳上的气孔和向蛋内渗透,蛋内粘稠蛋白变成稀的透明水样溶液,这时蛋白质完全变性,原来的束缚水变成自由水,但蛋白质分子的一、二级结构尚未受到破坏,已化清的蛋白还没有失去热凝固性。腌制初期是“化清期”,料液中的碱大量渗透入蛋内[9,26],所以料液碱浓度在这一阶段下降较快,蛋清碱浓度上升较快。10~14 d变化不大,但由于没有添加金属离子,所以蛋清碱浓度仍呈缓慢上升的趋势。该阶段进入凝固阶段,蛋白从稀水样凝固成具有弹性的透明胶体。蛋白质分子在NaOH的作用下,二级结构开始受到破坏,氧键断开,亲水基团增加,大量自由水变为结合水,并与蛋白质分子连接呈凝胶状[24,26-27]。从图中还能看出,5%浓度组的蛋清碱浓度变化幅度最大,这可能是由于料液中碱液浓度相对高,形成了相对较高的渗透压差,因此蛋清吸收碱的量最大;3%浓度组和4%浓度组的蛋清碱浓度变化波动较大,相对较典型,呈现先上升后下降的趋势,这也和其他研究者研究的结果一致[9]。
2.2加碱第一阶段碱诱导蛋清凝胶形成中动态流变性质的变化
图2是第一阶段不同NaOH浓度腌制过程中鸡蛋清的动态流变图,从图中可以看出,在碱处理的开始阶段,不同蛋清样品表现出G′和G″部分下降、部分上升的趋势,可能因为遇强碱后,蛋白质的氢键遭到破坏,蛋白质分子出现了一定程度的伸展和溶解。在进一步的碱处理中,G′和G″增加,0、2%、3%、4%、5%碱浓度组分别在2,4,8,6,12 d达到峰值,这表明蛋白质-蛋白质相互作用下凝胶网络的发展。此时网络结构的稳定已达到临界状态,经过碱进一步处理,结构稳定遭到破坏,表现出G′和G″的急剧减小。12 d时,5%碱浓度组腌制的蛋清的G′和G″大大增加,其他各组腌制的蛋清的G′和G″值均小于100 Pa。
存储模量(G′)是胶体蛋白的弹性响应,存储模量的大小也反映蛋白凝胶性的强弱[27]。由图2可知,不同NaOH浓度下的蛋白的凝胶强度也不同。G′迅速上升,原因是由于蛋白之间的交联作用,初步形成空间网络结构。凝胶减弱过程,G′迅速降低,可能是由于蛋白开始变性造成的结果。蛋清靠近蛋壳部分直接接触碱液出现部分化清现象导致蛋白的流动性增强,同时不同程度上破坏了蛋白的网络结构,导致G′明显降低,弹性减少,粘性增强[28]。
4%、5%碱浓度作用下蛋清的G′与G″在图2中6~8 d时间段几乎未减小,这是由于高碱浓度下蛋清化清期短,蛋清的化清期在8 d左右已经结束,蛋清开始形成凝胶。在不同时间,碱作用下蛋清经历了以下三个阶段:蛋白质分子溶解后,再用蛋清溶胶变成水合相,存储模量(G′)和损耗模量(G″)相对较小;随着NaOH溶液的渗透,蛋清开始凝固时,水被包裹在一个网络系统,蛋清蛋白开始伸展和交织以形成三维网状结构,G′和G″开始增加到最大值;NaOH进一步渗透,G′、G″开始减小,表明凝胶基质开始被破坏,这是由于凝胶溶解,结晶区的蛋白质结构开始松懈[26,29]。
综合料液碱浓度、蛋清碱浓度变化以及对蛋清凝胶过程中的动态流变性质的分析可以看出,不同碱浓度料液腌制效果明显不同,浓度越高,蛋清碱浓度变化相对越明显,效果也越好,且料液NaOH浓度为3%、4%、5%的组结构凝结速度最快,用于第一阶段料液浓度有利于缩短整个腌制时间。根据腌制效果对比,选取料液碱浓度3%、4%、5%三组为第一阶段腌制基础实验浓度。
2.3加碱第二阶段指标料液碱度
加碱第二阶段料液碱度各组整体变化(图3)趋势相似,且浮动较小,25 d之前料液碱度几乎不变。蛋清缓慢成熟,通过蛋壳上的气孔和向蛋内渗透,致使料液中碱度出现部分下降的现象。但25 d之后各组料液碱度呈现上升的趋势。出现上述变化趋势的原因可能是第二阶段更换料液后料液中的NaOH相较之前浓度普遍降低,且蛋清此时处于凝结后期,凝结基本完成,所以蛋清吸收碱速度变缓甚至停止。蛋清经历化清期后凝结,蛋清在碱作用下变性,在经过这一阶段后蛋清不再需要碱作用,但因为配料中未加入金属离子,无法形成难溶化合物堵塞蛋壳上的气孔,碱继续渗透会使得蛋清再化次清[30-32],而此时蛋清相对料液碱度较高,通过气孔渗透使得料液碱度再次出现上升。

图3 更换料液后皮蛋腌制各组料液碱度变化Fig.3 Alkalinity change of curing liquid during pickling period
皮蛋中的蛋白质完全凝固后,应当控制料液中的NaOH浓度,否则碱浓度过高会使其继续向皮蛋蛋清、蛋黄内渗透。当蛋白中的NaOH含量超过0.7%时,已经变性的蛋白质分子间由于相互作用形成空间结构将会被破坏,已经吸附的结合水又会释放出来以自由水的形式存在,己凝固的蛋白又会再次液化。这种现象称之为第二次化清,即俗称的“碱伤”[28]。因此更换料液后的作用时间不宜过长,料液浓度不宜过高。
2.4加碱第二阶段产品蛋清色差
表2为不同料液碱度对鸡蛋皮蛋腌制过程中L*值、a*值、b*值、W值变化的影响。从a*值可以看出,鸡皮蛋均呈红色。腌制15~25 d,皮蛋a*值逐渐升高,多组在25 d达到最高,更换料液后的高碱度组(NaOH浓度>2%)则整体上升较慢,且达最大值时值相对较低。在25 d后皮蛋a*值普遍出现下降趋势。可以看出不同腌制碱度对皮蛋红度影响程度也有较大差异。观察皮蛋L*值也可以看出,在25 d时L*值基本相等,并随之出现了不同的增减趋势。

表2 腌制过程中碱腌制浓度对蛋清颜色的影响Table 2 Effect of different NaOH concentration on egg white color in curing processing
在前25 d,各组皮蛋蛋清色泽a*值随着浸渍时间延长而增大,表现为皮蛋色泽由黄色逐渐转变为红褐色,这是因为蛋清中的游离态糖在NaOH的作用下,其醛基与蛋白质氨基发生变色反应,实质是美拉德反应;25~30 d,a*值逐渐下降,这是由于蛋清中部分NaOH渗透入蛋黄中,导致蛋清中的变色反应减弱,并且随着料液中碱渗透速率的降低,变色反应进一步减弱,表现为a*值不断下降。各组皮蛋蛋清色泽L*值随着浸渍时间延长而呈总体下降,表示蛋清色泽在不断变深,同时蛋白质三维网络状凝胶结构的形成,皮蛋蛋白质逐渐呈现为半透明或不透明。
W值是综合鸡皮蛋内L*、a*、b*值的一种颜色综合表示方式,能够反映产品的整体颜色变化并且与产品整体外观成显著正相关[19],即白度值W越大,感官可接受度越高。由表2的W值可知,在腌制过程中(15~35 d)蛋清的白度先降低后增高再降低,白度值在料液碱浓度4%更换为1%时(以下用4%~1%代替,其他浓度同)腌制30 d时达到峰值。而蛋黄中的W值会随着腌制时间的延长而逐渐增加,但是在腌制25~30 d后,均呈下降趋势。
综上所述,鸡皮蛋样品蛋白相比于其他皮蛋(普通无铅工艺腌制皮蛋)的L*值较高(80左右),用该方法腌制的皮蛋透明度好,峰值出现在25~30 d之间。同时3%~3%浓度和5%~1%浓度腌制时白度值在25 d时达到最大,4%~1%和4%~3%腌制时在30 d时达到最大,最大值为4%~1%浓度下腌制30 d时。故可以确定腌制时间选择25~30 d时感官接受度最佳。
2.5加碱第二阶段TPA质构
图4是不同碱浓度腌制蛋清的硬度、粘性、弹性、内聚性、咀嚼性随时间变化图。

图4 第二阶段不同碱浓度腌制蛋清的质构特性随时间变化图Fig.4 Change of Texture characteristic in preserved egg albumen during picking period注:第一阶段料液碱浓度A 3%;B 4%;C 5%。
由图可知,各组硬度呈先上升后下降的趋势,在25 d时蛋清的硬度达最大值,且4%~1%浓度腌制25 d时达到实验所测硬度最大值1061.856 g。各组弹性变化并不明显,整体呈先上升后下降波动的趋势,在第一阶段碱浓度为4%、5%的条件下腌制的皮蛋在25 d时蛋清完全凝固,转色效果好,与第一阶段碱浓度为3%时的弹性值0.655、0.894相近,蛋清也未出现碱伤。咀嚼性也表现出相似的变化,这是因为碱性条件下,当松散的蛋白质结构通过氢键与自由水结合时,蛋白质会聚集在一起形成凝胶的网络结构。但是由于NaOH继续进入皮蛋中,会使凝胶结构破坏,蛋白会再次液化,即二次化清,且此时的变化不可逆,再次液化的蛋白将不能再形成凝胶结构[28-30,32]。在皮蛋腌制前期,随着蛋内NaOH含量的增加,使蛋白充分变性、聚集形成坚实的网络状凝胶结构,表现为硬度、弹性和咀嚼性不断增加。在皮蛋腌制后期,由于蛋白中NaOH含量减少,改变了蛋白凝胶已达到的平衡状态,使蛋白质凝胶网络结构出现松散,所以表现为弹性和咀嚼性随腌制时间延长而有所降低;硬度则相反,由于蛋白中NaOH含量有所降低,避免了过量的碱对蛋白凝胶的“碱伤”,所以硬度仍然呈上升趋势。
不同浓度组皮蛋的粘性、内聚性、胶性无显著的变化趋势。可能的原因是在腌制前期,随着碱液与蛋清的相互作用,碱液已经破坏了蛋清内原有的稳定乳浊液,使蛋清逐渐凝固[29]。
综合蛋清TPA的结果说明:在本实验条件下,控制第一阶段碱浓度为4%时腌制25 d时,蛋清弹性好、硬度高、碱味淡。控制第一阶段碱浓度为5%时腌制25 d时,弹性相对无较大差异但硬度较差,但是咀嚼性较第一阶段低碱度腌制高。
2.6加碱第二阶段感官评价

表3 皮蛋感官品质比较Table 3 Comparison of sensory properties in different albumen
从表3中明显可以看出在25 d时,4%~1%、4%~3%两组浓度梯度条件下腌制产品具有较高的感官评分(83.38,80.89)。碱度过高或过低直接影响了料液中NaOH的渗透速率,随之影响蛋清蛋白的凝胶以及皮蛋色泽的变化,最终影响皮蛋的感官品质,表现为口感上和外观上的差异。从表中可以看出,蛋黄的感官评分集中在15分左右,这也表明蛋黄的口感和外观差异相对较小,这是由于碱渗透蛋黄速率较慢,蛋黄的变化相比蛋清较小。
3 结论
腌制第一阶段综合腌制过程中料液碱度变化、蛋清碱浓度变化、G′与G″值变化,可得出3%、4%、5%这三组吸收NaOH速度较快,通过观察化清所需时间较短,可有效缩短腌制时间,获得凝胶性、流变性较好的皮蛋。所以第一阶段选取的腌制基础NaOH浓度为3%、4%、5%。
在第二阶段更换不同浓度的低碱度料液的实验中,通过测定蛋清的TPA质构特性,得出各项具体指标进行分析。从数据上可以看出不同浓度组皮蛋的粘性、内聚性、胶性无显著的变化趋势,而咀嚼性、硬度、弹性有一定差异。在碱浓度为4%~1%、4%~3%腌制25 d时,蛋清弹性好、硬度高、碱味淡;在碱浓度为5%~1%、5%~3%腌制25 d时,弹性相对无较大差异但硬度较差,咀嚼性较3%~1%、3%~3%、4%~1%高;色差的结果显示,运用该方法腌制的鸡皮蛋白度较高、透明度较好,这就说明在腌制过程中合理的调控碱度以及腌制时间是控制皮蛋良好透明度的关键措施,而且峰值在25~30 d之间的四个组别中,白度越高人们接受程度越好,蛋清越透明,所以腌制时间应在该范围内最适宜;在感官评价中碱浓度为4%~1%、4%~3%两组得分明显高于其他组,4%~1%得分最高,且风味较其他组更好,易被大家接受。
综上所述,可得最佳工艺为第一阶段NaOH溶液浓度为4%,腌制14 d后更换料液,第二阶段更换为1% NaOH溶液浓度料液,继续腌制到25 d即可出缸。
[1]佚名. Q用鸡蛋和鸭蛋做皮蛋的做法、检验不一样吗?[J]. 农业工程技术·农产品加工,2006(5).
[2]欧阳珂珮,李洪军,贺稚非.我国蛋制品研究现状及发展前景[J]. 食品工业科技,2011(12):506-508.
[3]卜红宇,马美湖. 不同金属在皮蛋加工中代铅的研究[C].//第八届中国蛋品科技大会论文集. 武汉:中国畜产品加工研究会,2009:444-450.
[4]阎华,朱端卫.铜、锌、铁在皮蛋加工中作用差异研究[J]. 食品科学,2006,27(12):164-167.
[5]BU H Y,MA M H. Different Effects of Zinc Salts on Preserved Egg Processing[J]. Food Science,2011:136-144.
[6]周露. 不要忽视重金属对人体的伤害[J]. 健康生活,2016(12):30-31.
[7]汤钦林,胡卓敏. 不同浸泡时期料液NaOH浓度与温度对加锌工艺皮蛋质量的影响[J]. 长江大学学报:自科版,2007,4(2):95-97.
[8]叶阳,王洋,王凌云. 不同碱液对鸡蛋清凝胶特性的影响研究[J]. 食品工业科技,2013,34(3):147-149.
[9]杨有仙,赵燕,涂勇刚,等. 皮蛋腌制过程中碱度、pH及质构特性变化规律的研究[J]. 食品工业科技,2012,33(16):111-114.
[10]PU Y J. Study on New Copper-free Preserved Eggs Manufacturing Technique[J]. Journal of Anhui Agricultural Sciences,2013.
[11]马美湖. 禽蛋制品生产技术[M].北京:中国轻工业出版社,2003:464-469.
[12]喻冬香. 皮蛋的浸泡法制作工艺[J]. 现代农业科技,2011(12):333-333.
[13]吕峰,郑明锋,陈丽娇. 梯度控温腌制无铅皮蛋工艺[J]. 福建农林大学学报:自然科学版,2005.
[14]杜健,史书军,仝军,等. 生石灰与纯碱使用比例对松花蛋料液碱浓度的影响[J]. 黑龙江畜牧兽医,2005(4):74-75.
[15]赵改名,田玮. 生石灰用量对料液碱度和皮蛋加工的影响[J]. 河南农业科学,1997(3):35-36.
[16]张富新. 鸡蛋皮蛋加工中碱度的变化[J]. 食品与发酵工业,2004,30(10):81-83.
[17]孙静,黄茜,蔡朝霞,等. 皮蛋腌制过程中NaOH渗透规律的研究[C].//第九届中国蛋品科技大会论文集.2010:130-133.
[18]于巍,周坚. 草鱼盐溶蛋白保水性及流变性质的研究[J].食品与发酵工业,2007,33(10):72-75.
[19]龙门,宋野,杜庆飞,等. 鸡蛋松花蛋腌制中蛋白质凝胶特性及颜色变化[J]. 食品科学,2016,37(3):75-80.
[20]李军鹏. 皮蛋腌制动力学及品质评价模型的研究[D]. 武汉:华中农业大学,2009.
[21]魏建春,杨宝进,张一鸣. 影响浸泡法加工松花蛋质量的因素新探[J]. 现代食品科技,2007,23(8):46-48.
[22]Yang Y E,Wang Y,Wang L Y. Influence of different alkali on gel properties of hen egg white[J]. Science & Technology of Food Industry,2013.
[23]马力,谢林,苏赵. 松花蛋形成过程中碱液含量控制机理的微观研究[J]. 四川工业学院学报,2001,20(2):43-45.
[24]Zhang F X. Changes of alkalinity during preserved chicken egg processing[J]. Food and Fermentation Industries,2004,30(10):81-83.
[25]张蓉真,刘树滔,林晓辉,等. 皮蛋加工过程中蛋白质变化的研究[J]. 福建农业科技,1998(s1):69-70.
[26]涂勇刚,赵燕,徐明生,等. 皮蛋加工过程中流变与凝胶特性的变化规律[J]. 食品科学,2012(19):21-24.
[27]刘志东,郭本恒.食品流变学的研究进展[J].食品研究与开发,2006,27(11):211-215.
[28]Lau K,Dickinson E. Structural and rheological properties of aerated high sugar systems containing egg albumen[J]. Journal of Food Science,2004,69(5):232-239.
[29]罗序英,赵燕,涂勇刚,等. 皮蛋蛋白质凝胶形成及其调控的研究进展[J]. 食品工业科技,2012,33(23):383-387.
[30]李锡嘏,石凤仙. 锌法皮蛋新工艺料液中NaOH和Zn2+浓度变化与产品质量的关系[J]. 湖南农学院学报,1993(5):464-469.
[31]万速文,张声华. 皮蛋加工中OH的渗透过程[J]. 食品科学,1998(6):27-29.
[32]Chen Z,Li J,Tu Y,et al. Changes in gel characteristics of egg white under strong alkali treatment[J]. Food Hydrocolloids,2014,45:1-8.
