Sysmex全自动血细胞分析仪XE-2100性能验证
2018-01-20于淼琛潘立阳王贞
于淼琛,潘立阳,王贞
ISO15189 CNAS-CL02:2012 《医学实验室质量和能力认可准则》中对血液领域的要求中,检验方法和程序的分析性能验证内容至少应包括正确度、精密度和可报告范围[1]。根据认可要求,本实验对急诊检验室使用的Sysmex全自动血细胞分析仪XE-2100进行精密度、正确度、线性范围、临床可报告范围和参考范围验证。
1 材料与方法
1.1 标本来源 标本来源于大连医科大学附属第一医院住院、门急诊诊患者标本。
1.2 仪器与试剂Sysmex全自动血细胞分析仪XE-2100(简称XE-2100)及原装配套试剂、校准品、质控品。
1.3 方法
1.3.1 精密度验证取低、中、高三个水平的新鲜血,连续重复测定10次,计算批内精密度;取至少两个水平的质控品,每天测定四次,每次检测之间间隔2h,连续检测5d,一共收集20个数据进行计算,计算批间精密度。
1.3.2 正确度验证 使用定值全血样本混匀后连续进行5次测定,计算其平均值与靶值相比较。
1.3.3 携带污染率 取高浓度血液样本,混合均匀后连续测定三次,测定值分别为H1、H2、H3;再取低浓度血液样本,连续测定3次,测定值分别为L1、L2、L3。按公式计算携带污染率。携带污染率=(L1-L3)/(H3-L3)×100%
1.3.4 临床可报告范围 选取一份接近预期上限的高值全血样本(H),分别按 100%、80%、60%、40%、20%、10%、0%的比例进行稀释,每个稀释度重复测定3次,计算均值。将实测值与理论值作比较(偏离应小于10%),计算y=ax+b,验证线性范围。要求:a值在1±0.05范围内,相关系数r≥0.975。
2 结果
2.1 精密度验证 WBC、RBC、HGB、HCT、MCV、PLT的检测批内精密度和批间精密度结果均合格,见表1。
2.2 正确度验证 验证结果相符,见表2。
2.3 携带污染率 携带污染率结果见表3。
2.4 临床可报告范围 临床可报告范围通过线性获得,见表4。
3 讨论
《医学实验室质量和能力认可准则》(ISO15189)要求参加认可的实验室,在开展某一检测项目前需提供并保留相关的方法学验证实验数据[2],对开展某一新的检测项目,更换检测系统或仪器或改变检测试剂盒产商时,实验室需对其相关方法学分析性能予以验证,对产商提供的评价资料中的主要性能予以确认。本文依据CL1A'88[3]、EP15-A2[4]、EP9-A2[5]等对 Sysmex 全自动血细胞分析仪XE-2100上开展项目进行精密度、准确性、携带污染率和临床可报告范围进行验证。批内精密度/批间精密度均符合要求,表明本仪器检测结果重复性良好;校准品的相对偏倚均符合行业标准,说明仪器有较高的准确性;五个项目的相关系数均大于0.99以上,线性误差均小于2%,表明仪器实测值和理论值具有良好的相关性(检测浓度与稀释倍数呈线性相关);携带污染率检测结果显示,高值、低值标本之间交叉污染小[5,6]。线性范围的验证是确定临床可报告范围的基础,当仪器检测到超出线性范围的结果时,应视为不准确的测定值[6-13]。
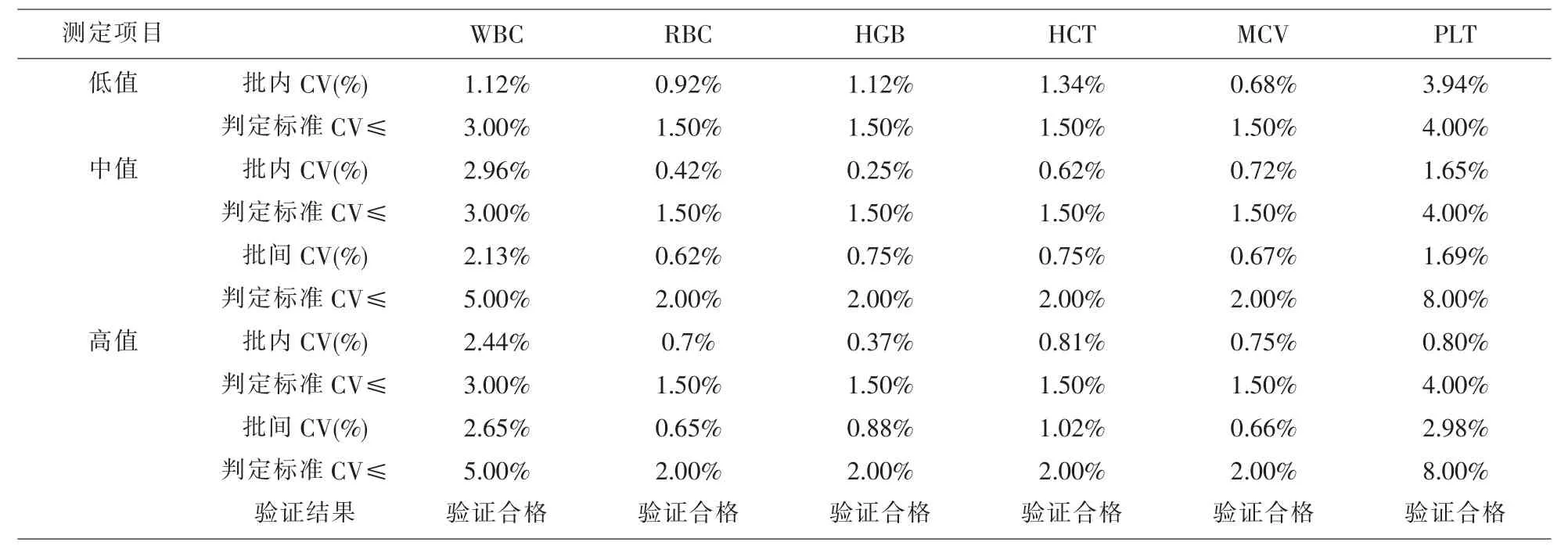
表1 精密度验证结果

表2 准确性验证结果

表3 携带污染率结果

表4 临床可报告范围
严格规范实验室检验方法的选择、评审及检测系统的分析性能评价程序,以保证所选用的检验方法和检验程序能满足临床与患者的需求,确认其符合相应的预期用途,确认检测系统的分析性能满足临床要求,保证检验结果的可靠性[14,15]。
综上所述,Sysmex全自动血细胞分析仪XE-2100检测结果准确、线性范围宽、携带污染低,性能良好,能够满足临床需要,适合大批量血常规检测分析。
