光动力疗法对大鼠龋齿模型的防龋效果及机制
2018-01-18马莹莹邹朝晖
马莹莹,邹朝晖
(1.郑州市口腔医院牙体牙髓科,河南 郑州 450000;2.天津医科大学口腔医学院牙体牙髓科,天津 300070)
龋齿是在以细菌为主的多种因素影响下,口腔内牙体硬组织发生慢性进行性破坏性感染性疾病[1],是与癌症和心血管疾病并列的人类三大重点防治疾病之一[2],研究龋病病因、寻找安全有效的防龋方法尤为重要。针对目前防龋方法的不足,有学者提出了光动力疗法(photodynamic therapy,PDT),该方法可有效杀灭细菌而不产生耐药性[3],在口腔感染性疾病的治疗中有很好的应用前景[4-6]。研究证实,PDT能有效抑制变异链球菌生长[7-9],对大鼠龋齿模型也有较好的防龋作用[10]。光敏剂是PDT的核心物质,血卟啉单甲醚(hematoporyrin monomethyl ethe,HMME)能产生较好的光动力效应。但关于以HMME为光敏剂的光动力疗法(hematoporyrin monomethyl ether-photodynamic therapy,HMME-PDT)对大鼠龋齿模型的防龋作用及机制的研究尚少。本研究旨在探讨HMME-PDT对大鼠龋齿模型的防龋效果及机制,为其用于龋病预防提供理论依据。
1 材料与方法
1.1动物21 d鼠龄、断奶的无特定病原体(specific pathogen free,SPF) 级Wistar雄性大鼠40只,体质量47.66~53.36 g,平均(50.51±2.85)g,由北京大学医学部实验动物科学部提供。
1.2细菌变异链球菌NCTC 10449由首都医科大学口腔医学院提供。
1.3主要试剂及仪器HMME(上海复旦张江生物医药股份有限公司);氟化钠(四川科伦药业股份有限公司);胰蛋白胨大豆肉汤固体培养基(trypticase soy agar,TSA)、胰蛋白胨大豆肉汤液体培养基(trypticase soy broth,TSB)(北京陆桥技术有限责任公司);致龋饲料(质量分数):蔗糖(56%),全麦粉(6%),精炼奶粉(28%),苜蓿粉(3%),脱水全肝粉(1%),酵母(4%),盐(2%);532 nm半导体激光器(中国医学科学院生物医学工程研究所);THERMD型电热培养箱(天津天宇技术实业有限公司);VS-1300U 型超净工作台(苏州净化设备有限公司);光学显微镜(日本OLMPUS公司);SS-550型扫描电镜(日本SHIMADZU公司);JS-1600小型离子溅金仪(北京和同创业科技有限责任公司)。
1.4实验方法
1.4.1变异链球菌悬液的制备常温下复苏变异链球菌NCTC 10449,超净工作台内用接种环挑取一环菌液接种于TSA上,置于电热培养箱,37 ℃下厌氧培养48 h。涂片检查,确定为纯培养后挑取TSA平板上单个菌落置于盛有5 mL TSB的试管中,置于电热培养箱,37 ℃下厌氧培养18~24 h,使其菌落数达到1×1011CFU·L-1,待用。
1.4.2大鼠龋齿模型的建立取21 d大鼠唾液培养,检测大鼠口腔内固有细菌的定植情况,并于 21~23 d鼠龄期间喂以含有抗生素的饮用水(青霉素 200 mg·L-1,链霉素1 500 mg·L-1)。于24 d鼠龄时取唾液培养,检测大鼠口腔内细菌的抑制状况,培养结果为阴性后停药。于25~27 d 鼠龄期间,以体积分数10%水合氯醛腹腔注射麻醉大鼠(3 mL·kg-1),每日清晨1次,连续3 d 给大鼠口腔内每颗磨牙各面接种1×1011CFU·L-1的变异链球菌100 μL,处理后30 min内禁食禁水。并喂以致龋饲料,同时将变异链球菌菌液和饮用水按1100体积比混合,给大鼠饮用。于28 d鼠龄时采集大鼠口腔刺激性唾液(每只100 μL)进行培养,通过平板菌落计数确认大鼠口腔内变异链球菌定植成功(>1011CFU·L-1),用于后续实验。
1.4.3动物分组与处理将建模成功的40只大鼠随机分为生理盐水组、单纯激光组、单纯光敏剂组、氟化钠组和HMME-PDT组,每组8只。各组大鼠用体积分数10%水合氯醛按3 mL·kg-1腹腔注射麻醉,上颌牙齿操作时采取仰卧位,下颌牙齿操作时采取俯卧位,用眼科开睑器撑开大鼠口腔,暴露磨牙进行处理;生理盐水组大鼠用浸有 150 μL 生理盐水的小棉球反复涂搽磨牙各面5 min;HMME-PDT组大鼠用浸有150 μL 40 mg·L-1HMME的小棉球放于磨牙各面上,避光孵育5 min后,用532 nm的半导体激光垂直照射磨牙牙齿各面,功率密度为 140 Wm·cm-2,照射时间为90 s,能量密度为 12.6 J·cm-2;单纯激光组大鼠不进行光敏剂HMME处理,仅用532 nm的半导体激光垂直照射磨牙各面,照射时间、功率密度、能量密度均同HMME-PDT组;单纯光敏剂组大鼠仅用浸有150 μL 40 mg·L-1HMME的小棉球放于磨牙各牙面上,避光孵育5 min,不进行激光照射;氟化钠组大鼠用浸有150 μL 2 g·L-1氟化钠溶液的小棉球反复涂搽磨牙各面5 min;各组大鼠每周处理1次,连续4周。
1.5观察指标
1.5.1大鼠磨牙牙面变异链球菌菌落计数自 28 d 鼠龄开始,每次处理完大鼠磨牙后,由同一位实验者用消毒棉式子按同一方向擦拭牙面,立即放入盛有2 mL消毒生理盐水的离心管中,震荡混匀,用无菌生理盐水进行10倍系列稀释至10-5,取 100 μL 悬浮液涂布于TSA固体培养基上,37 ℃下恒温厌氧培养48 h后,计算每升菌落数,用SPSS 16.0软件将数据进行对数转换[lg(CFU+1)]。
1.5.2大鼠磨牙平滑面和窝沟Keyes计分实验结束后(56 d时)处死大鼠,分组拔除牙齿,清水清洗,室温干燥,品红染色,流动清水冲洗掉多余的染液,室温干燥后,制作磨牙纵剖面,光学显微镜下观察龋齿情况,记录各组磨牙Keyes计分[11]。因磨牙平滑面(颊面、舌面和邻面)和窝沟(颌面)患龋率明显不同,将其分别进行记分。根据龋损破坏程度分为4级:牙釉质层(enamel only,E):龋坏仅仅局限于牙釉质;牙本质浅层(slight dentinal,Ds):龋坏累及牙釉质及牙本质外层1/4以内;牙本质中层(moderate dentinal,Dm):龋坏累及牙本质厚度的1/4~3/4;牙本质深层(extensive dentinal,Dx):龋坏累及深度超过牙本质厚度的3/4,甚至穿透牙本质全层。根据龋损破坏范围,将大鼠磨牙分为若干个牙面单位,将各组中每只大鼠磨牙相同面(平滑面、窝沟)相同级的龋分值相加,为此级的总龋分,总龋分除以8为每组平均Keyes计分。
1.5.3大鼠磨牙表面形态将牙齿放于体积分数10%的中性甲醛溶液中固定3 h,磷酸盐缓冲液冲洗3次,体积分数50%、70%、95%、100%乙醇梯度脱水,六甲基二硅胺烷浸泡3 min,干燥罐内干燥后,放入JS-1600小型离子溅金仪喷金,SS-550型扫描电子显微镜观察磨牙表面形态[12]。
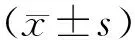
2 结果
2.1各组大鼠牙齿变异链球菌菌落数比较结果见表1。时间因素对大鼠口腔变异链球菌的生长没有影响(F=0.11,P>0.05),处理因素对大鼠口腔变异链球菌的生长有影响(F=230.89,P<0.05),且处理因素和时间因素存在交互效应(F=6.36,P<0.05)。生理盐水组、单纯光敏剂组、单纯激光组大鼠牙齿变异链球菌菌落数比较差异均无统计学意义(P>0.05);第1、2、3、4周处理后HMME-PDT组和氟化钠组大鼠牙齿变异链球菌菌落数均少于生理盐水组、单纯光敏剂组和单纯激光组(P<0.05);除第4周HMME-PDT组大鼠牙齿变异链球菌菌落数与氟化钠组比较差异无统计学意义(P>0.05)外,第1、2、3周处理后HMME-PDT组大鼠牙齿变异链球菌菌落数均少于氟化钠组(P<0.05)。
表1各组大鼠不同处理时间牙齿变异链球菌菌落数比较
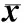
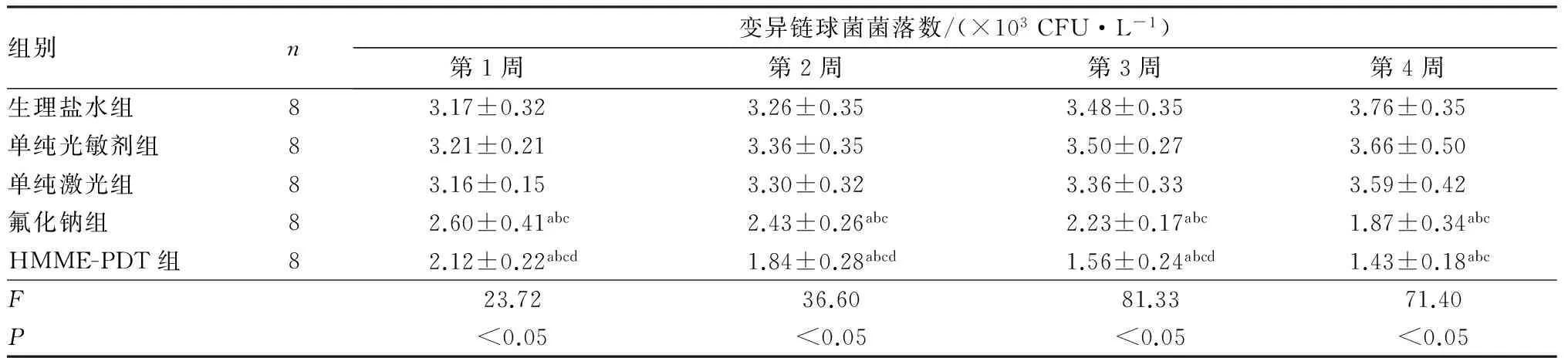
注:与生理盐水组比较aP<0.05;与单纯光敏剂组比较bP<0.05;与单纯激光组比较cP<0.05;与氟化钠组相比dP<0.05。
2.2各组大鼠平滑面龋齿Keyes计分比较结果见表2。各组大鼠平滑面龋齿均未检出Dx级龋损;HMME-PDT组和氟化钠组大鼠平滑面龋齿均未检出Dm级龋损。生理盐水组、单纯光敏剂组和单纯激光组大鼠平滑面龋齿E、Ds、Dm级龋损的Keyes计分两两比较差异均无统计学意义(P>0.05)。HMME-PDT组、氟化钠组大鼠平滑面龋齿E、Ds级龋损的Keyes计分均显著低于生理盐水组、单纯光敏剂组和单纯激光组(P<0.05),但HMME-PDT组与氟化钠组大鼠平滑面龋齿E、Ds级龋损的Keyes计分比较差异无统计学意义(P>0.05)。
表2各组大鼠平滑面龋齿Keyes计分比较
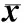

注:与生理盐水组比较aP<0.05;与单纯光敏剂组比较bP<0.05;与单纯激光组比较cP<0.05;“-”为未检出。
2.3各组大鼠窝沟龋齿Keyes计分比较结果见表3。各组大鼠窝沟龋齿中,仅生理盐水组检出Dx级龋损。生理盐水组、单纯光敏剂组和单纯激光组大鼠窝沟龋齿E、Ds、Dm 级龋损Keyes计分两两比较差异均无统计学意义(P>0.05)。HMME-PDT组、氟化钠组大鼠窝沟龋齿E、Ds、Dm 级龋损Keyes计分均显著低于生理盐水组、单纯光敏剂组和单纯激光组(P<0.05),但HMME-PDT组与氟化钠组大鼠之间窝沟龋齿E、Ds、Dm 级龋损的Keyes计分比较差异无统计学意义(P>0.05)。
表3各组大鼠窝沟龋齿Keyes计分比较
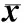
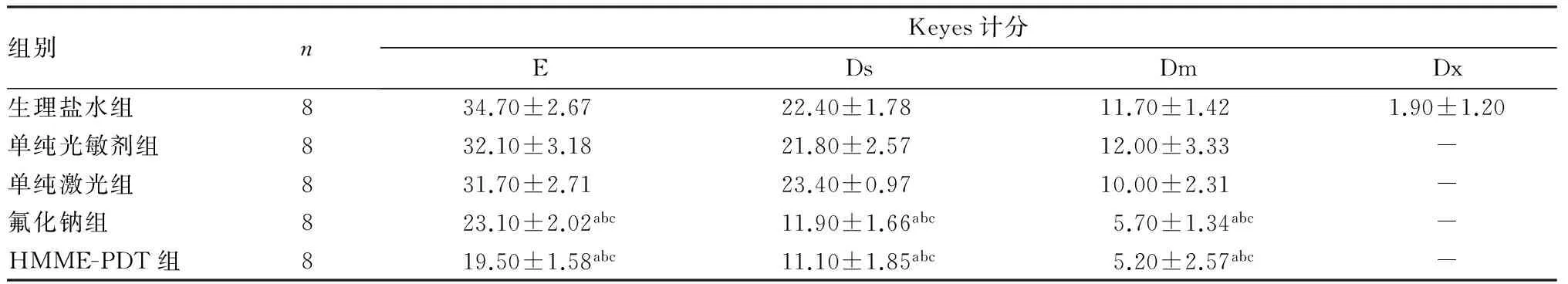
注:与生理盐水组比较aP<0.05;与单纯光敏剂组比较bP<0.05;与单纯激光组比较cP<0.05;“-”为未检出。
2.4各组大鼠磨牙表面形态扫描电镜显示,生理盐水组和单纯光敏剂组大鼠牙釉质表面粗糙,凸凹不平,有大量凹坑状脱矿区和划痕(图1A、图1B);单纯激光组大鼠牙釉质表面相对光滑,有少量圆形凹坑并可见凹坑内熔融状结构(图1C);氟化钠组大鼠牙釉质表面相对光滑,脱矿区较少,并可见到脱矿区的再矿化(图1D);HMME-PDT组大鼠牙釉质表面较平整,点状凹陷减少,深脱矿区少,且脱矿区域大多表浅(图1E)。

A:生理盐水组;B:单纯光敏剂组;C:单纯激光照射组;D:氟化钠组;E:HMME-PDT组。
图1各组大鼠磨牙表面形态扫描电镜图像
Fig.1Surfacemorphologyofrat′sodontoprisisdetectedbyscanningelectronmicroscopyimagesineachgroup
3 讨论
龋病是口腔中以细菌为主的多种因素复合作用所导致的牙体硬组织慢性进行性感染性病损,主要表现为无机质的脱矿和有机质的分解,随着病程进展,不仅破坏牙体组织,引起牙体缺损、牙痛、咀嚼功能减退或丧失,侵犯颌骨引起根尖周炎、骨髓炎等,甚至成为“慢性病灶”,严重影响机体的健康水平和生活质量。龋病预防一直是众多学者关注的焦点。变异链球菌是主要致龋菌,致龋菌在口腔内的产酸耐酸等代谢活动是龋病发生的直接原因,通过有效抑制或杀灭致龋菌的生长可起到防龋的目的。
PDI是一种联合光、光敏剂和组织中的氧分子,通过一系列的光化学反应选择性破坏病变组织,以达到治疗目的的新技术。在组织中加入光敏剂后,所有组织都会吸收,经过一段时间后,光敏剂会被正常组织逐渐代谢清除,而选择性潴留于病变组织中,随后经过适当波长光源照射后,光敏剂被激活,进一步将光能传递给周围组织,产生对细胞具有毒性的自由基,直接杀死细胞;或与周围的氧分子作用,产生活性氧分子(radical oxygen species,ROS),ROS可以与组织内的重要生物大分子如核酸和脂质、蛋白质等发生氧化还原反应,造成生物大分子活性物质丧失,影响其新陈代谢,导致细胞的死亡[13]。
光敏剂是PDI的核心物质,本研究所选用的HMME是一种性能稳定、组成单一、单态氧和活性氧物质产量多、在533 nm处具有特征吸收峰的光敏剂,能被532 nm的半导体激光有效激发,产生较好的光动力效应。氟化物应用于龋病预防已有多年,疗效确切,但存在耐氟菌株产生、氟使用安全性等问题,PDI是通过单态氧和ROS杀伤细菌,不产生耐药性,可重复使用,为龋病预防提供了一个新的途径。邹朝晖等[9]以20 mg·L-1的HMME为光敏剂,波长为 635 nm 的半导体激光为光源,在能量密度为 12.74 J·cm-2条件下照射变异链球菌形成的人工龋口腔生物膜90 s,能杀灭99.36%的变异链球菌。吴宝娣等[14]采用 20 mg·L-1的HMME溶液与变异链球菌定植的人工口腔生物膜37 ℃厌氧孵育 2 h,用 532 nm 激光照射90 s(光斑直径为1 cm,功率密度为 140 mW·cm-2),可抑制生物膜中99.64%的变异链球菌生长。本研究选用40 mg·L-1的HMME为光敏剂,532 nm半导体激光垂直照射牙面90 s(功率密度为140 mW·cm-2,能量密度为12.6 J·cm-2),结果显示,1、2、3、4周处理后,HMME-PDT组和氟化钠组大鼠牙齿变异链球菌菌落数均少于生理盐水组、单纯光敏剂组和单纯激光组,而且HMME-PDT组在前3周的牙齿变异链球菌菌落数均低于氟化钠组;另外,与生理盐水组、单纯激光组和单纯光敏剂组相比,在光滑面或窝沟龋的各级龋损中,HMME-PDT组大鼠的Keyes计分均显著降低,表明HMME-PDT对龋齿有明显的预防作用,这一结果也与菌落计数中变异链球菌数量减少的结果相吻合,表明PDT可能通过抑制或杀灭变异链球菌,减少变异链球菌的数量,从而起到预防龋病的作用,这一结果也与其他学者的研究结果相同[10,15-16]。虽然HMME-PDT组在前3周对变异链球菌的抑制作用强于氟化钠组,但2组Keyes计分比较差异无统计学意义,这表明防龋作用不仅与变异链球菌的数量减少有关,还可能与其他因素有关。扫描电镜结果显示,生理盐水组和单纯光敏剂组大鼠牙釉质表面粗糙不平,有大量的凹坑状脱矿区和划痕;单纯激光照射组大鼠牙釉质表面相对于生理盐水组和单纯光敏剂组较光滑,脱矿区少且可见到熔融状结构,表明激光照射可以改变牙齿表面结构;氟化钠组和HMME-PDT组大鼠牙釉质表面相对光滑,脱矿区较少且表浅,氟化钠组可见到部分脱矿区的再矿化。这一结果提示,虽然氟化钠组抑制变异链球菌的能力较HMME-PDT组弱,但Keyes计分却与后者没有明显差异的原因,可能与氟化钠组釉质脱矿的再矿化现象有关。
综上所述,HMME-PDT可通过减少变异链球菌数量、激光照射改变牙齿表面结构等对大鼠致龋模型起到明显的预防作用,但如何提高PDT的效应值得进一步研究。
[1] 樊明文.牙体牙髓病学[M].3版.北京:人民卫生出版社,2008:14-31.
[2] 王云霞,韩东超,隋丽娜,等.郑州市区学龄前儿童猛性龋流行病学调查[J].中华实用儿科临床杂志,2013,28(12):955-956.
[3] TAVARES A,CARVALHO C M,FAUSTINO M A,etal.Antimicrobial photodynamic therapy:study of bacterial recovery viability and potential development of resistance after treatment[J].MarDrugs,2010,8(1):91-105.
[4] HSU Y C,YANG D F,CHIANG C P,etal.Successful treatment of 7,12-dimethylbenz anthracene-induced hamster buccal pouch recancerouslesions by topical 5-aminolevulinic acid-mediated photodynamic therapy[J].PhotodiagnosisPhotodynTher,2012,9(4):310-318.
[5] COSTA A C,CAMPOS RASTEIRO V M,DA SILVA HASHIMOTO E S,etal.Effect of erythrosine-and LED-mediated photodynamic therapy on buccal candidiasis infection of immunosuppressed mice andCandidaalbicansadherence to buccal epithelial cells[J].OralSurgOralMedOralPatholOralRadiol,2012,114(1):67-74.
[6] XHEVDET A,STUBLJAR D,KRIZNAR I,etal.The disinfecting efficacy of root canals with laser photodynamic therapy[J].JLasersMedSci,2014,5(1):19-26.
[7] MÜLLER P,GUGGENHEIM B,SCHMIDLIN P R.Efficacy of gasiform ozone and photodynamic therapy on a multispecies oral biofilminvitro[J].EurJOralSci,2007,115(1):77-80.
[8] WOOD S,METCALF D,DEVINE D,etal.Erythrosine is a potential photosensitizer for the photodynamic therapy of oral plaque biofilms[J].JAntimicrobChemother,2006,57(4):680-684.
[9] 邹朝辉,高平,阴慧娟,等.光动力疗法对人工龋口腔生物膜菌斑的影响[J].中国激光,2009,36(10):2700-2704.
[10] 孙继军,王爱芹,王栋,等.光动力疗法防龋效果的动物实验研究[J].实用口腔医学杂志,2012,28(5):566-569.
[11] KEYES P H.Dental caries in the molar teeth of rats.II.A method for diagnosing and scoring several types of lesions simultaneously[J].JDentRes,1958,37(6):1088-1099.
[12] 张向宇,郭卯丁,李晓眠.柠檬提取物抗变形链球菌附着作用的研究[J].现代口腔医学杂志,2008,22(6):587-589.
[13] NAKONECHNY F,FIRER M A,NITZAN Y,etal.Intracellular antimicrobial photodynamic therapy:a novel technique for efficient eradication of pathogenic bacteria[J].PhotochemPhotobiol,2010,86(6):1350-1355.
[14] 吴宝娣,赵今.光动力疗法对人工口腔生物膜致龋变形链球菌抑制作用的研究[J].中国现代医生,2013,51(30):21-23.
[15] 常秀明,邹朝晖,阴慧娟.光动力疗法对牙菌斑生物膜内致龋菌的影响及作用机制的研究[J].口腔医学研究,2012,28(4):303-309.
[16] 张蕾,卢志山,孟磊,等.亚甲蓝-光动力疗法对大鼠口腔中变异链球菌的杀伤作用及其影响龋病发生的实验研究[J].牙体牙髓牙周病学杂志,2015,25(9):544-548.
