艾塞那肽治疗肥胖2型糖尿病并发阻塞性睡眠呼吸暂停综合征疗效观察
2018-01-18侯小丽吴述光郭悦鹏
侯小丽,吴述光,郭悦鹏
(1.新乡市第一人民医院内分泌科,河南 新乡 453000;2.新乡市中心医院呼吸内三科,河南 新乡 453000;3.新乡医学院第一附属医院呼吸科,河南 新乡 453100)
随着人们生活方式的改变,糖尿病患病率逐年增加,其中以2型糖尿病(type 2 diabetes mellitus,T2DM)更为显著,约占糖尿病患病总数的95%~97%[1],已成为继心脑血管疾病、肿瘤之后危害人类健康的重要慢性疾病之一。而约80%的T2DM患者属于超重或者肥胖者,肥胖曾被认为是联系T2DM和阻塞性睡眠呼吸暂停综合征(obstructive sleep apnea hypopnea syndrome,OSAHS)的纽带,三者的相关性不容忽视,常伴随出现。近年来,肥胖T2DM患者并发OSAHS成为研究热点,国内外研究证实,T2DM、OSAHS与肥胖症在发病机制上存在很多共同点,其中以脂类代谢紊乱及胰岛素抵抗最为显著[2-4]。临床工作中,口服降糖药物血糖控制不佳的T2DM合并OSAHS肥胖患者,联合胰岛素治疗可以有效降低血糖,但同时会增加患者体质量,从而增加心脑血管疾病的发病风险[5]。此类患者主要以减轻体质量、改善通气、增强机体胰岛素敏感性及改善胰岛素抵抗为主,经典的降糖方案往往难以达到改善以上指标的预期效果。有研究发现,人胰高血糖素样肽-1(glucagon-like peptide 1,GLP-1)的类似物艾塞那肽作为一种治疗T2DM的新药被应用于临床[6-7]。艾塞那肽的作用机制包括:有效控制血糖、改善β细胞功能,调节脂代谢、促进脂肪分解、减轻体质量并延缓胃排空。艾塞那肽是首个通过美国食品药品监督管理局批准的GLP-1受体激动剂,目前已被广泛应用于T2DM的治疗,而艾塞那肽对于OSAHS的影响,目前国内外研究数据较少。故本研究通过对40例T2DM合并OSAHS肥胖患者治疗前后指标变化情况的观察,来探讨艾塞那肽治疗OSAHS的效果。
1 资料与方法
1.1一般资料选择2014年8月至2016年8月新乡市第一人民医院内分泌科收治的T2DM合并OSAHS肥胖患者80例,男52例,女28例;年龄30~68(50.2±7.3)岁;病程1~10(7.1±2.2)a。纳入标准:体质量指数(body mass index,BMI)≥28 kg·m-2;空腹血糖(fasting blood glucose,FBG)水平为7.0~16.0 mmol·L-1,糖化血红蛋白(glycosylated hemoglobin,HbA1C)水平为7.5%~13.0%,肾功能正常,符合OSAHS临床诊断[8];无心、脑、肾等重要脏器损害及胃肠吸收功能不良。排除标准:1型糖尿病;糖尿病酮症酸中毒;严重肝肾功能不全患者;妊娠和哺乳期妇女;病毒性肝炎、药物、乙醇、Wilson病、全胃肠道外营养等引起的特殊脂肪肝疾病;严重脂代谢紊乱及其他内分泌性疾病;过度运动或应用影响糖代谢的药物;肝脏肿瘤、感染、胆道疾病、药物引起的肝酶升高;有胰腺炎病史、大量饮酒;精神异常以及对试验药物过敏的患者。采用随机数字表法将患者分为观察组和对照组,每组40例。2组患者均自愿参加本研究并签署知情同意书。观察组:男27例,女13例,年龄(48.0±6.2)岁,病程(7.0±1.2)a,BMI(30.9±4.3)kg·m-2,腰围(90.8±6.8)cm,FBG(12.2±1.2)mmol·L-1,HbA1C(11.2±1.1)%,总胆固醇(total cholesterol,TC)(6.6±1.4)mmol·L-1,三酰甘油(triglyceride,TG)(4.3±0.7)mmol·L-1,呼吸暂停低通气指数(apnea hypopnea index,AHI) (31.2±13.0)次·h-1,Epworth嗜睡量表(Epworth sleepiness scale,ESS)评分为12.8±5.4,睡眠最低血氧饱和度(the lowest pulse oxygen saturation in sleep,LSpO2)为(69.3±6.9)%;对照组:男25例,女15例,年龄(49.0±6.8)岁,病程(6.8±1.0)a,BMI(29.5±4.2)kg·m-2,腰围(91.6±7.5)cm,FBG(12.2±1.0)mmol·L-1,HbA1C(11.6±1.2)%,TC(6.1±1.2)mmol·L-1,TG(4.4±0.8)mmol·L-1,AHI (30.6±11.2)次·h-1,ESS评分为13.3±5.2、LSpO2为(70.1±8.1)%;2组患者上述各指标比较差异均无统计学意义(P>0.05)。
1.2治疗方法对照组患者给予盐酸二甲双胍片(中美上海施贵宝制药有限公司,国药准字H20023370)850 mg,口服,每日2次;观察组患者在对照组治疗的基础上加用艾塞那肽(美国 Baxter Pharmaceutical Solutions LLC,注册证号 H20140821),前4周每次5 μg,早、晚餐前1 h以上皮下注射,每日2次,之后改为每次10 μg,早、晚餐前1 h以上皮下注射,每日2次,2组疗程均为24周。
1.3睡眠监测受试者监测当日未服用镇静剂、咖啡及浓茶等。睡眠呼吸监测由专人完成。受试者使用便携式睡眠监测仪(ApneaLinkTM澳大利亚瑞斯迈公司)进行睡眠监测,由机器专用软件分析相关数据。
1.4观察指标分别于治疗前后留取2组患者肘静脉血5 mL,采用全自动生物化学分析仪(日本希森美康株式会社)检测外周血FPG、餐后2 h血糖(2-hour postprandial blood glucose,2 hPPBG)、TG及TC水平,采用高效液相层析柱法检测HbA1C水平;BMI、腰围;采用便携式睡眠监测仪监测2组患者治疗前后的AHI和LSpO2。
2 结果
2.12组患者治疗前后血糖水平比较结果见表1。治疗前2组患者HbA1C、FPG、2 hPBG水平比较差异均无统计学意义(P>0.05);治疗后2组患者HbA1C、FPG、2 hPBG水平均较治疗前明显下降,差异有统计学意义(P<0.05);治疗后,观察组患者HbA1C、FPG、2 hPBG水平显著低于对照组,差异有统计学意义(P<0.05)。
表12组患者治疗前后血糖指标比较
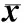

注:与治疗前比较aP<0.05;与对照组治疗后比较bP<0.05。
2.22组患者治疗前后BMI、腰围及TC、TG水平比较结果见表2。治疗前2组患者的BMI、腰围及TC、TG水平比较差异均无统计学意义(P>0.05);治疗后2组患者BMI、腰围及TC、TG水平均较治疗前明显下降,差异有统计学意义(P<0.05);治疗后,观察组患者BMI、腰围及TC、TG水平均显著低于对照组,差异有统计学意义(P<0.05)。
表22组患者治疗前后BMI、腰围及TC、TG水平比较
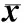

注:与治疗前比较aP<0.05;与对照组治疗后比较bP<0.05。
2.32组患者治疗前后呼吸功能参数比较结果见表3。治疗前2组患者AHI、ESS评分及SpO2、LSpO2水平比较差异均无统计学意义(P>0.05);治疗后2组患者AHI、ESS评分及SpO2、LSpO2水平均较治疗前明显下降,差异有统计学意义(P<0.05);治疗后,观察组患者AHI、ESS评分及SpO2、LSpO2水平均显著低于对照组,差异有统计学意义(P<0.05)。
表32组患者治疗前后呼吸功能参数对比
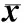
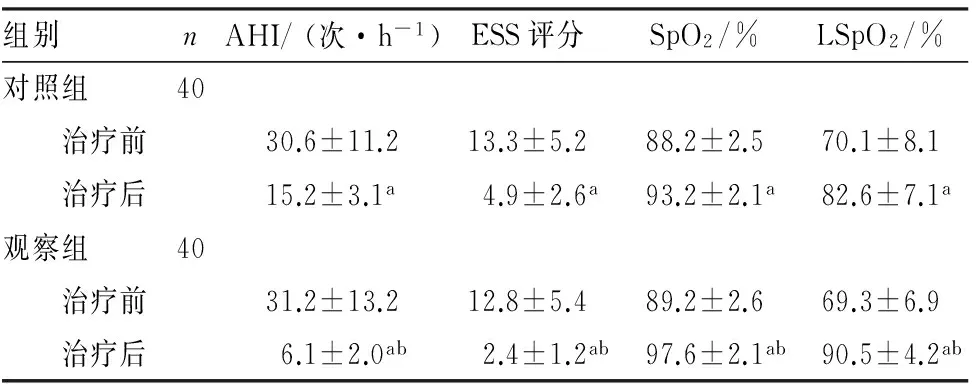
注:与治疗前比较aP<0.05;与对照组治疗后比较bP<0.05。
2.4不良反应2组患者均无严重低血糖事件发生。观察组患者出现恶心1例,呕吐1例,腹泻1例,不良反应发生率为7.5%(3/40);对照组患者出现恶心1例,呕吐1例,不良反应发生率为5.0%(2/40);2组患者不良反应发生率比较差异无统计学意义(χ2=6.320,P>0.05)。随着用药时间的推移,消化道症状逐渐减轻、消失,部分患者消化道症状可持续整个治疗过程中,但均可耐受,无需特殊处理。
3 结论
OSAHS是由于各种原因导致上呼吸道部分或全部阻塞,扰乱睡眠过程的正常通气和睡眠结构而引起的一系列病理生理变化,其主要的病理生理基础为睡眠过程中出现的间歇性呼吸暂停,夜间反复发生低氧血症、高碳酸血症和睡眠结构紊乱,导致内环境紊乱,同时影响到交感神经系统及下丘脑-垂体-肾上腺轴,使皮质醇等升高血糖的激素分泌增加[9-10]。患者发生OSAHS时,交感神经过度兴奋,瘦素分泌减少,胰岛素分泌增加,加重胰岛素抵抗。患者夜间睡眠质量下降,白天嗜睡,这种不良生活习惯,也会加重胰岛素抵抗,以上机制导致血糖进一步升高,导致T2DM的发生。80%的T2DM患者合并肥胖[11],肥胖导致颈部脂肪堆积,上呼吸道狭窄或塌陷,进而引起通气障碍,睡眠中更为严重,合并OSAHS时,如不及时进行纠正,心脑血管疾病的发病率明显增加。
T2DM 传统的降糖方式可能会引起低血糖、体质量增加及心血管疾病风险增高等。对于T2DM合并OSAHS的肥胖患者,传统方案更难以达到减轻体质量、有效降糖、改善通气的目的。对于T2DM伴OSAHS肥胖患者,减轻体质量具有十分重要的意义。艾塞那肽为此类糖尿病患者提供了一个新的治疗选择。研究证实,艾塞那肽能够抑制β细胞凋亡、增加β细胞数量、恢复β细胞功能,并改善第1时相胰岛素分泌、增加β细胞最大胰岛素分泌能力和调节胰高血糖素分泌;艾塞那肽还能抑制食欲,减轻体质量[12]。艾塞那肽的临床效果也在本研究中得到了证实,本研究中,对于T2DM合并OSAHS肥胖患者,在传统口服降糖药物二甲双胍的基础上加用艾塞那肽,积极治疗24周后,2组患者的血糖指标FBG、2 hPBG、HbA1C,心脑血管疾病风险因子指标如BMI、腰围、TC、TG及呼吸功能参数如AHI、ESS评分、SpO2和LSpO2等指标均较治疗前好转,且观察组较对照组好转更明显,差异均有统计学意义。2组患者不良反应发生率比较差异无统计学意义。
综上所述,对于T2DM合并OSAHS肥胖患者,艾塞那肽在降低血糖的同时,可明显减轻体质量,调节脂代谢、改善患者通气功能、纠正睡眠呼吸暂停低通气综合征,且低血糖反应发生率低,值得临床推广应用。
[1] GUSTAVSSON N,SEAJL T,LAO Y,etal,Delayed onset of hyperglycaemia in a mousemodel with impaired glucagon secretion demonstrates that dysregulated glucagon secretion promotes hyperglycaemia and type 2 diabetes[J].Diabetologia,2011,54(2):415-422.
[2] 林其昌,黄建钗,丁海波,等.福州市20岁以上人群阻塞型睡眠呼吸暂停低通气综合征流行病学调查[J].中华结核和呼吸杂志,2009,32(3):193-197.
[3] MARIN J M,CARRIZO S J,VICENTE E,etal.Long-tem cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure:an observational study[J].Lancet,2005,365(9464):1046-1053.
[4] YAMAUCHI M,NAKANO H,MAEKAWA J,etal.0xidative stress in obstructive sleep apnea[J].Chest,2005,27(5):1674-1679.
[5] 蒋建家,牟伦盼,苏劲波,等.艾塞那肽对口服降糖药治疗欠佳的肥胖2型糖尿病患者的疗效及安全性[J].中华糖尿病杂志,2011,3(4):305-308.
[6] ARAKAWA M,EBATO C,MITA T,etal.Effects of exendin-4 on glucose tolerance,insulin secretion,and beta-cell proliferation depend on treatment dose,treatment duration and meal content[J].BiochemBiophysRescommun,2009,390(3):809-814.
[7] 胡俊鹏,王涛,翁孝刚.利拉鲁肽和艾塞那肽对面型糖尿病肾病大鼠肾脏结构和功能的影响[J].新乡医学院学报,2017,34(4):255-260.
[8] ZSUGA J,GESZTELYI R,KEMENY-BEKE A,etal.Different of hyperglycemia on stroke outcome in non-diabetic and diabetic patients:a cohort study[J].NeumlRes,2012,34(1):72-79.
[9] 中华医学会儿科学分会呼吸学组睡眠协作组《中华实用儿科临床杂志》编辑委员会.无创正压通气治疗儿童阻塞性睡眠呼吸暂停综合征专家共识(草案)[J].中华实用儿科临床杂志,2016,31(19):1451-1455.
[10] 张静,李平华.阻塞性睡眠呼吸暂停综合征与青光眼的关系[J].眼科新进展,2014,34(8):790-793.
[11] SEINO Y,YABE D.Glucose-dependent insulinotropic polypeptide and glucagon-like peptide-1:incretin actions beyond the pancreas[J].JDiabetesInvestige,2013,4(2):108-130.
[12] NADKARNI P,CHEPURNY O G,HOLZ G G.Regulation of glucose homeostasis by GLP-1[J].ProgMolBiolTranslSci,2014,121:23-65.
