铀钛合金表面镍锌复合镀层的组织结构与耐蚀性能
2018-01-13柏艳辉靳涛唐清富文明刘侠和苏斌李文鹏
柏艳辉,靳涛,唐清富,文明,刘侠和,苏斌,李文鹏, *
(1.中国工程物理研究院材料研究所,四川 江油 621908;2.东北大学冶金学院,辽宁 沈阳 110004)
铀钛合金作为一种重要的工程材料,在能源和军事领域得到了广泛的应用[1],其中钛元素的添加量虽少,但能显著改善合金的机械性能。然而,铀的原子核外电子构型(5f36d17s2)决定了它具有较为活泼的化学性质,容易与环境(尤其是沿海及工业地区)中的活性介质发生化学、电化学作用而造成铀钛合金的腐蚀[2-4]。
为了减缓铀钛合金的腐蚀,同时防止放射性污染,防腐蚀保护层受到了国内外研究者的极大关注[5],这些研究主要集中在氧化膜[6]、有机涂层[7]及金属镀层[8-9]三方面。其中,电镀是研究最早、工业应用最为广泛的技术。在过去的半个世纪里,国内外研究人员对铀钛合金电镀进行了大量实验。在众多的镀层工艺中,Ni镀层[10-11]、Zn−Ni合金镀层[12-13]以及Ni+Zn复合镀层[8,14]在铀钛合金的防腐蚀应用中较具可行性。Ni镀层主要起到对环境中腐蚀介质的物理屏障作用,孔隙率决定了该镀层的防护性能,不能对铀钛合金基体提供长期有效的保护。Zn−Ni合金镀层孔隙率低,但其成分及均匀性较难控制。Ni+Zn复合镀层结合了电镀镍和电镀锌的各自优点,在美国空军的GAU-8/A机炮中得以成功应用[14]。但从已报道的情况来看,该复合镀层以往都是在氨基磺酸盐镀镍之后采用氰化物体系镀锌,对环境污染严重。因此,有必要从镀层防护性能的有效性及施镀过程的环境友好性两方面出发,对铀钛合金表面电镀进行相关研究。
本文通过电镀的方法在铀钛合金表面首先制备了一层Ni镀层,然后在无氰碱性镀锌液中制备了Zn镀层,并通过光学显微镜、扫描电镜、湿热腐蚀试验及电化学测量,对Ni+Zn复合镀层的组织结构及耐蚀性能进行研究。
1 实验
1.1 样品制备
铀钛合金试样的名义成分为U-0.75Ti,时效态,杂质总含量<0.4%,直径20 mm,长5 mm,经逐级打磨至1200#后采用1 400 g/L的FeCl3溶液进行蚀刻,再以硝酸清洗[15],随后电镀,最后采用铬酸溶液钝化并烘干。
电镀镍的溶液组成及工艺条件为:Ni(NH2SO3)2·4H2O 380 ~ 420 g/L,H3BO330 ~ 35 g/L,NiCl2·6H2O 7 ~ 10 g/L,分散剂 0.05 ~ 0.10 g/L,温度 45 ~ 50 °C,阴极电流密度 1 ~ 2 A/dm2,时间 36 ~ 40 min。
电镀锌的溶液组成及工艺条件为:ZnO 18 ~ 22 g/L,NaOH 80 ~ 100 g/L,添加剂15 ~ 20 mL/L,室温,阴极电流密度 2 ~ 3 A/dm2,时间 45 ~ 50 min。
钝化溶液组成及工艺条件为:CrO3180 ~ 200 g/L,H2SO410 ~ 12 mL/L,HNO318 ~ 20 mL/L,室温,6 ~ 10 s。
1.2 测试表征
采用截面观察法对镀层厚度进行原位测量。用中科科仪的KYKY-1010B扫描电子显微镜对试样表面镀层的微观形貌进行观察,加速电压为25 kV。
在 Cincinnati Sub-Zero的 EZT-570i型湿热腐蚀试验箱中进行湿热环境下的加速腐蚀实验,温度约70 °C,相对湿度80%,500 h后用扫描电镜观察样品的表面微观形貌。
通过失重法考察试样的腐蚀速率。将试样全浸泡在含50 μg/g Cl−的NaCl水溶液[9]中,过一段时间后取出并记录试样变化,试样用蒸馏水与酒精先后清洗后烘干并称重,电子天平的精度为0.01 mg。
采用普林斯顿PARSTAT 4000电化学综合测试仪对试样的开路电位(OCP)进行测试,试样为工作电极(暴露面积为1 cm2),饱和甘汞电极(SCE)为参比电极,铂片为辅助电极,腐蚀介质为含50 μg/g Cl−的NaCl水溶液,室温,测试时间为4 000 s。
2 结果与讨论
2.1 组织形貌分析
U–0.75Ti合金试样电镀镍和锌之后,在金相显微镜下对镀层截面进行观察,如图1所示。从中可以明显看出合金表面有两层镀层,利用图中比例尺测得镍镀层厚度约25 μm,锌镀层厚度约12 μm,总的镀层厚度约为37 μm。

图1 U–0.75Ti合金表面Ni/Zn复合镀层的截面形貌Figure 1 Cross-sectional morphology of Ni/Zn coatings on U–0.75Ti alloy surface
由图2可知,U–0.75Ti合金表面Ni镀层晶粒细小,球状沉积物颗粒之间衔接紧密,但也存在少量的孔洞(见图2a右上角);在Ni镀层表面电镀的Zn层致密,无孔洞,但表面分布着细小的白色颗粒物,这可能是Zn镀液中的ZnO粉末或其他杂质在电镀过程中沉积并吸附在镀层表面所致;铬酸钝化后可获得带龟裂纹的钝化膜,它是一层由碱式铬酸盐、Cr2O3等难溶物组成的薄膜[16]。
2.2 开路电位分析
电极电位随时间的变化曲线对研究镀层的耐蚀性能,分析镀层的腐蚀过程具有重要意义。图3是U–0.75Ti试样在50 μg/g Cl−水溶液中的开路电位随时间的变化曲线。随着时间的推移,3种试样的开路电位均趋于稳定。在4 000 s时,Ni+Zn复合镀层的开路电位稳定在−0.75 V左右,U–0.75Ti合金基体的开路电位稳定在−0.61 V附近,而Ni镀层(厚度约为25 μm)的开路电位大约在−0.21 V附近。在浸泡过程中,Ni+Zn复合镀层的开路电位均较裸露的U–0.75Ti合金低,说明相对于U–0.75Ti合金基体,复合镀层是阳极性保护镀层,表面的Zn钝化层在腐蚀过程中优先发生电化学腐蚀,对基体起到保护作用,而Ni镀层的开路电位比U–0.75Ti合金基体的开路电位要高,说明Ni镀层是阴极性保护镀层,其防护性能基于镀层的致密性,对基体起到物理屏障作用。此外,带Ni+Zn复合镀层试样的开路电位表现出先减小后增大,最后趋于稳定的变化过程,这与试样表面钝化膜在腐蚀介质中具有一定的自修复能力有关[17]。

图2 U–0.75Ti合金表面镀层的表面形貌Figure 2 Surface morphologies of the coatings on U–0.75Ti alloy

图3 U–0.75Ti合金及其表面分别电镀Ni单层和Ni/Zn复合层后在50 μg/g Cl−水溶液中的开路电位随时间的变化Figure 3 Variation of open circuit potential with time in 50 μg/g Cl− aqueous solution for U–0.75Ti alloy before and after being electroplated with a single Ni coating and Ni+Zn coatings, respectively
2.3 腐蚀速率分析
室温条件下,U–0.75Ti合金及其电镀试样在50 μg/g Cl−溶液中单位面积的失重以及浸泡过程中的平均腐蚀速率随时间的变化情况如图4所示。
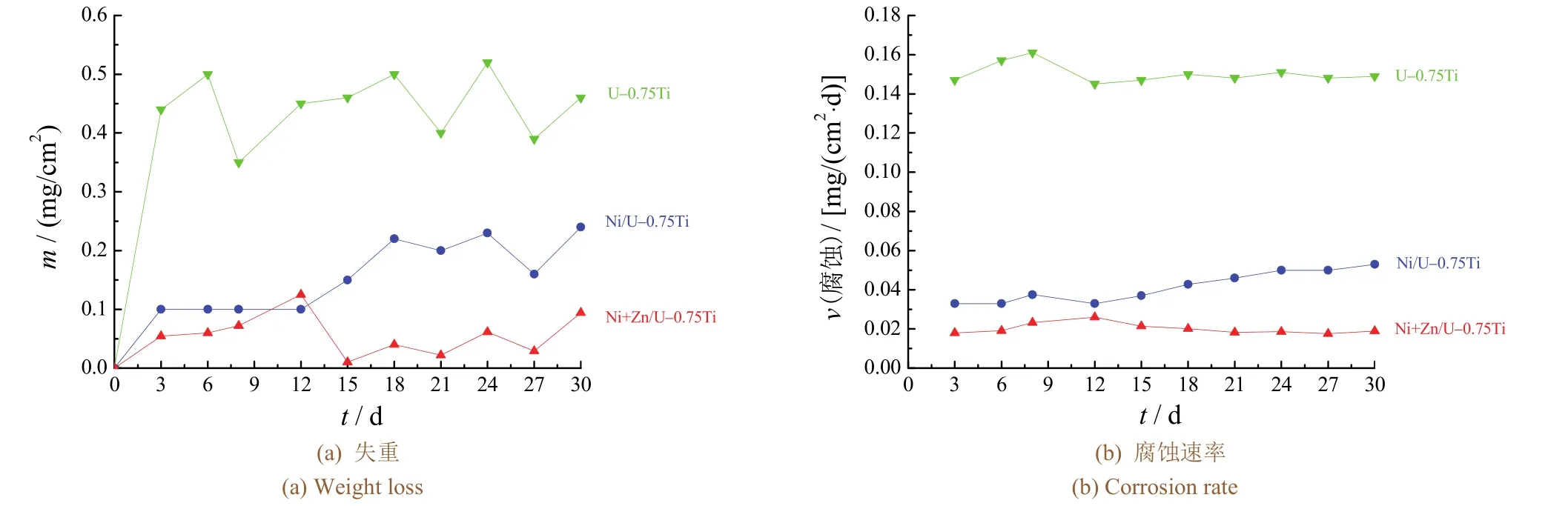
图4 U–0.75Ti合金及其表面分别电镀Ni单层和Ni/Zn复合层后在25 °C的50 μg/g Cl−溶液中的失重和腐蚀速率随时间的变化Figure 4 Variation of weight loss and corrosion rate with time in 50 μg/g Cl− aqueous solution at 25 °C for U–0.75Ti alloy before and after being electroplated with a single Ni coating and Ni+Zn coatings, respectively
没有镀层的U–0.75Ti合金样品在腐蚀介质中的失重在浸泡初期迅速增加并很快达到基本稳定,但在后续浸泡过程中腐蚀失重曲线有较大波动。同时,基体试样的平均腐蚀速率最大,在浸泡过程中表现出缓慢降低的趋势。这是由于表面腐蚀生成的疏松氧化物能在一定程度上阻止腐蚀,使腐蚀速率降低,但是这种效果有限,当氧化物膜层被破坏后,腐蚀速率又加大。如此反复,腐蚀产物膜层越来越厚。
Ni镀层样品的腐蚀速率整体较基体材料小。腐蚀失重曲线在腐蚀初期有较大增加后稳定了一段时间,这体现了Ni镀层对腐蚀介质的阻隔作用。但随着腐蚀的进行,腐蚀介质通过Ni镀层中的孔道到达基体/镀层界面,Ni镀层的腐蚀电位比基体的腐蚀电位高造成了局部电偶腐蚀,样品的腐蚀会加快,表现为12 d后平均腐蚀速率有一定增大。
带Ni+Zn复合镀层试样的平均腐蚀速率最低,浸泡12 d后其腐蚀动力学曲线呈现缓慢降低的趋势,这是由于当膜层受到破坏后,铬酸盐钝化膜表现出一定的自修复能力,保护了膜层的完整性,这与前述实验分析结果一致。
所有镀层样品的腐蚀动力学曲线均位于 U–0.75Ti合金腐蚀动力学曲线的下方,这表明 Ni镀层和Ni+Zn复合镀层均能对铀钛合金提供良好的保护,但它们的防护机理有所不同。从有效性来看,Ni+Zn复合镀层更佳。
2.4 耐湿热加速腐蚀性能
3种是试样在湿热腐蚀前后的宏观形貌对比见图5。通过SEM来表征湿热腐蚀后试样的表面微观形貌,结果如图6所示。

图5 原始及分别镀了单一Ni层和Ni/Zn复合镀层的U–0.75Ti合金在湿热腐蚀前(左)后(右)的外观Figure 5 Appearance of U–0.75Ti alloy and that electroplated with a single Ni coating or Ni+Zn coatings before (left) and after (right)damp heat corrosion test

图6 原始及分别镀了单一Ni层和Ni/Zn复合镀层的U–0.75Ti合金在湿热腐蚀后的微观形貌Figure 6 Microscopic morphologies of U–0.75Ti alloy and that electroplated with a single Ni coating or Ni/Zn coatings after damp heat corrosion test
湿热试验前,U–0.75Ti合金试样因在大气中存放而已经有一定程度的氧化;湿热试验后,其表面呈现黑色以及疏松的多孔状,说明腐蚀较为严重。Ni镀层试样的沉积物晶粒之间衔接较为紧密,湿热腐蚀试验后表面无鼓泡、起皮等不良现象,宏观形貌变化较小,说明Ni镀层抗湿热氧化腐蚀性能较优且稳定,有一定厚度的致密Ni镀层对U–0.75Ti合金基体具有良好的抗腐蚀作用。
Ni+Zn复合镀层在湿热氧化腐蚀之后失去原有光泽,表面出现形状不规则的腐蚀斑点,但无鼓泡、起皮等不良现象的发生。这是由于在湿热腐蚀过程中,环境中的氧和水汽与表面钝化层反应,在钝化膜的薄弱处优先发生腐蚀,生成氧化物、氢氧化物等疏松的腐蚀产物,导致点蚀微孔的出现。在腐蚀试验初期,锌钝化层在水环境中具有一定的自修复作用,可有效减缓复合镀层试样表面腐蚀斑点的出现。但当钝化层薄弱部分遭到破坏后,一般认为该复合镀层的腐蚀过程遵循溶解沉降机理[18]。Zn作为阳极不断溶解形成小孔,同时Zn2+离子与环境中的OH−离子在小孔周围生成Zn(OH)2沉淀。随着湿热腐蚀的继续进行,这些腐蚀产物逐渐扩展、破裂、剥落,最终将贯穿至Ni镀层/Zn镀层界面,导致Zn层失效。
3 结论
采用氨基磺酸盐镀镍与无氰碱性镀锌工艺在U–0.75Ti合金表面获得了总厚度约为37 μm的Ni+Zn复合镀层。在70 °C、相对湿度80%的条件下湿热腐蚀500 h后,该复合镀层的微观形貌仍较为完整;在含50 μg/g Cl−的电解质溶液中,该复合镀层具有比单一Ni镀层更低的腐蚀速率,对U–0.75Ti合金的保护作用更优。
[1]GREENHOLT C J, WEIRICK L J.The oxidation of uranium–0.75 wt% titanium in environments containing oxygen and/or water vapor at 140 °C [J].Journal of Nuclear Materials, 1987, 144 (1/2): 110-120.
[2]王庆富, 张鹏程, 王晓红, 等.贫铀表面脉冲电镀镍的电化学腐蚀行为[J].材料保护, 2007, 40 (3): 7-10.
[3]张延志.八氧化三铀和金属铀表层结构的XRD研究[D].绵阳: 中国工程物理研究院, 2003.
[4]SHI P, LI F F, WU Y P, et al.Effect of alloyed Ti on the microstructure and corrosion characteristics of a U–Ti alloy in a hydrogen environment [J].Corrosion Science, 2015, 93: 58-62.
[5]王庆富.铀上脉冲电镀镍的组织结构与性能研究[D].绵阳: 中国工程物理研究院, 2003.
[6]WEIRICK L J.Evaluation of metallic coatings for the corrosion protection of a uranium–3/4 weight percent titanium alloy [R].Livermore, CA: Sandia Laboratories, 19744.
[7]WEIRICK L J.Protective coatings for uranium alloys [C]// Proceedings of the Conference on Physical Metallurgy of Uranium Alloys, Vail, Colorado, USA,12 Feb 1974.Albuquerque, NM: Sandia Laboratories, 1974.
[8]赵文轩, 杨俊琴, 李冠兴.铀钛合金上镍/锌组合镀层工艺研究[C]// 中国核学会核材料会议论文集.[出版地不详]: 中国核学会, 1993: 17-25.
[9]ZHU S F, CHEN L, WU Y P, et al.Microstructure and corrosion resistance of Cr/Cr2N multilayer film deposited on the surface of depleted uranium [J].Corrosion Science, 2014, 82: 420-425.
[10]WEIRICK L J, LYNCH C T.Corrosion resistant coatings for uranium and uranium alloys [C]// Proceedings of Corrosion’77 NACE Meeting, San Francisco,CA, USA, 14 Mar 1977.Livermore, CA: Sandia Laboratories, 1977.
[11]WEIRICK L J, JOHNSON H R, DINI J W.Corrosion and protection of uranium alloy penetrators [R].Livermore, CA: Sandia Laboratories, 1975.
[12]DINI J W, JOHNSON H R.Corrosion resistance of zinc–nickel plated uranium/0.75 titanium alloy [J].Metal Finishing, 1980, 78 (8): 45-48.
[13]DINI J W, JOHNSON H R.Electrodeposition of zinc–nickel alloys coatings [C/OL]// Proceedings of the Workshop on Alternatives for Cadmium Electroplating in Metal Finishing, Gaithersburg, MD, USA, 4 Oct 1977.Albuquerque, NM: Sandia Laboratories, 1977.(2014–05–28) [2017–10–25].https://www.osti.gov/scitech/servlets/purl/5245172.
[14]WEIRICK L J.Corrosion testing of the General Electric Mantech GAU 8/A penetrator [R].Albuquerque, NM: Sandia Laboratories, 1977.(2010–10–15)[2017–10–25].http://prod.sandia.gov/techlib/access-control.cgi/1976/768055.pdf.
[15]DINI J W, JOHNSON H R.Plating on some difficult-to-plate metals and alloys [J].Plating and Surface Finishing, 1981, 68 (10): 64-69.
[16]卢燕平, 何英, 孟惠民, 等.锌镍合金镀层的铬酸盐钝化[J].北京科技大学学报, 1994, 16 (增刊): 27-31.
[17]张宏祥, 王为.电镀工艺学[M].天津: 天津科学技术出版社, 2002.
[18]施彦彦, 张昭, 张鉴清, 等.锌及其合金的大气腐蚀研究现状[J].中国腐蚀与防护学报, 2005, 25 (6): 373-379.
