丹酚促吸收剂及滴丸制备研究
2018-01-12赵风至陈思思刘利根石心红
赵风至,陈思思,刘利根,石心红
(中国药科大学中药制剂教研室,南京 211198)
丹酚(salvianolic)是从唇形科植物丹参(SalviamiltiorrhizaBge.)的干燥根及根茎中提取的一类既有咖啡酞缩酚酸结构又有新木脂素骨架的全水溶性成分,现代药理研究表明,丹酚具有抗血小板聚集、抗血栓形成、改善微循环、抗氧化损伤和多途径发挥心肌保护等作用[1-2]。
滴丸剂是基于固体分散体原理,将药物高度分散于水溶性基质中,有利于药物溶出,提高吸收率,同时减少胃肠道刺激性,便于携带和服用[3]。近年来丹参滴丸的研究不断深入和发展,但丹酚类易氧化,肠道吸收较差,口服吸收生物利用度低,寻找合适的促吸收剂对丹酚类的药剂学研究具有重要价值。癸酸钠(sodium caprate,SC)作为一种低毒高效的细胞旁路促吸收剂,已在瑞典、丹麦和日本的氨苄西林(axlium ampicillin)栓剂中应用[4]。研究表明,癸酸钠对丹酚类成分也有促吸收作用,但促吸收质量浓度较高,作为制剂辅料有待进一步筛选[5-6]。本实验考察了不同质量浓度癸酸钠对丹酚的促吸收效果,从提高制剂载药量的角度优选适宜的质量浓度,为其工业化生产提供研究基础。
1 仪器与材料
1.1仪器 DWJ-2000S型多功能滴丸实验机(烟台百药泰中药科技发展有限公司);Agilent HP1100(DAD检测器,安捷伦科技有限公司);BJ-1型崩解时限测试仪(天津市国铭医药设备有限公司);CPA225D十万分之一电子天平(赛多利斯科学仪器有限公司);恒流蠕动泵(上海沪西分析仪器厂有限公司);调速糖衣锅(江苏泰州市制药机械二厂)。
1.2试药 丹酚(自制,质量分数>75%);癸酸钠(南京宸翔医药研究有限责任公司,AR);Krebs-Ringer磷酸缓冲液(K-R缓冲液,pH值为6.0,河南标物生物科技有限公司);乙腈(TEDIA,南京晚晴化玻仪器有限公司);PEG6 000、PEG4 000(辽宁奥克医药辅料);二甲基硅油HTS-201(无锡花厅化工材料有限公司);石油醚(无锡市亚盛化工有限公司,60~90 ℃);欧巴代薄膜包衣预混剂(上海卡乐康包衣技术有限公司,胃溶型);纯化水(自制)。
1.3动物 雄性SD大鼠200~250 g,许可证:SCXK(沪)2013-0006。
2 方法与结果
2.1癸酸钠促吸收质量浓度筛选
2.1.1色谱条件及方法学考察 HPLC色谱条件:色谱柱:Kromasil C18柱(250 mm×4.6 mm,5 μm),流动相:乙腈(A相)-0.5 mL·L-1磷酸水(B相),梯度:0 min:19%A,81%B;15 min:23%A,77%B;30 min:25%A,75%B;40 min:90%A,10%B,45 min:90%A,10%B。检测波长:286 nm;流速:1.0 mL·min-1;柱温:35 ℃;进样体积:20 μL。
分别参照《中国药典》及文献[7-8]进行方法学验证,丹酚各成分在该条件下线性良好,精密度实验RSD值均小于2%,供试品溶液12 h内较稳定,各成分的加样回收率为99.31%~101.16%,RSD<2%,说明该方法准确度高,重复性好,专属性强。
2.1.2肠灌流液 本实验采用大鼠在体分肠段单向肠灌流实验[9],结合文献方法[10]初步考察了丹酚、丹酚+0.08 g·L-1SC、丹酚+0.2 g·L-1SC和丹酚+0.8 g·L-1SC在大鼠十二指肠、空肠和回肠的吸收情况,丹酚质量浓度均为0.8 g·L-1,结果见表1。
2.1.3在体肠灌流 取自由饮水禁食12 h的SD大鼠,腹腔注射200 g·L-1乌拉坦(1.0 g·kg-1)。待翻正反射消失,沿腹中线剪开3~4 cm的开口,小心分离出待考察肠段,于切口两端分别插管,并结扎固定,用37 ℃生理盐水冲洗肠段内容物,再用供试药液平衡,先以1.0 mL·min-l灌流10 min,然后将流速降至0.2 mL·min-l,开始计时,30 min后,进口处用装有供试液的已知质量的具塞小瓶灌流,出口处用另一已知质量的具塞小瓶收集,分别于记时后的45,60,75,90和105 min迅速更换供试小瓶和收集小瓶,称定其质量,计算灌入和收集的供试液质量,灌流液中取样1.0 mL,经0.45 μm的微孔滤膜过滤用于丹酚有效部位含量测定。实验结束后,将大鼠处死,剪下灌流的肠段,测量并记录其长度。
实验大鼠小肠段分为3段:自幽门以下1 cm处向下取10 cm为十二指肠段;幽门以下15 cm向下取10 cm为空肠段;盲肠上端20 cm向下取10 cm为回肠段。

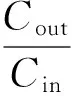
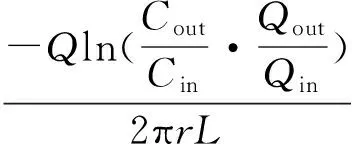
Qin和Qout分别为肠道进出口灌流液的体积(假定液体密度为1.0 g·mL-1);Cin和Cout分别为肠道进出口灌流液的质量浓度(μg·mL-1);L为灌流肠段的长度(cm);r为灌流肠段的横截面半径(cm);Q为灌流速度(0.2 mL·min-1);V为灌流肠段的体积,为πr2L。实验数据分析结果见表1。
表1不同质量浓度癸酸钠(SC)对丹酚的促吸收数据分析

Tab.1 Analysis of different concentrations of SC for the absorptin of salvianol (n=3,±s)
数据显示,质量浓度为0.08 g·L-1SC对丹酚在大鼠各肠段均无促吸收作用;质量浓度为0.2 g·L-1SC及0.8 g·L-1SC配伍丹酚在3个肠段促吸收倍数分别为0.71,1.41和1.10倍及0.60,1.64和1.17倍,回肠和空肠的促吸收明显优于十二指肠,癸酸钠质量浓度越高,促吸收越显著,考虑到促吸收剂作为辅料加入,直接影响制剂载药量,综合比较促吸收情况和载药量,选择了质量浓度为0.2 g·L-1SC作为滴丸制剂的促吸收剂用量,即占主药量的25%。
2.2丹酚滴丸处方工艺优化
2.2.1滴制评价 以滴制情况(滴速、拖尾、黏连)及滴丸外观(圆整度、硬度)为指标,评价滴制效果[11-12],以丸质量差异、崩解时限优选处方,具体评价标准见表2。丸质量差异及崩解时限按照《中国药典》2015年版[13]四部通则0108进行,丸质量差异得分:差异范围之内的丸数量/20×30。
表2滴制评分标准
Tab.2 Drops grading system

评分指标滴速拖尾黏连圆整度硬度1极慢严重严重类圆形轻压变形2慢略有拖尾略有黏连扁圆或椭圆重压变形3极快少数拖尾少数黏连圆球有空洞重压略变形4快极少数拖尾极少数黏连较好较好5适宜无拖尾无黏连好好
2.2.2单因素筛选 (1)基质:滴丸剂的基质考察了PEG4 000、PEG6 000以及两者一定比例的混合物,以熔融法制备药液。以药物与基质混合后熔融药液的黏稠度、滴制情况、滴丸圆整度和溶散时限等为指标,进行基质的筛选。结果单用PEG6 000时,药液黏稠,滴制差,且崩解慢;单用PEG4 000时滴制好,但滴丸硬度低;PEG6 000∶PEG4 000=1∶3时,药液均匀,滴制较好,硬度适宜,故选择基质组成为PEG6 000∶PEG4 000=1∶3。
(2)冷凝剂:考察了滴丸药液在相同高度的液体石蜡、蓖麻油、二甲基硅油中的沉降及成形情况,结果发现,滴丸在液体石蜡中沉降过快,不易固化成形,黏连严重;蓖麻油中沉降过慢,易拖尾,圆整度低;二甲基硅油中沉降适宜,圆整度高,故选择二甲基硅油作为冷凝剂。
(3)药质比:不加水时药物粉末和基质难以混熔,药物易抱团析出,药质比为1∶10时仍然不能滴制;适量加水(8%左右[14],加水过多,难以固化成形;加水太少,药液流动性差,滴制差)后,药质比为1∶3时,较易滴制,滴丸成品率高,药质比为1∶2时,滴制较好,但滴丸难以固化成形,所以选择药物基质配比为1∶3。
2.2.3正交优化 (1)滴丸制备方法:原料药和基质辅料均过100目筛,称取一定比例的原料药和基质辅料,混匀,置于玻璃圆底烧瓶中,保鲜膜封口,80 ℃水浴熔融,电动搅拌使药液均匀,迅速移至85 ℃水浴保温的滴灌,调控滴速,滴入冷凝的二甲基硅油(10~12 ℃),待滴丸沉降完全,取出,用石油醚洗涤3次除油,静置挥干石油醚,干燥器中保存。
(2)处方优化:见表3。根据单因素考察初步得出PEG6 000∶PEG4 000=1∶3,药质比为1∶3,加水量8%左右时滴制效果均较好,设计正交优化不同的药质比、不同的基质配比以及加水量,结果见表4。
表3处方优化的因素与水平
Tab.3 The factors and levels of formulation optimization
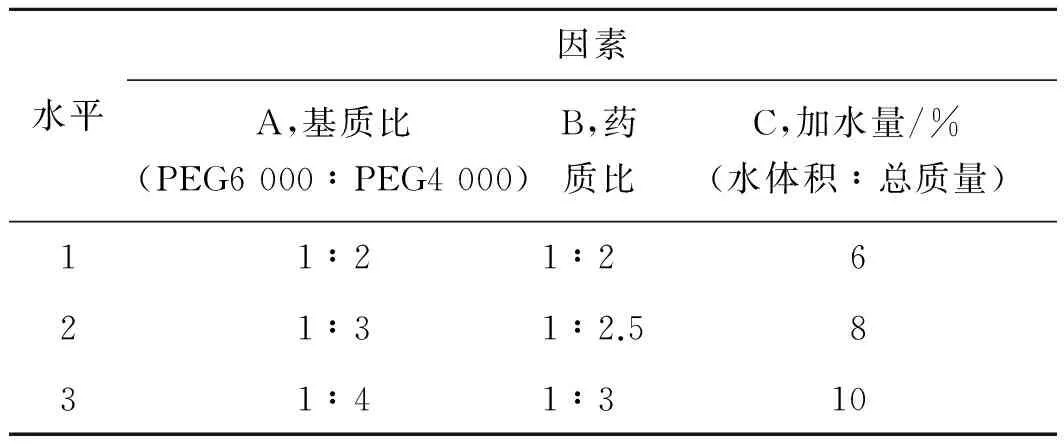
水平因素A,基质比(PEG6000∶PEG4000)B,药质比C,加水量/%(水体积∶总质量)11∶21∶2621∶31∶2.5831∶41∶310
由表4可知,最优处方为A3B3C3,PEG6 000∶PEG4 000=1∶4,药质比1∶3,加水量10%,且药质比影响较大,其次是加水量和基质比。即癸酸钠作为丹酚促吸收剂用量为47.6 g·kg-1时,具有较好的促吸收效果,同时滴丸成形质量高。
表4处方优化的正交实验结果
Tab.4 The results of orthogonal of formulation optimization

因素基质比药质比加水量外观得分丸质量差异得分崩解时限/min实验11111219.56.23实验212220245.57实验313321245.25实验421218215.40实验522323214.50实验623118245.20实验731317274.78实验832122215.10实验933219303.47均值140.16738.16738.833均值241.66743.66744.000均值345.33345.33344.333极差5.1667.1665.500
(3)工艺优化:滴距过大过小均会影响滴丸的收缩与圆整度,预实验发现滴距4~6 cm较佳;滴径大小直接影响滴丸的沉降与丸质量差异,同时药液保温温度也会影响滴速和滴丸收缩。拟调控药液保温温度、滴距和滴径来优化滴丸成品质量,按照因素水平表开展正交实验,确定最优工艺参数。正交实验因素水平表见表5,实验结果见表6。
表5滴制工艺参数的因素与水平
Tab.5 The factors and levels of process parameters

水平因素A,药液温度/℃B,滴距/cmC,滴径/mm17542.028052.538563.0
表6滴制工艺参数的正交实验结果
Tab.6 The results of orthogonal of process parameters

因素ABC实验结果崩解时限/min实验111143.04.23实验212235.04.17实验313336.55.05实验421240.54.40实验522339.05.10实验623136.54.20实验731336.55.18实验832141.04.10实验933238.04.58均值138.16740.00040.167均值238.66738.33337.833均值338.50037.00037.333极差0.5003.0002.834
极差数据显示:滴径>滴距>保温温度,最佳工艺参数为A2B1C1,药液保温温度80 ℃,滴距4.0 cm,滴径2.5 mm。
2.2.4防潮包衣 由于丹酚水溶性较强,喷雾干燥粉末极具引湿性,为增加滴丸制剂的稳定性,实验中参考文献[15-16],采用卡乐康高防潮胃溶型包衣粉,纯化水配制包衣液,控温40 ℃左右包透明衣,成品包衣平均增质量为3%~4%。包衣后滴丸崩解时限仍为4 min左右,增加了制剂稳定性,且不影响释药。
2.3验证实验 按照优选出的处方(PEG6 000∶PEG4 000=1∶4,药质比1∶3,促吸收剂4.76%,加水量10 %)及工艺参数(药液保温温度85 ℃,滴距4.0 cm,滴径2.5 mm)进行验证实验,验证结果见表7。
表7验证实验结果
Tab.7 The results of validation test

项目样品批号150817011508170615081704外观大小一致,圆整度高大小一致,圆整度高大小一致,圆整度高色泽均匀棕黄色均匀棕黄色均匀棕黄色平均丸质量/mg39.6540.1040.40丸质量差异 RSD/%1.6933.6722.529崩解时限/min3.684.133.93
所得滴丸圆整度好,色泽较均一,丸质量差异及崩解时限均符合《中国药典》2015年版四部通则0108的规定,说明处方工艺重复性高,质量可控。
3 结论与讨论
癸酸钠是唯一批准可以在商品中使用的促吸收剂[17],主要是通过调节紧密连接的孔径促进吸收,该过程具有可逆性,停药后可迅速恢复,毒性较小,因此癸酸钠作为口服吸收促进剂具有广阔的发展前景[18]。现有文献中研究者[19]考察癸酸钠的促吸收作用时用量多为0.2~5 g·L-1,占主药量的25%~250%,用量较大,作为制剂辅料,尤其中药制剂,辅料用量极大程度影响载药量及疗效。本实验结合制剂需求,设计质量浓度范围为0.08~0.8 g·L-1,进行大鼠肠吸收考察,综合比较选择适宜的质量浓度用于制剂辅料。
本实验考察了丹酚配伍癸酸钠在高温60 ℃、高湿92.5%和光照4 500 lx的影响因素实验,结果丹酚有效部位含量变化均小于5%,初步断定两者共存时,癸酸钠对丹酚稳定性影响不大。
滴丸的制备方法一般有熔融法和溶剂-熔融法2种[20],实验中发现将丹酚与熔融基质混合或过筛混合后熔融,均易出现药质分离现象,药液均匀性差,无法滴制;而将药粉与基质混匀熔融后加入适量水搅拌,有利于药粉在基质中的分散,药液流动性佳,滴制过程中不易析出沉淀,制成的滴丸颜色均匀。
考虑到丹酚滴丸制备过程高温及水的存在可能会对有效部位的含量产生很大影响,特别是丹酚水溶性成分,本研究考察了滴丸加水药液在85 ℃放置8 h的稳定性,按照滴丸药液的制备流程制备药液,分别于0,1,2,4,6和8 h取样,检测有效部位含量变化,结果药液8 h内含量变化RSD值为1.263%,说明高温滴制过程药液状态是稳定的。
[1] 戈升荣,俞一心,谢更新.丹酚酸的药理作用研究进展[J].中药材,2002,25(9):683-686.
[2] 赵娜,郭治昕,赵雪,等.丹参的化学成分与药理作用[J].国外医药植物药分册,2007,22(4):155-160.
[3] 王巍,陈建明. 滴丸剂的特点及其应用[J].药学实践杂志,2003,21(4):201-203.
[4] Lindmark T,Söderholm J D,Olaison G,et al.Mechanism of absorption enhancement in humans after rectal administration of ampicillin in suppositories containing sodium caprate[J].Pharm Res,1997,14(7):930-935.
[5] 陈慧慧.药物对丹参素和原儿茶醛的促吸收作用研究[D].广州:广东医学院,2012:5-50.
[6] Limin Zhou,Moses S S,Chow,et al. Effect of sodium caprate on the oral absorptions of danshensu and salvianolic acid B[J].Int J Pharm,2009,6(16):109-118.
[7] 薛静,叶正良,李德坤,等. HPLC同时测定丹参多酚酸中丹酚酸D、迷迭香酸、紫草酸、丹酚酸B的含量[J]. 中国实验方剂学杂志,2013,19(3):70-73.
[8] 程茜菲.高效液相色谱法同时测定丹参中6种化学成分的含量[J].西北药学杂志,2016,31(6):551-554.
[9] 袁勇,邢建国,李伟,等.田蓟苷在大鼠口服生物利用度屏障的研究[J].中国药理学通报,2014,30(4):590-591.
[10]吕晓艳.癸酸钠增强黄连素对2型糖尿病治疗作用及机制研究[D].吉林:吉林大学,2011:27-31.
[11]李杨秋,崔升淼,邢占磊.穿心莲内酯滴丸的制备工艺研究[J].时珍国医国药,2010,21(9):2381-2383.
[12]张丽军,曲秦.心痛宁滴丸增大载药量的工艺研究[J].西北药学杂志,2015,30(5):612-614.
[13]国家药典委员会.中国药典:2015年版:四部[S].北京:中国医药科技出版社,2015:11-12.
[14]诸葛周,戴德雄,朱莹.肿节风滴丸的制备工艺研究[J].中草药,2011,42(9):1759-1760.
[15]李绍婷,何文,郭咸希,等.薄膜包衣西罗莫司滴丸防潮性考察[J].中国药师,2014,17(10):1677-1678.
[16]李远文. 复方对乙酰氨基酚薄膜衣片的制备及质量评价[J].广州化工,2013,41(1):71-72,83.
[17]吕晓艳,白彩艳,陈加俊,等.癸酸钠对盐酸小檗碱在小肠各段促吸收作用的研究[J].中国老年学杂志,2010,30(17):2472-2474.
[18]杜函泽,吕晓艳,杜红伟,等.促吸收剂癸酸钠对黄连素在大鼠肠道吸收的促进作用[J].吉林大学学报:医学版,2011,37(1):35-40.
[19]梁红萍,邢丹丹,梁诗婷,等.不同浓度癸酸钠对总丹酚酸大鼠肠吸收的影响[J].中国药学杂志,2016,51(8):650-654.
[20]周长征.缓释滴丸的研究进展[J].中国实验方剂学杂志,2012,18(3):250-252.
