金沙排石冲剂的制备及质量标准研究
2018-01-10
桂林医学院附属医院,广西 桂林 541001
金沙排石冲剂的制备及质量标准研究
刘川玉邓俊刚唐建红*何洁
桂林医学院附属医院,广西 桂林 541001
目的制备金沙排石冲剂并建立其质量标准。方法采用水提醇沉工艺制成颗粒剂,采用薄层色谱法对广金钱草、泽泻、白芍、穿破石、炙甘草进行定性鉴别,采用高效液相色谱法进行白芍苷的含量测定。结果采用薄层色谱法对广金钱草、泽泻、白芍、穿破石、炙甘草进行定性鉴别,特征性强,重现性好。白芍苷的进样量在2.5~200.0 μg(r=0.9992)的线性范围良好,加样回收率为98.05%,RSD=1.65%(n=6)。结论该制剂制备方法合理、简便、可行,所建立的质量标准可为金沙排石冲剂的临床应用疗效提供保证。
金沙排石冲剂;质量标准;薄层色谱法;高效液相色谱法
“排石汤”是我院治疗泌尿系结石的临床验方,由广金钱草、海金沙、白芍、鸡内金、石韦、滑石粉、穿破石[1]、威灵仙、茯苓、泽泻、炙甘草等11味中药组成,具有清热利湿、利尿通淋、化瘀排石、解痉镇痛等功效,组方的特点是在常规治疗泌尿系结石基础上增加了养营和血、缓急止痛的芍药甘草汤[2],对泌尿系结石具有独特的疗效。为了便于临床使用,更广泛地发挥其疗效,研究采用水提醇沉工艺将该验方制成金沙排石冲剂,采用TLC法对其主要成分广金钱草、泽泻、白芍、穿破石和炙甘草进行定性鉴别,用HPLC法进行主要有效成分白芍苷的含量测定,现报告如下。
1 仪器与材料
1.1 仪器 FA2004电子天平(上海精密科学仪器有限公司);B2500S-MT型超声波清洗器 (必能信超声上海有限公司);Agilent HP1100系列高效液相色谱仪 (Agilent G1310A单元泵、Agilent ZORBAX SB-C18色谱柱、Agilent G1316A柱温箱、威玛色谱工作站、Agilent G1314A可变波长检测器,美国安捷伦公司)。
1.2 材料 硅胶G(薄层层析用化学纯,批号:1284211,青岛海洋公司);羧甲基纤维素(批号:1208011,青岛海洋公司);广金钱草(批号:120810)、穿破石(批号:130915)、鸡内金(批号:130701)、白芍(批号:20130605)、石韦(批号:130501)、威灵仙(批号:130315)、茯芩(批号:131001)、泽泻(批号:130915)、炙甘草(批号:131001)、海金沙(批号:121201)等以上10味药均购买于安徽井泉集团中药饮片有限公司;滑石粉(批号:20131005,柳州市神农中药饮片);白芍苷对照品(批号:20131130,北京坛墨质检科技有限公司);甲醇为色谱纯,水为超纯水。
2 方法与结果
2.1 处方与制备
2.1.1 处方 广金钱草30 g,海金沙15 g,鸡内金15 g,白芍15 g,石韦10 g,滑石粉10 g,穿破石15 g,威灵仙15 g,茯芩15 g,泽泻10 g,炙甘草10 g。
2.1.2 样品制备 将该处方中的药材备齐、净选,按处方5倍量投料加水煎煮1 h,煎煮两次合并煎煮液,减压浓缩至相对密度1.05~1.10,加95%乙醇沉淀过夜(至含50 %醇量),滤取上清液。减压低温浓缩至稠浸膏(60~65 ℃测定相对密度为1.20~1.25)。加入适量的蔗糖,用70%乙醇调整湿度制成软材,造粒机挤压过10目筛制成湿颗粒,60 ℃干燥,整粒,共得颗粒1 kg。用相同的方法制备3个批次的金沙排石冲剂。分别将处方中缺广金钱草、泽泻、炙甘草、白芍和空破石的药材备齐、净选,用相同方法分别制得各阴性样品。
2.2 质量控制
2.2.1 性状 本品为棕色颗粒,味甜。
2.2.2 广金钱草的薄层色谱鉴别 取3个批次的金沙排石冲剂适量研细,称约10.0 g,溶于20 mL纯水,稀盐酸调pH=2,三氯甲烷振摇提取2次,每次20 mL,弃去三氯甲烷液,用乙酸乙酯振摇提取2次,每次20 mL,合并乙酸乙酯提取液,蒸干,提取物加无水乙醇1 mL溶解,既得供试液。取广金钱草对照药材5 g,加水煮沸30 min,放冷,过滤,浓缩至20 mL,滤液同供试品溶液制备方法下从“稀盐酸调pH=2”开始制备成对照药材溶液。另取缺广金钱草的阴性样品5 g,按供试品溶液的制备方法制成阴性对照溶液。照薄层色谱法(通则0502)试验[3],吸取以上5 种溶液各10 uL,分别点于同一硅胶G薄层板上,以甲苯-甲酸乙酯-甲酸( 5∶4∶1)为展开剂,展开,取出,晾干,喷以2 %三氯化铝乙醇液,热风吹于,置紫外灯( 365 nm)下检视。结果,供试品色谱中,在与对照药材色谱相应的位置上,显相同的荧光斑点;阴性对照无干扰。具体如图1所示。
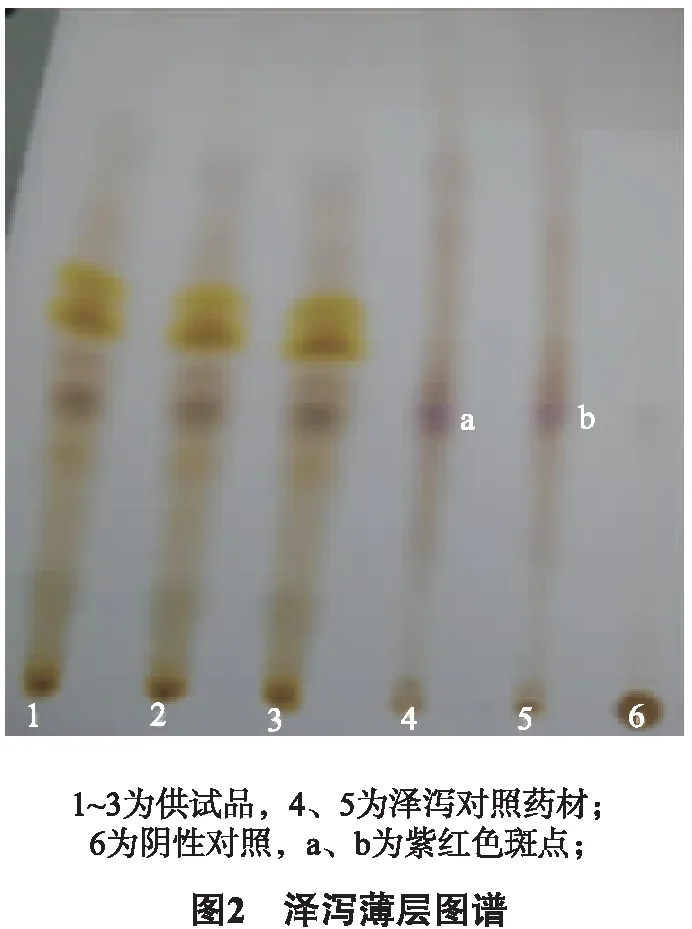
2.2.3 泽泻的薄层色谱 取3个批次的金沙排石冲剂适量研细,称约10.0 g,加水40 mL使溶解,加饱和食盐水2 mL,充分振摇,用乙醚振摇萃取2次,每次30 mL,合并乙醚液,蒸干,残渣加乙酸乙酯1 mL溶解,作为供试品溶液。取泽泻对照药材10 g,加水适量,煎煮30 min,滤过,滤液浓缩至约20 mL,按供试品溶液制备方法制备,作为对照药材溶液;取缺泽泻的阴性样品10 g,同法制成阴性对照溶液。照薄层色谱法(通则0502)试验,吸取上述5种溶液各10 μL,分别点于同一硅胶G薄层板上,以甲苯∶乙酸乙酯∶甲酸(10∶6∶0.2)为展开剂,展开,取出,晾干,喷以10 %硫酸乙醇溶液,105 ℃加热至斑点显色清晰[1]。供试品色谱中,在与对照药材色谱相应的位置上,显相同的紫红色斑点,阴性对照溶液无相应的斑点;阴性对照无干扰。如图2所示。
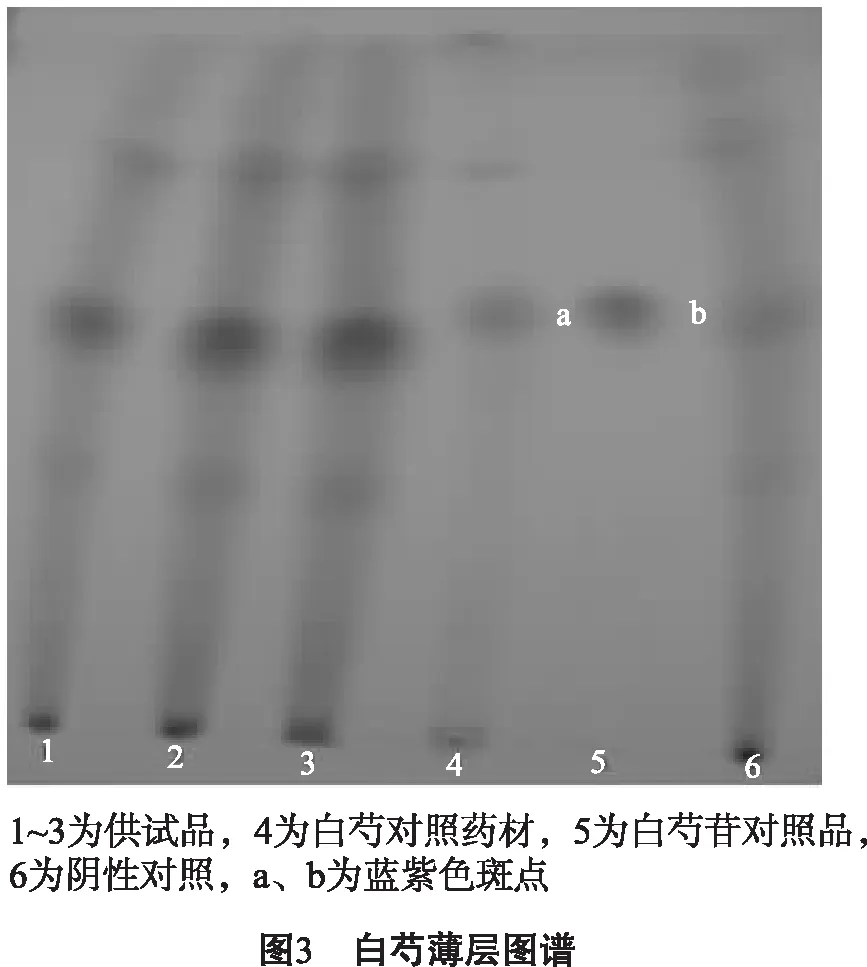
2.2.4 白芍的薄层色谱鉴别 取3个批次的金沙排石冲剂适量研细,称约10.0 g,加水40 mL使溶解,用20 mL水饱和的正丁醇振摇,提取2次,合并正丁醇液,以正丁醇饱和的水洗涤2次,合并正丁醇液,蒸干,残渣加乙醇1 mL溶解,作为供试品溶液。取白芍对照药材粗粉0.5 g,加乙醇10 mL,振摇5 min,滤过,滤液蒸干,残渣加乙醇2 mL溶解,作为对照药材溶液,另取白芍苷对照品适量,乙醇溶解,得标准对照品。取缺白芍的阴性样品,按供试品溶液的制备方法制成阴性对照溶液。照薄层色谱法 (通则0502)试验,吸取上述6种溶液各10 uL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶15∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,于105 ℃加热至斑点显色清晰[4]。结果,供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的蓝紫色斑点;在与对照品色谱相应的位置上,显相同的蓝紫色斑点;阴性对照溶液无相应的斑点;阴性对照无干扰。具体如图3所示。
2.2.5 炙甘草的薄层色谱 取3个批次的金沙排石冲剂适量研细,称约10.0 g,加甲醇50 mL,超声30 min,过滤,滤液蒸干,残渣加水40 mL使溶解,用正丁醇振摇提取3次,每次20 mL,合并正丁醇液,用水洗涤3次,每次20 mL,弃去水洗液,正丁醇液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。取炙甘草对照药材10 g,加水30 mL,煎煮30 min,滤过,取滤液10 ml,按供试品溶液同法制成对照药材溶液。取缺炙甘草样品10 g,同供试品溶液制备方法制得缺甘草的阴性对照溶液。照薄层色谱法 (通则0502)试验,吸取上述5种溶液各10 uL,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15∶1∶1∶1.5)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,紫外光灯(254 nm) 下检视。 供试品色谱中,与甘草对照药材色谱相应的位置上,显相同颜色斑点。阴性对照溶液无相应的斑点;阴性对照无干扰。具体如图4所示。

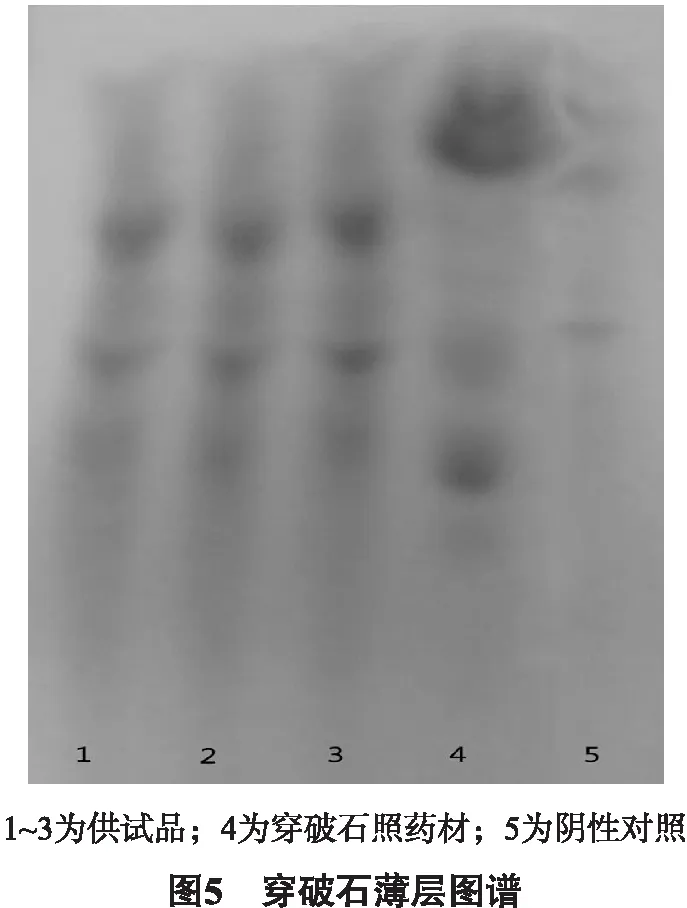
2.2.6 穿破石的薄层色谱 取3个批次的金沙排石冲剂适量研细,称约10.0 g,溶于20 mL的蒸馏水中,用乙酸乙酯提取2次每次20 mL,合并乙酸乙酯溶液,蒸干,残渣加甲醇1 mL溶解作为供试品。取穿破石对照药材8 g,加20 mL乙酸乙酯,超声30 min,过滤,滤液蒸干,残渣加甲醇1 mL溶解,作为穿破石的对照品。取缺穿破石的相同工艺制成的药材2 g,后面同供试品从“加20 mL蒸馏水溶解”起制备阴性对照品。照薄层色谱法(通则0502)试验,吸取上述5种溶液各10 uL,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲酸-水( 7∶3∶1)为展开剂,展开,取出,晾干,喷以9 %的三氯化铁溶液,斑点显色清晰。供试品色谱中,与穿破石对照药材色谱相应的位置上显相同颜色斑点。阴性对照溶液无相应的斑点;阴性对照无干扰。具体如图5所示。
2.3 含量测定
2.3.1 色谱条件 色谱柱为Zorbax C18(250 mm ×4.6 mm,5μm),流动相为甲醇-水(25∶75,V/V) ;流速为1.0 mL/min,检测波长为230 nm,柱温为25 ℃,进样量为20 μL。理论塔板数以白芍苷峰计算应不低于2000。
2.3.2 供试品、阴性对照与对照品溶液的制备 取金沙排石冲剂研细,精密称定2.0 g,置于50 mL容量瓶中,加50%甲醇适量,超声5.0 min,放冷,用50%甲醇稀释至刻度,摇匀,过滤,取续滤液经微孔滤膜滤过,作为供试品溶液。另取缺白芍的阴性样品,按供试品溶液的制备方法制备阴性对照溶液。精密称取干燥至恒重的白芍苷标准品10.0 mg,加50 %的甲醇溶解,定容于10 mL容量瓶中,制成每1 mL含1 mg的对照品溶液。
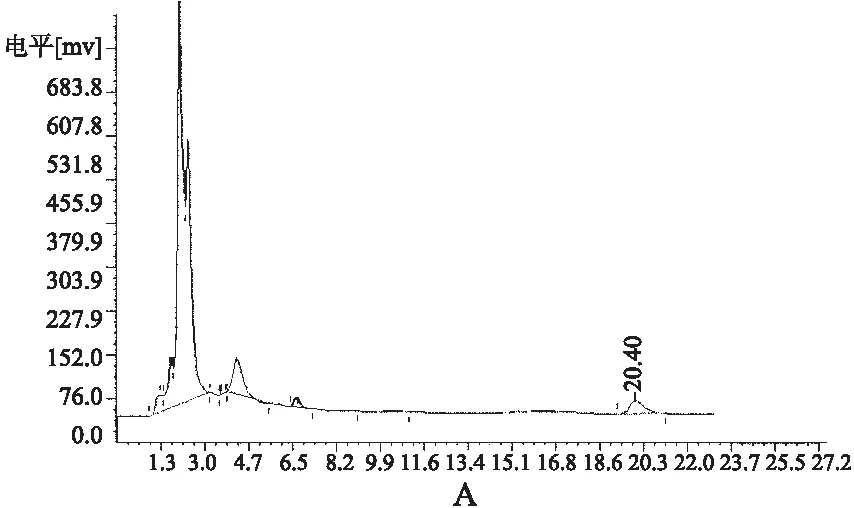
2.3.3 供试品、阴性对照与对照品溶液的高效疗相色谱 精密吸取对照品溶液、供试品溶液和阴性对照溶液等3种溶液,在“2.3.1”项下色谱条件进行测定。结果,白芍苷峰保留时间为14.36 min,杂质峰与样品峰分离完全,不干扰白芍苷的测定;理论塔板数按白芍苷峰计算不低于3000。白芍苷的HPLC如图6所示。

2.3.4 线性关系考察 精密吸取“2.3.2”项下对照品溶液适量,用50%甲醇稀释成浓度分别为200、100、50、25、10、5、2.5 μg/mL的对照品溶液系列,摇匀, 经微孔滤膜滤过,各取5 μL,按照“2.3.1”色谱条件进样测定。以白芍苷进样量(X,μg)对峰面积积分值(Y) 进行线性回归, 得回归方程为Y=21238X-59110(r=0.9992)。结果表明,白芍苷进样量在2.5~200.0 μg范围内与其峰面积积分值呈良好线性关系。
2.3.5 精密度试验 精密吸取“2.3.2”项下方法所得对照品溶液,按照“2.3.1”项下色谱条件重复进样测定5 次,测得白芍苷峰面积的RSD为2.17 %(n=5),表明仪器精密度良好。
2.3.6 重复性试验 取同一批金沙排石冲剂6份,分别按照“2.3.2”项下方法制备供试品溶液,按照“2.3.1”项下色谱条件进样测定,结果白芍苷平均含量为0.077 mg/g,RSD为1.67%,表明该方法重复性良好。
2.3.7 稳定性试验 精密吸取按照“2.3.2”项下所得同一份供试品溶液,分别于0、2、4、6、8 h,按照“2.3.1”项下色谱条件进样,测定白芍苷峰面积的RSD为1.01 %(n=5),表明供试品溶液在8 h内稳定。
2.3.8 加样回收率试验 取“2.3.5”项下已测知白芍苷含量的金沙排石冲剂6份,每份2.5g,精密称定,分别精密加入适量对照品溶液,按“2.3.2”项下方法制备供试品溶液,按照“2.3.1”项下色谱条件进样测定,计算加样回收率。结果白芍苷的平均回收率为98.05%,RSD为1.65%。
2.3.9 样品含量测定 取金沙排石冲剂样品3批,按“2.3.2”项下方法制备供试品溶液,按照“2.3.1”项下色谱条件进样测定,测定白芍苷含量。结果见表1。

表1 金沙排石冲剂中白芍苷含量测定结果(n=5)
3 讨论
泌尿系结石是临床的常见病和多发病,在中医又称尿石症、石淋,是指晶体物质在肾和膀胱内形成及下移所引起的一组疾病,在泌尿系疾病中列第3 位,是临床常见急症之一[5],其首要病因为湿热之邪蕴结于下焦,湿热相煎,犹如汤瓶在火中加热,久而久之则瓶中结成水垢[6],日久停留,气病及血,血亦因之不行[7]。湿热和瘀血为导致该病的病机,因此,用药多从清热利湿、活血化瘀、排石止痛立法,中医药治疗尿石症的疗效已得到临床验证,结石直径<1.0 cm 的排石总有效率达73%~98%[8]。经我院长期临床验证,验方排石汤对尿石症具有明显疗效,方中广金钱草清热解毒通淋、化瘀利尿排石,海金沙清热解毒、利水通淋,鸡内金通淋化坚消石,三金配合,具有良好的排石通淋效果;白芍养血柔肝止痛,并能减轻或消除炎症反应,与炙甘草配伍能松驰输尿管、膀胱等平滑肌[9],缓急止痛,利于结石排出;泽泻利水渗湿泄热,抑制结石形成[10];石韦利尿通淋排石并有保护肾脏的作用[11];威灵仙通络止痛;穿破石活血止痛;茯苓利水,诸药相合,共奏清热利湿、利尿通淋、化瘀排石止痛之功。
排石汤在我院临床应用多年,其疗效明显,为保证临床疗效和推广应用,本研究团队将研究可知,该冲剂排石汤研制成金沙排石冲剂,并建立质量控制方法。研究可知,该冲剂制备工艺简单可行。经专属性、重复性考察,方中金钱草、穿破石、泽泻、炙甘草、白芍,可用于薄层色谱鉴别试验,本项目初拟选择石韦中主要成分绿原酸作为研究对象[12],但实验中发现在阴性对照溶液中相同的位置也检测出绿原酸,因广金钱草也含有绿原酸而对实验产生干扰。前期研究证实,白芍苷含量可作为白芍饮片汤剂质量标准研究对象,以白芍苷为质量控制指标,方法简便、准确、可靠,可用于金沙排石冲剂中白芍苷的质量控制[13],故选择白芍苷作为质量控制指标。采用HPLC法测定芍药苷时,曾以甲醇-水(30∶70)流动相来试验[14],但样品峰和杂质峰分离不好。经对流动相的多次筛选,最终选用甲醇- 水(25∶75)为流动相测定,色谱图中样品峰与杂质峰分离效果好,重现性好。
研究结果显示,本制备方法简便可行,薄层色谱准确度较高,分离度好,含量测定方法可靠,重现性和精密度较好,可用于金沙排石冲剂的制备及质量评价。
[1]广西壮族自治区食品药品监督管理局编.广西壮族自治区中药饮片炮制规范[M].南宁:广西科学技术出版社,2007:276.
[2]沈映君.中药药理学[M].北京:人民卫生出版社,2002.
[3]国家药典委员会.中华人民共和国药典[M].北京:中国医药技出版社,2010.
[4]熊带水,范宋玲,宁德山.利尿胶囊质量标准的研究[J].中成药,2002,24(12):926-926.
[5]王玲,饶春恺.中成药治疗泌尿系统结石的研究进展[J].医药导报,2012(3):344-347.
[6]张宁,刘宁,郑丰杰.刘景源教授辨治尿路结石经验述要[J].世界中医药,2016,11(10):2066-2068.
[7]王峻, 陈铭, 黄坚.崔学教诊治泌尿系结石经验撷萃[J].广州中医药大学学报, 2016, 33(2): 255-258.
[8]许旭敏, 林峰.中医药防治尿石症的研究进展[J].深圳中西医结合杂志, 2014, 24(1): 123-125.
[9]许琦彬,钟良玉,诸力伟,等.白芍总苷辅助治疗系统性红斑狼疮伴发葡萄膜炎的疗效分析[J].中国现代应用药学, 2015,32(2):202-205.
[10]王沙燕,邓常青,石之嶙,等.泽泻对肾结石形成的抑制作用研究[J].广州中医药大学学报,2003,20(4):294-296.
[11]邵绍丰,张爱鸣,刘耀,等. 单味中药金钱草、石韦、车前子对大鼠肾结石肾保护作用的实验研究[J].浙江中西医结合杂志,2009,19(6):342-344.
[12]林素梅,农英高,莫海玲,等.高效液相色谱法测定排石Ⅰ号颗粒剂中绿原酸的含量[J].中国药师,2008,11(2):207-208.
[13]刘川玉,唐建红,邓俊刚.HPLC测定金沙排石冲剂中芍药苷的含量[J].国际中医中药杂志,2016,38(7):633-636.
[14]黄欣,苏乐群,韩玉东,等.反相高效液相色谱法测定少腹逐淤微粉颗粒中芍药苷的含量[J].中国药房,2005,16(6):457.
PreparationMethodandQualityStandardsResearchofJinshapaishiGranules
LIU Chuanyu DENG Jungang TANG Jianhong*HE Jie
Affiliated hospital of Guilin medical University, Guilin 541001, China
ObjectiveTo establish the preparation method and the quanlity standards of Jinshapaishi granules.MethodsJinshapaishi granules were prepared with the water decoction and alcohol precipitation technique. Alisma plantago-aquatica Linn, radices paeoniae alba , Cudrania cochin chinensis , Glycyrrhiza uralensis Fisch were identified by thin layer chromatography(TLC). The contents of Albiflorin were determined bu high performance liquid chromatography(HPLC).ResultsThe TLC method used in the identification of Alisma plantago-aquatica Linn, radices paeoniae alba , Cudrania cochin chinensis , Glycyrrhiza uralensis Fisch was highly specific with good reproducibility. Using the HPLC method to determinate the albiflorin in the granules,the linear range of it was from 2.5 μg to 200 μg (r=0.9992) and the average recovery rates was 98.05%,RSD=1.65%(n=6).ConclusionThe preparation method was reasonable, simple and feasible,and the estabilished quality standards can provide the guarantee for clinical efficacy.
Jinshapaishi Granules; Quality Standard; TLC;HPLC
广西中医药科技专项课题(GZZJ13-18)。
刘川玉(1965-),男,汉族,本科,副主任药师,研究方向为中药学。E-mail:1046728261@qq.com
唐建红(1967-),女,汉族,硕士研究生,副主任药师,研究方向为中药学。E-mail:tih@glmv.edu.cn
R284.2
A
1007-8517(2017)23-0029-05
2017-10-20 编辑:邓佳丽)
