乳化纳米铁修复硝基苯污染含水层研究
2018-01-09温春宇于锦秋张霞龙任黎明吉林大学环境与资源学院地下水资源与环境教育部重点实验室吉林长春130012
董 洋,温春宇,于锦秋,张霞龙,任黎明,董 军 (吉林大学环境与资源学院,地下水资源与环境教育部重点实验室,吉林 长春 130012)
硝基苯是一种剧毒有机物质,被美国环保总局(EPA)称为优先控制污染物[1].由于其低水溶性、化学性质稳定、难以被降解可长期存在于地下环境中,对人类健康及环境造成严重危害[2-3].目前,国内外很多学者通过多种方式修复硝基苯污染,主要包括:生物法[4],电化学法[5],以及吸附法[6-7].
纳米铁由于较高的反应活性、比表面积大、环境友好型等特点,被广泛应用于污染土壤及地下水的修复[8-9].大量研究表明,纳米铁能够有效去除重金属离子、有机污染物等[10-11].然而较强的磁吸引力会导致颗粒团聚,使得纳米铁颗粒受到重力作用而沉降,在地下环境中难以迁移.除此之外,纳米铁颗粒表面易形成铁氧化物保护层,阻碍污染物与反应活性中心接触,大大降低了对污染物的修复效果[12].因此可通过对纳米铁颗粒表面进行改性来提高胶体稳定性和迁移能力,例如聚合物改性[12-13]等.研究表明,植物油改性纳米铁(EZVI)可在铁表面形成均匀油膜, 抑制团聚[14];将乳化油注入地下后能够缓慢释放液相基质,形成生物屏障系统,并且刺激含水层中多种微生物活性,能够长期修复有机物污染[15-16];以及HCO3-、SO42-等在纳米铁降解硝基苯过程有重要作用[17].
本文在前期研究的基础上,在三维模拟槽中进行修复实验,以中砂为实验介质,以硝基苯为目标污染物,研究乳化纳米铁对硝基苯污染含水层的修复机理及效果,分析多项水文地球化学指标在修复硝基苯污染含水层过程中的变化规律,及对修复效果的影响.
1 材料与方法
1.1 实验材料
纳米铁采用液相还原法制备.反应方程式如式(1):

乳化纳米铁由纳米铁、乳化油、水按一定比例混合,并超声 30min.实验所用去离子水均经氮气通气 10min,制备纳米铁的过程在氮气保护条件下进行.油质量分数为1%,纳米铁浓度为5g/L.100mg/L硝基苯溶液作为污染物通入模拟槽.以上试剂均为分析纯.
1.2 实验方法
实验在三维有机玻璃模拟槽中进行,装置如图1所示.模拟槽尺寸 200cm×40cm×100cm,模拟槽正面和背面共 85个取样口,以槽左下角处为位置零点,沿水流方向为 y轴,垂直水流方向x轴,垂直水面方向为z轴. 0.25~1mm河砂填装高度为62cm,每填充5cm夯实以保证介质均匀性,孔隙度为34.9%.注入井长为25cm,以滤布包裹垂直安置在(x,y)=(20cm,46cm),即分布在 z轴的范围为 18~43cm.在槽左侧布水区以蠕动泵通入 10PV(孔隙体积)水,逐渐驱替介质空隙中的空气,并使介质均匀稳定.通过注入井注入9L乳化纳米铁,在左侧布水区连续通入自来水,20d后以20cm/d的流速通入100mg/L硝基苯污染液,定期取水样并分析以下指标:硝基苯,苯胺, pH值, Eh, NO3-, NO2-, SO42-及硫化物.温度为室温.

图1 三维模拟槽装置示意Fig.1 Schematic of 3D tank
1.3 测试方法
本实验中水相硝基苯和苯胺浓度采用高效液相色谱 Agilent 1260测定分析:1mL样品由0.22μm 滤膜过滤后转移至进样瓶用 HPLC测定;pH值采用便携式 pH计进行测定; 2mL样品0.45μm 滤膜过滤后转移至进样瓶采用戴安离子色谱仪分析NO3-, NO2-及 SO42-浓度;硫化物采用NN二甲基对苯二胺盐酸盐光度法测定.
1.4 数据处理方法
作图采用Tecplot、Origin8.5软件.
2 结果与讨论
2.1 硝基苯的降解规律
如图2和图3所示,在注入硝基苯第5d,理论上硝基苯最远迁移至100cm处,实际上在模拟槽底层硝基苯迁移了 80cm,上层迁移距离小于46cm(注入井位置),并且此时,仅在注入井附近检测到苯胺,最大浓度约为19.4mg/L,说明含水层中注入乳化纳米铁能够降解硝基苯,有效控制硝基苯污染羽,阻止其污染下游区域.在第 14d,y轴100~150cm 处硝基苯浓度可降低到检出限(本方法中检出下限为 20μg/L)以下,苯胺作为生成物在此区域的浓度达到30mg/L以上.21d后,各监测时间点硝基苯浓度沿水流方向下降,并且逐渐形成两个硝基苯浓度低于检出限的区域.相对应的,苯胺浓度在这两个区域积累,表现为较大值,均大于 30mg/L.在第 40d,硝基苯沿水流方向推移,但仍然保持两个浓度较小区域.
综上所述,注入乳化纳米铁能够有效降解硝基苯,控制其污染羽.铁还原降解硝基苯反应涉及6个电子转移,总反应方程式为[18]:


图2 模拟槽内硝基苯分布(mg/L)Fig.2 Distribution of NB in the tank (mg/L)
此外,注入乳化油能够刺激厌氧条件和多种土著微生物生长.本课题组通过实验证明乳化油的注入能够刺激异化铁还原菌将自然矿物中的 Fe(III)转化为 Fe(II),进而修复硝基苯污染[19-20].丁琳洁等[21]通过模拟槽实验表明注入乳化油能够对土著微生物进行驯化,在硝基苯污染场地,具有降解硝基苯能力和铁还原功能的微生物成为优势菌群;能够降解苯胺的微生物也大量生长.
向地下含水层注入乳化纳米铁,可通过化学还原反应与生物还原反应协同作用对硝基苯进行降解,能够在 40d保持较高的降解效率,同时生成易于生物降解、毒性较低的苯胺.因此,注入乳化纳米铁对硝基苯污染含水层有很好的修复效果.
2.2 水文地球化学指标的变化
2.2.1 pH值、Eh及Fe2+变化 pH值和Eh是表示乳化纳米铁反应的重要地球化学指标.零价铁被注入到地下环境中会与水反应释放 OH-,因此 pH值是监测零价铁活性的重要指标.注入乳化纳米铁后,在注入井附近 pH值可达到 8.6.pH值的增加主要是因为铁与硝基苯反应消耗了地下水中的 H+,如公式(2),以及铁与水反应,并释放OH-,如公式(3)、式(4).

从图4(a)中可以看出,注入硝基苯 14d,注入井下游部分区域pH值仍为8左右,这是由于铁不断与硝基苯反应消耗H+.而在模拟槽上层为弱酸性是由于乳化油密度比水小,向上迁移并被水解产生H+.21d后,注入井下游pH值不断下降,这是由于乳化油水解可产生多种水溶性脂肪酸与OH-发生中和反应.在第 40d,模拟槽上层部分区域仍保持弱酸性,这是由于乳化油不断地释放H+,因此有助于纳米铁对硝基苯的降解;然而,模拟槽内大部分区域pH值降低至7.7以下,说明乳化油的添加能够缓解纳米铁在地下环境中形成的碱性条件,减小对环境造成不良影响.

图3 模拟槽内苯胺分布(mg/L)Fig.3 Distribution of AN in the tank(mg/L)
图4(b)为模拟槽内Eh的变化.从 14~40d,注入井下游Eh保持在-80~-150mV的范围内,这说明乳化纳米铁的注入会产生较强的还原环境,有助于降解硝基苯.许超等[22]通过实验说明微生物对O2的消耗以及Fe2+的产生都会引起Eh下降,因此Eh的降低可说明本实验中可能存在微生物异化还原,产生Fe2+对硝基苯进行降解.在40d,模拟槽内大部分区域 Eh保持较低的水平,因此乳化纳米铁的注入可引起较长时间的还原环境.注入乳化纳米铁会引起模拟槽内 pH值升高与 Eh的下降,说明存在铁还原与微生物还原共同降解硝基苯,因此强化对硝基苯的修复效果.
铁在不同 pH值溶液中存在着不同的形态,图5中,注入乳化纳米铁后,注入井下游区域的pH值在6.6~8.2范围内,Eh保持在-80~-180mV,因此在此条件下铁主要以 Fe2+存在.Fe2+可与硝基苯反应生成苯胺[23],同时其对乳化纳米铁降解硝基苯有一定的促进作用[17].

图4 模拟槽内pH值与Eh分布Fig.4 Distribution of pH and Eh in the tank
Gu等[24]通过模拟柱实验发现,尽管铁的腐蚀作用会产生二价铁,但在出水中几乎未检测到水溶相二价铁,这是由于产生了FeCO3等沉淀.本实验出水中检测到 Fe2+生成,浓度变化如图6所示.通过结果可知乳化纳米铁注入地下含水层中,能够刺激土著异化铁还原菌生长,对硝基苯进行生物降解[22].在第5d时Fe2+浓度可达85mg/L,在模拟槽运行过程中,浓度不断降低,然而在40d仍能保持20mg/L,这说明乳化纳米铁的注入能够发生较强的生物反应,协同纳米铁化学还原反应强化对硝基苯去除.
2.2.2 SO42-还原反应与 NO3-还原反应 SO42-和NO3-可作为电子受体,与硝基苯争夺电子,这不利于乳化纳米铁对硝基苯的降解.Sheu等[16]通过场地研究表明,注入乳化纳米铁后会引起还原反应与还原反应.硫化物与作为还原反应与还原反应的产物,可反映两种还原反应的程度.进水和的浓度分别为36.54mg/L和3mg/L.图7中,在进水口浓度较大,高达 32mg/L,而模拟槽中层浓度小于 2mg/L.硫化物作为还原反应的产物,分布情况与正相反,模拟槽内大部分区域,硫化物的浓度为0.8mg/L以下;在注入井下游区域,浓度最大为2mg/L左右.总体上来说,整个模拟槽内硫化物的浓度较低,这可能是由于产生了黑色硫化铁沉淀.SO42-的消耗与硫化物的产生说明注入乳化纳米铁后可能引起 SO42-还原,反应方程式为[25]:
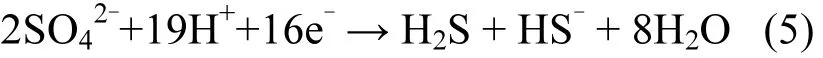

图5 铁化合物Eh-pH图Fig.5 Eh-pH diagram of ferric compounds
从方程式上看,SO42-可能与硝基苯争夺电子从而抑制乳化纳米铁对硝基苯的降解.然而,在模拟槽运行期,SO42-的分布情况与硝基苯分布相似,这可能是由于硝基苯对模拟槽内土著SO42-还原菌抑制作用较强,在硝基苯污染区域 SO42-还原反应强度低,而当区域内硝基苯被降解后,SO42-还原菌可继续作用将 SO42-还原[21],这说明硝基苯对 SO42-还原菌有抑制作用,但不能将其杀死.有研究表明,SO42-能够去除铁表面的铁氧化物和铁的氢氧化物,增加铁表面的活性位点数目[26],从而强化纳米铁对硝基苯的修复效果.
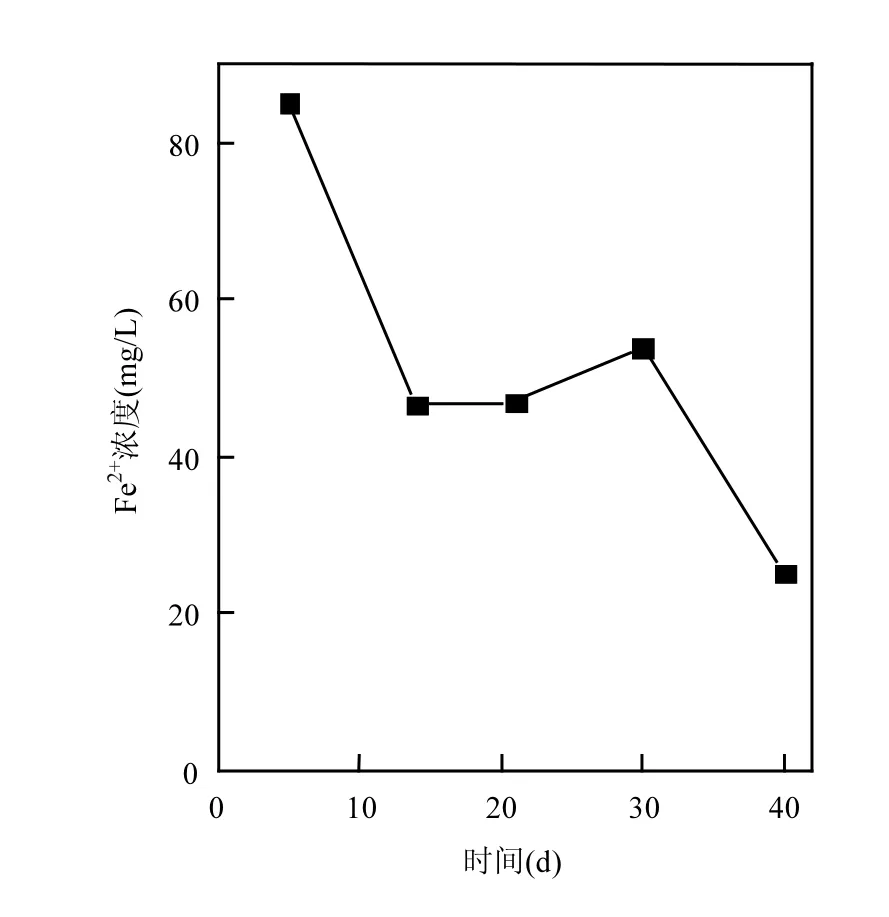
图6 模拟槽出水Fe2+浓度变化Fig.6 Variations of effluent Fe2+ concentration of the tank
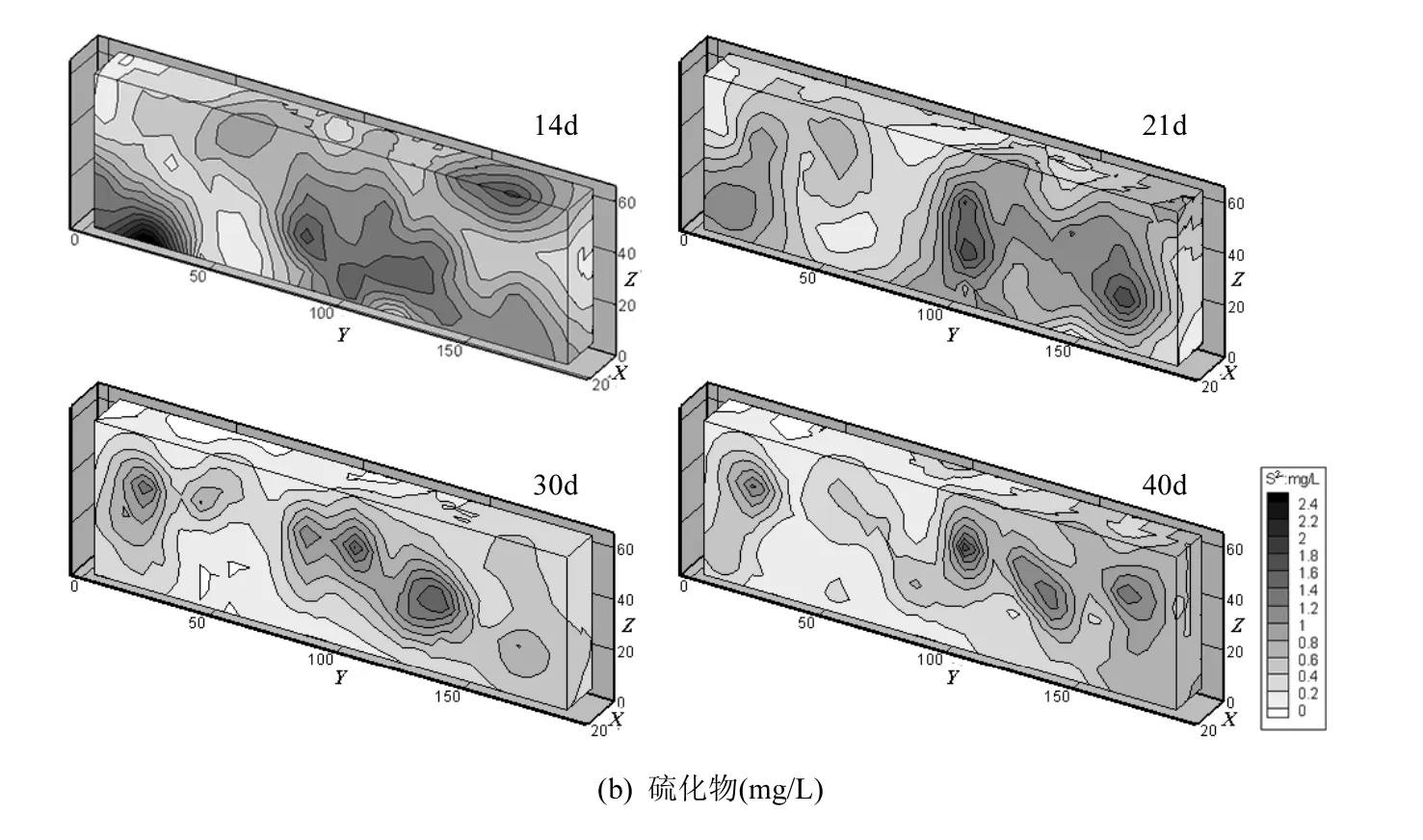
图7 模拟槽内SO42-与硫化物分布Fig.7 Distribution of sulfate and sulfide in the tank
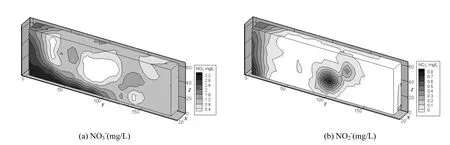
图8 第14d模拟槽内NO3-与NO2-分布Fig.8 Distribution of nitrate and nitrite in the tank at Day 14
由图8可以看出,注入井下游出现NO3-浓度较小的区域,与之相对应,此处 NO2-浓度较高,可达到1mg/L.NO3-作为电子受体被消耗并生成,说明注入乳化纳米铁后环境中发生了还原反应.然而其他检测时间未检测到,这可能是由于以下两个原因:1) 背景环境中浓度较低,导致还原反应不明显;2)被还原为 N2[25]:

因此,硫化物、NO2-的生成说明注入乳化纳米铁后模拟槽内发生了 SO42-还原反应和 NO3-还原反应.
3 结论
3.1 注入乳化纳米铁会引起生物还原反应与化学还原反应协同降解硝基苯,强化对硝基苯污染含水层的修复效果.
3.2 模拟槽中pH值保持在6.6~8.2,说明乳化油水解产生的有机酸可与 OH-发生中和反应,降低了乳化纳米铁对地下环境的影响.化学还原反应和生物还原反应发生导致pH值升高和Eh降低,促进对硝基苯的降解.
3.3 注入乳化纳米铁后发生 SO42-还原反应和NO3-还原反应,然而对硝基苯的修复效果无明显影响.
[1] Aysegul L, Mirat D G. The effect of humic acids on nitrobenzene oxidation by ozonation and O3/UV processes [J]. Water Research,2003,37(8):1879-1889.
[2] Gu D, Shao N, Zhu Y, et al. Solar-driven thermo- and electrochemical degradation of nitrobenzene in wastewater:Adaptation and adoption of solar STEP concept [J]. Journal of Hazardous Materials, 2017,321:703-710.
[3] Wang J, Lu H, Zhou Y, et al. Enhanced biotransformation of nitrobenzene by the synergies of Shewanella species and mediator-functionalized polyurethane foam [J]. Journal of Hazardous Materials, 2017,252-253:227-232.
[4] Li T, Deng X, Wang J, et al. Biodegradation of nitrobenzene in a lysogeny broth medium by a novel halophilic bacterium Bacillus licheniformis [J]. Marine Pollution Bulltin, 2014,89:384-389.
[5] Velmurugan M, Karikalan N, Chen S M, et al. Studies on the influence of beta-cyclodextrin on graphene oxide and its synergistic activity to the electrochemical detection of nitrobenzene [J]. Journal of Colloid and Interface Science,2016,490:365-371.
[6] Dai Y J, Zhang D F, Zhang K X. Nitrobenzene-adsorption capacity of NaOH-modified spent coffee ground from aqueous solution [J]. Journal of the Taiwan Institute of Chemical Engineers, 2016,68:32-238.
[7] Qin Q D, Xu Y. Enhanced nitrobenzene adsorption in aqueous solution by surface silylated MCM-41 [J]. Microporous and Mesoporous Materials, 2016,232:143-150.
[8] Zhang W X. Nanoscale iron particles for environmental remediation: an overview [J]. Journal of Nanoparticle Research,2003,5(5):323-332.
[9] Grieger K D, Fjordboge A, Hartmann N B, et al. Environmental benefits and risks of zero-valent iron nanoparticles (nZVI) for in situ remediation: risk mitigation or trade-off [J]. Journal of Contaminant Hydrology, 2010,118(3/4):165-83.
[10] Ponder S, Darab J. Remediation of Cr(VI) and Pb(II) aqueous solutions using supported nanoscale zero-valent iron [J].Environment Science Technology, 2000,34:2564-2569.
[11] Sun Y, Li J, Huang T, et al. The influences of iron characteristics,operating conditions and solution chemistry on contaminants removal by zero-valent iron: A review [J]. Water Research,2016,100:277-95.
[12] Zhao X, Lv L, Pan B C, et al. Polymer-supported nanocomposites for environmental application: A review [J].Chemical Engineering Journal, 2011,170(2/3):381-394.
[13] 张永祥,常 杉,李 飞,等.稳定型纳米零价铁去除地下水中2_4_二氯苯酚 [J]. 环境科学, 2017,38(6):2385-2392.
[14] Dong J, Wen C Y, Liu D F, et al. Study on degradation of nitrobenzene in groundwater using emulsified nano-zero-valent iron [J]. Journal of Nanoparticle Research, 2015,17:31.
[15] Liang S H, Kuo Y C, Chen S H, et al. Development of a slow polycolloid-releasing substrate (SPRS) biobarrier to remediate TCE-contaminated aquifers [J]. Journal of Hazardous Materials,2013,254-255:107-115.
[16] Sheu Y T, Lien P J, Chen K F, et al. Application of NZVI-contained emulsified substrate to bioremediate PCE-contaminated groundwater — A pilot-scale study [J]. Chemical Engineering Journal, 2016,304:714-727.
[17] Dong J, Ding L J, Wen C Y, et al. Effects of geochemical constituents on the zero-valent iron reductive removal of nitrobenzene in groundwater [J]. Water and Environment Journal,2013,27(1):20-28.
[18] Mu Y. Reductive degradation of nitrobenzene in aqueous solution by zero-valent iron[J]. Chemosphere, 2004,54(7):789-794.
[19] Dong J, Ding L J, Chi Z F, et al. Kinetics of nitrobenzene degradation coupled to indigenous microorganism dissimilatory iron reduction stimulated by emulsified vegetable oil [J]. Journal of Environmental Sciences (China), 2017,54:206-216.
[20] 生 贺,于锦秋,刘登峰,等.乳化植物油强化地下水中Cr的生物地球化学还原研究 [J]. 中国环境科学, 2015,35(6):1693-1699.
[21] 丁琳洁, Y-ESO强化原位生物反应带修复硝基苯污染含水层研究 [D]. 长春:吉林大学, 2016.
[22] 许 超,董 军,马小兰,等.微生物异化还原铁氧化物体系对硝基苯的降解作用 [J]. 中国环境科学, 2011,31(9):1472-1476.
[23] Liu C C, Tseng D H, Wang C Y. Effects of ferrous ions on the reductive dechlorination of trichloroethylene by zero-valent iron[J]. Journal of Hazardous Materials, 2006,136(3):706-713.
[24] Gu B, Phelps T J, Liang L, et al. Biogeochemical Dynamics in Zero-Valent Iron Columns: Implications for Permeable Reactive Barriers [J]. Environment Science Technology, 1999,33:2170-2177.
[25] Tang G P, Watson B D, Parker C J, et al. U(VI) Bioreduction with Emulsified Vegetable Oil as the Electron Donor- Microcosm Tests and Model Development [J]. Environment Science Technology, 2013,47(7):3209-3217.
[26] Lipczynskako C, Milburn R, Sprah G, et al. Degradation of carbon-tetrachloride in the presence of iron and sulfurcontaining-compounds [J]. Chemosphere, 1994,29:1477-1489.
