继发性卵巢纤维肉瘤并广泛盆腹腔种植1例并文献复习
2018-01-02陈真真黄鹏余晓辉张庆华敖启林黄磊
陈真真,黄鹏,余晓辉,张庆华,敖启林,黄磊*
(1江汉大学医学院妇产科,武汉430056;2湖北省黄冈市妇幼保健院妇产科,黄冈438000;3华中科技大学附属同济医院病理学研究所暨华中科技大学同济医学院病理系,武汉430030;4武汉市中心医院妇科,武汉430014)
病例报道
继发性卵巢纤维肉瘤并广泛盆腹腔种植1例并文献复习
陈真真1#,黄鹏2#,余晓辉1,张庆华4,敖启林3,黄磊4*
(1江汉大学医学院妇产科,武汉430056;2湖北省黄冈市妇幼保健院妇产科,黄冈438000;3华中科技大学附属同济医院病理学研究所暨华中科技大学同济医学院病理系,武汉430030;4武汉市中心医院妇科,武汉430014)
目的探讨一例右侧卵巢卵泡膜纤维瘤腹腔镜术后出现继发性卵巢纤维肉瘤合并盆腹腔广泛转移的临床病理特征、诊断、治疗及前次手术应用旋切器对预后的影响。方法分析卵巢纤维肉瘤光镜及免疫组织化学各项指标的病理特点,旋切器应用的适应症并复习相关文献。结果卵巢卵泡膜纤维瘤术后发生的卵巢纤维肉瘤有可能不是继发性病变,而是由于前次使用旋切器后失去完整肿瘤形态引起病理取材上的漏诊引起的,对于卵巢实质性肿瘤,不推荐使用旋切器粉碎取出。结论应避免腹腔镜手术使用旋切器粉碎卵巢实质性包块导致病理取材的困难,使恶性肿瘤漏诊;旋切碎屑导致盆腹腔播散种植及加速病变恶化增殖。
卵巢;纤维肉瘤;性索间质肿瘤;腹腔镜;粉碎器
本文报告1例继发性卵巢纤维肉瘤患者,术中探查发现患者盆腔内可见广泛种植病灶,呈明显恶性表现。患者发病前1年8个月在外院因右侧卵巢良性肿瘤行腹腔镜手术并切除了患侧附件,因肿瘤为实质性,术中以旋切器将切除组织粉碎后取出盆腔。术后多家单位病理诊断均提示为良性卵巢性索间质肿瘤。但是1年8个月后发现患者为盆腔广泛转移性卵巢纤维肉瘤。通过对患者病情的梳理,重点从病理学角度分析了患者的继发性病变的原因,并予以报道如下。
材料与方法
1 临床资料
患者64岁,女,因彩超发现盆腔包块入院。患者入院前10余天体检发现盆腔包块,近一周尿频,无尿痛、尿急,无阴道不规则出血及排液,大便正常。妇检:外阴已婚式,阴道通畅,宫颈肥大,数个纳氏囊肿,盆腔可及一巨大包块,质硬,形态不规则包块上级位于底部脐下三指,活动欠佳,无明显压痛。2016年4月1日我院子宫附件彩超示子宫萎缩,宫颈多发囊肿,子宫上方盆腔内实质性非均质包块,来源于左侧卵巢可能性大,考虑为左侧卵巢癌,压迫左侧输尿管,左肾轻度积水,左、右侧髂窝、盆壁及腹膜后多处低回声区,考虑为转移灶及转移性淋巴结肿大,腹腔积液。甲胎蛋白、癌胚抗原、糖类抗原199正常,糖类抗原125:107.70U/mL。盆腔MRI增强示:1、盆腔肿物,考虑卵巢来源恶性肿瘤并盆腔淋巴结、腹膜多发转移;2、小肠受侵待排;3、盆腔积液;4、宫颈管囊肿。
既往史:2014年8月11日因“盆腔包块”于外院行腹腔镜下右侧附件切除术,术中未行冰冻切片快速病理检查。术中使用旋切器粉碎取出右侧附件实质性包块。术后病检示:右侧卵巢性索间质肿瘤。2014年8月18日于上级医院病理切片会诊意见:右侧卵巢卵泡膜纤维瘤。术后3月患者复查盆腔彩超未见明显异常。后未行定期复查。
处理:2016年4月12日行剖腹探查术。术中先切除子宫前方巨大分叶状包块送术中快速病理检查提示为卵巢性索间质肿瘤,考虑为卵泡膜纤维瘤。一般认为卵泡膜纤维瘤属良性,但临床亦有术中广泛转移或术后因肿瘤转移复发而死亡者。多数学者认为从病理学上很难区别肿瘤的良恶性质[1],有学者认为良恶性卵泡膜细胞瘤鉴别的主要依据应为临床表现中有无恶性行为[2]。本病例因术中所见遍布种植转移病灶,为恶性表现,经患者家属同意,行经腹全子宫切除术+左侧附件切除术+盆腔淋巴结清扫术+大网膜部分切除术+阑尾切除术。
2 HE染色与免疫组织化学染色
术中切除标本经10%福尔马林固定、常规脱水、石蜡包埋后切片,一部分切片行HE染色,另一部分进行Calretinin、SMA、Vimentin、PHH3、WT-1、CD56、CD99、CD10、Desmin、Melan-A、Pan-CK、S-100、a-inhibin、Ki-67免疫组织化学SP法染色。
结 果
1 巨检
直径约20cm不规则分叶状包块,质脆,见血管增生,位于子宫前方;另见一直径约4.0cm种植病灶位于膀胱浆膜面,子宫浆膜面见大小不等豌豆样种植病灶多处,直肠前壁和乙状结肠浆膜面见多发粟粒状种植病灶,右侧输尿管中下段部位见一直径约4.0cm种植病灶,左侧输尿管下段近膀胱开口部位见一直径约5.0cm种植病灶压迫输尿管,左输尿管中段膨大,见一直径约2.0cm种植病灶侵犯输尿管,阑尾肿胀欠光滑,表面见多发结节;探查盆壁、肝脏、大网膜部位未扪及转移病灶。
2 病理检查
左侧卵巢纤维肉瘤(肿块大小15cm*11cm*6cm)(图1)。免疫组化:Calretinin、SMA、Vimentin、PHH3、WT-1、CD56 均 (+),CD99 部分(+),CD10、Desmin、Melan-A、Pan-CK、S-100、a-inhibin均(-),Ki-67 LI:约50%。左盆腔淋巴结10/19枚,右盆腔淋巴结0/21枚可见肿瘤细胞转移。左输卵管中段、下段及盆腔转移灶可见肿瘤细胞转移。大网膜组织未见明显病变。腹腔冲洗液镜下呈血细胞背景,可见间皮细胞、中性粒细胞、淋巴细胞,未见肿瘤细胞。
3 诊断与治疗
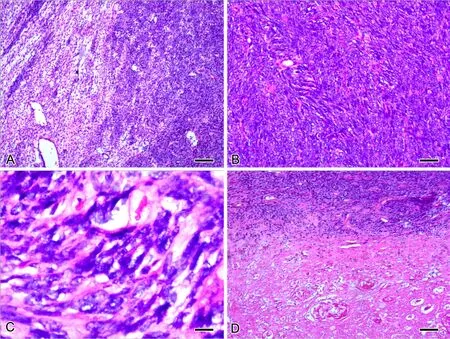
图1 卵巢纤维肉瘤病理学特征。A,肉瘤高级别和低级别区域移行;B,瘤细胞生长活跃、密集;C,瘤细胞异型性明显;D,肿瘤坏死,提示肉瘤的线索;比例尺:A,100µm;B,50µm;C,20µm;D,100µmFig. 1 Ovary fibrosarcoma pathology. A, high and low grade transitional regions of sarcoma; B, highly dense and actively dividing tumor cells; C,atypical tumor cells; D, tumor necrosis suggested sarcoma; scale bar: A, 100µm; B, 50µm; C, 20µm; D, 100µm
根据病理学诊断为左侧卵巢纤维肉瘤IIIC期。术后给与卡铂400mg腹腔化疗一次,后行AP方案化疗6个疗程,化疗结束时体检肿瘤因子全部正常,盆腔MRI检查未发现明显转移病灶。化疗结束后1个月,患者上腹部MRI平扫示:肝右后叶包膜下异常信号灶,考虑为转移可能性大。化疗结束后3月余,盆腔MRI发现患者有盆腔转移迹象,建议行局部放疗,但因患者无特殊不适,拒绝放疗。化疗结束后4月余,发现肿瘤全面复发和转移。2017年3月6日至4月11日行盆腔放疗。至2017年9月肝脏病灶长至10cm,同时发现左侧骶髂关节处骨转移。9月29于我院行腹腔镜下肝脏新生物切除术。同时发现左侧骶髂关节处骨转移。术后病检:腹腔肿瘤结合病史及免疫组化,符合卵巢纤维肉瘤转移。免疫组化:BCL-2和α-inhibin(+),Calretinin部分(+),β-Catenin、CA125、WT-1、H-Caldesmon 均(-),Ki-67 LI约20%。现患者腹腔种植转移瘤术后一月,于我院肿瘤内科观察治疗中。
讨 论
1 临床特点
查阅大量文献,卵巢纤维肉瘤好发于围绝经期及绝经后女性,临床表现无特异性,多以腹部包块或腹痛为首发表现,肿瘤大小5cm~23cm不等(平均11.5cm)[3]。妇科彩超可能多表现为单侧附件肿物,伴有不均匀回声增强及较大实性区域,血流信号可能丰富,但并无特异超声表现。卵巢纤维肉瘤也没有特异性肿瘤标志物。卵巢纤维肉瘤是极为罕见的恶性肿瘤,约占卵巢恶性肿瘤的1%,可能起源于卵巢未分化的卵泡膜外部的间叶组织和卵巢门的纤维成分,也可源于卵巢良性纤维瘤或卵泡膜纤维瘤的恶变[4]。卵泡膜纤维瘤与卵巢纤维肉瘤同属性索间质肿瘤,具有同源性。而卵泡膜细胞瘤、卵泡膜纤维瘤、纤维瘤为一个连续变化的瘤谱[5]。
大部分卵巢泡膜纤维瘤为良性,极少数生物学行为为恶性,多数学者认为卵巢泡膜纤维瘤约有2%~5%的恶变率,多发生在60岁以后[6]。多数报道的恶性卵泡膜瘤实际上是纤维肉瘤或弥漫性颗粒细胞瘤[7]。卵巢纤维肉瘤为绝对意义上的恶性肿瘤,其恶性度高、预后差。一文献报道2例误诊为良性卵泡膜纤维瘤的I期恶性卵泡膜纤维瘤患者,仅行单纯手术治疗后1年5个月死于肿瘤扩散转移[6]。本例患者化疗结束后1月有复发转移迹象,化疗结束后4月肝脏、盆腔全面转移。此后行盆腔局部放疗,腹腔转移瘤切除术。预后差。
2 分析
腹腔镜手术具有创伤小、术后恢复快、术后住院时间短、术中出血量少、切口美观等优点。然而任何技术设备均具有两面性,在粉碎器使用过程中可能会出现以下两种预期外损害:一是粉碎器造成腹腔组织的损伤。据美国FDA和MedSun器械数据库统计,1993~2013 年间由粉碎器所造成的损伤有55例,约占总数的 0.007%~0.02%[8]。但有学者认为其低于真正的损伤发生率。良性组织的破坏和散布与急性并发症密切相关,如急性腹膜炎,腹内脓肿、肠梗阻。粉碎术的另一个主要问题是病理标本的粉碎造成原有组织形态丧失。卵巢及其肿瘤性病变的取材规范:首先称重并测量卵巢;然后经卵巢门部及其最大径切开卵巢,每隔1cm~2cm切除一块肿瘤组织送检,重点关注实性、乳头状、坏死或出血区。尤其对于黏液性肿瘤,因为有局部出现重度非典型增生或者浸润性病变可能,尤其强调多层次取材[9]。实质性卵巢肿瘤经过旋切后成为条索状,及不规则零散的碎屑组织,病理科医生在取材时完全凭借经验触摸粉碎组织取材,完全无法按照规范取材,无法判断卵巢门位置,无法行1cm~2cm间距的多处取材,从而使病理科医生诊断困难,导致恶性肿瘤的延误诊断和旋切器造成预期外恶性肿瘤的扩散风险,最终导致患者术后病理分期增加,并造成不良预后[10]。
美国FDA于2014年4月17日发出关于腹腔镜电动子宫肌瘤粉碎器应用的通告:不建议临床继续应用腹腔镜电动子宫肌瘤粉碎器于腹腔镜子宫切除术或子宫肌瘤剔除术[11]。腹腔镜电动肌瘤粉碎器在手术使用过程的电动刀头旋转切割,可将未保护的子宫碎片组织“发射”向腹腔内各个方向。引起良性病变组织及术前未诊断的隐匿性子宫恶性肿瘤组织的腹腔内播散问题。
国内凌斌教授早于 FDA警告提出一种腹腔镜辅助旋切子宫肌瘤标本袋专利技术,将肿瘤组织标本植入相对密闭的保护袋内,在腹腔镜监测下破碎取出,避免恶性肿瘤医源性播散,已获得相关发明专利,并在临床率先开展应用[12]。将瘤体放在一个袋子中旋切,理论上可避免切碎的瘤体播散,但是旋切袋的安全性及有效性仍有待证实。
粉碎器使用的禁忌症之一为已知或可疑有恶变组织者。卵巢实性肿瘤为恶性的可能性较大,所以对于卵巢实质性肿瘤,不推荐使用粉碎器。若必须用,切除的标本应先放入相应大小的旋切标本袋中进行旋切操作,避免瘤体的播散。
此病例结合术中所见及病检结果,考虑该患者为卵巢继发性纤维肉瘤并广泛腹腔种植。造成这种结果的原因是:a 病理取材上的漏诊:可能因为前次腹腔镜手术切除的右侧附件为实质性包块,使用旋切器粉碎取出,病理科医生在取材时完全凭借经验触摸粉碎组织取材,难以全面取材,极易导致漏诊;b 使用旋切器导致的实质性肿瘤在盆腔内播散和种植;c 术中未进行冰冻切片快速病理检查。卵巢纤维肉瘤诊断主要靠病理学,术中冰冻病理有时能提示为梭形细胞恶性肿瘤,但是梭性细胞病变级别低时,术中快速病理检查难以诊断;d 该患者腹腔镜良性肿瘤切除术后没有定期随诊,术后1月和3月有随访,后未复查。
3 治疗及预后
卵巢纤维肉瘤的首选治疗手段为手术,个案报道手术方式差异很大,术后辅助治疗也有较大不同。2016 NCCN卵巢癌诊治指南推荐,对于恶性性索间质瘤Ⅱ~Ⅳ期患者可选择铂类为基础的化疗或者对局限性病灶进行放射治疗[13]。有资料表明手术切除联合化疗组患者的2年生存率明显较高[3]。目前,各种手术及辅助治疗方式对生存的影响无统一结论。本病例该患者行经腹全子宫切除术+左侧附件切除术+盆腔淋巴结清扫术+大网膜部分切除术+阑尾切除术。术后给与卡铂400mg腹腔化疗一次,后行AP方案化疗6个疗程。
卵巢纤维肉瘤罕见,约占卵巢恶性肿瘤的1%。且恶性度高、预后差。2年总生存率约为55.9%[14]。常见复发部位为盆腔,肝脏是最常见的远处转移部位。转移方式以血行为主。本例患者化疗结束后1月有复发转移迹象,化疗结束后4月肝脏、盆腔发现转移。后行盆腔局部放疗,肝脏转移瘤切除术。预后差。本例患者手术病理分期为FIGO IIIC期,Ki-67约50%,均为预后不良的高危因素。
[1] FoxH, LangleyFA. Tumors of the Ovary. 1st ed. London:WhitefriarsPres Ltd, 1976, 119-133.
[2] 李英勇,侯志勇. 28例卵巢性索间质肿瘤临床及病理分析. 中国实用妇科与产科杂志,1995,11(6):345-346.
[3] 谢敏,李艺,戴林,等. 原发性卵巢纤维肉瘤一例并文献复习. 中国妇产科临床杂志,2015,16(4):370-371.
[4] Lee HY, Ahmed Q. Fibrosarcoma of the ovary arising in a fibrothecomatous tumor with minor sex cord elements. A case report and review of the literature. Arch Pathol Lab Med,2003, 127(1): 81-84.
[5] 廖欣,李明华. 卵巢原发纤维肉瘤1例.华西医学,2009,24(6):1599-1600.
[6] 郑园园,袁吟迅,张品南. 168例卵巢卵泡膜纤维瘤临床病理研究. 医学信息,2014,27(10):28.
[7] 回允中,主译.女性生殖道病理学(第一版).北京:北京大学医学出版社,2005,607-619.
[8] Milad MP, Milad EA. Laparoscopic morcellator -related complications. J Minim Invasive Gynecol, 2014, 21(3): 486-491.
[9] Westra WH, Hruban RH, Phelps TH, etal. Surgical Pathology Dissection: An Illustrated Guide, Second Edition. Springer, 2002, 161-163.
[10] 武化拓,马焱,李莉.腹腔镜下旋切器误用于子宫肉瘤 6例分析并文献复习.国际妇产科学杂志,2017,44(3):307-311.
[11] 朱兰,范融. 腹腔镜电动子宫肌瘤粉碎器临床应用的去向. 中国实用妇科与产科杂志,2016,32(1):20-23.
[12] 赵卫东,周虎.子宫肌瘤恶变及腹腔镜下播散的预防.中国实用妇科与产科杂志,2016,32(2):155-158.
[13] 卢淮武,谢玲玲,林仲秋.《2016 NCCN卵巢癌临床实践指南(第 1版)》解读.中国实用妇科与产科杂志,2016,32(8):761-768.
[14] Huang L, Liao LM, Wang HY, et al. Clinicopathologic characteristics and prognostic factors of ovarian fibrosarcoma:the results of a multi-center retrospective study. BMC cancer, 2010, 10: 585-594.
Secondary ovarian fibrosarcoma with extensive pelvic and abdominal metastasis: a case report and literature review
Chen Zhenzhen1, Huang Peng2, Yu Xiaohui1, Zhang Qinghua4, Ao Qilin3, Huang Lei4*(1 Department of Obstetrics & Gynecology, Jianghan Medical School, Jianghan University, Wuhan 430056, China; 2 Department of Obstetrics & Gynecology, Huanggang Maternal & Infant Health Hospital, Huanggang 438000, China; ³Institute of Pathology, Tongji Hospital and Department of Pathology, Tongji Medical School, Huazhong University of Science and Technology, Wuhan 430030,China; 4Department of Obstetrics & Gynecology, Central Hospital of Wuhan, Wuhan 430014, China)
ObjectiveA case report on ovarian fibrosarcoma with extensive pelvic and abdominal metastasis secondary to a right ovarian thecoma after laparoscopic surgery. The discussion included its clinicopathological features, diagnosis, treatment, and the impact of previous utilization of pulverizer on prognosis.MethodsThe pathological features of ovarian fibrosarcoma were evaluated based on light microscopy and immunohistochemistry. Indications for pulverizer usage and related literature were reviewed.ResultsThe ovarian fibrosarcoma might be primary tumor instead of secondary to ovarian thecoma. The misdiagnosis was likely due to an inappropriate preparation of tumor tissues for pathological evaluation, in which the usage of pulverizer damaged tumor sample integrity.ConclusionPulverizer is not recommended for surgical removal of ovarian parenchymal tumors during laparoscopic surgery. Its usage increases the difficulty of pathological sampling hence the chance of misdiagnosis, meanwhile the tumor tissue debris generated by rotating excision may spread to pelvic and abdominal cavities hence accelerate the disease progression.
Ovarian fibrosarcoma; sex cord-stromal tumor; laparoscope; pulverizer
卵巢纤维肉瘤是极为罕见的恶性肿瘤,约占卵巢恶性肿瘤的1%,其可能起源于卵巢未分化的卵泡膜外部的间叶组织和卵巢门的纤维成分,也可源于卵巢良性纤维瘤或卵泡膜纤维瘤的恶变[1]。卵巢纤维肉瘤好发于围绝经期及绝经后女性,其恶性度高,预后差。本文报告1例64岁女性卵巢纤维肉瘤,结合旋切器在临床的应用并就其临床病理组织学特点、治疗及预后进行分析。
R361
A
10.16705/ j. cnki. 1004-1850. 2017. 06. 010
2017-05-08
2017-11-07
陈真真,女(1990年),回族,硕士研究生;黄鹏,女(1973年),汉族,副主任医师
#相同贡献作者
*通讯作者(To whom correspondence should be addressed):whhlmail@126.com
