直肠癌术后早期肠梗阻21例临床分析
2017-12-27皖南医学院第一附属医院弋矶山医院胃肠外科肿瘤内科安徽芜湖241001
(皖南医学院第一附属医院 弋矶山医院 1.胃肠外科,2.肿瘤内科,安徽 芜湖 241001)
·临床医学·
直肠癌术后早期肠梗阻21例临床分析
左学良1,蔡 娟2,王俊峰1,梁林虎1,武 健1
(皖南医学院第一附属医院 弋矶山医院 1.胃肠外科,2.肿瘤内科,安徽 芜湖 241001)
目的:探讨直肠癌术后早期肠梗阻的原因,并总结预防和治疗方法。方法回顾性分析直肠癌手术患者1182例,术后并发早期肠梗阻21例,总结其临床资料和防治措施。结果21例直肠癌患者中Dixon手术15例(71.4%),Miles手术6例(28.6%)。术后吻合口瘘10例(47.6%),小肠与盆底或腹壁粘连成角5例(23.8%),小肠单纯粘连2例(9.5%),造口旁小肠内疝2例(9.5%),造瘘口狭窄1例(4.8%),肠道多发癌1例(4.8%)。再次手术14例(66.7%),其中再次腹腔镜探查4例(28.6%),剖腹探查10例(71.4%),20例治愈,1例未愈。直肠癌术后早期完全性肠梗阻非手术治疗成功率远低于不全性肠梗阻,两组间差异具有统计学意义(P<0.05),再次腹腔镜手术较开腹手术减少了术后住院时间,两组间差异具有统计学意义(P<0.05)。结论直肠癌术后早期肠梗阻最常见的原因是吻合口瘘(Dixon术)和肠粘连(Miles术),腹内疝也是较常见的原因,同时需特别注意较少见的肠道多发癌可能。术后早期完全性肠梗阻非手术治疗成功率低,对于保守治疗效果不佳的患者应尽早选择手术时机并合理选择手术方式。
直肠肿瘤;肠梗阻;预防;治疗
早期肠梗阻是直肠癌术后常见的并发症,也是早期再次手术的主要原因,指发生在手术后1个月内的梗阻[1]。因临床特点不同,包括早期炎性肠梗阻和机械性肠梗阻等,炎性肠梗阻以腹胀为主,一般经积极保守治疗后可缓解[2],而机械性肠梗阻临床病因复杂,大多需要再次手术治疗。目前对于肠梗阻手术时机和手术方式的选择仍然是困扰外科医生的主要难题,既往已有文献报道Miles术后肠梗阻的原因分析[3],但直肠癌手术方式繁多,术后梗阻的原因复杂,目前对于再次手术时机和手术方式的选择探讨较少。本研究回顾性分析直肠癌术后并发早期肠梗阻21例的临床资料,并探讨再次手术时机和手术方式的选择。
1 资料与方法
1.1 一般资料 2012年3月~2017年2月在弋矶山医院胃肠外科行直肠癌手术的患者1182例,术后并发早期肠梗阻21例,发生率1.8%,其中男性18例,女性3例,年龄47~85岁。行Dixon手术15例,Miles手术6例;腹腔镜手术12例,开腹手术9例。出现肠梗阻的时间为2~24 d。
1.2 纳入标准 本组研究中早期肠梗阻的纳入标准:①术后1个月内肠道功能短暂恢复,后出现腹痛、腹胀、呕吐伴或不伴肛门停止排气排便的患者,有肛门排气为不完全肠梗阻,无肛门排气为完全肠梗阻;②胃管引流量多,听诊肠鸣音可正常或亢进,但不减弱;③腹部X线或腹部CT可见大小不一的气液平面;④排除术后复发引起的肠梗阻。
1.3 临床处理 21例患者全部先行非手术治疗,对于吻合口瘘的患者行腹腔冲洗,对于造瘘口狭窄的患者每日扩肛。保守治疗后患者症状不缓解,腹部X线平片气液平面不消失均采取手术治疗。
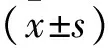
2 结果
2.1 直肠癌术后早期肠梗阻的原因 21例患者中,吻合口瘘10例(47.6%),小肠与盆底粘连成角3例(14.3%),小肠与腹壁粘连成角2例(9.5%),小肠单纯粘连2例(9.5%),造口旁小肠内疝2例(9.5%),造瘘口狭窄1例(4.8%),肠道多发癌1例(4.8%)。
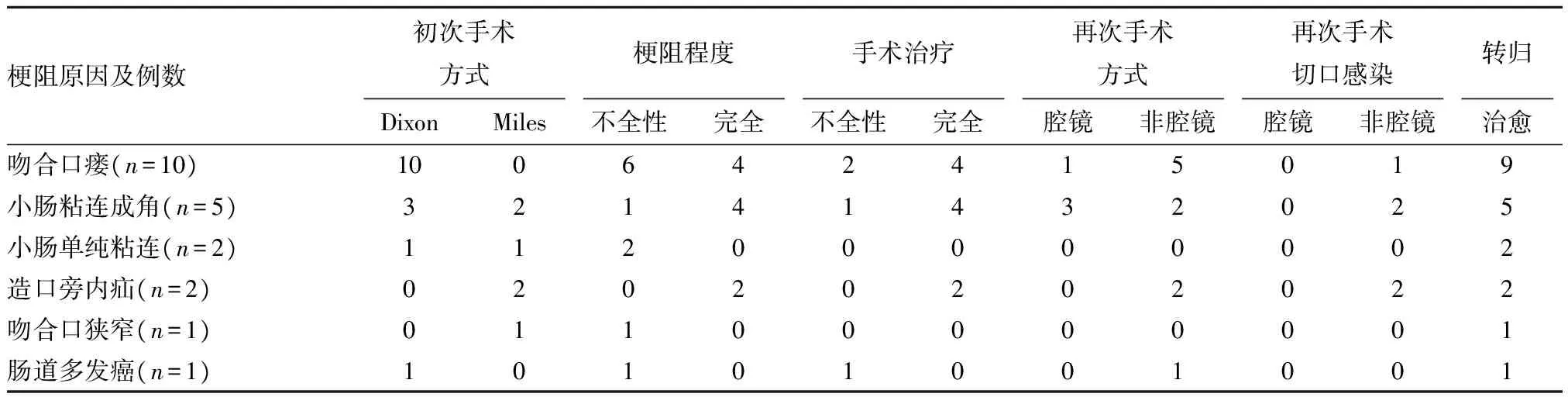
2.2 直肠癌术后早期肠梗阻的治疗 10例吻合口瘘患者中4例经双套管腹腔冲洗引流后瘘口愈合,梗阻缓解,6例保守治疗无效行近端结肠造口术,2例造口旁内疝患者行小肠内疝复位术,2例小肠单纯粘连患者经非手术治疗后梗阻缓解,5例小肠粘连成角患者行肠粘连松解术,1例造瘘口狭窄病例经扩肛后梗阻逐渐缓解,1例直肠癌并肠梗阻患者,术前肠镜直肠肿瘤处无法通过,急诊Dixon术后不全性肠梗阻,术后行腹部CT检查并发结肠肝曲癌,再次行右半结肠切除后梗阻缓解。1例吻合口瘘合并肠梗阻术后感染性休克患者家属放弃治疗未愈,其余20例全部治愈,见表1。
表1 直肠癌术后早期肠梗阻21例临床资料
梗阻原因及例数初次手术方式梗阻程度手术治疗再次手术方式再次手术切口感染转归DixonMiles不全性完全不全性完全腔镜非腔镜腔镜非腔镜治愈吻合口瘘(n=10)100642415019小肠粘连成角(n=5)32141432025小肠单纯粘连(n=2)11200000002造口旁内疝(n=2)02020202022吻合口狭窄(n=1)01100000001肠道多发癌(n=1)10101001001
对于再次手术时机的选择,如为不全性梗阻,可以先保守治疗,一周后如不能缓解可考虑手术,如果为完全梗阻,治疗24~48 h症状不能缓解应尽早手术。直肠癌术后早期完全性肠梗阻非手术治疗成功率远低于不全性肠梗阻,二者间差异具有统计学意义(P<0.05),见表2。
对于再次手术方式的选择,如果初次为腹腔镜手术,再次手术时可以先选择腹腔镜探查,本组21例直肠癌手术,再次手术14例,腹腔镜4例,腹腔镜手术较开腹手术减少了术后住院时间,两组间差异具有统计学意义(t=-2.403,P<0.05),腹腔镜术后无切口感染(0%),剖腹探查术后切口感染5例(50%),可能由于病例数较少,在术后切口感染发生率上未见明显统计学差异(P>0.05),见表3。
表2 不全性肠梗阻和完全性肠梗阻治疗方式比较n(%)
表3 腹腔镜和非腔镜再次手术后住院时间和术后切口感染比较

腔镜手术(n=4)非腔镜手术(n=10)tP再手术后住院时间/d11.50±7.4125.10±10.182.4030.033术后切口感染n(%)0(0)5(50)-0.221∗
*Fisher精确概率。
3 讨论
直肠癌术后早期肠梗阻缺乏典型的机械性梗阻临床表现,但又常合并机械性梗阻的病因,经非手术治疗大多数患者症状不能缓解,需要再次手术治疗,因此总结早期肠梗阻的原因和防治措施具有重要的临床意义。
3.1 原因 直肠癌Dixon术后早期肠梗阻最常见的原因是吻合口瘘,而Miles术后梗阻多由肠粘连引起,约占80%[3]。①吻合口瘘:术前新辅助放化疗、超低位保肛或术前梗阻肠道准备不充分的直肠癌患者术后吻合口瘘的发生率较高[4],容易引起肠功能障碍,多数为不全性梗阻;②肠粘连:多数发生于Miles术后,小肠易坠入盆底或与腹壁粘连形成梗阻;③腹内疝:常见于Miles术后,Miles术后可能形成两个空隙,一是造口的结肠与侧腹壁之间的空隙,二是盆腔腹膜关闭后与盆底之间的空隙,当空隙关闭不全时,小肠容易疝入空隙引起梗阻[5];④造瘘口狭窄、缺血;⑤肠道多发癌:近年来关于肠道多发癌的报道较多,术前梗阻的患者肠镜无法到达回盲部,术前CT也易漏诊,术中探查不仔细等原因遗留近端结肠肿瘤;⑥其他原因:吻合口狭窄、肠扭转、肠缺血坏死等也可以引起早期肠梗阻。
3.2 诊治 依据临床表现和辅助检查,直肠癌术后早期肠梗阻的诊断并不困难,有文献报道多层螺旋CT对早期肠梗阻的病因和梗阻部位有重要的诊断价值[6]。对于不明原因的梗阻,应先行保守治疗,在治疗过程中积极寻找病因。①非手术治疗:禁食,胃肠减压,肠外营养支持,维持水电解质平衡,应用生长抑素等;对于吻合口瘘患者应尽早双套管腹腔持续负压冲洗[7]。②手术治疗:直肠癌术后肠梗阻不要盲目趋向保守治疗,当患者症状不缓解或出现绞窄性肠梗阻时应考虑及时手术治疗。③手术方式的选择:随着腔镜技术的普及,越来越多的术者选择腹腔镜直肠切除,而且腹腔镜已经不是肠梗阻手术的绝对禁忌,对于腹部膨隆不明显的患者,如果初次手术方式为腹腔镜,再次手术可以选择腹腔镜探查,能够更有效地寻找梗阻原因和减少术后住院时间。
3.3 预防 为避免术后早期肠梗阻的发生,术前完善准备、术中仔细操作和术后精心护理极其重要。①术前纠正合并症,维持机体良好的营养状况,尽量减少术前禁食时间和多次口服药物行肠道准备;②对于吻合口瘘的高危人群,在保证淋巴结清扫的前提下,保留左结肠动脉,保证吻合口的良好血供[8];③术中发现吻合不满意,可行预防性末端回肠造瘘[9];④关闭Miles术后的两个空隙,如果张力过大难以关闭可以考虑顺其开放,不要刻意关闭成小的腔隙,否则更容易导致内疝的发生;⑤关腹前理顺肠管,放置通畅引流,减少术后渗出引起粘连;⑥术后造瘘口要定期护理,对怀疑狭窄者应早期扩张人工肛门。
总之,直肠癌术后早期肠梗阻病因复杂,我们在临床上应注意早期发现和预防。对于已经出现的肠梗阻病例应在非手术治疗的同时积极寻找病因,经过保守治疗效果不佳的完全性肠梗阻患者应尽早合理选择手术时机和手术方式,最大程度地减少术后并发症的发生。
【参考文献】
[1] 俞宏斌,沈福兴,朱炜,等.直肠癌术后早期肠梗阻57例临床诊治探讨[J].中国基层医药,2017,24(3):382-386.
[2] 张忠涛,李宇.术后早期炎症性肠梗阻的诊断与治疗理念[J].中华普外科手术学杂志(电子版),2011,5(3):261-264.
[3] 杨万友,毛学文,张一民.直肠癌Miles术后早期肠梗阻的原因与诊治[J].中国现代医学杂志,2010,20(11):1747-1748.
[4] PARK JS,CHOI GS,KIM SH,etal.Muhicenter analysis of risk factors for anastomotic leakage after laparoscopic rectal cancer excision:the Korean laparoscopic colorectal surgery study group[J].Ann Surg,2013,257(4):665-671.
[5] JWT TOH,R LIM,A KESHAVA,etal.The risk of internal hernia or volvulus after laparoscopic colorectal surgery:a systematic review[J].Colorectal Disease,2016,18(12):1133-1141.
[6] 张晓丹,王文红,李鹏,等.MSCT对直肠癌术后肠梗阻的诊断价值及临床意义[J].中华普通外科杂志,2015,30(1):27-30.
[7] 张渝科,谭云火,吴国庆,等.改良双套管持续负压冲洗引流对腹部创伤术后肠瘘疗效观察[J].创伤外科杂志,2016,15(3):309-313.
[8] ARBMAN G.High tie in anterior resection for rectal cancer confers no increased risk of anastomotic leakage[J].Br J Surg,2012,99(4):127-132.
[9] 张勇,郭子健,曹华祥,等.低位直肠癌保肛中预防性造口的临床应用分析[J].中华普外科手术学杂志(电子版),2016,10(2):133-136.
Earlyintestinalobstructionfollowingrectalcancersurgery:Clinicalanalysisin21cases
ZUOXueliang,CAIJuan,WANGJunfeng,LIANGLinhu,WUJian
Department of Gastrointestinal Surgery,The First Affiliated Hospital of Wannan Medical College,Wuhu 241001,China
Objective:To investigate the causes for early incidences of intestinal obstruction after rectal cancer resection for following preventive and management strategies.Methods:Clinical data were initially retrieved in 1182 cases undergone rectal cancer surgery, then retrospective analysis was performed in the 21 cases complicated with early postoperative intestinal obstruction.Results:In the 21 cases,15 received Dixon′s operation(71.4%) and 6 Miles surgery(28.6%).Anastomotic fistula occurred in 10 cases(47.6%),adhesion angles of small bowel to pelvic floor or abdominal wall in 5(23.8%),simple intestinal adhesion in 2(9.5%),parastomal internal hernia in 2(9.5%),stoma stenosis in 1(4.8%),and multiple colorectal cancer in 1(4.8%).Fourteen cases underwent reoperation(66.7%),4 laparoscopic exploration(28.6%) and 10 laparotomy(71.4%).Twenty patients were cured, and failure in one.Patients complicated with early postoperative complete intestinal obstruction following rectal cancer surgery had significantly lower management rate by non-operative modality than that with incomplete intestinal obstruction.The difference was significant(P<0.05).Postoperative hospital stay was shorter in patients undergone laparoscopic reoperation than those received laparotomy(P<0.05).Conclusion:The most common causes of early intestinal obstruction after rectal cancer surgery are associated with anastomotic fistula (Dixon operation) and intestinal adhesion (Miles surgery) besides intra-abdominal hernia. Special attention should also be paid to the rare occurrence of multiple colorectal cancers in operation. Successful management rate by non-operative modality seems lower for early postoperative complete intestinal obstruction. Rational surgical options should be implemented for patients with poor conservative treatment.
rectal neoplasm;intestinal obstruction;prevention;treatment
1002-0217(2017)06-0539-03
皖南医学院中青年科研基金项目(WK2016F04)
2017-06-20
左学良(1984-),男,主治医师,讲师,(电话)15156300128,(电子信箱)zuoxueliang0202@126.com。
R 735.3;R 656.7
A
10.3969/j.issn.1002-0217.2017.06.008
