盐酸介质中复配缓蚀剂对N80钢缓蚀效果分析研究
2017-12-261b西北大学化工学院载能技术与应用研究所陕西710069南洋理工大学材料科学与工程学院新加坡639798
, , , , ,1b(1.西北大学 a.化工学院;b.载能技术与应用研究所, 陕西 西 710069;2.南洋理工大学 材料科学与工程学院, 新加坡 639798)
试验研究
盐酸介质中复配缓蚀剂对N80钢缓蚀效果分析研究
胡军1a,2,王甜甜1a,王祯1a,樊安1a,郑茂盛1a,1b
(1.西北大学 a.化工学院;b.载能技术与应用研究所, 陕西 西安 710069;2.南洋理工大学 材料科学与工程学院, 新加坡 639798)
针对N80钢在盐酸溶液中的腐蚀,利用曼尼希碱与钨酸钠复配缓蚀剂作为盐酸溶液中N80钢的缓蚀剂,通过X射线光电子能谱、电化学实验分析研究了N80钢在不同配比缓蚀剂中的缓蚀行为。研究结果表明,曼尼希碱与钨酸钠缓蚀剂复配使用后,随着配比的增大,腐蚀电流密度逐渐减小,容抗弧半径逐渐增大,当曼尼希碱与钨酸钠缓蚀剂浓度均为0.000 2 mol/L(配比为1∶1)时,缓蚀效率最高。微观分析表明,缓蚀剂复配后Fe2p结合能均大于单独使用两种缓蚀剂时的结合能,表明复配后钨酸钠缓蚀剂在N80钢表面形成的沉淀膜可以有效弥补N80钢在曼尼希碱吸附膜中的空隙,两者结合形成了致密的膜层,有效提高了缓蚀效率。
N80钢; 缓蚀剂; 复配; X射线光电子能谱; 电化学实验
N80钢是一种常用的石油套管材料,常被用于油气开采和输送,使用时往往处于高温、高压或CO2、H2S酸性气体、Cl-等环境中[1-3]。这些腐蚀介质对金属的腐蚀可能会导致N80钢性能下降、使用寿命减短,甚至材料失效,对油气开采和运输过程的安全性与可靠性造成很大威胁。因此,降低N80钢在腐蚀介质中的腐蚀速率对石油行业具有重要意义。目前,国内外采用的金属腐蚀防护方法主要有电化学保护法、涂层法及缓蚀剂法等。其中,缓蚀剂法因具有低毒、高效、便捷的特点而被广泛应用[4]。任晓光等研究了2-巯基苯并咪唑与复配缓蚀剂对N80钢在HCl介质中的缓蚀性能,结果表明,2-巯基苯并咪唑的加入抑制了电极阳极的腐蚀过程,而它与十六烷基三甲基溴化铵和硫脲复配后的缓蚀效果优于单独使用2-巯基苯并咪唑的性能[5]。Mahendra Yadavd等采用不同的氨基酸混合物作为盐酸溶液中N80钢的复配缓蚀剂进行实验,结果显示,复配缓蚀剂具有很好的协同效应,缓蚀效率随复配缓蚀剂浓度的增大而增加[6]。但对复配后缓蚀机理的研究较少。
针对N80钢在盐酸溶液中的腐蚀情况,笔者采用X射线光电子能谱(XPS)仪,研究了N80钢在加入单独曼尼希碱、单独钨酸钠缓蚀剂和它们通过不同配比形成的复配缓蚀剂的HCl腐蚀溶液中形成膜的表面、膜层深度的元素含量变化和结合能变化,以及复配缓蚀剂在N80钢表面作用的缓蚀机理,同时采用电化学实验方法对得出的结论进行了相应的验证。
1 N80钢缓蚀性能实验
1.1 实样制备
实验中选用的材料为N80钢,其具体化学成分见表1。
用线切割法将N80钢加工成5 mm×5 mm×3 mm的小方块和规格为Ø14.5 mm×3 mm的圆片,用400#、800#和1 000#金相砂纸将样品测试面逐级打磨,再用抛光机将其抛光。最后依次用乙醇和重蒸水清洗,干燥后备用[7]。

表1 N80钢化学成分 %
1.2 实验设计
本次共设计了8组实验,分别对应于8种不同的腐蚀溶液,见表2。
实验样品均为分析纯,实验用重蒸水。将样品N80钢放在相应的腐蚀溶液中浸泡18 h,待其形成稳定的表面吸附膜之后,利用X射线光电子能谱仪对样品表面进行XPS测试。X射线光电子能谱仪采用的是日本岛津-Kratos AXIS UltraDLD,Al-Kα为激发源,能量为1 486.68 eV,靶电流为10 mA,分析器传输能量为50 eV,溅射速度为2.4 nm/s,溅射角度为30°。以样品N80钢表面碳的结合能定标。对XPS数据采用Avantage软件进行分峰以及拟合处理[8]。

表2 8组不同腐蚀溶液组成
利用Parstat2273电化学工作站测得在N2环境下60 ℃时第③~⑧组实验的极化曲线和电化学阻抗谱。因为样品除了浸泡时受外界环境中O2对它的影响外,X射线光电子能谱仪检测过程中不存在O2对样品的影响,故选用N2环境最接近XPS实验检测条件。
在自腐蚀电位下进行电化学交流阻抗测试,扫描频率为0.01~100 000 Hz,施加的体系扰动电压幅值为5 mV,测试电位为开路电位。测定极化曲线时扫描速度为5 mV/s,扫描电位为-500~500 mV(相对于开路电位)。
2 N80钢缓蚀性能实验结果与讨论
2.1 XPS分析
2.1.1膜层表面XPS全谱分析
15%(质量分数)盐酸中加入3种缓蚀剂后N80钢的XPS全谱图见图1。

图1 3种缓蚀剂溶液中N80钢XPS全谱图
从图1中曲线a可以看出,金属表面膜的主要元素为C、N、O、Fe和Cl[9]。其中,C元素来自样品和缓蚀介质,N元素来自缓蚀介质,O元素来自缓蚀介质与外界环境,Fe元素来自样品,Cl元素来自溶液。N元素的存在证明曼尼希碱确实吸附在了N80钢的表面,但Cl元素的峰仍然存在,表明曼尼希碱在金属表面形成的膜结构不稳定,因此,N80钢表面仍受到了腐蚀。
从图1中曲线b中可以看出,浸泡18 h后形成沉淀膜的主要元素为C、Fe、Se、Cl、O、W和Na。其中,C、Fe和Se元素来自样品,Cl元素来自溶液,O元素来自缓蚀介质和外界环境,W和Na元素来自缓蚀介质。W和Na元素峰的存在揭示了钨酸钠在金属N80钢表面沉淀的事实。同样,因为钨酸钠在金属表面形成的膜层不够稳定,所以在检测中仍然出现了Cl元素的峰[10]。
从图1中曲线c可以看出,复配缓蚀剂中所形成膜的表面主要元素为C、N、O、Fe、Se、W和Na。其中,C元素来自样品与缓蚀介质,N元素来自缓蚀介质,O元素来自缓蚀介质与外界环境,Fe和Se元素来自样品,Na和W元素来自缓蚀介质。检测结果中未出现Cl元素的峰,表明腐蚀产物不存在或含有极少量氯化物。这是因为复配后形成了致密的膜层,使得腐蚀氯离子很难扩散到金属表面,N80钢表面被保护了起来,有效提高了缓蚀效率。
加入不同配比缓蚀剂溶液后N80钢的XPS全谱图见图2。
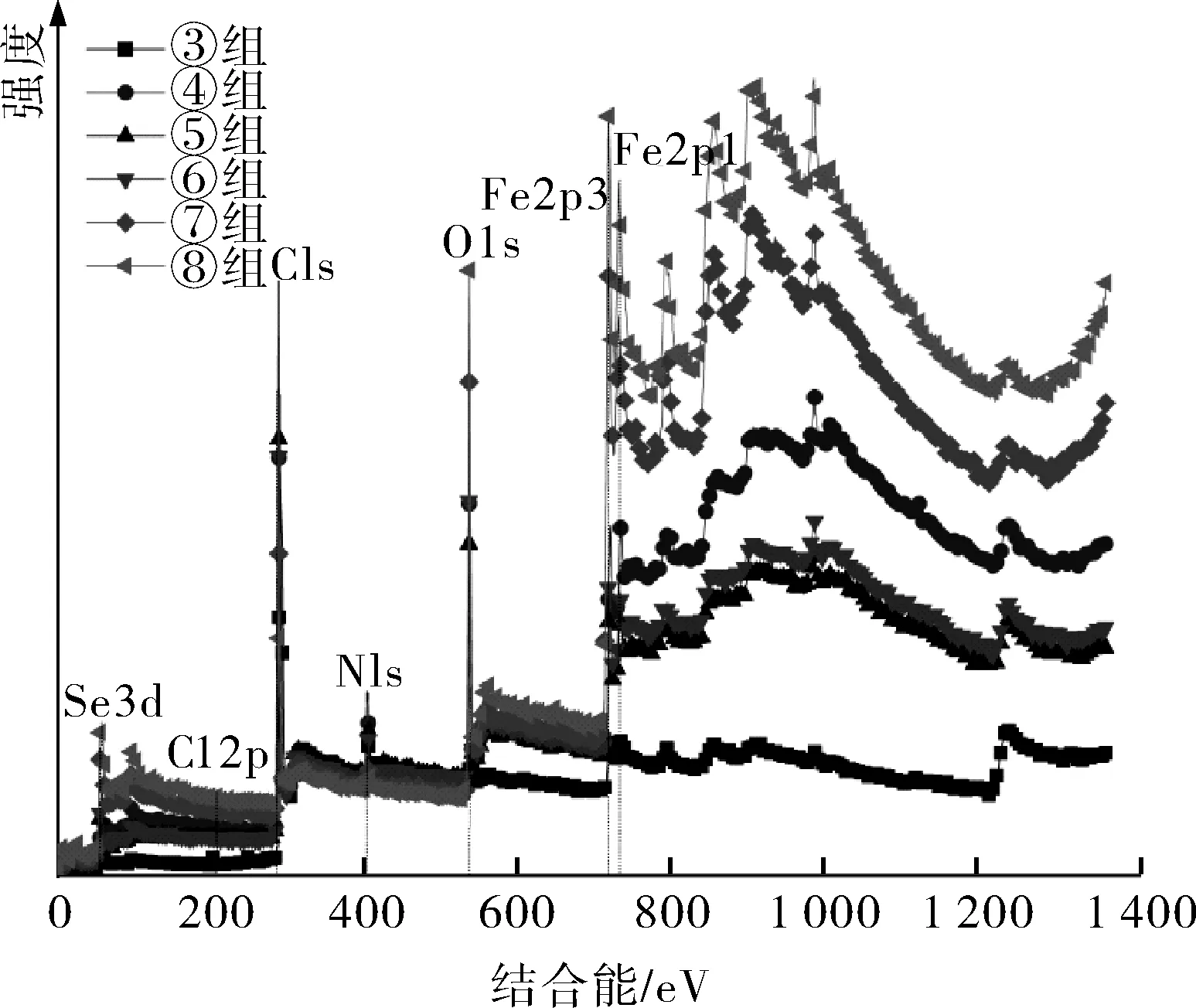
图2 加入不同配比缓蚀剂溶液后N80钢XPS全谱图
从图2中可以看出,随着缓蚀剂配比的增大,Fe和O元素的峰强度逐渐增强,Cl元素的峰强度逐渐降低。不同配比的缓蚀剂会在N80钢表面形成不同稳定性或者致密性的膜层结构。Cl元素质量分数越低,Fe元素的质量分数越多,说明膜层结构越稳定,形成的保护膜的覆盖度越大,N80钢被保护得越好。
对比图2中各配比下的全谱图以及表3所列的N80钢表面主要元素质量分数数据发现,改变缓蚀剂配比,Cl和Fe元素的质量分数也会发生相应的变化。当缓蚀剂配比为1∶1时,未检测到Cl元素,同时Fe元素质量分数最高,达到10.79%,说明此配比条件最有效,复配缓蚀剂的缓蚀效果最好。

表3 加入不同配比缓蚀剂溶液后N80钢表面主要元素含量
2.1.2膜层元素结合能分析
当物体(体系)由2个或多个部分组成时,各组成部分之间存在一定相互吸引力使其结合在一起,结合能表示了各组成部分结合的紧密程度。被测元素的结合能变化与其周围的化学环境有关,根据这一变化可以推测出该元素的化学结合状态和价态[11]。结合能数值越大,分子(原子或原子核)的结构就越稳定。
N80钢在8组腐蚀溶液中的表面Fe2p结合能见表4。当加入单独曼尼希碱时,Fe2p结合能为707.19 eV;当加入单独钨酸钠时,Fe2p结合能为709.13 eV。这说明钨酸钠中的钨酸根与金属表面铁的结合能力更强,形成的膜层结构更稳定。加入复配缓蚀剂后的Fe2p结合能均大于单独使用曼尼希碱或钨酸钠缓蚀剂时的Fe2p结合能,说明复配后表面形成的保护膜致密程度更好。复配后,随着曼尼希碱浓度的减小,其分子数随之减少,更多的钨酸根与Fe2+结合沉淀在了吸附膜的空隙处,使得缓蚀效果逐步提升。当曼尼希碱与钨酸钠浓度均为0.000 2 mol/L(配比为1∶1)时,Fe2p的结合能最大,为711.50 eV,表明此时膜层结构最稳定,对N80钢的保护作用最有效。

表4 N80钢在8组腐蚀溶液中表面Fe2p结合能
N80钢在浓度为0.000 2 mol/L的曼尼希碱与0.000 2 mol/L的钨酸钠复配缓蚀剂中浸泡18 h后,在刻蚀时间为250 s时的XPS谱中检测到了C、N、O、Fe和Na元素,其质量分数分别为w(C)=25.17%、w(N)=0.77%、w(O)=35.56%、w(Fe)=36.12%和w(Na)=2.38%。在1∶1复配缓蚀剂的腐蚀溶液中,N80钢表面膜层上浸泡形成的C、N、O、Fe、Na的光电子谱线以及Fe的俄歇谱线峰图见图3。
XPS的谱线结构除了有光电子谱线外,还存在着卫星峰(伴峰)、俄歇电子谱线、自旋-轨道分裂和鬼峰[12]。

图3 1∶1复配缓蚀剂腐蚀溶液中浸泡形成的N80钢表面膜层XPS谱线峰图
图3a中结合能为283.77 eV的C的s主峰C1s峰表示缓蚀剂分子中的C-C或者C-H键[13]。图3b中N的s主峰N1s位于398.28 eV的主峰是缓蚀剂分子中的N-H键,这是缓蚀剂分子吸附在N80钢表面的证据。同时在主峰的两侧还存在着不同强度的卫星峰/伴峰[14,15]。图3c中结合能为528.98 eV处表示腐蚀溶液中的溶解氧,而结合能为530.48 eV的峰为曼尼希碱分子中的C-O键。查阅关于含有不同价态Fe化合物的XPS谱文献[13]以及XPS手册可以知道,单质Fe的Fe2p3结合能峰值为706.75 eV,Fe2O3的Fe2p3结合能峰值为710.70 eV,且它们与其对应的Fe2p1结合能的峰间距分别为13.2和13.6,即Fe2p1结合能分别为719.45 eV和724.30 eV。据此可以推断图3d中,705.68 ~718.68 eV为金属表面的单质铁,708.38~721.78 eV为N80钢表面的单质铁与氧反应形成的Fe2O3。图3e中结合能为1 072.94 eV的Na1s(Na的s主峰)峰对应于缓蚀剂分子中的Na+。图3f为Fe的俄歇电子能谱线,其(指Fe的俄歇电子)动能与入射光的能量hv(h为普朗克常量,v为入射光的频率)无关[16],位于784.0 eV和846.0 eV的特征峰表明Fe(Ⅱ)和Fe(Ⅲ)同时存在于N80钢的表面,说明除了缓蚀剂分子与金属表面的单质Fe反应生成二价铁之外,溶解在腐蚀溶液中的氧同样参与了吸附过程,氧化了金属表面的Fe,促进了缓蚀剂分子在N80钢表面的吸附。
2.2 电化学分析验证
2.2.1电化学阻抗谱
对于金属-液体系的界面,交流阻抗行为表现为高频区域的电化学反应控制和低频区域的扩散控制[17]。N2环境下60 ℃时N80钢在未加入缓蚀剂和加入不同配比缓蚀剂盐酸腐蚀溶液中的Nyquist阻抗谱见图4(阻抗值Z在电化学实验中被定义为复数Z,Z(w)=Zre(w)+jZim(w),横坐标Zre=|Z|cosθ,纵坐标Zim=|Z|sinθ)。从图4可以看出,未加入缓蚀剂时,腐蚀反应阻力小,因此容抗弧的半径也比较小。这是由于盐酸中的Cl-从溶液扩散到了金属表面,对N80钢表面造成了一定的腐蚀。加入不同配比的缓蚀剂后,其阻抗谱均表现出比未加缓蚀剂时更大的容抗弧。而在高频区域,容抗弧代表电荷传递电阻,说明加入缓蚀剂后,腐蚀反应阻力增大,缓蚀剂在金属表面形成的保护膜减缓了腐蚀反应速度,抑制了Cl-从溶液扩散到金属表面的过程[18]。对比发现,当缓蚀剂配比为1∶1时,容抗弧的半径最大,说明此配比条件下N80钢表面受到的腐蚀最轻。
等效电路图指用一些电学元件以及电化学元件构成一个与测试所得电化学阻抗谱相同阻抗频谱的电路。经过对比分析,本实验中采用误差最小的R(Q(R(QR)))等效电路图,见图5。图5中,Rs为腐蚀溶液电阻,Rf为膜电阻,Rct为电荷转移电阻,Ω·cm2;Cf为金属表面的膜电容,Cdl为双电层电容,F/m2。

图4 N80钢在未加入及加入不同配比缓蚀剂腐蚀溶液中的阻抗谱

图5 N80钢在腐蚀溶液中的等效电路图
③组~⑧组中电荷转移电阻Rct的拟合误差依次为1.94×10-3、2.34×10-3、3.68×10-3、2.06×10-3、0.16×10-3、1.30×10-3,均在10%以内,说明实验结果与拟合结果较为一致,等效电路图的拟合数据见表5。
由表5可以看出,加入一定配比的缓蚀剂后,溶液中的电荷转移电阻Rct均迅速增大,双电层电容迅速降低。Rct的大小反映了电极-溶液界面电化学反应速度的快慢。当金属表面覆盖了缓蚀剂膜层后,膜对电荷传递的阻碍作用改变了电极-溶液界面的阻抗响应,表现为Rct增大,即高频区的容抗弧半径增大[19],同时表现为双电层电容降低。表明加入缓蚀剂后,缓蚀剂膜对Cl-在溶液中的扩散起到了阻碍作用,使得腐蚀反应速度减小。对不同配比的缓蚀剂,其电荷转移电阻和双电层电容的变化程度不一样。当电荷转移电阻增大程度相差不大时,双电层电容越低,表示缓蚀效果越好。综合考虑,缓蚀效果最好的缓蚀剂配比为1∶1,说明曼尼希碱和钨酸钠缓蚀剂对N80钢在盐酸溶液中的腐蚀有较好的缓蚀作用。

表5 等效电路图拟合的电化学参数
根据交流阻抗谱中的电荷传递电阻,利用式(1)可以计算出金属表面所形成保护膜的覆盖度,计算结果见表5。

(1)

从表5数据可以看出,膜层覆盖度随加入不同配比缓蚀剂的变化而变化。膜层覆盖度越大,金属表面受到的腐蚀越轻。当缓蚀剂配比为1∶0.1和1∶1时,膜层覆盖度分别为99.85%和99.83%,相对其它组覆盖程度最大。
2.2.2极化曲线
利用腐蚀电极极化曲线方程(2)对极化数据进行拟合,N2环境下60 ℃时N80钢在未加入和加入不同配比缓蚀剂腐蚀溶液中的拟合极化曲线见图6,腐蚀动力学数据见表6。
(2)
式中,J和Jcorr分别为加入缓蚀剂和未加入缓蚀剂时的腐蚀电流密度,A/cm2;ΔE为有电流通过时电极的极化值,V;βa为阳极极化曲线斜率,βc为阴极极化曲线斜率,mV。
材料在腐蚀介质中腐蚀电流密度的大小是评价其耐腐蚀性能的重要指标之一,腐蚀电流密度越大,材料腐蚀越严重,反之耐腐蚀性能越好[20]。从图6的极化曲线可以看出,N2环境下加入缓蚀剂后,曲线较未加入缓蚀剂时均出现了左移,即阴极腐蚀电流密度减小,而阳极腐蚀电流密度未发生明显变化,表明复配缓蚀剂对N80钢在盐酸中的腐蚀主要表现为控制阴极反应。缓蚀剂配比为1∶0.5、1∶0.8和1∶1时,腐蚀电位出现了负移,表明在加入缓蚀剂后,金属表面形成的膜层对阴极反应的阻滞能力大于对阳极反应的阻滞能力。表6中腐蚀电流密度的变化与极化曲线一致。未加入缓蚀剂的腐蚀电流密度为86.98×10-5A/cm2,加入缓蚀剂后腐蚀电流密度迅速减小,最小为0.06×10-5A/cm2,此时缓蚀剂的配比为1∶1,说明此配比条件下的缓蚀效果最佳。
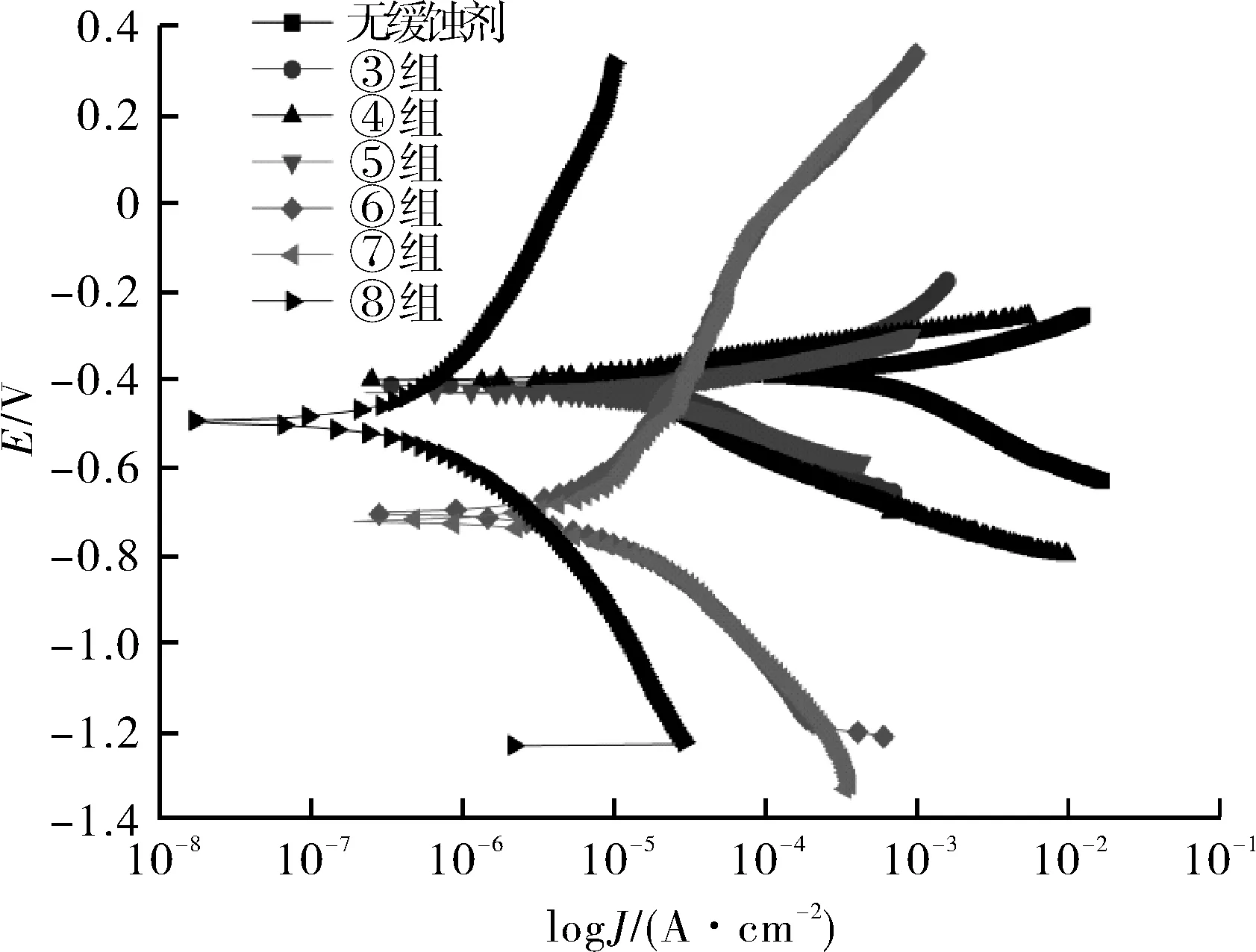
图6 N80钢在未加入及加入不同配比缓蚀剂腐蚀溶液中极化曲线

表6 N80钢在未加入及加入不同配比缓蚀剂腐蚀溶液中动力学参数
3 结语
采用XPS、电化学实验分析研究了N80钢在不同配比缓蚀剂盐酸溶液中的缓蚀行为。XPS实验结果表明,曼尼希碱与钨酸钠缓蚀剂复配使用后,在N80钢表面形成更加致密的膜层结构,且当配比为1∶1时,Fe2p的结合能最大,复配效果最好。电化学实验结果显示,复配缓蚀剂对N80钢在盐酸中的腐蚀主要表现为控制阴极反应,曼尼希碱与钨酸钠的配比为1∶1时腐蚀电流密度最小,缓蚀效果最好,膜层覆盖度为99.83%。XPS分析结果与电化学实验结果一致。
[1] 何庆龙,孟惠民,俞宏英,等.N80油套管钢CO2腐蚀的研究进展[J].中国腐蚀与防护学报,2007,27(3):186-192.
(HE Qing-long,MENG Hui-min,YU Hong-ying,et al. Recent Developments in Carbon Dioxide Corrosion of N80 Well Tube Steel[J]. Journal of Chinese Society for Corrosion and Protection,2007,27(3):186-192.)
[2] 张清,李全安,文九巴,等.不同H2S分压下N80油管钢的CO2/H2S腐蚀行为[J].腐蚀与防护,2008,29(3):133-134,146.
(ZHANG Qing,LI Quan-an,WEN Jiu-ba,et al. CO2/H2S Corrosion Behavior of Tubular Steel N80 at Different H2S Partial Pressures[J]. Corrosion & Protection,2008,29(3):133-134,146.)
[3] 李金波,郑茂盛.Cl-对N80油套管钢钝化膜半导体性能的影响[J].西安交通大学学报,2006,40(11):1325-1328.
(LI Jin-bo,ZHENG Mao-sheng. Influence of Cl-on Semiconductive Properties of Passive Film Formed on N80 Oil Tube Steel[J]. Journal of Xi’an Jiaotong University,2006,40(11):1325-1328.)
[4] 王英,曹祖宾,孙微微,等.缓蚀剂的分类和发展方向[J].全面腐蚀控制,2009,23(2):24-26.
(WANG Ying,CAO Zu-bin,SUN Wei-wei,et al. The Category and the Development Directions of Corrosion Inhibitors[J]. Total Corrosion Control,2009,23(2):24-26.)
[5] 任晓光,赵映璐,谢超然,等.2-巯基苯并咪唑与复配缓蚀剂对N80钢在HCl介质中的缓蚀性能[J].全面腐蚀控制,2014,28(2):52-56.
(REN Xiao-guang,ZHAO Ying-lu,XIE Chao-ran,et al. Inhibition of 2-Mercaptobenzimidazole with Complex Inhibitors for N80 Steel in HCl Solution[J]. Total Corrosion Control,2014,28(2):52-56.)
[6] Yadav M,Sarkar T K,Purkait T. Amino Acid Compounds as Eco-friendly Corrosion Inhibitor for N80 Steel in HCl Solution:Electrochemical and Theoretical Approaches[J]. Molecular Liquids,2015,212:731-738.
[7] Jun Hu,Yun Wang,Lijun Yu,et al. An Investigation of a Combined Thiourea and Hexamethyleneteramine as Inhibitors for Corrosion of N80 in 15%HCl Solution:Electrochemical Experiments and Quantum Chemical Calculation[J]. International Journal of Corrosion,2015:1-12.
[8] El-moneim A A,Akiyama E,Habazaki H,et al. XPS and Electrochemical Studies on the Corrosion Behavior of Sputter-deposited Amorphous Mn-Nb Alloys in a Neutral Chloride Solution[J]. Corrosion Science,1998,40(9):1513-1531.
[9] 于静敏,柳鑫华,梁英华.钨酸盐作海水缓蚀剂可行性讨论[J].表面技术,2006,35(5):60-64.
(YU Jing-min,LIU Xin-hua,LIANG Ying-hua. Research on Feasibility of Tungstate as Seawater Corrosion Inhibitor[J]. Surface Technology,2006,35(5):60-64.)
[10] 任晓光,周继敏,刘丹,等.曼尼希碱及其复配缓蚀剂对N80钢的缓蚀性能[J].钻井液与完井液,2010,27(2):72-73.
(REN Xiao-guang,ZHOU Ji-min,LIU Dan,et al. Corrosion Inhibition of Mannich Base Corrosion Inhibitor to N80 Steel[J]. Drilling Fluid & Completion Fluid,2010,27(2):72-73.)
[11] 张强基.X光电子谱术[J].理化检验-物理分册,2002,38(3):133-138.
(ZHANG Qiang-ji. X-Ray Photoelectron Spectroscopy[J]. Physical Testing and Chemical Analysis Part A:Physical Testing,2002,38(3):133-138.)
[12] Zarrok H,Zarrouk A,Hammouti B,et al. Corrosion Control of Carbon Steel in Phosphoric Acid by Purpald-Weight Loss,Electrochemical and XPS Studies[J]. Corrosion Science,2012,64:243-252.
[13] 谢景林.X射线光电子能谱仪应用-特殊样品测量及复杂图谱解析[J].现代仪器,2009,15(5):16-20.
(XIE Jing-lin. Application of X-ray Photoelectron Spectroscopy: Detection and Analysis of Special Sample and Complex Spectrum[J]. Modern Instruments,2009,15(5):16-20.)
[14] 左长明,赵纯培,陈红,等.铀表面氧化层的X射线光电子能谱研究[J].四川大学学报(自然科学版),1998,35(3):424-428.
(ZUO Chang-ming,ZHAO Chun-pei,CHEN Hong,et al. XPS Study of Oxide Layers on the Surface of Uranium[J]. Journal of Sichuan University(Natural Science Edition),1998,35(3):424-428.)
[15] Descostes M,Mercier F,Thromat N,et al. Use of XPS in the Determination of Chemical Environment and a Data Basis in Binding Energies for Fe and S Reference Compounds and Applications to the Evidence of Surface Species of an Oxidized Pyrite in a Carbonate Medium[J]. Applied Surface Science,2000,165:288-302.
[16] 吴正龙.X射线诱导俄歇电子能谱(XAES)的应用[J].现代仪器,2009,15(1):58-61.
(WU Zheng-long. Application of X-ray Induced Auger Electron Spectroscopy(XAES)[J]. Modern Instruments,2009,15(1):58-61.)
[17] Yun Wang,Jun Hu,Yuqi Wang,et al. A New Method for Preventing Corrosion Failure:Thiourea and Hexamethylenetetramine as Inhibitor for Copper,Bull[J]. Korean Chem. Soc.,2016(37):1797-1811.
[18] Tokuda K,Gueshi T,Matsuda H. Voltammetry at Partially Covered Electrodes:Part II. Linear Potential Sweep and Cyclic Voltammetry[J]. Electroanal. Chem.,1979(1):29-38.
[19] 王春涛.金属铜腐蚀的防护[M].北京:中国石化出版社,2006:32-37.
(WANG Chun-tao. Metal Copper Corrosion Protection[M]. Beijing:China Petrochemical Press Co. Ltd.,2006:32-37.)
[20] 胡军,王赟,余历军,等.硫酸银对氯离子环境下Alloy690缓蚀特性的电化学分析[J].化工学报,2014,65(10):4032-4038.
(HU Jun,WANG Yun,YU Li-jun,et al. Electrochemical Analysis of Inhibition by Silver Sulfate for Alloy690 in Chloride Solution[J]. CIESC Journal,2014,65(10):4032-4038.)
CorrosionInhibitionEffectResearchofCompoundCorrosionInhibitorforN80SteelinHClSolutionMedium
HUJun1a,2,WANGTian-tian1a,WANGZhen1a,FANAn1a,ZHENGMao-sheng1a,1b
(1.Northwest University,a. School of Chemical Engineering;b.Institute of Energy Technology and Application,Xi’an 710069,China;2.School of Materials Science and Engineering,Nanyang Technological University,Singapore 639798,Singapore)
The behavior of compound corrosion inhibitors was investigated based on X-ray photoelectron spectroscopy and electrochemical experiment. Mannich base and sodium tungstate were compounded as corrosion inhibitors. A series solution concentration and combine proportion was used for both Mannich base and sodium in the research. The results indicated that along with the increasing of the proportion, the corrosion current density decreases while the capacitance arc radius increases gradually. When the Mannich base and sodium tungstate concentration are both 0.000 2 mol/L and combined in a ratio of 1∶1, a maximum corrosion efficiency was obtained. In addition, microscopic analysis showed that compound corrosion inhibitor owns Fe2p binding energy larger than that the two single corrosion inhibitor either. It illustrated that sodium tungstate precipitation had effectively filled the lap in the Mannich base adsorption film and formed a dense film on N80 steel material surface, and an enhanced corrosion inhibition efficiency was obtained.
N80 steel;inhibitor;compound;X-ray photoelectron spectroscopy;electrochemical experiment
1000-7466(2017)06-0001-08
2017-05-30
国家自然科学基金(21676216);中国博士后基金(2014M550507,2015T81046);陕西省教育厅专项基金(14JK1751);陕西省工业攻关项目(2014K08-28)
胡 军(1982-),男,陕西西安人,副教授,博士,从事腐蚀与防护研究工作。
TG174.41
A
10.3969/j.issn.1000-7466.2017.06.001
(张编)
