脂蛋白相关磷脂酶A2免疫荧光层析法的建立及临床应用
2017-12-25,,,,
,,,,
(1.南华大学附属第一医院检验科,湖南 衡阳 421001;2.广州市微米生物科技有限公司)
·技术与方法·
脂蛋白相关磷脂酶A2免疫荧光层析法的建立及临床应用
谢海涛1,汤永平2*,解巧丽2,张晓丽2,潘秀华2
(1.南华大学附属第一医院检验科,湖南 衡阳 421001;2.广州市微米生物科技有限公司)
目的建立脂蛋白相关磷脂酶A2免疫荧光层析定量测定方法,并对其进行临床应用评价。方法
利用双抗体夹心法,研制脂蛋白相关磷脂酶A2时间分辨免疫荧光层析试纸条,通过检测其线性范围、最低检测限、精密度等指标进行实验室性能评估;选取230例临床血清样本,同时使用本方法和美国Diadexus公司的脂蛋白相关磷脂酶A2试剂进行比对试验,进行临床应用评估。结果脂蛋白相关磷脂酶A2免疫荧光层析定量测定试剂线性范围为20 μg/L~1 000 μg/L,最低检测限为10 μg/L,重复检测不同浓度的脂蛋白相关磷脂酶A2蛋白,批次内及批次间变异系数均小于10%;本试剂与美国的Diadexus公司的试剂检测临床样本的总符合率为90.87%,Kappa值为0.804,相关系数r=0.968,相关性具有统计学意义(P<0.01)。结论免疫荧光层析法测定脂蛋白相关磷脂酶A2,各项分析指标均能达到临床要求,且便捷准确,可用于临床血清样本的快速检测。
脂蛋白相关磷脂酶A2; 免疫荧光层析; 动脉粥样硬化
脂蛋白相关磷脂酶A2(lipoprotein-associated phospholipase A2,Lp-PLA2)是心血管疾病中一种新的炎症酶,能水解氧化低密度脂蛋白(low density lipoprotein, LDL),产生溶血磷脂酰胆碱(lysophosphatidylcholine,Lyso-PC)和氧化型游离脂肪酸(oxidized free fatty acids,ox-FA),促进动脉粥样硬化(atherosclerosis,AS)的形成和发展,其与临床疾病的关系日益受到关注。近年来研究认为对Lp-PLA2水平的检测可以识别心脑血管病高危个体[1]。
Lp-PLA2由PLA2G7基因编码,又被称为血小板活化因子乙酰水解酶(platelet activating factor-AH,PAF-AH),属于磷脂酶家族中PLA2的一种,是丝氨酸依赖的磷脂酶,其催化活性不需要Ca2+。迄今为止,已知Lp-PLA2有两种类型:血浆型Lp-PLA2与细胞型Lp-PLA2。血浆型Lp-PLA2分子量为45 kDa;细胞型Lp-PLA2包括:Lp-PLA2II、Lp-PLA2 Ib[2]。人血浆Lp-PLA2主要由成熟的巨噬细胞、单核细胞、T淋巴细胞、肥大细胞、肝细胞等分泌生成,并受炎性介质的调节,如γ干扰素和脂多糖抑制其分泌,血小板活化因子(platelet-activating factor,PAF)促进其分泌。Lp-PLA2的主要作用包括:产生二十烷酸类炎性介质、参与磷脂重建及生物膜的稳定平衡、脂蛋白的代谢、细胞信号传递、宿主反应、促进机体坏死组织自体消失等[3]。
目前实验研究及流行病学研究结果揭示了Lp-PLA2能生成的多种促炎产物,并参与从动脉粥样斑块形成到斑块不稳定的各个阶段,具有促进炎症反应作用,成为新的心脑事件独立预测因子。所以,建立灵敏便捷的Lp-PLA2检测方法对冠心病的早期诊断预后有重要意义[4]。目前国内各大医院多使用进口试剂盒如美国Diadexus公司的Lp-PLA2产品进行Lp-PLA2检测,操作繁琐、测定时间长,本文拟采用时间分辨免疫荧光层析技术建立快速检测Lp-PLA2试剂盒。
1 材料与方法
1.1标本来源230例临床血清由南华大学附属第一医院检验科提供。
1.2材料与试剂Lp-PLA2单克隆抗体1#和2#,Lp-PLA2蛋白均购于上海领潮生物科技有限公司;羊抗鼠IgG、吸水垫、硝酸纤维素膜(NC膜)、PVC板、聚酯纤维素膜等购于上海杰一生物有限公司;荧光微球购自德国默克公司;比对试剂购自美国Diadexus公司(酶联免疫法)。
1.3仪器与设备HM3030三维平面点膜喷金仪购于上海金标生物科技有限公司;C6M切条机购于上海韩感电子科技有限公司;免疫荧光检测仪购于广州蓝勃生物科技有限公司。
1.4 Lp-PLA2免疫荧光层析试剂的制备试纸条由卡壳、PVC底板、吸收垫、硝酸纤维素膜(CN95)、结合垫、样品垫构成。用划膜仪将羊抗鼠IgG(0.5 g/L)和Lp-PLA2的单克隆抗体2#(1g/L)分别包被在硝酸纤维素膜上,作为质控线和检测线,于35 ℃恒温箱中干燥8 h,即为反应膜;将Lp-PLA2单克隆抗体1#按碳化二亚胺法偶联到纳米荧光微球上,抗体与微球的比例为1∶3,用点膜喷金仪喷于聚酯纤维素膜上,于35 ℃恒温箱中干燥8 h,即为结合垫;将聚酯纤维素膜浸泡在含有20 g/L海藻糖、5 g/L BSA的0.2 mol/L硼酸—硼砂缓冲液(pH=8.0)中,待液体扩散均匀后,取出放置于架子上室温晾干,即为样品垫。组装与检测原理如图1所示。
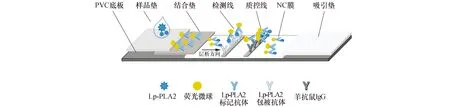
图1 Lp-PLA2免疫荧光层析试剂原理
1.5试剂性能分析
1.5.1 标准曲线的建立 用0.01 mol/L PBS (pH7.4)配制0、20、100、200、500、1 000 μg/L的Lp-PLA2蛋白溶液,取样75 μL滴至测试卡孔中,10 min后放置于荧光检测仪测试,每个浓度点重复测试3次。采用双对数拟合模型,以Lp-PLA2蛋白浓度对数值为横坐标,相应浓度的检测线与质控线荧光信号比值(T/C)的对数值为纵坐标,绘制剂量—反应曲线。
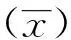
1.5.3 精密度 取三个批次的Lp-PLA2试剂,分别检测40、200、600 μg/L的Lp-PLA2蛋白,每批次重复检测10次,计算测试浓度的变异系数(coefficient variation,CV),并将三批次的检测结果分析,计算批次间的变异系数。
1.5.4 准确度 用20、100、200、500、1 000 μg/L的Lp-PLA2蛋白重复测定3次,按拟合的方程计算出相应的浓度,计算与标示浓度的相对偏差。
1.5.5 干扰实验 为考察血液中常见干扰物对试剂的影响,在不同浓度的血红蛋白、甘油三酯、胆红素中分别加入Lp-PLA2蛋白,使Lp-PLA2终浓度为40 μg/L、200 μg/L、600 μg/L,重复测试3次,并计算其相对偏差的平均值,观察检测结果相对偏差的变异系数是否在10%以内,而判定干扰物对样本测试是否有干扰。
1.5.6 临床应用对比 本方法与美国Diadexus公司Lp-PLA2试剂同步测试230例临床样本,绘制四格表,以Diadexus试剂测试结果为参照,分析本方法的符合率,并进行卡方试验及相关性评价。
2 结 果
2.1建立Lp-PLA2标准曲线配制20、100、200、500、1 000μg/L的Lp-PLA2蛋白进行检测,每个浓度重复3次测试,将荧光检测仪检测的信号值T/C与测试样品的浓度进行双对数拟合,T/C值对数值为纵坐标,样品浓度对数值为横坐标,双对数拟合方程为Y= 0.9908X- 1.4772,R2= 0.9993。结果表明二者线性关系良好,标准曲线可以很好的反映荧光信号值与样品浓度的关系,即荧光信号值越高,样品浓度越高。本试剂最低检测限为10 μg/L,方法学的线性范围为20~1 000 μg/L。见图2。

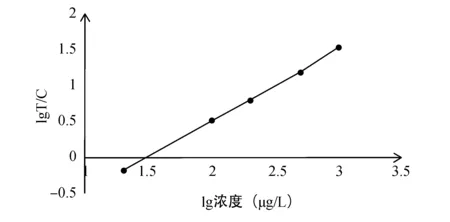
图2 Lp-PLA2双对数拟合标准曲线注:T/C为检测线与质控线荧光信号比值
2.3精密度从表1可知,用40、200、600 μg/L的Lp-PLA2蛋白,每批次重复检测10次,本试剂的批次内CV<10%,批次间CV<10%,结果表明试剂精密度较好。

表1 批次内与批次间精密度分析
注:40、200、600 μg/L的Lp-PLA2蛋白,每批次重复检测10次,求均值
2.4准确度用20、100、200、500、1 000 μg/L的Lp-PLA2蛋白,每批次重复测定3次,从表2可知,本试剂在检测20~1 000 μg/L范围内的Lp-PLA2的相对偏差均小于±15%,结果表明试剂的准确度较好。
2.5干扰实验从图3、图4、图5可知当血红蛋白浓度低于5 g/L,甘油三酯浓度低于10 g/L时,胆红素浓度低于0.2 g/L,对低(40 μg/L)、中(200 μg/L)、高(600 μg/L)浓度的Lp-PLA2蛋白重复测试3次,检测结果CV在10%以内,具有良好的精密度,此时干扰物对样本测试无干扰。
2.6本试剂与比对试剂的临床符合率用SPSS统计软件对考核数据进行统计学分析,从本试剂与比对试剂的对比结果(表3)可知两者总符合率为90.87%,阳性符合率为79.34%,阴性符合率为98.55%,调整一致性90.74%。本试剂与比对试剂阴阳性一致性检验结果Kappa值为0.804(表4),两者一致性较好。
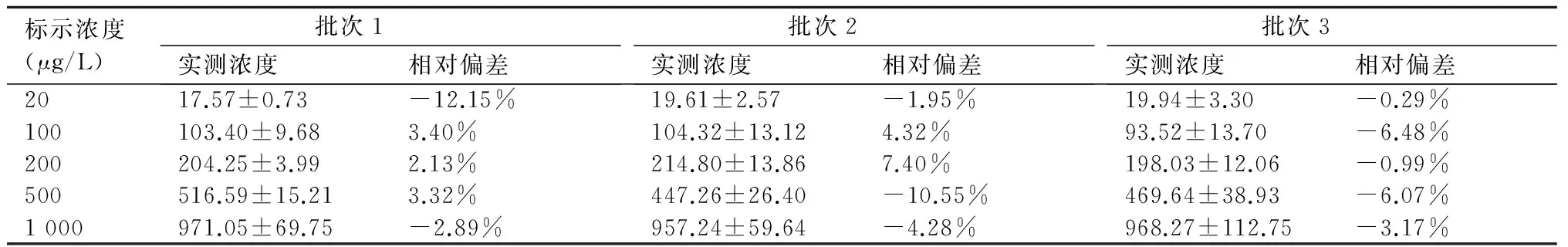
表2 批次内与批次间准确度分析
注:每批次试剂测试20、100、200、500、1 000 μg/L的Lp-PLA2蛋白,每个浓度测试3次,求均值
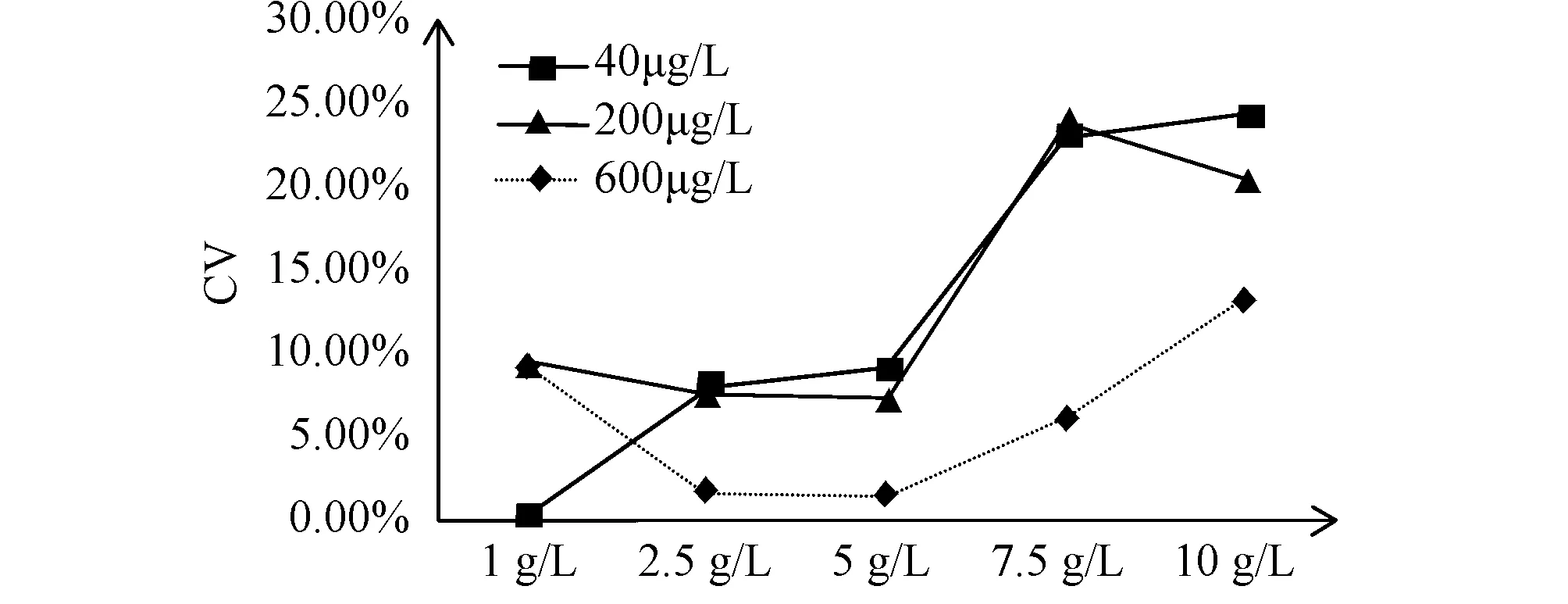
图3 血红蛋白干扰实验
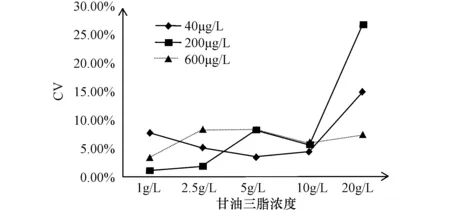
图4 甘油三脂干扰实验
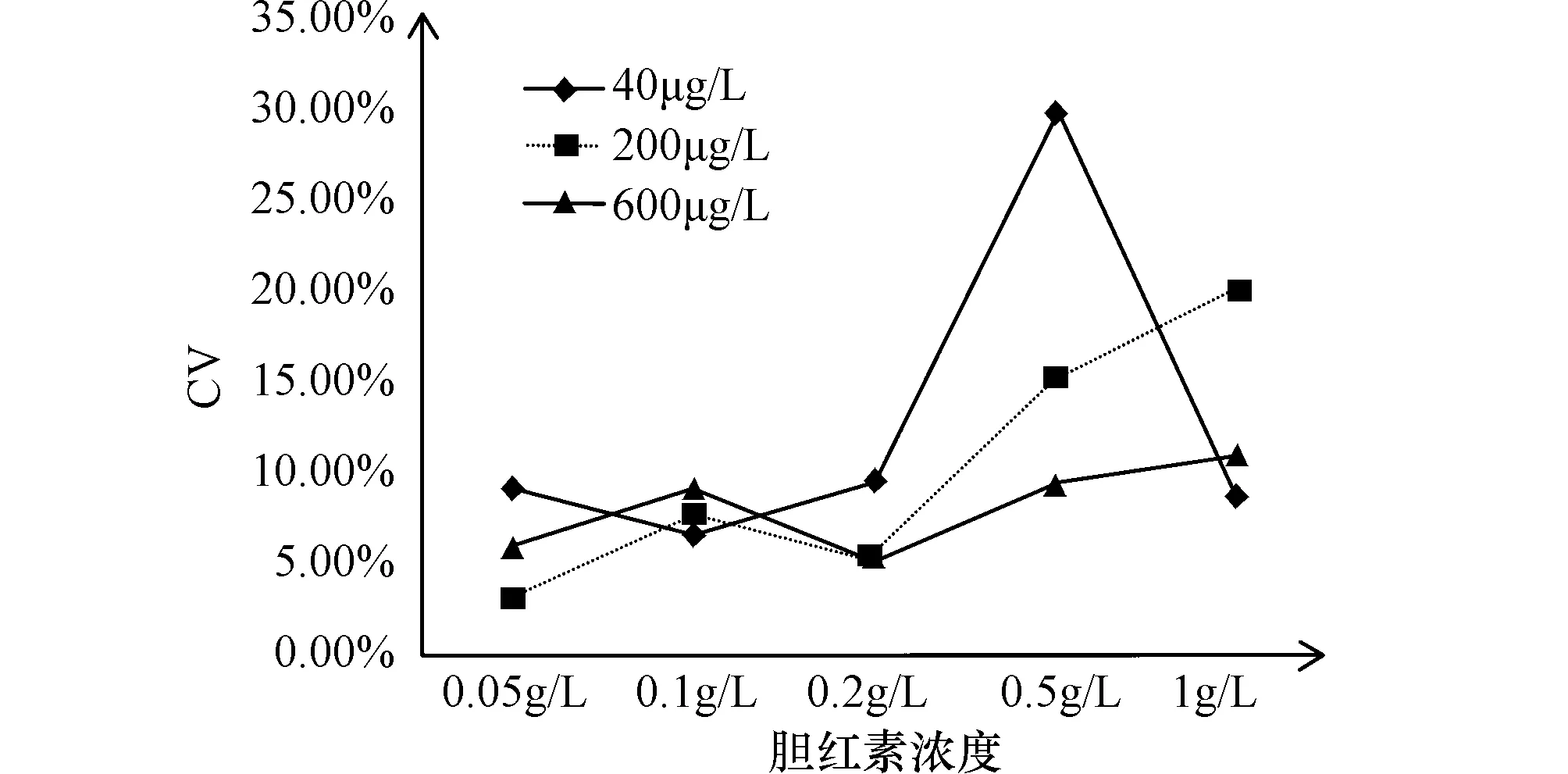
图5 胆红素干扰实验
2.7本试剂与比对试剂检测结果相关性分析将两种试剂检测结果进行相关性分析,结果显示研制的Lp-PLA2免疫荧光定量测定试剂与美国Diadexus公司的Lp-PLA2定量试剂盒(酶联免疫法)测值之间有良好的线性回归关系,回归方程为Y= 1.205X-15.550(n=230),相关系数r=0.968;P值小于0.01,相关性具有统计学意义(表5,图6),两者结果一致性较好。

表3 本试剂与美国Diadexus试剂比对结果分析(例)

表4 临床样本比对测试Kappa值(n=230)
a:不假定零假设;b:使用渐进标准误差假定零假设

表5 临床样本检测值相关系数(n=230)
**,在0.01 水平(双侧)上显著相关
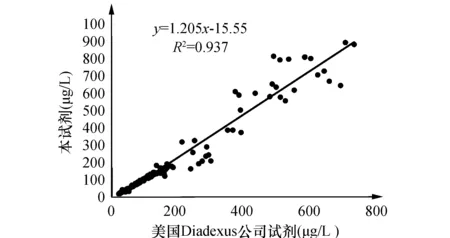
图6 本试剂与PLAC试剂相关性分析
3 讨 论
动脉粥样硬化是一种严重危害人类健康的常见病,是冠心病、脑血管病和血栓栓塞性疾病等缺血性心脑血管病的主要病理基础。斑块形成,斑块由稳定变成不稳定,不稳定斑块容易破裂,引起凝血反应,致使血小板凝聚,血栓形成,这是造成冠心病的主要原因[5-6]。Lp-PLA2水平与心脑血管疾病呈显著正相关,是血管炎症的独立预测因子,因此对心脑血管栓塞性疾病的预测、治疗和预后的判断具有重要意义[7-9]。
本试剂采用时间分辨免疫荧光层析技术(time-resolved fluorescent immune-chromatographic assay,TRFICA) ,以三价镧系元素及其螯合物标记抗体分子,层析待反应体系发生后,用时间分辨法检测信号。Eu3+螯合物的发光特点:stokes位移大,激发光谱与发射光谱不重叠,可减少由激发光引起的特异杂散光对检测的干扰,提高检测的灵敏度与准确度;荧光寿命长,检测中在每个激发光脉冲过后采用延缓测量时间的方式,待短寿命背景荧光物质消失后,再检测长寿命Eu3+鳌合物发射的特异性荧光,可以避免本底荧光对待测物的干扰,提高检测精密度;时间分辨荧光激发波长较宽,发射光谱范围较窄,极大地降低了本底荧光,实现了高信噪比[10-14]。
与比对试剂相比,本方法具有以下优势:(1)最低检出限和精密度与进口试剂相当;(2)操作过程简单,测定时间短,10 min即可得实验结果,不需要昂贵的仪器设备,测试结果基本不受环境因素干扰,适合临床应用;(3)既可以用于大规模临床样本测试,又可单人份检测,减少患者等待时间。
本方法试剂灵敏度为10 μg/L,线性范围为20 μg/L~1 000 μg/L,精密度良好(批次内与批次间CV均小于10%),测试浓度与Lp-PLA2校准品相对偏差小于±15%,当血红蛋白浓度低于5 g/L、甘油三酯浓度低于10 g/L时、胆红素浓度低于0.2 g/L,检测结果CV在10%以内,精密度较好,此时干扰物对样本测试无干扰;与酶联免疫法相比,两种方法相关性良好(r=0.968)。
综上所述,本法建立的Lp-PLA2免疫荧光层析试剂性能达到了相关检测标准,具有灵敏度高、特异性好、定量检测准确、操作简单、快速诊断、配套仪器小巧智能、成本较低等优点,既能满足大型医院门诊科室随来随检的诊疗需求,又适合在社区农村基层医院中进行推广使用。
[1] Maiolino G,Bisogni V,Rossitto G,et al.Lipoprotein-associated phospholipase A2 prognostic role in atherosclerotic complications[J].World Cardiol,2015,7(10):609-620.
[2] Reddy KJ,Singh M,Bangit JR,et al.The role of lipoprotein-associated phospholipase A2 on cardiovascular disease risk assessment and plaque rupture:a clinical review[J].J Clin Lipidol,2009,3(2):85-93.
[3] 胡大一.脂蛋白相关磷脂酶A2临床应用专家建议[J].中华心血管病杂志,2015,43(10):843-847.
[4] 黄美容.LP-PLA2的原核表达、抗体制备及表位分析[D].重庆:重庆医科大学,2011:1-64.
[5] 刘俊田.动脉粥样硬化发病的炎症机制的研究进展[J].西安交通大学学报:医学版,2015,36(2):141-152.
[6] 吴宜娟,王丽娟,张雄.血小板活化因子乙酰水解酶临床治疗研究进展[J].热带医学杂志,2011,11(9):1097-1098.
[7] Dallmeier D,Koenig W.Strategies for vascular disease prevention:the role of lipids and related markers including apolipoproteins,low-density lipoproteins (LDL)-particle size,high sensitivity C-reactive protein (hs-CRP),lipoprotein-associated phospholipase A2 (Lp-PLA2) and lipoprotein(a) (Lp(a))[J].Best Pract Res Clin Endocrinol Metab,2014,28(3):281-294.
[8] 田凤.脂蛋白a、ApoB/ApoA与冠状动脉病变的相关性研究[D].新疆:石河子大学,2014:1-27.
[9] Gerber Y,Dunlay S M,Jaffe A S,et al.Plasma lipoprotein-associated phospholipase A2 levels in heart failure:Association with mortality in the community[J].Atherosclerosis,2009,203(2):593-598.
[10] 朱岚,周衍,黄飚,等.铁蛋白时间分辨荧光免疫层析法的建立及临床应用[J].现代免疫学,2016,36(1):50-53.
[11] 郭明明,周衍,周剑波,等.荧光微球时间分辨免疫层析技术定量检测甲胎蛋白的研究[J].免疫学杂志,2015,31(10):897-901.
[12] 刘鑫.荧光免疫层析分析仪的设计分析[J].生命科学仪器,2015,13(3):23-26.
[13] 李阳,王云龙.免疫层析技术的研究进展[J].中国卫生检验杂志,2015,25(22):3978-3980.
[14] 张兆威,李培武,张奇,等.农产品中黄曲霉毒素的时间分辨荧光免疫层析快速检测技术研究[J].中国农业科学,2014,47(18):3668-3674.
Theestablishmentandclinicalapplicationofimmunofluorescencechromatographyassayforlipoprotein-associatedphospholipaseA2
XIE Haitao,TANG Yongping,XIE Qiaoli,et al
(DepartmentofClinicalLaboratory,theFirstAffiliatedHospital,UniversityofSouthChina,Hengyang421001,Hunan,China)
ObjectiveTo explore the quality of a reagent for quantitative immunofluorescence chromatography assay and evaluate the clinical value for diagnosis of lipoprotein-associated phospholipase A2.MethodsBased on the technology of double-antibody sandwich method,the lipoprotein-associated phospholipase A2 immunofluorescence chromatography strip was established.The performance of kit was evaluated by the range of linearity,sensitivity,accuracy and precision.The kit for Lipoprotein-Associated Phospholipase A2 was compared with Diadexus PLAC Test ELISA Kit made in USA by the parallel experiment in 230 serum specimens.The clinical application were evaluated.ResultsThe minimum limit of detection was 10μg/L.The linear range of lipoprotein-associated phospholipase A2 kit was 20~1 000μg/L.The coefficient of variation values for low,median and high concentration calibrators respectively were all less than 10%.The total coincidence rate of lipoprotein-associated phospholipase A2 kit and PLAC Test ELISA Kit was 90.87%,Kappa was 0.804,r=0.968.The date showed there was no significant difference between the results of two kits.ConclusionsThe immunofluorescence chromatography method targeted at the lipoprotein-associated phospholipase A2 protein was convenient,rapid and sensitive.It is an excellent technique and readily applicable for clinical use.
lipoprotein-associated phospholipase A2; immunofluorescence chromatography; atherosclerosis
10.15972/j.cnki.43-1509/r.2017.05.025
2016-10-17;
2017-02-27
2015年科技型中小企业技术创新资金(合同编号:201501010052).
*通讯作者,E-mail:346853531@qq.com.
R446.11
A
蒋湘莲)
