回顾与展望:我国伦理委员会研究知识图谱分析*
2017-12-22陈勇川
杨 竟,陈勇川
(第三军医大学第一附属医院,重庆 400038,ymyj610@126.com)
回顾与展望:我国伦理委员会研究知识图谱分析*
杨 竟,陈勇川**
(第三军医大学第一附属医院,重庆 400038,ymyj610@126.com)
历经近三十年发展,伦理委员会已成为涉及人的生物医学研究中不可或缺的角色。伦理委员会研究以问题为导向,从理论研究到实践研究,取得了丰硕的成果。综合运用CiteSpaceⅢ和CNKI文献可视化分析作为测量和绘制工具,绘制1991年至今的伦理委员会研究的知识图谱,发现其发文量呈现出波浪上升趋势,近几年数量激增,研究方向集中在伦理审查、临床试验、知情同意、受试者等方面。研究主题从宏观层面向微观层面深入,且与整个伦理实践的发展相契合。既有研究主要集中在法规政策分析、伦理委员会的多学科视角剖析、管理与实践、审查机制、监管与评价五个方面。现有研究缺乏符合我国国情的提炼总结、理论与实践分离、微观层面研究较少。随着我国伦理委员会的发展,微观层面的伦理研究将成为下一步研究的重点。
伦理委员会;知识图谱;伦理审查
1987年伦理委员会这个名词在我国首次提出,1988年协和医科大学张琚提出我国建立伦理委员会的初步设想,1991年我国在北京、天津等地开始伦理委员会建设的尝试[1]。经过近三十年的发展,伦理委员会从理论到实践,从星火到燎原,成为涉及人的生物医学研究中不可或缺的重要角色。伦理委员会的健全和能力体现出一个国家生物医学研究的水平,伦理委员会研究水平对伦理委员会的发展水平也能起到十分重要的作用。因此,有必要梳理国内伦理委员会研究的分布和演化,总结近三十年来伦理委员会研究的热点、重点及趋势。本研究以1991年至今伦理委员会研究的论文为样本,以可视化方式绘制成知识图谱,展示国内伦理委员会研究的发展,审视研究现状,探究发展趋势,为我国伦理委员会的研究与实践提供参考。
1 数据来源与方法
本文文献来自中国知网(CNKI),检索条目为期刊。目前伦理委员会的主要功能为伦理审查,因此本文检索主题词设定为“伦理委员会”或“伦理审查”。因论文主要分布在医药卫生一般理论(含医学哲学与医学伦理学)、药学领域,法律与哲学领域也有少量,本文搜索时将中图分类号限定为R0(医药卫生一般理论)或R9(药学)。我国伦理委员会最初建立是在1991年,因此文献来源年限设定为1991-今。来源类别为全部期刊,检索时间为2017年6月18日。通过检索共获取期刊论文1151篇。
若单纯依靠手动检索和文献阅读,耗时过长,难度过大,因此本文综合运用CiteSpaceⅢ和CNKI计量可视化分析作为测量和绘制工具,获取1991年至今的伦理委员会研究知识图谱。CiteSpaceⅢ软件系统是由美国德雷塞尔大学华人学者陈超美博士开发的一款主要用于计量和分析科学文献数据的信息可视化软件,用来分析科学和技术领域发展的知识图谱,直观地展现科学知识领域的信息全景,识别某一科学领域中的关键文献、热点研究和前沿方向[2]。目前已在图书情报、管理、科技政策、教育学等领域得到广泛应用。同时,CNKI自身所带的计量可视化分析较之CiteSpaceⅢ具有较大便捷性,也方便研究设计的重现和复制,故本文也同时采用了CNKI文献可视化分析作为研究工具。
2 我国伦理委员会研究的基本情况
2.1 文献分布年代
论文的发表量在某种程度上可以反映一段时间内某领域的发展程度。绘制相应的曲线分布对文献分布做历史的、全面的统计,对评价该领域所处的阶段、预测发展趋势和动态具有重要意义[3]。图1为1991年至今伦理委员会知识图谱研究论文数量年代分布。
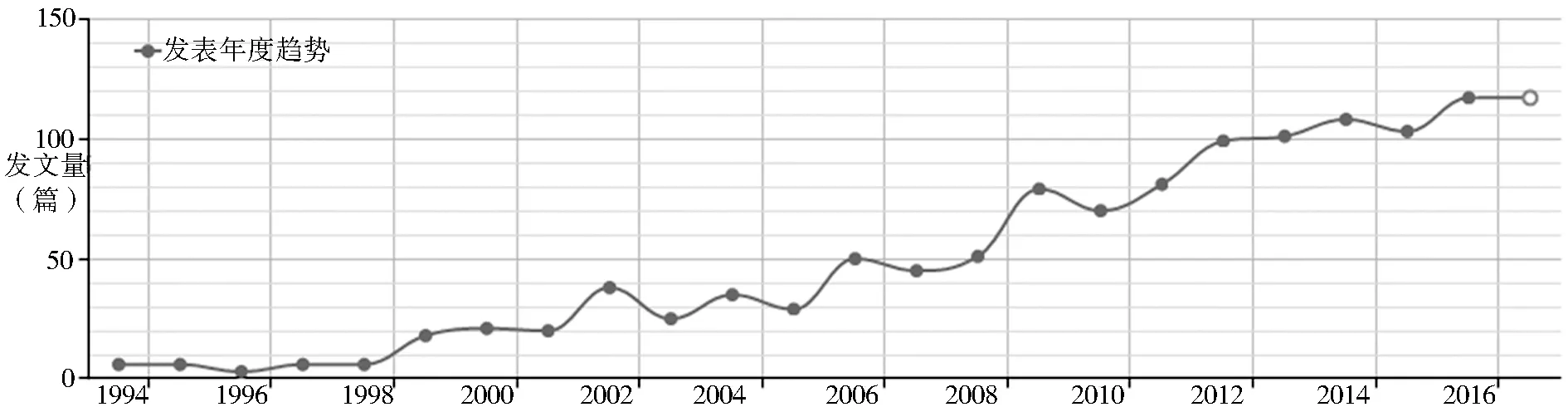
图1 1991年至今知识图谱研究论文数量年代分布图
统计显示,1991-1993年没有关于伦理委员会研究的论文。从1994年才开始出现,这时的论文主要是普及伦理委员会这个概念以及引进国外伦理委员会的做法,可视为伦理委员会研究的开端。接下来的4年,伦理委员会相关论文的数量每年都在5篇左右波动,且都停留在理论研究阶段。到1998年,原卫生部颁布《涉及人的生物医学研究伦理审查办法(试行)》,1999年国家药品监督管理局颁布《药品临床试验管理规范》,对伦理委员会工作做出初步要求,伦理委员会研究也随之打破了纯理论研究的状态,开始涉及医学伦理工作实践,1999年开始出现诸如《医学伦理委员会审查临床试验方案的程序及标准》《新药临床试验的原理与操作——临床试验的伦理学考虑》等审视伦理委员会如何审查临床试验的论文。2003年,国家药品监督管理局修订了《药物临床试验质量管理规范》,并于2003年9月1日正式实施。2005年,中华医学会系列杂志在稿约中率先加入有关医学伦理方面的要求[4],以倒逼机制促使伦理委员会审查的执行。因此自2003年开始,发文量迅速增长。2010年国家食品药品监督管理局颁布《药物临床试验伦理审查工作指导原则》,为伦理委员会工作提供了具体的操作指南,此后论文数量一直呈现稳定增长的趋势,2013年论文破百,2014年达到阶段性小高峰。预计2017年发文量仍然有所上升。
2.2 主要研究力量
院校学者和医疗机构伦理委员会成员是伦理委员会研究的核心力量。表1是1991年至今伦理委员会研究发文量前20位的作者。表2是1991至今伦理委员会研究发文量前20位的研究机构。南京中医药大学附属医院、北京大学、哈尔滨医科大学、山东大学等医学院校及医疗机构的研究成果丰硕,成为研究主体。尤其是南京中医药大学附属医院,以熊宁宁、汪秀琴(后任职于南京医科大学第一附属医院)、刘芳、蒋萌等学者组成的研究团队,为伦理委员会在我国的发展贡献出大量文章,起到强有力的推动作用。
此外,从研究单位的地域分布来看,伦理委员会研究主要集中在中东部地区,依次为江苏、北京、上海、黑龙江、山东。这在很大程度上反映出学术研究仍然呈现出中西部发展不平衡的现象,这与经济、社会、文化的发展程度是密不可分的。
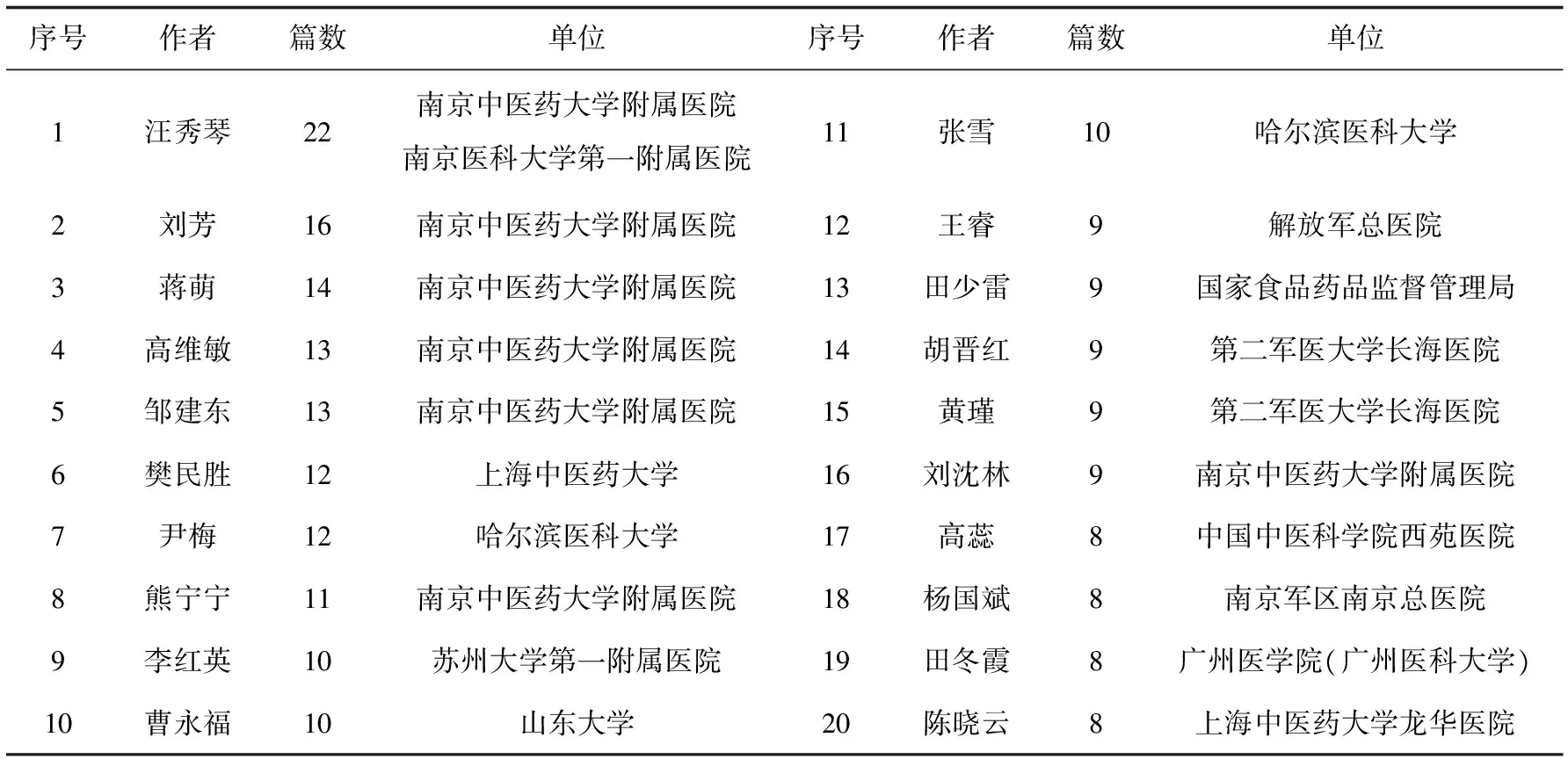
表1 1991至今伦理委员会研究发文量前20位的作者
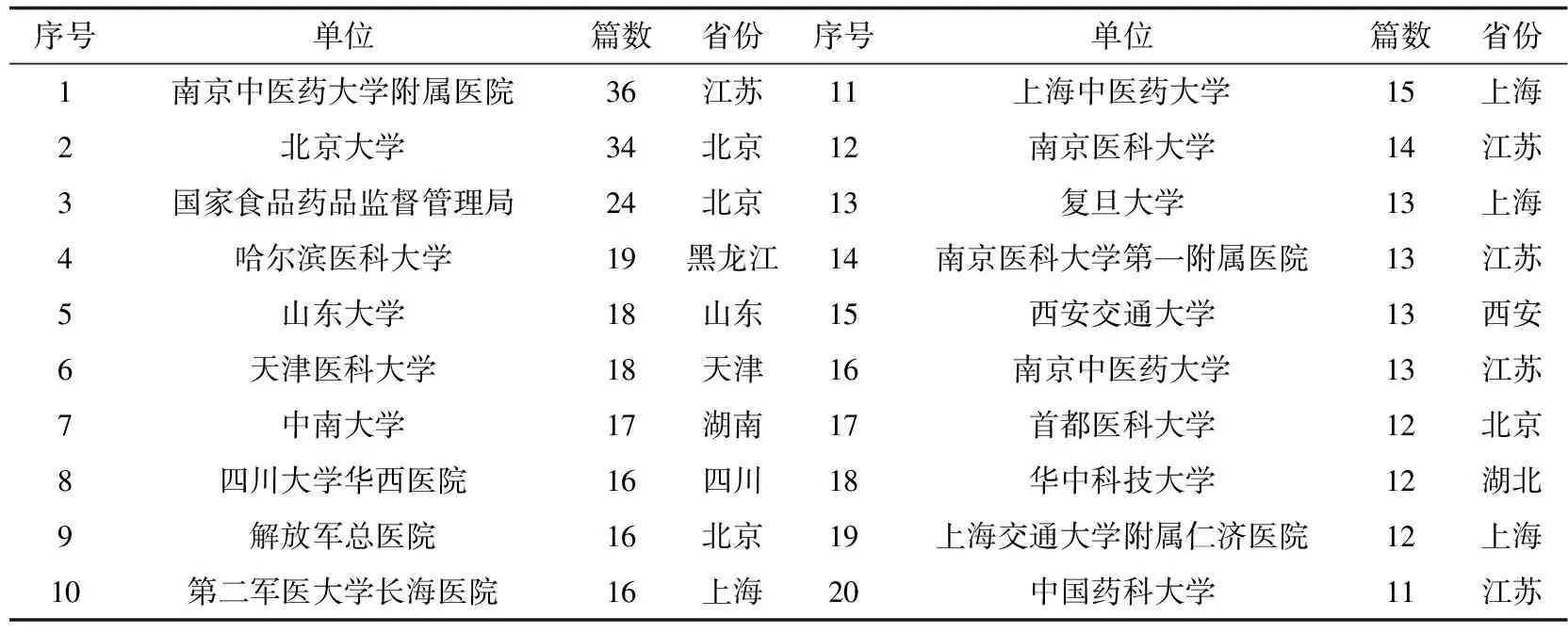
表2 1991至今伦理委员会研究发文量前20位的研究机构
2.3 文献期刊分布
分析论文在期刊中的分布,可以确定伦理委员会研究领域的主要阵地,从而为读者进行论文定位、投稿和提供指引。我国关于伦理委员会研究的论文主要集中在《中国医学伦理学》与《医学与哲学(A)》这两本刊物,其共计发文量超过所有刊物发文量的50%,是医学伦理学研究的主要刊物。其他期刊主要集中在药学领域,如《中国新药杂志》《中国临床药理学杂志》《中国处方药》等,主要原因在于我国伦理委员会是伴随药物临床试验的发展而建立成长的,根据1995年原卫生部《临床药理基地管理指导原则》,最初的伦理委员会也是建立在药理基地的,与药学有着不可分割的历史渊源,见表3。
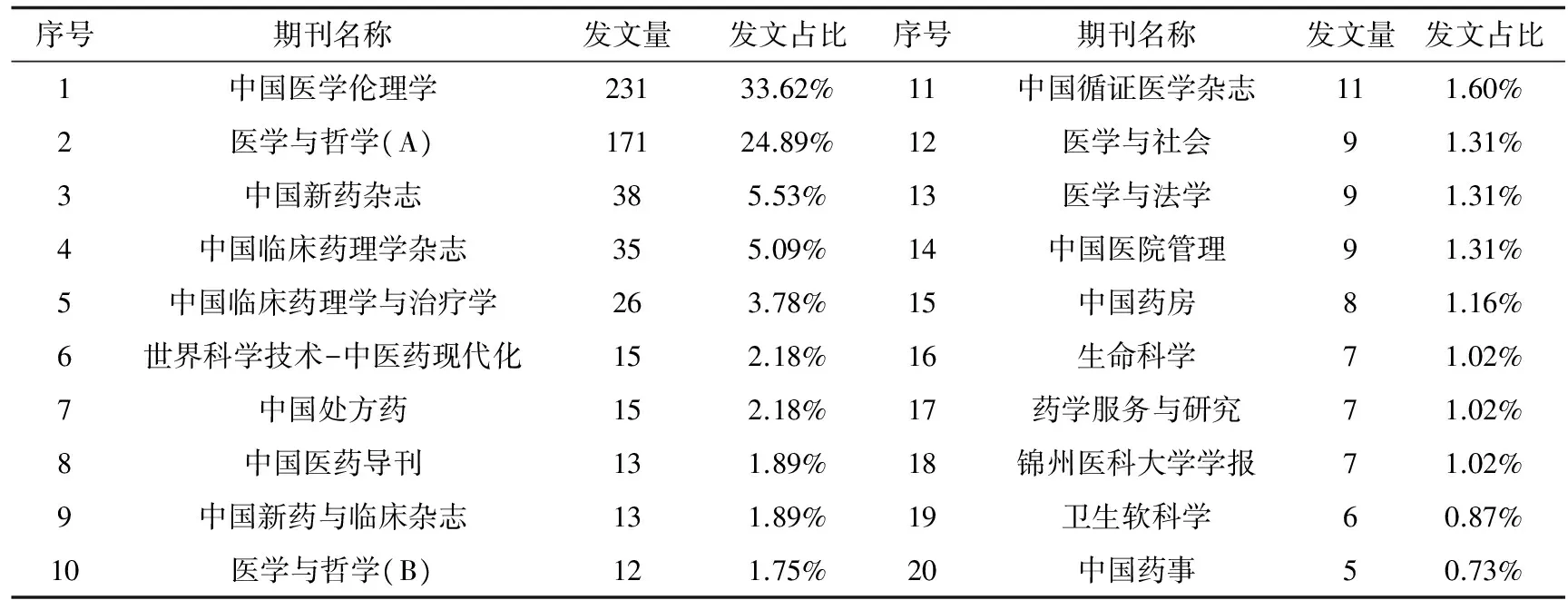
表3 我国伦理委员会研究文献期刊分布
2.4 高被引文献
高被引文献往往反映着该文献作者的学术影响力、选题高度、普遍意义、研究水平,以及刊物的影响力。对被高引文献的分析,可以反映某个时段该领域的研究热点。表4是1991至今伦理委员会研究前20位的被高引文献。可以看到,伦理委员会在我国发展二十余年来,“实战”工作已经取得一些成果。面对实践中出现的问题,有学者通过翻译、引进国外的文献、经验和做法供国内学者和伦理工作人员参考,如下表中3;有学者对伦理委员会运行现状和组织管理进行了梳理和反思,如下表中6、9、20;有学者对伦理委员会一线工作程序提供了路径,如下表中4、8、13。
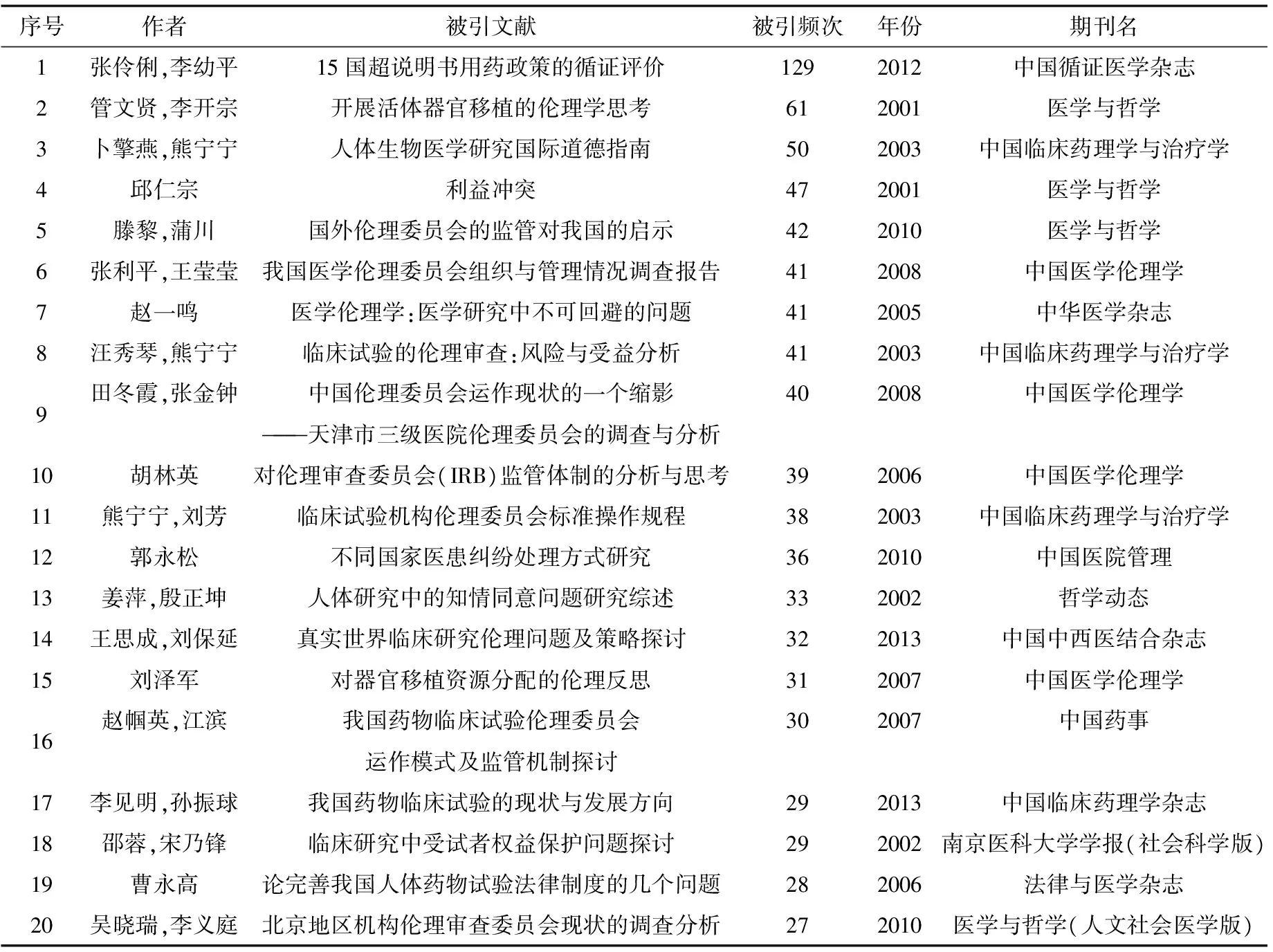
表4 1991至今伦理委员会研究前20位的被高引文献
3 我国伦理委员会研究的热点和特点
表5中为1991至今我国伦理委员会研究前40位的高频关键词,高频关键词可反映出研究的聚焦和热点。排名前10的关键词主要集中在:伦理审查(171)、伦理委员会(150)、临床试验(117)、药物临床试验(64)、知情同意(63)、医学伦理(45)、临床研究(44)、伦理(37)、受试者(37)、伦理学(36)。可见对伦理委员会的研究主要集中在伦理审查、临床试验、知情同意、受试者等具体方面。
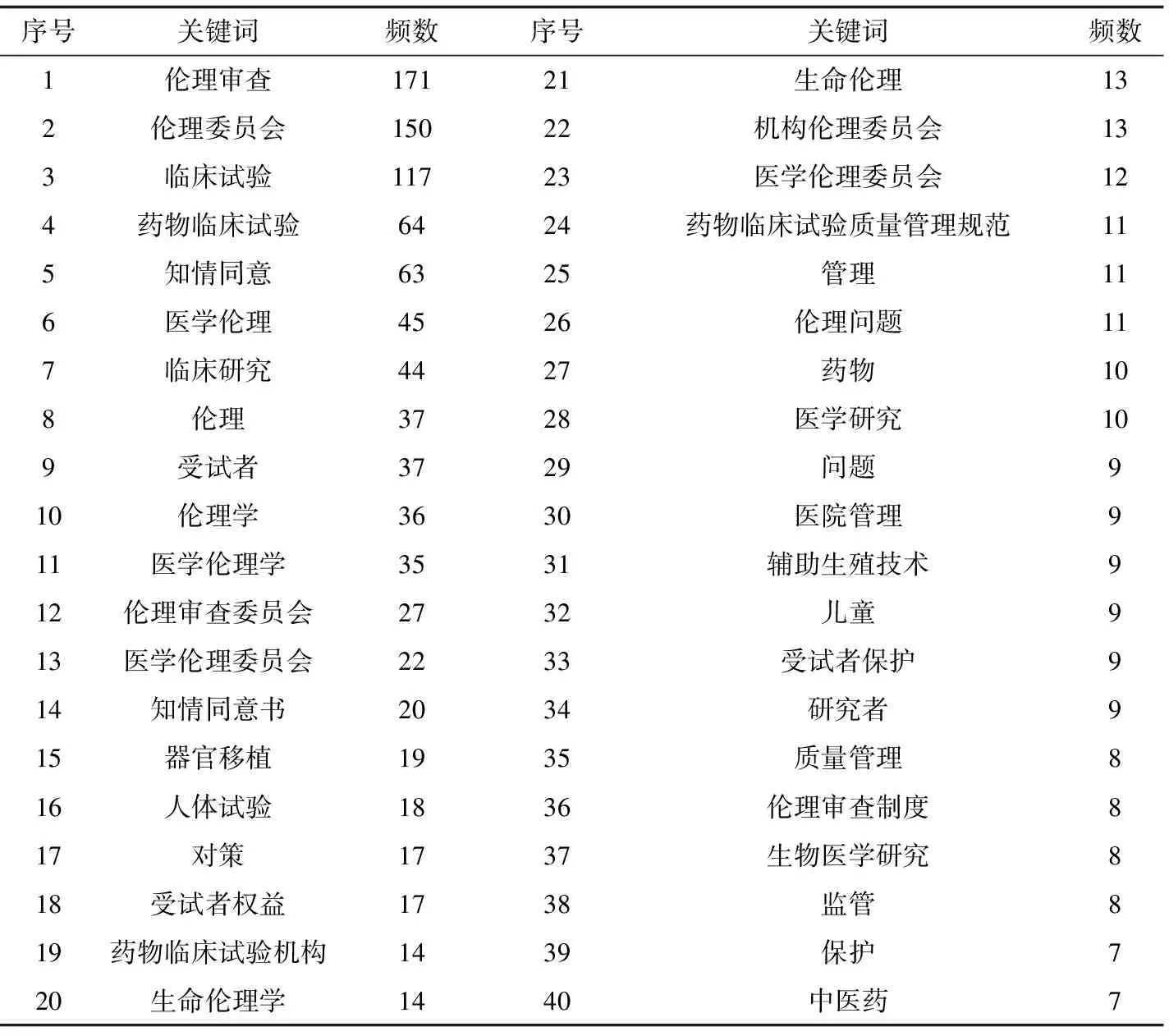
表5 1991至今我国伦理委员会研究前40位的高频关键词
为体现1991至今研究热点的变化,本文利用CitespaceIII软件中突现词探测功能,通过探测主题词词频的时间分布,构建突现词年代分布图,依靠词频的动态变化来探索演变轨迹及前沿趋势[5]。本文突现词的年代分布图见图2,频次设定为5,即图中出现都是频次大于5的突现词。字号越大,代表突现词出现的频次越高。因1991、1992、1993年无相关文章,时区图谱从1994年绘制。
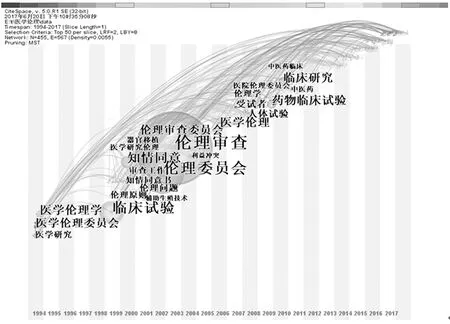
图2 1994至今我国伦理委员会研究的突现词时区图谱
图2可见我国伦理委员会研究随着时间推移而发生的演变和趋势。总结起来,研究内容主要呈现以下几个特点:
第一,研究主题从宏观层面向微观层面深入。1994-1998年,研究的突现词很少,主要集中在“医学伦理学”“医学伦理委员会”等宏观词汇;1998年以后,研究的主要突现词增多,以“伦理委员会”“临床试验”“伦理审查”为主,并伴随“知情同意”“审查工作”“伦理问题”“受试者”等涉及伦理委员会具体工作的相对微观的词汇。但总体上而言,这些突现词都属于宏观词汇,说明我国目前对伦理委员会的研究仍然处于从宏观到微观过渡的阶段,还未真正进入微观层面。
具有工业价值的外生钼矿床主要有:(1)产于煤系地层中的钼矿床;(2)产于碳质粘土岩及碳、硅质粘土岩(即黑色页岩)中的钼矿床;(3)固体沥青页岩中的钼矿床等。这些外生钼矿床中,主要是与碳质有机成分密切相关,而且往往和铀、钒、锗等有用元素共生。但是由于其中含钼较贫而且赋存状态复杂,所以目前还未能有效提取,只能作为将来研究利用的对象。
第二,研究主题与整个伦理实践的发展是相契合的。学术研究服务于学术实践,因此我们在理解伦理学术研究的时候必须结合当前伦理发展的实践。在时区图谱内,1998年、1999年恰好是原卫生部颁布《涉及人的生物医学研究伦理审查办法(试行)》,国家药品监督管理局颁布《药品临床试验管理规范》的时间点,两个文件的颁布是我国临床试验的转折点,反映出医学伦理实践领域的重大变革,使伦理委员会审查工作的执行有法可依、有据可循,因此这个时间段内高频突现词开始涉及“审查工作”“知情同意”“伦理原则”等内容。2003年《药物临床试验质量管理规范》的修订和颁布,使之后一段时间内“伦理审查”“伦理委员会”成为热点,这时我国的伦理审查机制也随之在上海、江苏等发达地区萌芽,在2009年左右发展壮大。不难看出,伦理委员会研究始终是与国家政策指南紧密相关,与国家临床研究发展方向相适应的。
第三,近几年的研究内容无新的热点出现。从图2中可见,从2014年开始就没有出现与伦理委员会和伦理审查相关、出现频次大于5的突现词,这意味着近几年的论文研究内容还是以2014年以前的热点为主。原因可能在于当前我国伦理委员会的发展由深度拓展转变为广度拓展,从“深挖”转变为“普及”,开始呈现“燎原”的局面。
4 伦理委员会研究的聚类图谱
图3是伦理委员会研究的聚类图谱,呈现的是1991至今的研究图景全貌。图谱以伦理委员会和伦理审查为中心,连接着医学伦理、医学伦理学、临床试验、药物临床试验、知情同意等分支,并且分散着审查工作、受试者、伦理原则、伦理问题等节点。由此可见,我国已初步形成以伦理委员会为中心的研究体系,逐渐聚合一些专题研究。基于经典文献研究和聚类图谱分析,本文对研究的知识框架和发展脉络进行梳理,可得出这二十余年以来伦理委员会研究的五个板块:
一是伦理委员会法规政策分析。解琴(2009)对《药物临床试验机构资格认定复核检查工作方案》进行了解读,汪旻晖、卢建平等(2014)将中国与ICH药物临床试验质量管理规范做出了比较研究,江一峰、王頔等(2015)对2013版《赫尔辛基宣言》的修订及其意义进行了分析研究,赵迎盼、陆芳等(2015)对《药物临床试验质量管理规范》(修订稿)进行了解读,张弨、王晓玲、母双等(2015)对《儿科人群药物临床试验技术指导原则(征求意见稿)》进行了解读。
二是伦理委员会的多学科视角剖析。目前其他学科对伦理委员会的剖析一般集中在法律与管理两个方面。滕黎、蒲川(2009)对伦理审查委员会的法律地位进行了初探,沈铭贤、胡庆澧、丘祥兴(2010)从政治学的角度“实质正义与程序正义”解读了伦理委员会SOP,李志强、蔡昱(2011)也从医学伦理法律化的视角对伦理委员会法律问题进行了探析,韩梅、王思成(2013)从法律视角对临床试验受试者权益保护进行了分析并提出建议。
三是伦理委员会的管理与实践。这主要是从伦理委员会的建设、运行现状和伦理工作经验、体会两方面进行分析。在伦理委员会的建设、运行现状方面,黄瑾、刘厚佳、胡晋红(2009)对中国大陆部分多中心临床试验伦理审查模式现状进行了调查,田冬霞(2009)对中美伦理审查委员会管理机制进行了比较与分析,吴晓瑞、李义庭(2010)对北京地区机构伦理审查委员会现状进行了调查分析,蔡昱、张金钟等(2013)对天津市伦理委员会现状进行调查分析,王香平、李晓玲、王育琴(2012)对我国医院伦理委员会现状及国际认证进行了分析,伦理工作经验、体会方面,李晓、吕晓东、于萍(2013)介绍了伦理审查中知情同意书主审表使用,李红英、徐溢涛、郜翀(2013)对伦理委员会档案建设及其监管进行了研究,盛艾娟、王美霞等(2015)阐述了伦理委员会秘书的职责。
四是伦理委员会的审查机制。包括国内外伦理审查现状、实践、体会及启示。汪秀琴、熊宁宁(2010)就临床研究中的不良事件如何伦理审查作出了分析,张雪、尹梅等(2013)对伦理审查委员会跟踪审查的困境进行了讨论,并提出建议,张金钟(2013)对生物医药研究伦理审查的体制机制建设进行了研究,汪秀琴、罗晓琼(2013)探讨了多中心临床试验应如何进行中心伦理审查,张海洪、丛亚丽、沈如群(2014)探讨了伦理委员会持续审查制度建设,陈勇川、杨竟(2016)为临床科研课题申报和实施中的伦理审查难题提出了解决之道。
五是伦理委员会的监管与评价。滕黎、蒲川(2010)讨论了国外伦理委员会的监管对我国的启示,董平平、王丽宇(2012)探究了建立医学伦理审查监管体制的程序,马喜桃、陆华等(2014)对SIDCER、AAHRPP认证和CAP认证进行了比较研究。

图3 1991至今伦理委员会研究的聚类图谱
5 伦理委员会研究的薄弱环节与前瞻趋势
通过梳理和分析1991至今国内伦理委员会研究的文献,我们可以比较清晰地把握二十年来该领域研究的基本脉络和热点。但这些研究还存在一些薄弱环节,需要我们在未来的研究中不断加强和改进。
第一,研究中国理论和中国经验欠缺。尽管我国各地如江苏、上海率先开展了伦理委员会实践的探索,也从区域层面采用“实用主义”范式对该地区的经验和启示进行了描述和介绍,但借鉴国外伦理管理、审查先进经验的痕迹仍然较重,缺乏我国本土的、符合我国国情的提炼总结。
第二,存在理论研究与实践研究分离的状况[6]。通过笔者实际工作接触与对文献的梳理,发现有些伦理委员会对伦理实践中的棘手问题想当然地解决,并未很好地利用伦理学理论和方法进行头脑武装。几千年来,我国积累了丰富的、具有中国特色的伦理学知识,但其重要理念和精华并未很好地嵌入到伦理委员会的审查工作中。
第三,研究内容上,关于微观层面的研究太少。究其原因,可能源于我国伦理委员会发展的历史不长,还未能引起广泛的重视和关注,使得研究仅限于伦理委员会的执行层面,并未深入下去。这需要研究人员进行更加深入细致的探讨。
随着我国伦理委员会的发展,微观层面的伦理研究预计将成为研究的重点,适应伦理委员会改革的新趋势,促进伦理委员会的管理水平和审查能力的提升,未来的伦理委员会研究有待理论和实践的双重创新。主要体现在以下几个方面:
第一,推进伦理委员会的中国化、本土化研究。我国伦理委员会发展二十余年,但尚未形成中国语境的管理、审查和研究体系。未来的研究应立足我国自身的思想观念、医疗环境和社会现实,从国家层面进行规律的提炼和总结。在引进国外理论知识的同时,也要实现与本土知识的融合。目前伦理委员会工作已引起国家卫生计生部门与国家食品监督管理局的重视,并着手调研工作,期望在改革过程中进一步加强本土关怀,紧密结合国情,而非生搬硬套国外经验。
第二,侧重理论与实践的有机结合。期望今后的培训培养不仅局限在执行层面,更应将二者结合,“知其然,也要知其所以然”,用伦理学理论和视角去分析研究方案问题和受试者问题。长此以往,便可打造一支同时具备医学背景与丰富伦理学知识的研究队伍,加快促进我国医学伦理的发展。
[1] 关鑫,樊民胜.我国医学伦理委员会建设和发展的若干思考[J].医学与哲学(人文社会医学版),2007,12(28):1-5.
[2] 侯建华,胡志刚.CiteSpace软件应用研究的回顾与展望[J].现代情报,2013,33(04):99-103.
[3] 邱平军,杨思洛,宋艳辉.知识交流研究现状可视化分析[J].中国图书馆学报,2012(2):78-79.
[4] 翟临明,刘冰.重视医学研究中的伦理学问题[J].中华病理学杂志,2005,34(1):27.
[5] 王亚茹,韩瑞波.我国行政体制改革趋势:一个分析框架[J].重庆社会科学,2017(3):5-17.
[6] 邱仁宗.伦理学研究要多接地气[N].健康报,2016-10-28(005).
RetrospectandProspect:AnalysisofKnowledgeMappingDomainofEthicsCommitteeStudyinChina
YANGJing,CHENYongchuan
(theFirstAffiliatedHospitalofThirdMilitaryMedicalUniversity,Chongqing400038,China,E-mail:ymyj610@126.com)
Through the development of close to 30 years, ethics committee has become an indispensable part of biomedical research involving human beings. The research into ethics committee is problem-orientated and has made rich research results from theoretical research to practical research. By using software CiteSpaceⅢ and analytic visualization of CNKI literature as measuring and drawing tool, this paper made the mapping knowledge domain of ethics committee study since 1991 and found that the published articles amount showed a wave upward trend, the quantity increased sharply in recent years and the research focused on ethical review, clinical trial, informed consent, human subjects, etc. The research topics developed from macro level to micro level and fitted with the development of whole ethical practice. The existing research mainly focused on five aspects of the analysis of laws and regulation, multidisciplinary perspective analysis of ethics committees, the management and practice, the review mechanism and supervision and evaluation. The existing research lacked many summaries accordance with China’s national condition; the theory was separate from practice; the research on the micro-level was less. With the development of ethics committee in China, the ethics research on micro-level will become the focus of next step.
Ethics Committee; Mapping Knowledge Domain; Ethical Review
2015年第三军医大学人文社会科学基金,项目编号:2015XRW21
**通信作者,E-mail: zwmcyc@163.com
R-052
A
1001-8565(2017)12-1522-08
10.12026/j.issn.1001-8565.2017.12.16
2017-09-13〕
〔修回日期2017-11-09〕
〔编 辑 吉鹏程〕
