中介素与肾上腺髓质素对局灶性脑缺血大鼠脑 微循环的影响
2017-12-21路月英贾娜娜刘振刚田景瑞
郭 鑫,王 静,王 萌,路月英,贾娜娜,刘振刚,田景瑞,苑 杰
(1.华北理工大学附属医院神经内科,河北 唐山 063000; 2.唐山职业技术学院,河北 唐山 063000; 3.华北理工大学心理学院,河北 唐山 063000; 4.华北理工大学附属医院神经外科,河北 唐山 063000; 5.华北理工大学基础医学院,河北省慢性疾病重点实验室,唐山市慢性病临床基础研究重点实验室, 河北 唐山 063000; 6.华北理工大学精神卫生研究所,河北 唐山 063000)
中介素与肾上腺髓质素对局灶性脑缺血大鼠脑 微循环的影响
郭 鑫1,王 静2,王 萌1,路月英3,贾娜娜3,刘振刚4,田景瑞5,苑 杰6*
(1.华北理工大学附属医院神经内科,河北 唐山 063000; 2.唐山职业技术学院,河北 唐山 063000; 3.华北理工大学心理学院,河北 唐山 063000; 4.华北理工大学附属医院神经外科,河北 唐山 063000; 5.华北理工大学基础医学院,河北省慢性疾病重点实验室,唐山市慢性病临床基础研究重点实验室, 河北 唐山 063000; 6.华北理工大学精神卫生研究所,河北 唐山 063000)
研究报告
目的探讨中介素(intermedin, IMD)与肾上腺髓质素(adrenomedullin, ADM)对局灶性脑缺血大鼠脑微循环的影响。方法采用大脑中动脉闭塞法构建脑缺血(cerebral ischemia, CI)大鼠模型,将40只SPF级雄性SD大鼠随机分为3组:脑缺血模型+生理盐水[CI+NS(normal saline,NS)]组、CI模型+ADM处理(CI+ADM)组与CI模型+IMD处理(CI+IMD)组,采用激光多普勒测定仪监测脑表面微循环灌注量的变化。结果CI+NS组、CI+ADM组与CI+IMD组大鼠脑表面微循环灌注量的比较,差异有显著性(P< 0.05),事后多重比较发现,CI+IMD组大鼠脑表面微循环灌注量均高于CI+NS组与CI+ADM组。结论IMD可以改善局灶性脑缺血大鼠脑微循环,且疗效优于ADM。
中介素;肾上腺髓质素;脑缺血;微循环;大鼠
缺血性脑卒中是造成全球死亡和残疾的主要原因之一,给患者及社会带来了沉重的负担[1]。尽管缺血性脑卒中发病原因多种多样,但脑血流减少所致的脑微循环障碍是造成疾病发
生发展的中心环节。脑微循环受到诸多神经体液因素的调节,对维持中枢神经系统内环境的稳态有重要作用。有研究表明,缺血性脑卒中发生后,不仅微循环先于脑组织发生损害,而且梗死灶及其周围脑组织,甚至对侧大脑半球同样会出现不同程度的微循环障碍[2]。因此,尽早改善微循环是减轻缺血脑组织损伤的重要手段。只有尽早恢复血液供应,改善微循环,阻断脑缺血病理过程,增加脑组织供血供氧,维持代谢水平,从而促进脑缺血患者神经功能的恢复[3,4]。目前,大量基础研究和临床实践均证实,很多治疗措施,除可改善缺血区局部的微循环外,还可通过改善全脑微循环代谢而缓解其神经功能缺损症状[5, 6]。
中介素(intermedin, IMD)[7]属于降钙素基因相关肽超家族的成员,其与同家族的肾上腺髓质素(adrenomedullin, ADM)[8]的氨基酸序列和功能存在一定相似性,故IMD又称为ADM-2。IMD和ADM的分布广泛,具有多种生物学效应,与多个系统疾病的发生发展密切相关[9]。有研究显示,IMD和ADM可通过舒张脑血管,改善脑缺血的局部血流供应,对脑微循环和血脑屏障具有调节功能,但尚未形成统一定论[10,11]。因此,本研究采用大脑中动脉闭塞法构建脑缺血(cerebral ischemia, CI)大鼠模型,并分别进行IMD和ADM药物干预,观察并分析大鼠脑缺血侧脑表面微循环灌注量的变化,从而为临床治疗脑缺血疾病提供新的实验依据。
1 材料和方法
1.1 实验动物
SPF级雄性SD大鼠40只,10~12周龄,体重(280±20)g,购于北京维通利华实验动物技术有限公司[SCXK-(军)2014-0001],于华北理工大学动物实验中心屏障实验室[SYXK(冀)2010-0038]中饲养,饲养环境:清洁级,温度维持在22~25℃,相对湿度40%~70%,自由进食进水,术前禁食12 h、不禁水。并按实验动物使用的3R原则给予人道的关怀。
1.2 主要试剂与仪器
ADM(美国Solarbio试剂公司);IMD(美国Solarbio试剂公司);线栓、10%水合氯醛、碘伏、纤芯、棉签、无菌纱布、1/2弧度头皮缝合针、3-0缝合线等。
激光多普勒血流监测仪(瑞典Perimed公司);大鼠脑立体定向仪(上海奥尔科特生物科技有限公司);显微外科手术器械(上海医疗器械公司);颅骨钻、微量进样泵、微量进样器(100 μL)、手术固定台等。
1.3 实验方法
1.3.1 实验动物分组及处理
将40只SD大鼠随机分为3组,分别为脑缺血模型+生理盐水[CI+NS(normal saline, NS)]组、CI模型+ADM处理(CI+ADM)组与CI模型+IMD处理(CI+IMD)组。3组大鼠均采用MCAO法制作脑缺血大鼠模型,在大鼠缺血2 h时,3组大鼠分别给予侧脑室注射50 μL生理盐水、1.0 nmol/kg IMD[13]+ 50 μL生理盐水和1.0 nmol/kg ADM[14]+ 50 μL生理盐水,同时采用激光多普勒测定仪监测脑表面微循环灌注量。
1.3.2 构建脑缺血大鼠模型

图1 激光多普勒测定仪设置与固定Fig.1 Setup and fixation of the laser Doppler tester
参照Longa[12]法,采用大脑中动脉闭塞法制作CI大鼠模型。经腹腔注射10%水合氯醛(0.3~0.4 mL/100 g)后大鼠翻正反射消失,显示大鼠麻醉成功。将大鼠固定在实验台上,呈仰卧位,颈部备皮消毒后,沿颈部正中线偏右侧做纵行切口,钝性分离皮下组织,分离出颈总动脉(common carotid artery, CCA)、颈外动脉(external carotid artery, ECA)和颈内动脉(internal carotid artery, ICA),在ECA处置两根手术线,距分叉5 mm处结扎第1根手术线,在线结远心端3 mm处结扎第2根手术线,于两线结间离断血管。此时,用动脉夹夹闭CCA近心端和ICA远心端。然后轻轻提起ECA,用神经外科显微剪垂直于ECA近分叉处剪口,导入浸润生理盐水的线栓,牵拉ECA残端线结,使ECA与ICA近似成一直线(线栓与颈部正中线、水平面均呈30°~45°),缓缓推进线栓至ICA关闭处,松开ICA动脉夹,快速插入线栓16~18 mm遇阻力时,轻轻退出线栓1~2 mm,调整角度后再次插入,当遇阻力后停止,此时线栓正好插至颅内的大脑前动脉,堵住大脑中动脉的开口。大鼠如出现呼吸、心跳变快,部分大鼠会出现大小便失禁,是造模成功的一个判断方法。记录时间,固定线栓,松开CCA动脉夹,确定无出血后缝合伤口。
1.3.3 激光多普勒测定仪监测
用无菌纱布将大鼠颈部伤口包裹,用大鼠脑立体定向仪将大鼠头部固定,呈俯卧位,将微量进样器固定于大鼠脑立体定向仪上,将手术区(3 cm × 2 cm)反复消毒3次,用手术刀沿纵轴线将大鼠头皮全层切开,暴露出颅骨骨膜,用颅骨钻在颅骨额顶部打孔一圈,去除探测区颅骨及硬脑膜,将激光监测探头安装并固定好,通过与前囱点的中间横向距离、背腹距离及前后距离,监测脑表面微循环灌注量(见图1)。
1.3.4 神经功能评分(neurological severity scoring, NSS)
分别在第3天和7天对3组大鼠进行神经功能评分。使用以下参数作为评分标准,包括运动测试、感官测试、平衡测试、反射缺失和异常运动。正常为2~3分,最严重为18分。
1.4 统计学方法
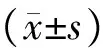
2 结果
2.1 大鼠死亡情况
在实验过程中,死亡大鼠共10 只,其中CI+NS组死亡4只,死亡率为28.6%;CI+ADM组和CI+IMD组分别死亡3只,死亡率为23.1%,并在实验中将死亡大鼠补齐,保证每组大鼠存活10只。3组大鼠死亡率比较,差异无显著性(χ2=0.145,P> 0.05)。
2.2 大鼠脑表面微循环灌注量的检测结果
激光多普勒监测结果显示:CI+NS组大鼠脑表面微循环灌注量平均值为1.91 PU/S左右(见表1、图2),分别注射ADM与IMD后发现,ADM使大鼠脑表面微循环灌注量平均值增加至14.76 PU左右(见表1、图3),IMD使大鼠脑表面微循环灌注量平均值增加至81.87 PU左右(见表1、图4)。
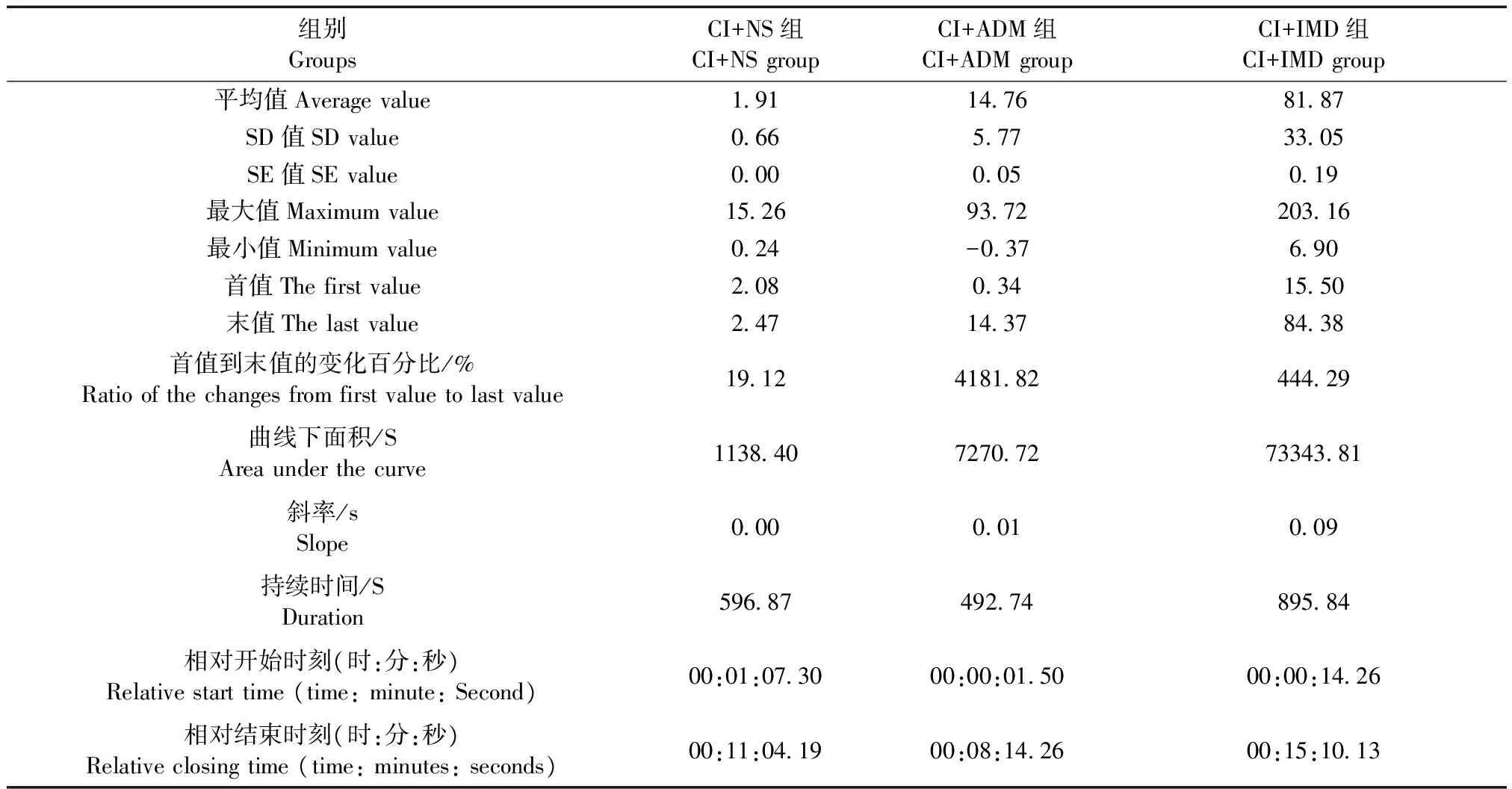
表1 大鼠脑表面微循环灌注Tab.1 Cerebral surface microcirculation perfusion in the rats

注:Ta:脑缺血大鼠急性期稳定期。图2 CI+NS组大鼠脑表面微循环灌注量的监测结果Note.Ta: Stable phase of the acute phase of cerebral ischemia in a rat.Fig.2 Cerebral surface microcirculation perfusion in a rat of the CI+NS group
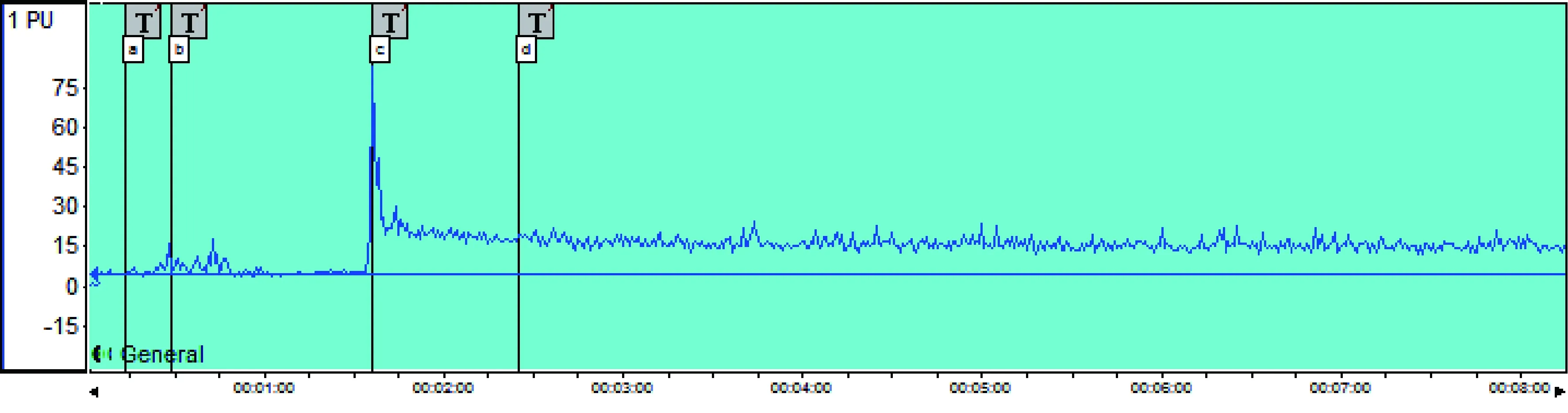
注:Ta:开始注射;Tb:注射结束;Tc:快速反应期;Td:稳定期。图3 CI+ADM组脑表面微循环灌注量的监测结果Note.Ta: Start of injection. Tb: End of injection;Tc: Quick response period;Td: Stable period.Fig.3 Cerebral surface microcirculation perfusion in a rat of the CI+ADM group

注:Ta:开始注射;Tb:注射结束。图4 CI+IMD组脑表面微循环灌注量的监测结果Note.Ta: Start of injection;Tb: End of injection.Fig.4 Cerebral surface microcirculation perfusion in a rat of the CI+IMD group
2.3 3组大鼠脑表面微循环灌注量的比较
结果显示,CI+NS组、CI+ADM组与CI+IMD组大鼠脑表面微循环灌注量的比较,差异有显著性(P< 0.05),事后多重比较发现,CI+IMD组大鼠脑表面微循环灌注量均高于CI+NS组与CI+ADM组。(见表2、图4)
2.4 3组大鼠NSS评分的比较
结果显示,CI+NS组、CI+ADM组与CI+IMD组大鼠第3天和第7天NSS评分的比较,差异有显著性(P< 0.05),事后多重比较发现,CI+IMD组大鼠脑第3天和第7天NSS评分均低于CI+NS组与CI+ADM组。(见表3)

注:CI+IMD组与CI+NS组相比,* P< 0.05;CI+IMD组与CI+ADM组相比,#P< 0.05。图5 3组大鼠脑表面微循环灌注量的比较Note.CI+IMD group compared with CI+NS group, *P< 0.05;CI+IMD group compared with CI+ADM group,#P< 0.05.Fig.5 Comparison of cerebral surface microcirculation perfusion in the 3 groups表2 3组大鼠脑表面微循环灌注量的比较Tab.2 Comparison of cerebral surface microcirculation perfusion in the 3 groups of rats

①CI+NS组①CI+NS②CI+ADM组②CI+ADM③CI+IMD组③CI+IMDFP事后多重比较Posthoccomparisons脑表面微循环灌注量/PU/SCerebralsurfaceperfusionvolume210±0781541±6567948±302953426<0001①<③;②<③

表3 3组大鼠第3天和第7天NSS评分的比较Tab.3 NSS scores of the 3 groups of rats on the 3rd and 7th days
注:CI+IMD组与CI+NS组相比,*P< 0.05;CI+IMD组与CI+ADM组相比,#P< 0.05。
Note.CI+IMD group compared with CI+NS group,*P< 0.05;CI+IMD group compared with CI+ADM group,#P< 0.05.
3 讨论
脑缺血和再灌注损伤机制一直是基础和临床研究的重要课题,近年来研究发现,脑缺血损伤所引起的微循环障碍涉及一个复杂的病理生理过程,是一个快速的级联反应。脑血流减少后,细胞处于缺血、缺氧状态,所需能量主要依赖于葡糖糖的无氧酵解生成ATP来提供,其代谢产物为乳酸,导致脑细胞能量供应不足和酸中毒[15]。由于能量供应不足,影响膜电位的形成,电压依赖性钙通道开放,Ca2+内流,导致细胞内Ca2+超载,使自由基清清除相关的酶如超氧化物歧化酶、过氧化物酶、过氧化氢酶等活性下降,抗氧化物下降,体内自由基所处的动态平衡状态受到破坏,氧自由基产生蓄积,损害微循环[16,17]。脑组织受损后,会产生大量炎性介质如白细胞介素、肿瘤坏死因子、血小板激活因子等,进一步加重微循环损伤[18]。此外,脑缺血后微循环障碍可能与兴奋性氨基酸(excitatory amino acid, EAA)毒性作用密切相关[19,20]。缺血后的神经元释放大量的EAA,特别是谷氨酸(Glu),同时能量减少,重摄取能力下降,导致突触后膜Glu受体过度激活,与其偶联的离子型通道开放,加速信号传递,使中枢神经系统出现快速代谢异常,进一步加重神经元及其所处的微环境缺血、缺氧状态[21]。因此,尽早改善微循环,阻断脑缺血病理过程,不仅可以减轻缺血脑组织损伤,而且对脑缺血患者神经功能的恢复具有重要意义。本研究本研究通过对脑缺血大鼠分别进行IMD和ADM药物干预,探讨IMD与ADM对局灶性脑缺血大鼠脑微循环的影响,为临床治疗脑缺血疾病提供新的实验依据。
本研究发现,CI+NS组、CI+ADM组与CI+IMD组大鼠脑表面微循环灌注量及NSS评分的比较,差异均有统计学意义,事后多重比较发现,CI+IMD组大鼠脑表面微循环灌注量均高于CI+NS组与CI+ADM组,且CI+IMD组大鼠脑第3天和第7天NSS评分均低于CI+NS组与CI+ADM组即IMD可以改善局灶性脑缺血大鼠脑微循环,且疗效优于ADM。IMD在中枢神经系统中广泛分布,特别是下丘脑、垂体,其可与细胞表面受体复合物 CRLR/RAMPx结合后发挥生物学效应。RAMP分为3种亚型,ADM与CRLR/RAMP2或3结合,而IMD无选择地作用于CRLR/RAMP1、2或3,并且相对于ADM亲和力更强[7],故相比ADM,IMD的作用可能更为强大、广泛。IMD和ADM均可促进垂体催产素(OXT)的生成[22],有学者在大鼠中枢神经系统中分别给予IMD和ADM发现,IMD引起OXT上升的程度比ADM更为明显,且几乎是ADM的2倍,该机制可能与IMD激活交感神经系统有关[23]。有研究证实,IMD可以降低大鼠外周阻力,舒张容量血管,降低血压,具有剂量依赖性,且作用比ADM强[24]。
经分析,IMD可能通过以下途径来改善脑缺血大鼠脑微循环。首先,IMD的扩血管作用。IMD与其受体结合后,可通过激活腺苷酸活化酶(cAMP)和一氧化氮合酶(eNOS),调节门控离子通道,发挥其扩血管作用[25,26]。其次,IMD的促血管生成作用。IMD可作为新的血管生成因子,促进血管内皮生长因子(VEGF)的合成[27],增加其受体活性,可提高细胞外信号调节激酶1/2(ERK1/2)及苏氨酸激酶(Akt)的磷酸化水平,从而促进毛细血管和微动脉的生成[28,29]。第三,IMD的抗炎、抗氧化应激作用。IMD可以通过减少活性氧产物生成,抑制炎症因子释放,缓解缺氧导致的炎症和氧化应激反应[29,30],降低氧自由基生成和钙超载,提高细胞活性,减少细胞凋亡,从而发挥神经保护作用[31,32],而且还可以在炎症环境下,减少血管渗出,保护血脑屏障[33]。第四,IMD的中枢性升压作用。有研究发现,大鼠经侧脑室注射IMD后发现,心率加快,平均动脉压升高,比IMD作用效应更为持久、明显,而且这种作用可被酚妥拉明所阻断,提示可能与交感神经系统有关[13]。此外,IMD还可以通过磷脂酰肌醇3-激酶(PI-K)途径,使蛋白激酶B激活,在磷酸化靶蛋白,进一步发挥调节糖酵解的作用[34]。
综上所述,本研究通过对脑缺血大鼠分别进行IMD和ADM药物干预,并观察大鼠脑缺血侧脑表面微循环灌注量的变化后发现,IMD可以改善局灶性脑缺血大鼠脑微循环,且疗效优于ADM,这对于进一步深入了解IMD和ADM的药理作用具有重要的理论意义,同时为临床治疗脑缺血疾病提供一定的参考价值。
[1] Mozaffarian D, Benjamin EJ, Go AS, et al. Executive Summary: Heart Disease and Stroke Statistics—2016 Update: A report from the American Heart Association [J]. Circulation, 2016, 133(4): 447-454.
[2] 黄如训. 重视改善缺血性脑血管病的微循环障碍 [J]. 中国现代神经疾病杂志, 2004, 4(2): 72-74.
[3] Bragin DE, Kameneva MV, Bragina OA, et al. Rheological effects of drag-reducing polymers improve cerebral blood flow and oxygenation after traumatic brain injury in rats [J]. J Cereb Blood Flow Metab, 2017, 37(3): 762-775.
[4] 王媛, 赵海军, 卢岩, 等. 针刺对MCAO大鼠神经功能恢复及脑微循环血流量的影响 [J]. 江苏中医药, 2013, 45(7): 70-72.
[5] Bragin DE, Peng Z, Bragina OA, et al. Improvement of impaired cerebral microcirculation using rheological modulation by drag-reducing polymers [J]. Adv Exp Med Biol, 2016, 923: 239-244.
[6] 曾兆禄, 韩继超, 薛云, 等. 针刺结合丹红注射液对大鼠脑缺血再灌注损伤的保护作用 [J]. 中国比较医学杂志, 2016, 26(2): 62-66.
[7] Roh J, Chang CL, Bhalla A,et al. Intermedin is a calcitonin/calcitonin gene-related peptide family peptide acting through the calcitonin receptor-like receptor/receptor activity-modifying protein receptor complexes [J]. J Biol Chem,2004, 279(8): 7264-7274.
[8] Kitamura K, Kangawa K, Kawamoto M, et al. Adrenomedullin: a novel hypotensive peptide isolated from human pheochromocytoma [J]. Biochem Biophys Res Commun, 1993, 192(2): 553-560.
[9] 邱淑怡, 高云. 中介素在各系统的研究进展 [J]. 神经解剖学杂志, 2012, 28(6): 627-630.
[10] 席聪, 安睿, 李海勋, 等. rAAV-PR39-ADM防治大鼠脑缺血/再灌注损伤的研究 [J]. 中国药理学通报, 2015,31 (5): 641-647.
[11] 冯佳越, 陈晓平. 中介素/肾上腺髓质素-2对心血管系统作用的研究进展 [J]. 心血管病学进展, 2012, 33(4): 510-513.
[12] Longa EZ, Weinstein PR, Carlson S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats [J]. Stroke, 1989, 20(1): 84-91.
[13] Ren YS, Yang JH, Zhang J, et al. Intermedin 1-53 in central nervous system elevates arterial blood pressure in rats [J]. Peptides, 2006, 27(1): 74-79.
[14] 季淑梅, 胡圣爱, 何瑞荣. 侧脑室注射肾上腺髓质素对大鼠脑内心血管相关核团儿茶酚胺神经元及c-fos表达的影响 [J]. 中国应用生理学杂志, 2005, 21(2): 146-9.
[15] 杨清麟, 李良. 缺氧对星形胶质细胞DNA甲基化及组蛋白乙酰化相关酶的表达影响 [J]. 中国比较医学杂志, 2014, 24(1): 26-30.
[16] Lee SY, Kim JH. Mechanisms underlying presynaptic Ca2+transient and vesicular glutamate release at a CNS nerve terminal during in vitro ischemia [J]. J Physiol, 2015, 593(13): 2793-2806.
[17] 沈洁, 从长慧. 异氟烷预处理对大鼠肝缺血再灌注时脑线粒体钙及线粒体转运通道的影响 [J]. 中国比较医学杂志, 2014, 26(3): 25-29.
[18] Xie W, Fang L, Gan S, et al. Interleukin-19 alleviates brain injury by anti-inflammatory effects in a mice model of focal cerebral ischemia [J]. Brain Res, 2016, 1650: 172-177.
[19] Wong AC, Ryan AF. Mechanisms of sensorineural cell damage, death and survival in the cochlea [J]. Front Aging Neurosci, 2015,7: 58.
[20] 许保磊, 王蓉. 兴奋性氨基酸转运体2在神经退行性变中的作用 [J]. 中国比较医学杂志, 2012, 22(10): 67-71.
[21] Sakurai T, Akanuma S, Usui T, et al. Excitatory amino acid transporter 1-mediated l-glutamate transport at the inner blood-retinal barrier: possible role in L-glutamate elimination from the retina [J]. Biol Pharm Bull, 2015, 38(7): 1087-1091.
[22] Hashimoto H, Uezono Y, Ueta Y. Pathophysiological function of oxytocin secreted by neuropeptides: A mini review [J]. Pathophysiology, 2012, 19(4): 283-298.
[23] Takahashi K, Morimoto R, Hirose T, et al. Adrenomedullin 2/intermedin in the hypothalamo-pituitary-adrenal axis [J]. J Mol Neurosci, 2011, 43(2): 182-192.
[24] Bell D, Gordon BJ, Lavery A, et al. Plasma levels of intermedin (adrenomedullin-2) in healthy human volunteers and patients with heart failure [J]. Peptides, 2016, 76: 19-29.
[25] Chauhan M, Balakrishnan M, Vidaeff A, et al. Adrenomedullin2 (ADM2)/Intermedin (IMD): A potential role in the pathophysiology of preeclampsia [J]. J Clin Endocrinol Metab, 2016, 101(11): 4478-4488.
[26] Pang Y, Li Y, Lv Y, et al. Intermedin restores hyperhomocysteinemia-induced macrophage polarization and improves insulin resistance in mice [J]. J Biol Chem, 2016, 291(23): 12336-12345.
[27] 赵海红, 李荣山, 乔晞, 等. intermedin对肾脏缺血再灌注损伤后血管再生相关因子表达的影响 [J]. 中华肾脏病杂志, 2011, 27(12): 912-916.
[28] Wei P, Yang XJ, Fu Q, et al. Intermedin attenuates myocardial infarction through activation of autophagy in a rat model of ischemic heart failure via both cAMP and MAPK/ERK1/2 pathways [J]. Int J Clin Exp Pathol,2015,8(9):9836-9844.
[29] 齐永芬. Intermedin与血管损伤性疾病 [J]. 中国病理生理杂志, 2015,31(10): 1809.
[30] Wang Y, Tian J, Guo H, et al. Intermedin ameliorates IgA nephropathy by inhibition of oxidative stress and inflammation [J]. Clin Exp Med, 2016, 16(2): 183-92.
[31] Armstrong D, Stratton RD. Free radicals: their role in brain function and dysfunction [M]. John Wiley & Sons, Inc, 2016.
[32] Wang Y, Tian J, Qiao X, et al. Intermedin protects against renal ischemia-reperfusion injury by inhibiting endoplasmic reticulum stress [J]. BMC Nephrol, 2015, 16: 169.
[33] Chen L, Kis B, Hashimoto H, et al. Adrenomedullin 2 protects rat cerebral endothelial cells from oxidative damage in vitro [J]. Brain Res, 2006, 1086(1): 42-49.
[34] Poyner DR, Sexton PM, Marshall I, et al. International Union of Pharmacology. XXXII. The mammalian calcitonin gene-related peptides, adrenomedullin, amylin, and calcitonin receptors [J]. Pharmacol Rev, 2002, 54(2): 233-246.
Promotingeffectofintermedinandadrenomedullinoncerebralmicrocirculationinratmodelsofcerebralischemia
GUO Xin1, WANG Jing2, WANG Meng1, LU Yue-ying3, JIA Na-na3, LIU Zhen-gang4, TIAN Jing-rui5, YUAN Jie6*
(1.Department of Neurology, Affiliated Hospital of North China University of Science and Technology, Tangshan 063000, China; 2.Tangshan Vocational and Technical College, Tangshan 063000; 3.School of Psychology, North China University of Science and Technology, Tangshan 063000; 4.Department of Neurosurgery, Affiliated Hospital of North China University of Science and Technology, Tangshan 063000; 5.School of Basic Medical Sciences, North China University of Science and Technology,Hebei Key Laboratory for Chronic Diseases, Tangshan Key Laboratory for Preclinical and Basic Research on Chronic Diseases, Tangshan 063000; 6.Institute of Mental Health, North China University of Science and Technology, Tangshan 063000)
ObjectiveTo explore the effect of intermedin (IMD) and adrenomedullin (ADM) on cerebral microcirculation in rats with cerebral ischemia.MethodsRat cerebral ischemia (CI) model was established by middle cerebral artery occlusion. 40 SPF male adult Sprague-Dawley (SD) rats were randomly divided into three groups: CI+NS (normal saline) group, CI+ADM group and CI+IMD group, which were used to observe the changes of brain surface microcirculatory perfusion with a laser Doppler flowmeter.ResultsThe differences of brain surface microcirculatory perfusion were statistically significant among the CI+NS group, CI+ADM group and CI+IMD group (F=53.426,P< 0.05). Multiple comparison showed that the brain surface microcirculatory perfusion in the CI+IMD group was higher than that of the CI+NS group and CI+ADM group.ConclusionsIntermedin can improve the cerebral microcirculation in rats with cerebral ischemia, and its therapeutic effect is better than adrenomedullin.
Intermedin; Adrenomedullin; Cerebral Ischemia; Microcirculation; Rats
河北省硕士研究生创新自助项目(CXZZSS2017072);华北理工大学研究生创新项目(2017S04);河北省中医药管理局2016年度中医药类科研计划课题(2016079)。
郭鑫(1990-),女,硕士研究生,专业:神经病学。E-mail: Drguoxin@126.com
苑杰(1968-),男,教授,主任医师,研究方向:①心脑血管病,特别是相关危险因素的防控和治疗等;②躯体性疾病合并抑郁症的诊治;③抑郁症的发病机制和影响因素研究。E-mail: tsphyj@126.com
R-33
A
1671-7856(2017) 12-0066-07
10.3969.j.issn.1671-7856. 2017.12.012
2017-05-19
