5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸的合成研究
2017-12-19王先恒赵长阔
王先恒,赵长阔,钟 艳,黄 梅,袁 智,曹 颖,徐 浪
(遵义医学院药学院,贵州 遵义 563099)
5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸的合成研究
王先恒,赵长阔*,钟 艳,黄 梅,袁 智,曹 颖,徐 浪
(遵义医学院药学院,贵州 遵义 563099)
以2-丁酮为起始原料,依次与甲酸乙酯反应得到2-甲基-3-氧代-丁醛2(酮酯缩合)、与氰基乙酰胺缩合成5,6-二甲基-3-氰基-2-羟基吡啶3、氰基水解得到5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸1,总收率为30.1%。
2-丁酮;缩合;合成;5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸
烟酸以及2-吡啶酮是一类重要的医药合成中间体[1-2],例如水溶性的维生素B3以及烟酰胺,是人体必需的维生素,辅酶Ⅰ和辅酶Ⅱ的组成部分,参与体内脂质代谢,就是最简单的烟酸结构[1,3-4];治疗特发性肺纤维化,对肺、肾、心脏、肝脏等器官纤维化也有很好疗效的药物吡非尼酮就含有2-吡啶酮的结构[5-6]。随着药理研究的深入开展,发现从真菌或其代谢产物中分离得到3-羧酸-2-吡啶酮衍生物结构显示出很好的生物活性[7-8]:例如,从山毛榉树枯叶中的冬青生菌MFC-870中分离得到冬青生菌素H(Ilicicolin H),具有抗炭疽杆菌活性[9];从白僵菌属真菌的二级代谢产物中分离得到的Tenellin也具有较强的生物活性[7]。

此类活性天然产物的结构修饰或模拟也吸引了很多化学及药物工作者的关注,并也获得了活性较多的新化合物[10]。
5,6-二甲基-3-羧基-2-吡啶酮(化合物 1),是一种3-羧酸-2-吡啶酮衍生物,多篇文献中公开了包含此片段的活性物质[11-12]。Chen在PCT专利文献WO2007129195A2中公开了包含化合物1的活性结构,通过调节JNKs激酶 (c-Jun N-ter minal Kinases),降低胰岛素分泌的葡萄糖阈值,从而降低血糖值[11];Yamagishi在 PCT专利WO2011058766A1中公开了包含化合物1的TTX-S通路抑制剂,主要用于治疗TTX-S通路有关的脑神经或精神失调[12]。
5,6-二 甲 基-3-羧 基-2-吡 啶 酮 (5,6-Dimethyl-2-oxo-1,2-dihydro-pyridine--3-carboxylic acid,1), 也称为 5,6-二甲基-2-羟基烟酸;CAS No.为51727-05-0。对于化合物1,文献报道的合成路线不多:仅Dornow[13]报道了以5,6-二甲基-2-氨基烟酸胺a为原料,与亚硝酸钠在H2SO4溶液中反应得到化合物1,收率为60%;反应通过水解酰胺键,以及将吡啶环上连接的氨基通过重氮化及水解重氮盐得到羟基。3-氧代丁醛与丙二酸衍生物c在乙醇溶剂中环合得到6-甲基-2-氨基烟酸胺 c(a的类似物)。

Scheme 1 5,6-二甲基-2-羟基烟酸3的合成路线[13]
朱卓越等[14]报道了以丙二醛、2-腈基乙酰胺为起始原料,通过胺化得到2-羟基-3-氰基吡啶(f),丙二醛通过将10%HCl溶液滴加入甲醇缩丙二醛中现场制备,三乙胺中和HCl后,与2-腈基乙酰胺在加热条件下环合得到2-羟基-3-氰基吡啶f,通过氧化铝柱层析以59%的收率得到目标产物。

Scheme 1 2-羟基-3-氰基吡啶e的合成路线[14]
由于Dornow[13]报道的路线中原料a不易制备,且反应需要用到重氮化反应,用到大量硫酸,三废处理困难,同时该反应不适合其它3-羧酸-2-吡啶酮类似物的合成。因此,参考以上2-羟基-3-氰基吡啶3的合成方法[14],发展了一条以2-丁酮为起始原料,依次与甲酸乙酯反应、与氰基乙酰胺缩合成吡啶环、氰基水解得到5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸(1)的合成路线。
1 材料与仪器
2-丁酮、NaH (60%的矿物油)、氰基乙酰胺(分析纯,国药集团化学试剂有限公司);甲酸乙酯、乙二醇二甲醚、乙醚、冰醋酸、哌啶、乙醇、浓硫酸(化学纯,成都市科龙化工试剂厂);硅胶薄层板(青岛海洋化工厂);蒸馏水(自制)。
Varian 400 MHz核磁共振波谱仪 (TMS作内标,安捷伦科技有限公司);电热恒温鼓风干燥箱(上海精宏实验设备有限公司,DMG-914M型);LC-10ATVP型高效液相色谱仪(日本岛津公司);暗箱三用紫外分析仪 (上海司乐仪器有限公司,81-2型)。
2 合成方法与讨论
2.1 化合物1的合成路线
以2-丁酮为起始原料,依次与甲酸乙酯反应得到2-甲基-3-氧代-丁醛 2(酮酯缩合)、与氰基乙酰胺缩合成5,6-二甲基-3-氰基-2-羟基吡啶 3、氰基水解得到 5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸1,总收率30.1%。
2.1.1 2-甲基-3-氧代丁醛2的制备
将 2-丁酮(20.0 g,278 mmol)、甲酸乙酯(22.6 g,305 mmol)和干燥的乙二醇二甲醚150 mL置于圆底烧瓶中,冰水浴中向混合物缓慢加入NaH(60%,12.2 g,305 mmol)的乙二醇二甲醚(50 mL)溶液中,滴加时间在1 h以上。然后将反应液缓慢升至室温,并在室温下搅拌过夜。停止反应,将乙醚150 mL倒入混合物中,有浅黄色固体沉淀析出;过滤收集固体,用乙醚洗涤,得到化合物3 21.8 g,收率为79%。
2.1.2 2-羟基-5,6-二甲基吡啶-3-腈3的制备
将氰基乙酰胺(17.6 g,210 mmol),哌啶乙酸盐 (通过向乙酸2 mL中加入哌啶和水6 mL制备,直到混合物呈碱性)和水100 mL置于圆底烧瓶中,然后加入化合物 3(21.0 g ,210 mmol)。 将所得混合物加热回流3 h,然后冷却至室温。将混合物于搅拌下加入乙酸酸化,直到混合物呈酸性,滤出固体。过滤得到粗产品,将粗品用乙醇及水的混合溶剂重结晶,得到目标产物3(12.7 g,41%)。
2.1.3 5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸1的制备
将化合物 3 (11.5 g,78 mmol) 和稀硫酸(50%,w/w,65 mL)的混合物在油浴150℃下加热2 h。停止反应,经反应液冷却至室温,倒入100 mL水中,搅拌,得到黄色沉淀。过滤收集固体产物,洗涤和干燥,得到粗产品。将粗产品用乙酸做溶剂进行重结晶,得到纯品的化合物1 12.1 g,为灰白色固体,收率93%。1H NMR (300 MHz,DMSO-d6) δ 2.10 (s, 3H), 2.32 (s, 3H), 8.19(s, 1H), 13.22 (s, 1H);LC-MS 168 (MH)+;HPLC: >95% (Purity).
2.2 讨论
2.2.1 缩合反应
我们采用了不含α-氢的甲酸乙酯和2-丁酮在碱的作用下发生缩合反应。并对不同的碱及溶剂进行了一定的优化,最终发现在NaH作用下,以DME为溶剂,以76%的较高收率得到中间体化合物2,如下Scheme 3所示[12]。

Scheme 3 化合物2的合成法[12]
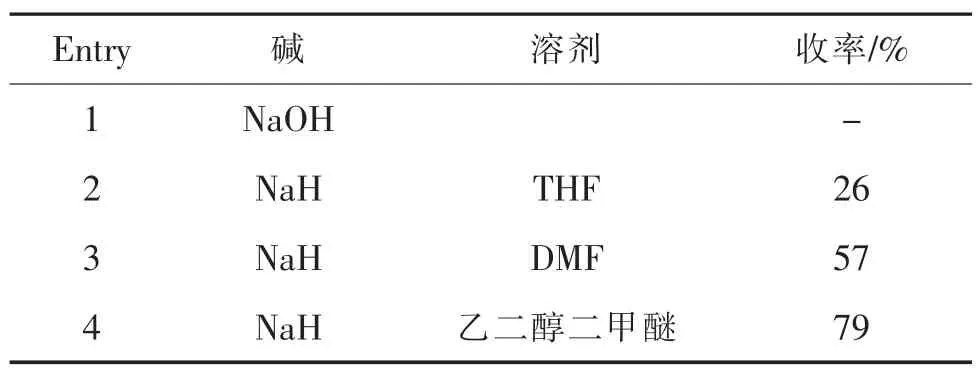
表1 常规条件下制备化合物2的工艺优化Table 1 Process optimization for preparation of compound 1 under normal reaction condition
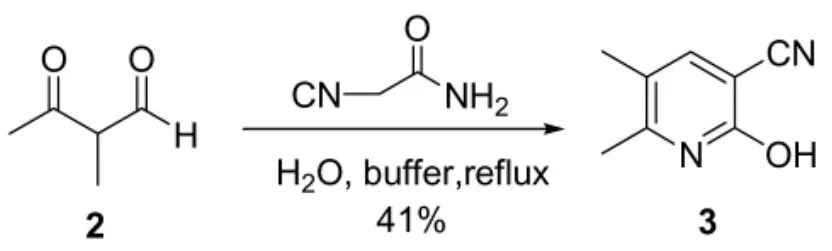
参照2-羟基-3-氰基吡啶的合成方法,将2-
2.2.2 成环反应甲基-3-氧代丁醛2与氰基乙酸胺反应,在哌啶乙酸盐催化下,回流3 h得到期望的化合物3,不过,该反应收率不高,经过优化后也只有41%。
2.2.3 水解反应
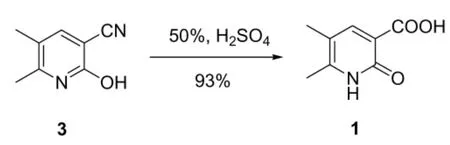
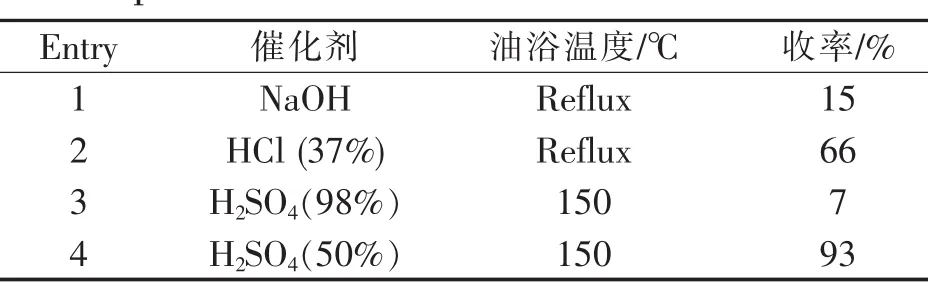
表2 在正常反应条件下制备化合物1的工艺优化Table 2 Process optimization for preparation of compound 1 under normal reaction condition
氰基的水解反应在酸性和碱性条件下都可以进行,我们进行了简单的工艺条件优化,结果发现,2-羟基-5,6-二甲基吡啶-3-腈3在50%的硫酸条件下,油温150℃,加热反应2 h,以93%的收率得到目标化合物。
3 结论
以2-丁酮为起始原料,依次与甲酸乙酯反应得到2-甲基-3-氧代-丁醛2(酮酯缩合)、与氰基乙酰胺缩合成5,6-二甲基-3-氰基-2-羟基吡啶3、氰基水解得到 5,6-二甲基-2-氧代-1,2-二氢吡啶-3-甲酸1,总收率为30.1%。
[1] 关静,霍艳艳,董春娇.烟酸类药物的研究进展[J].沈阳医学院学报,2011,13(2):110-112.
[2] 张明峰,吕志良,李科.2-吡啶酮类衍生物的生物活性及合成方法的研究进展[J].药学实践杂志,2012,30(4): 248-253.
[3] 赵水平.烟酸类调脂药物研究进展[J].临床药物治疗杂志, 2010,8(2):5-8.
[4] 李钟玉,李临生.烟酸、烟酰胺的研究进展[J].化工时刊, 2003,17(2):6-9.
[5] 陈钰清,闫永吉,仇美华,等.吡非尼酮抗纤维化作用的研究进展[J].临床药物治疗杂志,2016,14(5):1-7.
[6] 邵明香,王维亭,赵专友,等.抗肺纤维化新药吡非尼酮[J].现代药物与临床, 2013, 28(3): 409-414.
[7] 赵圣印,黄婧,程健,等.4-羟基-2-吡啶酮类化合物的合成研究进展[J].有机化学,2012,32(4):651-660.
[8] 唐玉敏,李晶,赵圣印.4-羟基-2-吡啶酮类天然生物碱的研究进展[J].有机化学,2011,31(1):9-21.
[9] Hayakawa S,Minato H,Katagori K.Ilicicolins,antibiotic from cylindrocaldium ilicicola[J].J Antibiot, 1971, 24:653-654.
[10]辛伟翔,潘淼,赵圣印.4-羟基-2(1H)-吡啶酮-3-甲酰胺类冬青生菌素类似物的合成与生物活性[J].化学研究, 2015,26(2): 153-157.
[11]Chen P,Hong Y,Humphries P S,et al.4-Pyrimidine-5-aminopyrazole compounds as JNK modulators and their preparation,pharmaceutical compositions and use in the treatment of diseases :WO,2007129195A2[P].2007-11-15.
[12]Yamagishi T,Arano Y,Morita M,et al.Aryl carboxamide derivatives as TTX-S channel blockers,and use thereof:WO,2011058766 A1[P].2011-05-19.
[13]Dornow A,Neuse E.The reaction of amidines with β-dicarbonyl compounds[J].Chemische Berichte, 1951,84:296-304.
[14]朱卓越,黄淑芳.3-溴-1,6-萘啶-5 (6H)-酮的合成[J].华中师范大学学报(自然科学版),2012,46(4):432-434.
Research on Synthesis of 5,6-Dimethyl-2-oxo-1,2-dihydropyridine-3-carboxylic acid
WANG Xian-heng,ZHAO Chang-kuo*,ZHONG Yan,HUANG Mei,YUAN Zhi,CAO Ying,XU Lang
(School of Pharmacy, Zunyi Medical University, Zunyi,Guizhou 563099,China)
Starting from 2-butanone,5,6-dimethyl-2-oxo-1,2-dihydropyridine-3-carboxylic acid 1 was synthesized through 3 steps, in turn reacted with ethyl formate, then cyanoacetamide to form pyridine ring through condensation,and finally hydrolysis of the cyano group.Total yield of the target compound was 30.1%.
2-butanone;condensation;synthesis;5,6-dimethyl-2-oxo-1,2-dihydropyridine--3-carboxylic acid
1006-4184(2017)11-0024-04
2017-08-24
贵州省科技合作计划项目(黔科合LH字[2014]7545号);贵州省科技合作计划项目(黔科合LH字[2015]7531号);遵义医学院博士启动资金([2013]F-633)。
王先恒(1978-),女,贵州遵义人,博士,副教授,研究方向:新药设计与合成、临床药学研究等。
*通信作者:赵长阔,E-mail:zhaochangkuo@163.com。
