利福平纳米脂质载体的制备及质量评价
2017-12-19胡建军余莉陈海林林薇金海英宁波大学医学院附属医院药剂科浙江宁波315020
胡建军,余莉,陈海林,林薇,金海英(宁波大学医学院附属医院药剂科,浙江宁波315020)
利福平纳米脂质载体的制备及质量评价
胡建军*,余莉,陈海林,林薇,金海英#(宁波大学医学院附属医院药剂科,浙江宁波315020)
目的:制备利福平(RFP)纳米脂质载体(RFP-NLCs),提高其水溶性,并评价其质量。方法:以液固脂质材料油酸及单硬脂酸甘油酯为脂质材料,大豆卵磷脂为乳化剂,泊洛沙姆188为非离子型表面活性剂,采用熔融-超声乳化法制备RFP-NLCs。以粒径和包封率的综合评分为指标,以脂质材料的用量、液态脂质材料比例、投药量和大豆卵磷脂-泊洛沙姆188质量比为因素,采用正交试验优化处方。测定最优处方所制脂质载体的形态、粒径、多分散指数(PDI)、Zeta电位、包封率、载药量和体外释放度。结果:最优处方中脂质材料用量为150 mg,液态脂质比例为30%,RFP用量为10 mg,大豆卵磷脂-泊洛沙姆188的质量比为1∶3。所制RFP-NLCs的外观较圆整,粒径为(124.07±3.25)nm,PDI为0.104±0.010,Zeta电位为(-31.07±2.94)mV,包封率为(80.90±2.59)%,载药量为(4.81±0.68)%(n=3)。与RFP原料药比较,RFP-NLCs体外释放度明显减缓,12 h内的累积释放度为63.2%,释药行为符合Weibull方程。结论:筛选处方可成功制备RFP-NLCs;所制RFP-NLCs粒径小、包封率较高,具有体外缓释特征。
利福平;纳米脂质载体;制备;质量评价
利福平(Rifampicin,RFP)系抗结核一线用药,对结核杆菌及其他分枝杆菌均有强大的杀菌作用。但由于临床上RFP用药剂量大、作用时间长,易造成严重的胃肠道毒副作用及肝损伤,以致患者依从性较差、治疗失败率升高[1-5]。纳米脂质载体(Nano-structured lipid carriers,NLCs)为第二代脂质纳米粒,是在固体脂质中加入化学性质不同的液态脂质,使纳米粒变成结晶缺陷型或无定形型结构,以达到提高难溶性药物水溶性和载药量的目的,且具有缓释特性[6-8]。本研究采用熔融-超声乳化法制备RFP-NLCs,采用正交试验优化处方,并评价其质量,以期为开发新型RFP给药剂型提供参考。
1 材料
1.1 仪器
Agilent 1200型高效液相色谱仪(美国Agilent公司);Nano-ZS型粒径分析仪(英国Malvern公司);HT7700型透射电子显微镜(日本Hitachi公司);OptimaMAX型超速离心机(美国Beckman公司);Scientz-ⅡDN型超声波细胞粉碎机(宁波新芝生物科技股份有限公司)。
1.2 药品与试剂
RFP原料药(沈阳双鼎制药有限公司,批号:13050301,纯度:>98%);RFP对照品(中国食品药品检定研究院,批号:110757-201004,纯度:>99%);单硬脂酸甘油酯(法国Gattefosse公司,批号:127339);油酸(上海阿拉丁生化科技股份有限公司,批号:141021);注射用大豆卵磷脂(上海太伟药业有限公司,批号:20130201);泊洛沙姆188(德国Basf公司,批号:WPAF538B);甲醇为色谱纯,其他试剂均为分析纯。
1.3 其他
透析袋(美国Viskase公司,截留分子量:7 000 Da)。
2 方法与结果
2.1 RFP-NLCs的制备
称取处方量的单硬脂酸甘油酯、油酸和RFP,加入少量甲醇,置于70℃恒温水浴中熔融,作为油相;另称取处方量的乳化剂大豆卵磷脂和泊洛沙姆188,分散于20 mL水中,作为水相;待水相加热至与油相相同的温度,在磁力搅拌下将水相滴加到油相中形成初乳;趁热将初乳超声3 min(300 W,3 s间隔)后,冷却至室温,0.45 μm微孔滤膜过滤,即得RFP-NLCs。同法制备不含RFP的NLCs,作为空白对照。
2.2 RFP的含量测定方法
2.2.1 色谱条件色谱柱:Platisil ODS(150 mm×4.6 mm,5 μm);流动相:甲醇-0.02 mol/L磷酸二氢钾(65∶45,V/V);流速:1.0 mL/min;柱温:35℃;检测波长:254 nm;进样量:20µL。在该色谱条件下,辅料不干扰RFP的测定。
2.2.2 线性关系精密量取RFP对照品适量,加甲醇稀释成质量浓度分别为50.0、20.0、10.0、5.0、2.0、1.0 μg/mL的系列对照品溶液,按“2.2.1”项下色谱条件进样测定,以峰面积(A)对质量浓度(c)进行线性回归,得RFP的回归方程为:A=89.944c+49.97(r=0.999 9,n=6)。结果表明,RFP检测质量浓度在1.0~50.0 μg/mL范围内与峰面积呈良好的线性关系,RFP的定量限为0.5 μg/mL(以信噪比≥10计)。
2.2.3 精密度、准确度与稳定性取低、中、高质量浓度(2.0、10.0、40.0 μg/mL)的RFP对照品溶液,分别按“2.2.1”项下色谱条件进样测定,同日内测定5次考察日内精密度;每日测定1次,连续测定5 d考察日间精密度;以测定值/真实值×100%计算回收率。结果,RFPNLCs混悬液的日内、日间精密度RSD均小于2%(n=5);低、中、高浓度样品的平均回收率分别为(96.51±1.32)%、(97.03±1.43)%、(97.50±1.15)%(n=3)。同一批次制备的RFP-NLCs混悬液放置24 h后再进样测定,考察稳定性。结果,稳定性试验中含量的RSD为1.25%(n=6)。
2.3 包封率与载药量的测定
精密量取RFP-NLCs混悬液,4℃下225 000×g离心60 min。取上清液1 mL,置于10 mL量瓶中,用甲醇稀释至刻度,经0.22 μm微孔滤膜过滤,取续滤液,按“2.2.1”项下色谱条件进样测定游离RFP的含量,记作W1;取离心后沉淀物,蒸馏水洗涤3次,真空冷冻干燥后精密称定总质量,记作W。另精密量取RFP-NLC混悬液1 mL,置于10 mL量瓶中,用甲醇稀释至刻度,100 W超声10 min,经0.22 μm微孔滤膜过滤,取续滤液按“2.2.1”项下色谱条件进样测定RFP总含量,记作W0。计算RFP-NLCs的包封率和载药量:包封率(%)=(W0-W1)/W0×100%,载药量(%)=(W0-W1)/W×100%。
2.4 正交试验优化处方
2.4.1 试验设计与结果根据单因素预试验结果,选择对RFP-NLCs制备工艺、理化性质影响较大的因素,即脂质材料的用量(A,mg)、液态脂质比例(B,%)、投药量(C,mg)和大豆卵磷脂-泊洛沙姆188质量比(D)为考察因素。每个因素选取3个水平,按正交设计L9(34)表设计试验,以粒径(y1)和包封率(y2)的综合加权评分值[y,y=50×(1-y1/y1max)+50×y2/y2max]为考察指标,筛选RFP-NLCs处方。因素与水平见表1,正交试验设计与结果见表2,方差分析结果见表3。

表1 因素与水平Tab 1Factors and levels

表2 正交试验设计与结果Tab 2Orthogonal test design and results

表3 方差分析结果Tab 3Results of variance analysis
由表2和表3可知,各因素对综合加权评分值的影响程度依次为A>C>D>B,其中A和C对综合加权评分值有显著影响(P<0.05)。以综合加权评分值越大为标准,筛选得到最优处方为A2B1C2D3,即脂质材料用量为150 mg,液态脂质比例为30%,RFP用量为10 mg,大豆卵磷脂-泊洛沙姆188质量比为1∶3。
2.4.2 验证试验按“2.4.1”项下优化的处方制备3批RFP-NLCs,采用Nano-ZS型粒径分析仪检测其粒径、多分散指数(PDI)和Zeta电位,按“2.3”项下方法检测其包封率和载药量。结果显示,所制RFP-NLCs的平均粒径为(124.07±3.25)nm,PDI为0.104±0.010,Zeta电位为(-31.07±2.94)mV,包封率为(80.90±2.59)%,载药量为(4.81±0.68)%(n=3)。
2.5 外观形态
取按最优处方制备的RFP-NLCs适量,以2.0%磷钨酸溶液负染,使用HT7700型透射电子显微镜观察其外观形态。结果显示,RFP-NLCs外观形态圆整,大小及分布较均匀。透射电镜图见图1。

图1 RFP-NLCs的透射电镜图Fig 1TEM photograph of RFP-NLCs
2.6 体外释药
精密称取RFP原料药和按最优处方制备的RFPNLCs适量(约含RFP 2 mg),分散于2 mL释放介质[含1%乙二胺四乙酸二钠(EDTA-2Na)和1%Na2SO3的磷酸盐缓冲液(PBS),pH为7.4]中[9],装入处理好的透析袋中,密封后置于100 mL释放介质中,于(37±0.5)℃恒温水浴下以75 r/min振荡。分别于15、30、60 min和1、2、4、6、8、10、12、24、36、48 h各取样2 mL,同时补充2 mL同温释放介质。按“2.2.1”项下色谱条件进样检测释放液中RFP的含量,计算累积释放度,并以累积释放度(Q)为纵坐标、时间(t)为横坐标作图,绘制释放曲线。RFP原料药和RFP-NLCs的体外释药曲线见图2。
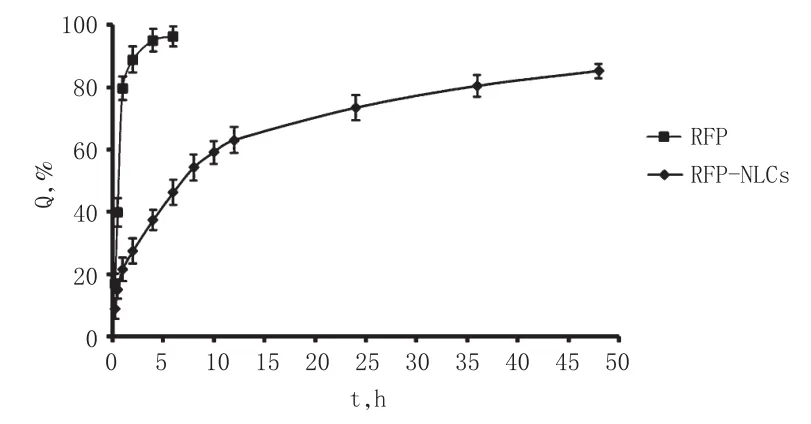
图2 RFP原料药和RFP-NLCs的体外释药曲线(n=3)Fig 2The in vitro drug release curves of RFP raw materials and RFP-NLCs(n=3)
由图2可见,RFP原料药释药迅速,4 h时的累积释放度已达到95.1%;而RFP-NLCs释药前期有少量突释,12 h时的累积释放度为63.2%,之后平稳释药,48 h时的累积释放度为85.2%。此外,分别用零级动力学方程、一级动力学方程、Higuchi方程和Weibull方程对RFP-NLCs的体外释药行为进行拟合,结果显示,其释药行为符合Weibull方程[lnln(1/1-Q)=0.564 9lnt-1.486 1,R2=0.995 3]。
3 讨论
笔者曾采用溶剂分散法、薄膜超声分散法制备RFPNLCs,但所制RFP-NLCs的粒径明显大于熔融-超声乳化法,且较不稳定。综合考察,选用熔融-超声乳化法制备RFP-NLCs。文献[10-11]表明,液态脂质比例在0~40%范围为宜,其包封率随液态脂质的比例升高,先增大后减少。通过正交试验,本试验最终选择30%的油酸比例。泊洛沙姆188为非离子型表面活性剂,与大豆卵磷脂合用,能插入磷脂单分子层形成稳固的混合层,可减小粒径,亦能提高稳定性。
RFP在水中几乎不溶,选择普通溶出介质难以实现漏槽条件。因此,本试验参考文献[9]中相关内容,选择含1%EDTA-2Na和1%Na2SO3的PBS(pH 7.4)作为释放介质。由体外释药曲线可见,RFP-NLCs具有一定的突释性,后期平缓释药,呈现明显的缓释特性。
综上所述,本研究筛选的处方可成功制备RFPNLCs,所制RFP-NLCs粒径小、包封率较高、具有体外缓释特征。
[1]Riccardi G,Pasca MR.Trends in discovery of new drugs for tuberculosis therapy[J].J Antimicrob,2014,67(9):655-659.
[2]Riccardi G,Pasca MR,Buroni S.Mycobacterium tuberculosis:drugresistanceandfutureperspectives[J].Future Microbiol,2009,4(5):597-614.
[3]Gallardo CR,Comas DR,Figuls MRI,et al.Fixeddoseco-mbinationsofdrugsversussingledrug formulations for treating pulmonary tuberculosis[J].CochraneDatabaseSystRev,2016,doi:10.1002/14651858.CD009913.pub2.
[4]Alsultan A,Peloquin CA.Therapeutic drug monitoring in the treatment of tuberculosis:an update[J].Drugs,2014,74(9):1061.
[5]荆颖,黄淑萍,王倩,等.利福平药动学影响因素的研究进展[J].中国药房,2017,28(12):1726-1728.
[6]Slavomira D,Souto EB,Silva AM.Nanotoxicology appli-ed to solid lipid nanoparticles and nanostructured lipid carriers-a systematic review of in vitro data[J].Eur J Pharm Biopharm,2014,87(1):1-18.
[7]Beloqui A,Solinís MÁ,Rodríguezgascón A,et al.Nanostructuredlipidcarriers:promising drugdeliverysystemsforfutureclinics[J].Nanomed Nanotechnol,2015,12(1):143-161.
[8]Singh H,Jindal S,Singh M,et al.Nano-formulation of rifampicin with enhanced bioavailability:development,characterizationandin-vivo safety[J].Int J Pharm,2015,12(1):143-161.
[9]曹佳薇,倪坚军,姚君,等.利福平脂质体温敏型原位凝胶的制备及其体外释药特征研究[J].中国现代应用药学,2016,33(2):183-187.
[10]孙珊珊,王慧云,王飞飞,等.阿德福韦酯纳米脂质载体的制备及处方优化[J].中国药房,2017,28(16):2259-2261.
[11]Shao Z,Shao J,Tan B,et al.Targeted lung cancertherapy:preparationandoptimizationof transferrin-decorated nanostructured lipid carriers as novel nanomedicine for co-delivery of anticancer drugs and DNA[J].Int J Nanomedicine,2015,10:1223-1233.
Preparation and Quality Evaluation of Rifampicin Nano-structured Lipid Carriers
HU Jianjun,YU Li,CHEN Hailin,LIN Wei,JIN Haiying(Dept.of Pharmacy,the Affiliated Hospital of Medical College,Ningbo University,Zhejiang Ningbo 315020,China)
OBJECTIVE:To prepare rifampicin(RFP)nano-structured lipid carriers(RFP-NLCs)to improve its watersolubility,and evaluate its quality.METHODS:Using liquid-solid lipid materials oleate and glyceryl monostearate as lipid materials,soy lecithin as emulsifier,poloxamer 188 as nonionic surfactant,melting-ultrasonic emulsification was used to prepare RFP-NLCs.Using the comprehensive scores of particle size and encapsulation efficiency as indexes,the amount of lipid materials,proportion of liquid lipid materials,dosage,and mass ratio of soy lecithin-poloxamer 188 as factors,orthogonal test was adopted to optimize the formulation.The morphology,particle size,polydispersity index(PDI),Zeta potential,encapsulation efficiency,drug loading and in vitro release degree of prepared lipid carriers with optimal formulation were evaluated.RESULTS:In the optimal formulation,the amount of lipid materials was 150 mg,proportion of liquid lipid materials was 30%,amount of RFP was 10 mg,and mass ratio of soy lecithin-poloxamer 188 was 1∶3.Prepared RFP-NLCs had rounded appearance,particle size was(124.07±3.25)nm,PDI was 0.104±0.010,Zeta potential was(-31.07±2.94)mV,encapsulation efficiency was(80.90±2.59)%,and drug loading was(4.81±0.68)%(n=3).Compared with RFP raw materials,in vitro release degree of RFP-NLCs significantly slowed down,and the cumulative release degree within 12 h was 63.2%,which was in line with Weibull equation.CONCLUSIONS:Screened formulation can successfully prepare RFP-NLCs;the prepared RFPNLCs have small particle size and high encapsulation efficiency,and the in vitro drug release shows certain sustained-release characteristics.
Rifampicin;Nano-structured lipid carriers;Preparation;Quality evaluation
R943
A
1001-0408(2017)34-4879-03
DOI10.6039/j.issn.1001-0408.2017.34.33
*药师。研究方向:医院药学、药物新剂型。电话:0574-87035223。E-mail:526416166@qq.com
#通信作者:副主任药师,硕士。研究方向:医院药学。电话:0574-87035223。E-mail:13736053092@163.com
2017-06-05
2017-08-28)
(编辑:邹丽娟)
