高效课堂,就这么简单
——基于一堂习题课引发的思考
2017-12-14颜建河
颜建河
河北
高效课堂,就这么简单
——基于一堂习题课引发的思考
颜建河

当下,高效课堂是我们每位教师对课堂教学的追求,打造高效的课堂离不开学生这个主体。学生不参与课堂教学,学生之间、师生之间的互动交流就不能实现,这样的课堂教学效率怎么会高呢?新课程标准告诉我们,在教学活动中,教师应成为组织者、引导者、促进者和参与者,教师的教学方法应该灵活多样。教学过程是师生交往共同发展的互动过程,要通过讨论、研究、实验等多种教学组织形式,引导学生积极主动的学习,培养学生掌握和运用知识的能力,要关注每个学生,使每个学生都得到充分发展。
然而,长期以来我们所形成的授课方式基本上就是“满堂灌”。灌知识、灌方法,鲜有师生互动,基本上谈不上激活体悟、启迪智慧、开拓潜能。这样的教学方式符合现代教育思想、符合新课标理念吗?如何打造高效课堂?其实很简单,观念是第一位,其次再次才是方法。本文基于一堂习题课引发的思考来展示高效课堂的魅力所在,真正促进教学效率和质量的提高。
一、案例展示,发现问题
思维是智力的核心,思则明,明则通,通则变。从“一题一问”到“一题多变”,沟通知识的联系,增强大脑中思维的内在模式。我们知道,教材中的多数问题,只要求回答一个方向的问题,对于有些习题可适当作些扩展、演变,增加设问,起到“一题多练”“一题多得”的作用。特别是鼓励学生自己进行改编训练,以收到“举一反三”“触类旁通”之功效。
【案例】有机物A、B的化学式不同,它们只可能含碳、氢、氧元素中的2种或3种。如果将A、B不论以何种比例混合,只要其物质的量之和不变,完全燃烧时所消耗的氧气和生成的水的物质的量也不变,那么A、B组成必须满足的条件是________。若A是CH4,则符合上述条件的化合物B中,相对分子质量最小的是________(写化学式),并写出相对分子质量最小的,含有甲基(—CH3)的B的两种同分异构体的结构简式:________。
【分析】这是一道确定有机物结构及判断符合题意的有机物所必须满足条件的题目,试题综合性强,有一定难度。问题提出后,学生很容易根据题意得出:A、B分子中所含氢原子数必须相同。这是因为A、B不论以何种比例混合,只要其物质的量之和不变,完全燃烧时生成水的物质的量也不变。然而,A、B分子中的碳原子数有何种关系呢?如何来确定?这是题中的难点和关键。要解决这一难点问题,教师就要了解学生已经有的经验和认知,了解学生在“这个问题上”已经“知道了什么”,在将要解决的内容中,可能遇到的思维障碍是什么,以及对于“这个问题”是如何展开“思考”的。同时,难点的突破,就是要使问题退回到学生思维的“最近发展区”,符合学生认知规律,让学生经历“跳一跳”才能摘到桃子,让学生的“学习”效益最大化。
二、互动交流,探求方法
华罗庚先生说过:“把一个比较复杂的问题‘退’成最简单最原始的问题,把这最简单最原始的问题想通了,想透了,然后再……来一个飞跃上升。”这是一个非常精辟的思维方法。这里的“退”是为了“进”。“退”够了、“退”到“起始点”正是为了看清问题的一般规律,就会有左右逢源,水到渠成的功效。如何突破难点?如何使问题由“难”变“易”?基于此,把问题退回到最核心的概念和本质上,明确内容所蕴含的核心思想。搭建学生得以攀爬的“支架”,使学生一步一个台阶,循序渐进、节节攀登,使课堂真正回归到知识生成,学生思维发生的“原生态”。这样的设计、自然顺畅,层层递进,使学生在一步步减缓难度的情况下,使意义建构在经验基础之上。同时,要根据学生实际调整设问,用小步子设问控制难度,启发诱导。
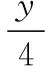
这时,教师可再提出问题:为什么它们的化学式不同,但耗氧量却相同呢?经过师生之间的交流讨论,学生很快明白:“C3H6O2可改写为(C2H6)(CO2)”,并从中发现组分“(CO2)”不耗氧,所以等物质的量的C2H6和C3H6O2完全燃烧时所耗氧量相等。据此,可推知它们不论以何种比例混合,只要其物质的量不变,则耗氧量也不变。
经过上述引导、讨论,可总结出如下规律:“等物质的量的各种有机物(只含C、H或O)完全燃烧时,化学式中相差若干个‘(CO2)’组分,则耗氧量相同。”
从上述结论,学生很容易解决案例中的各个问题。根据题意知,A与B分子中若相差n个碳原子,则必须差 2n个氧原子,即相差n个“(CO2)”组分(n为正整数)。若A为CH4,则B为(CH4)(CO2),即为C2H4O2,其结构简式为CH3COOH、HCOOCH3,最终完成题目的解答。
在完成上述题目的解答后,不能认为万事大吉了。殊不知,就此结束可能会有很多的缺憾和不足,知识很难学活、用活,能力很难有大的提高。倘若学生在做完一道题目后,能及时地进行反思、总结,他们将会有更大的收获。此时,教师可再提出迁移拓展练习。
三、拓展练习,巩固创新
教学中,对于涉及的“难点”,即“难以攀登的大山”进行“解体”“退化”,设计一系列的问题串、变式串,注重它的问题性、指向性、适切性、探究性和有效性,切实达到突破难点的目的。例如,通过案例的分析,师生间进行互动交流,探求方法,进而找到了解决烃及其衍生物耗氧量的求解对策。即抓住如下两个非常基础的反应:
上述反应式可称之为有机物燃烧时,碳、氢元素的耗氧规律。即烃类物质燃烧的耗氧量决定于碳、氢原子数,燃烧后生成水量的多少由分子中所含氢原子数决定;烃的含氧衍生物燃烧的耗氧量决定于分子中所含碳、氢、氧原子数,燃烧后生成水的量由分子所含氢原子数决定。依据这一基础反应,可总结出一系列的规律。同时,还可运用这些规律去解决涉及这方面的各种计算问题,且其方法简捷、高效。
【拓展练习】1.有机物完全燃烧时耗氧与生成CO2的物质的量之比分别为①1∶1;②3∶2;③1∶2。试分别求其有机物的化学式(只含C、H或O)。
【分析与解答】依据所学知识可知,有机物化学式中每含1 mol C,就得消耗1 mol O2,并生成1 mol CO2,所以当耗O2与生成CO2的量相等时,其组成可写为Cm(H2O)n;当耗O2的物质的量大于生成的CO2的量时,说明分子组成中除“(H2O)”组分后的残基中必含C和H,故其分子组成可写为(CxHy)m(H2O)n;当耗O2的物质的量小于生成的CO2的量时,说明分子组成中除“(H2O)”组分后的残基中必含C和O,故其分子组成可写为(CxOy)m(H2O)n。这样,题目中的各个问题便可迅速给予解决。其正确答案如下:
①依据通式Cm(H2O)n进行讨论:若m=1、n=1,则化学式为CH2O(甲醛);若m=2、n=2,则化学式为C2H4O2(乙酸或甲酸甲酯);若m=6、n=6,则化学式为C6H12O6(葡萄糖或果糖)……
②依据通式(CxHy)m(H2O)n可得出:
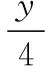
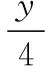
3 2

所以,可将其通式进一步改写为(CH2)m(H2O)n,并进行如下讨论:若m=1、n=1,则化学式为CH4O(甲醇);若m=2、n=1,则化学式为C2H6O(乙醇或甲醚);若m=3、n=1,则化学式为C3H8O(丙醇或甲乙醚)……
③依据通式(CxOy)m(H2O)n可得出:
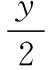
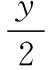
1 2

所以,可将其通式进一步改写为(CO)m(H2O)n,并进行如下讨论:若m=1、n=1,则化学式为CH2O2(甲酸)……
【拓展练习】2.某些只含C、H、O的有机物,完全燃烧后,耗O2与产生CO2的物质的量之比为3∶4。试回答:
(1)这些有机物分子中,相对分子质量最小的化合物的化学式为________。
(2)某两种碳原子数相同的上述有机物,若它们的相对分子质量分别为a和b(a (3)在这些有机物中有一种化合物,它含有两个羧基。取0.263 g该化合物恰好能跟25.0 mL 0.100 mol·L-1的NaOH溶液完全中和,由此可以得知该化合物的相对分子质量是________,并推出它的化学式应是________。 【分析与解答】依据题意知,耗O2的量少于生成CO2量,可设其通式为(CxOy)m(H2O)n。则有 3 4 所以可推出这些有机物的通式为(C2O)m(H2O)n。 (1)若m=n=1,则化学式为C2H2O2,且相对分子质量最小,为乙二醛,结构简式为OHC—CHO。(2)A、B两物质所含碳原子数相同,则m必相同,允许变化的是n,所以b-a必是18的整数倍。(3)若设该有机物的通式为HOOC—R—COOH,则有 M2 0.263 g 0.025 L×0.100 mol·L-1 即该有机物的相对分子质量为210。又知:40m+18n=210,且m、n必为正整数,所以只有当m=3、n=5时符合题意,故D的化学式为(C2O)3(H2O)5,即为C6H10O8。结构简式为HOOC—(CHOH)4—COOH(四羟基己二酸)。 河北省衡水市故城县教育局教研室)