不同养殖场家蝇成虫体表携带细菌的分离与鉴定
2017-12-13,,,,,,,2,,2
,,,, , ,,2, ,2
·论著·
不同养殖场家蝇成虫体表携带细菌的分离与鉴定
陈丹1,庄桂芬1,黄振东1,薛志静1,刘婧1,李妍1,张瑞玲1,2,张忠1,2
目的研究不同养殖场内家蝇成虫体表携带细菌数量和类别。方法采用网捕法对不同养殖场的家蝇进行采样,利用振荡洗脱法分离其体表细菌,对获得细菌的16S rDNA基因扩增后进行分离分子鉴定。结果不同养殖场内家蝇密度、体表携带细菌数量和种类有统计学差异,且家蝇密度与体表携带细菌数量和携带的细菌属数呈线性相关关系。在养殖场内分离到的家蝇体表携带细菌中,葡萄球菌属、克雷伯氏菌属、埃希菌属、沙雷氏菌属分布较广,同时分离的细菌中多为条件致病菌,存在疾病传播风险。结论养殖场家蝇密度反映出养殖场的整体管理水平;养殖场孳生的家蝇可机械性携带条件致病菌,存在将细菌传播给人类的风险,需要进一步加强对养殖场蝇类防控及携带细菌的监控。
家蝇;养殖场;体表细菌;机会致病细菌;蝇传疾病
家蝇是重要的医学媒介生物,为世界性分布的昆虫,且食性广泛,活动能力强,特别喜欢孳生于居民区、养殖场、食品加工厂、垃圾处理场等场所,不仅会对人产生视觉污染,而且可以传播疾病,影响畜牧业健康生产,可将病原菌从重度污染的区域带向居民区,造成疾病的发生与流行。
蝇类传播疾病通常分为机械传播和生物传播,其中以机械性传播为主,可传播包括细菌、原生动物、病毒、寄生虫卵囊和卵等30多种病原体[1-8]。蝇类对病原体的机械性传播主要通过粪口传播途径和体表携带两种途径,这主要与蝇类体表布满鬃毛,爪垫上有纤毛等结构有关;同时,蝇类在取食时边吃、边吐、边排便的摄食习性,增加了其携带的病原体污染水、食物、用具等物体表面的机会,从而造成人类的感染[9-10]。
目前,家蝇是养殖场重点防控的媒介生物,特别是在一些养殖条件较差的小型养殖场和散户型养殖场,家蝇孳生非常严重,并影响周边居民的正常生活。由于家蝇在养殖场、周边住户、养殖户等生态环境之间不断窜扰,有将体表携带病原体传给人类的风险。因此,需要加强对蝇类体表携带病原体的检测研究,为蝇类传播的疾病提供风险评估,并制定合理的防控预案。
1 材料与方法
1.1采样地点 采样地点位于山东省泰安市岱岳区和济南市平阴县,共包括9个养殖场的10个采样点。分别为:泰安市岱岳区朱康村猪舍(东经116.9°,北纬36.2°)、泰安市岱岳区高庄村猪舍(东经116.9°,北纬36.2°)、济南市平阴县绿环托佩克种猪场(东经116.4°,北纬36.3°)、泰安市岱岳区鱼东村奶牛场(东经116.9°,北纬36.2°)、泰安市岱岳区同和奶牛养殖专业合作社粮仓和犊牛舍(东经117.4°,北纬36.2°)、泰安市岱岳区西孙村奶牛场(东经116.9°,北纬36.2°)、泰安市岱岳区西孙村养鸡场(东经116.9°,北纬36.2°)、泰安市岱岳区西孙村养鸭场(东经116.9°,北纬36.2°)和泰安市岱岳区鱼池村鸭场(东经116.9°,北纬36.2°)。
1.2蝇类的采集方法 蝇类的采集采用网捕法,在养殖场蝇类成虫聚集处随机扫3网,将网捕到的苍蝇经乙醚麻醉后分装到10 mL离心管中,采集所用器材均经无菌处理。回实验室后,将各种蝇类进行分类鉴定,将鉴定出的家蝇进行体表细菌的分离与鉴定。
1.3蝇类体表细菌的分离方法 家蝇体表携带细菌的分离方法采用振荡洗脱法。将家蝇样品按采集地点各取10头家蝇分别置于50 mL离心管中,再加入20 mL无菌水和10 μL吐温80,震荡洗脱3~5 min。取体表洗脱液稀释50倍后,各取100 μL,涂板,24 h后,计数各平板中菌落数量。培养2 d后,挑取形态不同的菌落三区划线法接种到新的牛肉膏蛋白胨固体培养基上进行分离纯化,直至分离到单一的菌落。
1.4蝇类体表携带细菌的鉴定 将分离到的单菌落置于LB液体培养基内摇菌过夜,然后采用CTAB法提取各细菌DNA,并对16S rDNA的V3高变区进行PCR扩增,取阳性PCR产物送北京华大基因公司进行序列测定。将测序结果所测序列提交到GenBank中进行序列对比,从GenBank数据库中获得有关种的公认标准序列数据,取相似度最高的为鉴定结果,相似率gt; 99% 视为同种,95%~99%则为同一属,lt;95% 则认为同一科。一般均可鉴定到属。
2 结 果
2.1不同养殖场家蝇的密度 不同养殖场采集到的家蝇数量有统计学差异(F=56.41,P=0.0001),其中,以开放式奶牛养殖场采集到的家蝇最多,泰安市岱岳区鱼东村奶牛场和西孙村奶牛场家蝇密度平均为88.3头/网和89.3头/网,其次是养鸡场和养鸭场,平均约为75头/网,而管理水平较高的同和奶牛养殖合作社内,在粮仓和犊牛舍内家蝇密度分别为33头/网和41头/网。对于3家养猪场来说,由于管理水平不同,家蝇数量也有较大差异,其中做到了粪便当日清理的泰安市岱岳区高庄村猪舍,家蝇密度较低,平均为24头/网;而在济南绿环托佩克种猪场,仅养殖种猪用于品种改良和配种,养殖数量较少,管理水平较高,因此家蝇密度最低,约为18.7头/网;相反管理比较粗放的泰安市岱岳区朱康村猪舍中,家蝇密度较高,约为44.7头/网(图1)。

注:各字母代表的养殖场如下所示,下同。a:泰安市岱岳区朱康村猪舍f:泰安市岱岳区同和奶牛养殖专业合作社犊牛舍b:泰安市岱岳区高庄村猪舍g:泰安市岱岳区西孙村奶牛场c:济南绿环托佩克种猪场h:泰安市岱岳区西孙村养鸡场d:泰安市岱岳区鱼东村奶牛场i:泰安市岱岳区西孙村养鸭场e:泰安市岱岳区同和奶牛养殖专业合作社粮仓j:泰安市岱岳区鱼池村鸭场图1 不同养殖场家蝇的密度(头/网)Fig.1 Population density of Musca domestica in different livestock farms

图2 不同养殖场家蝇体表分离到的细菌数量(105/头)Fig.2 Number of bacteria isolated from body surface of Musca domestica in different livestock farms
2.2不同养殖场家蝇体表携带细菌数量 不同养殖场家蝇体表携带细菌数量有统计学差异(F=248.95,P=0.0001),其中以开放式奶牛养殖场家蝇体表携带细菌数量最高(泰安市岱岳区鱼东村奶牛场和泰安市岱岳区西孙村奶牛场),捕获的家蝇体表携带细菌数量平均约为1×106个/头,而管理水平较高的同和奶牛养殖合作社内,在粮仓和犊牛舍内捕获的家蝇体表携带细菌数量平均约为8×104个/头。对养猪场来说,济南绿环托佩克种猪场内家蝇体表携带细菌数量最低,平均约为2×105个/头,而管理水平较低的高庄村猪舍中家蝇体表携带细菌量最高,平均约为6×105个/头。3个禽类养殖场家蝇体表携带细菌数量相近,平均约为7×105个/头(图2)。
2.3不同养殖场家蝇体表携带细菌的种类 不同养殖场家蝇体表携带细菌的种类也有区别。其中在3个养猪场分离到细菌13属,在4个奶牛场分离到细菌27属,1个养鸡场分离到8属,2个养鸭场分离到15属。
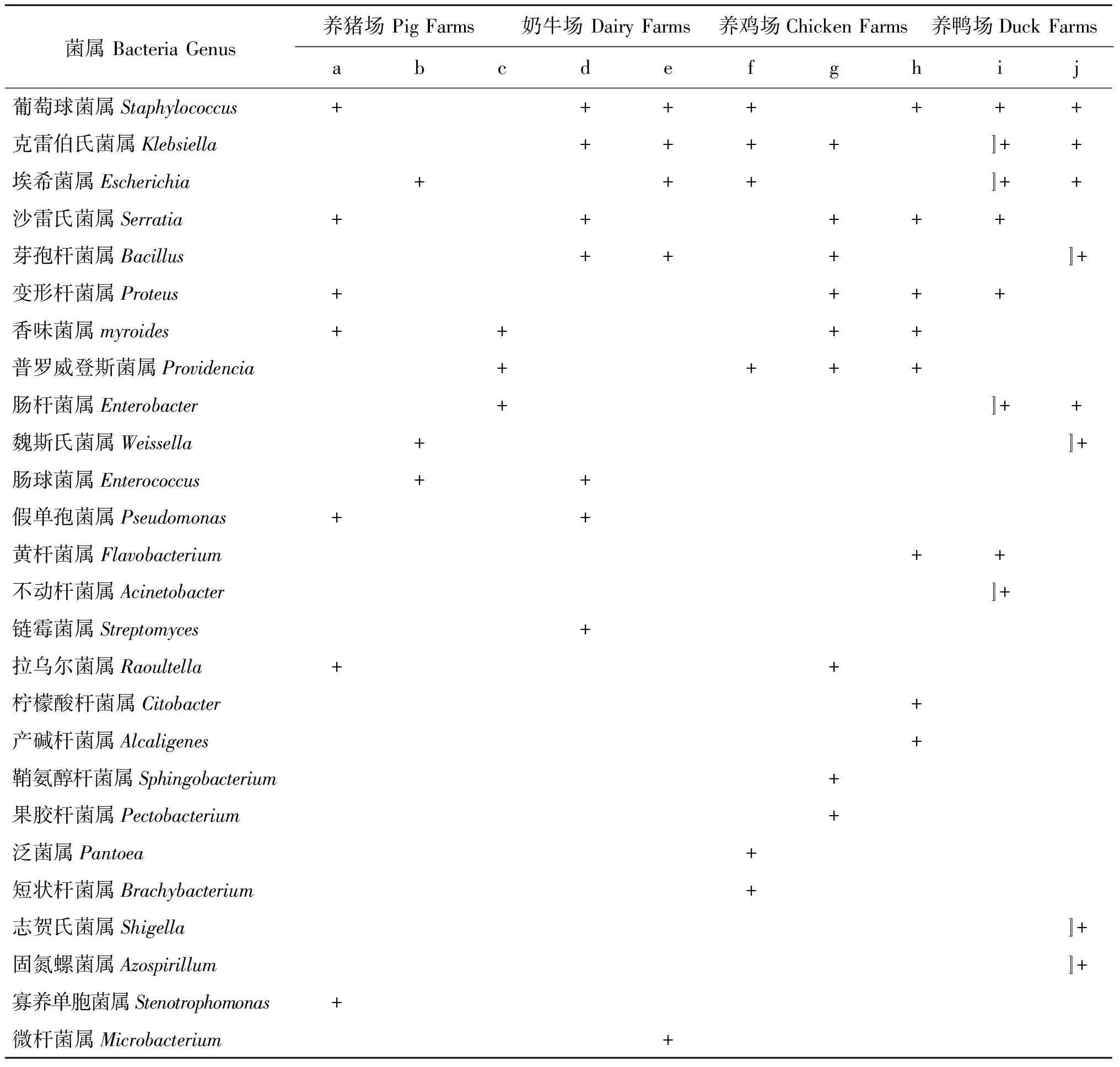
就分离到的细菌来说,葡萄球菌属、克雷伯氏菌属、埃希菌属、沙雷氏菌属为养殖场家蝇体表广泛存在细菌,在本研究的5-7个养殖场内的家蝇体表均分离到。芽孢杆菌属、变形杆菌属、香味菌属分布也比较广,在调查的4个养殖场内的家蝇体表分离到。而不动杆菌属、链霉菌属、拉乌尔菌属、柠檬酸杆菌属、产碱杆菌属、鞘氨醇杆菌属、果胶杆菌属、泛菌属、短状杆菌属、志贺氏菌属、固氮螺菌属、寡养单胞菌属和微杆菌属等13属细菌分布较窄,仅在1个养殖场蝇类体表分离到。其它细菌可在2-3个养殖场内的家蝇体表分离到(表1)。
在分离到的细菌中,革兰氏染色阴性菌有19属,占73%;革兰氏染色阳性细菌7属,占27%,分别为葡萄球菌属、芽孢杆菌属、魏斯氏菌属、肠球菌属、链霉菌属、短状杆菌属和微杆菌属。养殖场家蝇体表分离到的细菌中,多数为条件致病菌,对从业人员和周围人群存在一定的威胁。
2.4不同养殖场家蝇数量与其体表携带细菌数量和细菌属数的关系 养殖场家蝇数量与其体表携带细菌数量及细菌属数均成线性相关关系(图3)。说明养殖场管理水平越高,家蝇的密度越低,家蝇体表携带细菌的数量和种类越少,因此可以由养殖场孳生家蝇的数量反映出养殖场的整体管理水平。

图3 不同养殖场家蝇密度与家蝇体表分离到细菌数量(A)和菌属数(B)的相关性Fig.3 Correlations of Musca domestica adults’ population density with the isolated bacteria numbers (A) and the number of isolated bacteria genus (B)
表1 不同养殖场家蝇体表携带细菌种类
Tab.1 Genus of bacteria isolated from body surface of Musca domestica in different livestock farms
菌属BacteriaGenus养猪场PigFarms奶牛场DairyFarms养鸡场ChickenFarms养鸭场DuckFarmsabcdefghij葡萄球菌属Staphylococcus+++++++克雷伯氏菌属Klebsiella++++〛++埃希菌属Escherichia+++〛++沙雷氏菌属Serratia+++++芽孢杆菌属Bacillus+++〛+变形杆菌属Proteus++++香味菌属myroides++++普罗威登斯菌属Providencia++++肠杆菌属Enterobacter+〛++魏斯氏菌属Weissella+〛+肠球菌属Enterococcus++假单孢菌属Pseudomonas++黄杆菌属Flavobacterium++不动杆菌属Acinetobacter〛+链霉菌属Streptomyces+拉乌尔菌属Raoultella++柠檬酸杆菌属Citobacter+产碱杆菌属Alcaligenes+鞘氨醇杆菌属Sphingobacterium+果胶杆菌属Pectobacterium+泛菌属Pantoea+短状杆菌属Brachybacterium+志贺氏菌属Shigella〛+固氮螺菌属Azospirillum〛+寡养单胞菌属Stenotrophomonas+微杆菌属Microbacterium+
3 讨 论
家蝇是养殖场孳生的最常见蝇类,国内外对养殖场家蝇的研究,多集中于对蝇类的控制,而对不同养殖场家蝇体表携带病原体的研究尚少[11]。
由于家蝇主要孳生于养殖场的禽畜粪便、饲料残渣、动物尸体等养殖废弃物上。养殖场家蝇的密度受到废弃物处理状况的影响,在废弃物处理较好的养殖场内,家蝇的密度显著低于管理粗放的养殖场。如在本研究中鱼东村奶牛场和西孙村奶牛场为完全开放式养殖,养殖场内存在多个养殖户,养殖废弃物乱堆乱弃现象严重,家蝇密度较高;而在养殖规范程度较高的同和奶牛养殖合作社,养殖环境为封闭式,养殖废弃物严格日清,成年奶牛舍、犊牛舍、粮草仓、废弃物处理区等均进行严格隔离,且定期进行蝇类防治,家蝇密度则较低。在养猪场,家蝇的密度也受到养殖场管理水平的影响,在养殖粗放的朱康村养殖场,养殖环境较差,废弃物、污水较多,孳生的家蝇也较多;而在附近的高庄村养殖场,管理水平较高,废弃物处理较好,养猪场内比较整洁,因此家蝇孳生数量较少;在济南绿环托佩克种猪场,由于养殖数量较少,与周边存在树林等隔离带,且经常进行防治,因此家蝇的数量相对较低。在禽类养殖场,虽然均为封闭式养殖,但由于养殖废弃物处理不及时,饲料存在堆放现象,且产生粪便中的蛋白等营养物质含量相对丰富,更适合家蝇等蝇类的孳生。
本研究结果表明,养殖场家蝇的密度与其体表携带细菌数量和种类呈线性相关关系,因此养殖场家蝇的密度在一定程度上反映出养殖场的整体管理水平。养殖场内家蝇主要孳生于养殖废弃物(包括粪便、饲料残渣等),其中存在的大量细菌及其它病原体,家蝇在孳生过程中,粘附于体表,通过家蝇飞行携带到其它区域,造成病原体的传播。
家蝇体表携带的细菌多为机会性致病细菌,如Butler等[12]在野生家蝇体表分离到了鲍曼不动杆菌(Acinetobacterbaumanni)、蜡样芽孢杆菌(Bacilluscereus)、短小芽孢杆菌(Bacilluspumilus)、苏云金杆菌(Bacillusthuringiensis)、阪崎肠杆菌(Cronobactersakazakii)、大肠埃希菌(EscherichiacoliO157:H7)、甲基杆菌(Methylobacteriumpersicinum)、痢疾志贺菌(Shigelladysenteriae)、腐生葡萄球菌(Staphylococcussaprophyticus)和木糖葡萄球菌(Staphylococcusxylosus)等细菌。当蝇类得到有效控制的时候,腹泻病和志贺氏菌病发生率可下降42%和85%[13],儿童的腹泻比例可下降23%[14]。Shane[15]等研究表明,家蝇还可传播引起急性肠道传染病的空肠弯曲菌。在英国,空肠弯曲菌引起腹泻的发生与蝇类的密度密切相关,靠近养殖场或动物活动区居民感染弯曲杆菌的比例较高,而在卫生条件较好的城市,感染率则较低[11]。
本研究中,在养殖场家蝇体表分离到的细菌中存在条件致病菌,多数来自养殖废弃物,而通过家蝇传播有污染鲜牛奶、禽蛋等食品中的风险,影响食品安全。另外,养殖场的从业人员以妇女和老年人为主,在散户型养殖场内,养殖区与居住区的分隔不明显,因此,家蝇体表携带的条件致病菌传播给从业人员和居住区的老人、儿童的风险更高,需要引起足够的重视。在国家倡导健康养殖的主题下,养殖场内医学媒介生物的无害化控制也应作为重要课题,以减少养殖场内病原细菌通过蝇类在内部传播或扩散到周边,引起疾病的发生和流行。
[1] Tan SW, Yap KL, Lee HL. Mechanical transport of rotavirus by the legs and wings ofMuscadomestica(Diptera: Muscidae) [J]. J Med Entomol, 1997, 34(5): 527-531. DOI:10.1093/jmedent/34.5.527
[2] Greenberg B. Flies and disease: Vol. II[M]. Princeton: Princeton University Press, 1973.
[3] Bidawid SP, Edeson JF, Ibrahim J, et al. The role of non-biting flies in the transmission of enteric pathogens (Salmonellaspecies andShigellaspecies) in Beirut, Lebanon[J]. Ann Trop Med Parasitol, 1978, 72(2): 117-121.DOI:10.1080/0034983.1978.11719291
[4] Fotedar R, Banerjee U, Singh S, et al. The housefly (Muscadomestica) as a carrier of pathogenic microorganisms in a hospital environment [J]. J Hosp Infect, 1992, 20(3): 209-215.DOI:10.1016/0195-6701(84)90015-x
[5] Iwasa M, Makino S, Asakura H, et al. Detection ofEscherichiacoliO157:H7 fromMuscadomestica(Diptera: Muscidae) at a cattle farm in Japan [J]. J Med Entomol, 1999, 36(1): 108-112. DOI:10.1093/jmedent/36.1.108
[6] Kobayashi M, Sasaki T, Saito N, et al. Houseflies: not simple mechanical vectors of enterohemorrhagicEscherichiacoliO157:H7 [J]. Am J Trop Med Hyg, 1999, 61(4): 625-629.DOI:10.4269/ajtmh.1999.61.625
[7] Wales AD, Carrique-Mas JJ, Rankin M, et al. Review of the carriage of zoonotic bacteria by arthropods, with special reference to Salmonella in mites, flies and litter beetles [J]. Zoonoses Pub Health, 2010, 57(5): 299-314. DOI:10.1111/j.1863-2378.2008.01222.x
[8] Chen JM, Li YL, Gao SW, et al. Research to biological diversity and carries the pathogenic microorganisms of flies at Mawei Port[J]. J Inspect and Quarant, 2009, 19 (6): 21-27. (in Chinese)
陈佳木, 李亚伦, 高思维, 等. 马尾口岸蝇类生物多样性和携带病原微生物情况的研究[J]. 检验检疫学刊, 2009, 19(6): 21-27.
[9] Olsen AR. Regulatory action criteria for filth and other extraneous materials III. Review of flies and foodborne enteric disease [J]. Regul Toxicol Pharmacol, 1998, 28(3): 199-211.DOI:10.1006/rtph.1998.1271
[10] De Jesus AJ, Olsen AR, Bryce JR, et al. Quantitative contamination and transfer ofEscherichiacolifrom foods by houseflies,MuscadomesticaL. (Diptera: Muscidae) [J]. Int J Food Microbiol, 2004, 93(2): 259-262. DOI:10.1016/j.ijfoudmicro.2003.12.003
[11] Nichols GL. Fly transmission ofCampylobacter[J]. Emerg Infect Dis, 2005, 11(3): 361-364. DOI:10.3201/eid.1103.040460
[12] Butler JF, Garcia-Maruniak A, Meek F, et al. Wild Florida house flies (Muscadomestica) as carriers of pathogenic bacteria [J]. Florida Entomol, 2010, 93(2): 218-223. DOI:10.1653/024.093.0211
[13] Cohen D, Green M, Block C, et al. Reduction of transmission of shigellosis by control of houseflies (Muscadomestica) [J]. Lancet, 1991, 337(8748): 993-997.DOI:10.1016/0140-6736(91)92657-N
[14] Chavasse DC, Shier RP, Murphy OA, et al. Impact of fly control on childhood diarrhoea in Pakistan: community randomised trial [J]. Lancet, 1999, 353(9146): 22-25.DOI:10.1016/S0140-6736(98)03366-2
[15] Shane SM, Montrose MS, Harrington KS. Transmission ofCampylobacterjejuniby the house fly (Muscadomestica) [J]. Avian Dis, 1985, 29(2): 384-391.DOI:10.2307/1590499
BacteriaonbodysurfaceofMuscadomesticaadultsfromdifferentlivestockfarms
CHEN Dan1, ZHUANG Gui-fen1, HUANG Zhen-dong1, XUE Zhi-jing1, LIU Jing1, LI Yan1, ZHANG Rui-ling1,2, ZHANG Zhong1,2
(1.CollaborativeInnovationCenterfortheOriginandControlofEmergingInfectiousDiseases,TaishanMedicalUniversity,Tai’an271016,China; 2.DepartmentofPathogenicBiology,TaishanMedicalUniversity,Tai’an271016,China)
This study aims to isolate and identify the bacteria from the surface ofMuscadomesticaadults in different livestock farms. The adults ofMuscadomesticawere collected with sweep nets, then the surface of adult flies were washed with sterile water,and the eluted bacteria cultured with LB culture medium. The DNA of the bacteria isolated was extracted, 16SrDNA fragment was amplified through general PCR, and the 16SrDNA sequence was blasted with bacteria sequence in NCBI. Results showed that the number ofMuscadomesticaadults and the bacteria from their surface had significant different in different livestock farms. The population density ofMuscadomesticaadults had linear correlation with the number of bacteria fromMuscadomesticaadults and the number of bacteria genus. Among the bacteria isolated fromMuscadomesticaadults,Staphylococcus,Klebsiella,EscherichiaandSerratiawere the most common genus in the livestock farms. Most of the bacteria isolated from livestock farm house flies were opportunistic human bacterial pathogen, and the risk of bacterial pathogens spread to people was existed. The population density of house flies reflected the management level of different livestock farms. The house flies could mechanical transmit opportunistic human bacterial pathogen from livestock residue to human. So the house flies control and the monitoring of bacteria on body surface of house flies carried should be strengthened.
Muscadomestica; livestock farms; bacteria on the body surface of house flies; opportunistic bacteria; fly borne diseases
Zhang Zhong, Email: nasonia@163.com
10.3969/j.issn.1002-2694.2017.11.001
国家自然科学基金(Nos.81401693,81572028,81271874)和山东省科技发展计划项目(No.2014GSF121007)联合资助
张 忠,Email: nasonia@163.com
1.泰山医学院新发传染病溯源及防控协同创新中心,泰安 271016; 2.泰山医学院基础医学院,泰安 271016
R384
A
1002-2694(2017)11-0951-05
Supported by the National Natural Science Foundation of China (Nos. 81401693, 81572028 and 81271874), the Science and Technology Development Projects of Shandong Province (No. 2014GSF121007)
2016-09-08编辑王晓欢
