高效液相色谱-原子荧光光谱联用法测定牛肝菌中无机汞、甲基汞、乙基汞的不确定度评估
2017-12-11毛永杨李智高田金兰
毛永杨,杨 桐,苏 涛,李智高,田金兰
高效液相色谱-原子荧光光谱联用法测定牛肝菌中无机汞、甲基汞、乙基汞的不确定度评估
毛永杨1,杨 桐2,苏 涛1,李智高1,田金兰1
(1.大理州食品检验检测院,云南 大理 671000;2.大理市洱海保护管理局,云南 大理 671000)
采用高效液相色谱-原子荧光联用法测定牛肝菌中无机汞、甲基汞、乙基汞,通过建立评估的数学模型,分析不确定度的主要来源,计算出不确定度的各主要分量,得出合成不确定度和扩展不确定度。结果表明:影响结果不确定度的主要因素是浓度因素、仪器、样品不均匀性及回收率,其中浓度因素主要受标准曲线拟合的影响。该评估系统可为今后采用高效液相色谱-原子荧光联用法测定食用菌中无机汞、甲基汞、乙基汞的不确定度评估提供参考。
高效液相色谱-原子荧光联用法;汞形态;不确定度;牛肝菌
汞及其化合物广泛存在于自然界中,汞的毒性与其存在的形态密切相关,有机汞的毒性大于无机汞,在有机汞中甲基汞的毒性最大。无机汞在生物体烷基化的作用下可生成甲基汞、乙基汞等有害物质,汞及其化合物被动植物吸收后通过食物链的富集作用进入人体,其富集倍数可达106~107[1-3]。牛肝菌对土壤及生长环境中的汞具有较强的生物富集作用[4],因此分析牛肝菌中不同形态汞的含量对避免人体因食用含高毒性有机汞造成汞中毒具有重要的意义[5]。目前在新修订的食品安全国家标准GB 5009.17—2014《食品中总汞及有机汞的测定》[6]中增加了甲基汞的测定方法(高效液相色谱-原子荧光联用法),但标准中所规定的样品前处理方法主要是针对有甲基汞限值规定的鱼类产品且该方法未涉及乙基汞的测定方法,因此本研究有针对性的建立了适用于食用菌基质,且能同时测定无机汞、甲基汞、乙基汞含量的快速检测方法。由于该方法为非国家标准检测方法,为确保检测结果的准确性、可比性及符合测量结果的表达、质量评定、方法确认、量值溯源[7-8]等方面的要求,对该方法进行不确定度评估具有重要的应用价值。本实验依据JJF 1059.1—2012《测量不确定度评定与表示》[9]以及CNAS-GL06《化学分析中不确定度的评估指南》[10]规定的程序和方法,对高效液相色谱-原子荧光联用法测定牛肝菌中的无机汞、甲基汞、乙基汞的实验方法进行不确定度评估,分析不确定度的主要来源,找出影响检测结果的主要因素,为评估检测结果的科学性和检测结果的质量水平提供可靠的理论依据。
1 材料与方法
1.1 材料与试剂
牛肝菌 市售;乙腈、乙酸铵为色谱纯;氯化钾、硝酸、硼氢化钾、氢氧化钾、盐酸均为优级纯;其他试剂均为分析纯;无机汞(Hg2+)标准溶液(100 µg/mL±0.8%)、甲基汞(CH3Hg+)标准溶液(76.6 µg/g±2.9 µg/g)、乙基汞(C2H5Hg+)标准溶液(75.3 µg/g±2.8 µg/g) 国家标准物质中心。
1.2 仪器与设备
1260高效液相色谱仪 美国Agilent公司;9780原子荧光光谱 北京海光公司;Milli-Q超纯水处理系统(出水电阻率18.2 MΩ·cm) 美国Milli-pore公司;涡旋振荡器 美国Thermo公司;高速台式冷冻离心机 德国Eppendorf公司;AB-204s电子天平 瑞士Mettler Toledo公司。
1.3 方法
1.3.1 样品前处理
准确称取试样0.25 g(精确到0.000 1 g)于15 mL离心管中,加入3.0 mL的1.5% KCl-1.0%硫脲与盐酸的混合提取剂充分混合,置于2 500 r/min的涡旋混合器上振荡提取10 min,4 ℃、9 000 r/min离心10 min,取出上清液,再向离心管中加入3.0 mL混合提取剂重复提取1 次;合并2 次提取液,加入0.8 mL的氨水,用纯水定容至10 mL,用0.22 μm的滤膜过滤后分析测定,同时做空白对照。
1.3.2 标准溶液的配制
1.3.2.1 单标储备液的配制
分别准确称取甲基汞标准溶液130.55 mg、乙基汞标准溶液132.80 mg,用纯水定容至10 mL配制成质量浓度为1 000 µg/L的标准储备液;用20~200 µL移液器准确吸取100 µL的无机汞标准溶液,用纯水定容至10 mL配制成质量浓度为1 000 µg/L的无机汞标准储备液,4 ℃避光保存。
1.3.2.2 混合标准液的配制
分别用1 mL的单标线吸量管各吸取1 mL的无机汞、甲基汞、乙基汞的标准储备液于10 mL容量瓶中,用纯水定容至刻度,配制成质量浓度为100 µg/L的混合标准溶液;再分别使用100~1 000 µL移液器吸取混合标准溶液500 µL、1 mL的单标线吸量管吸取混合标准溶液1 mL、2 mL的单标线吸量管吸取混合标准溶液2 mL、500~5 000 µL的移液器吸取混合标准溶液4 000 μL、5 mL的单标线吸量管吸取混合标准溶液5 mL于不同的10 mL容量瓶中,用纯水定容至刻度,配制成质量浓度分别为5、10、20、40、50 µg/L的混合标准工作液。
1.3.3 仪器条件
1.3.3.1 高效液相色谱工作条件
色谱柱:C18反相色谱分离柱(250 mm×4.6 mm,5 μm);流动相:5.0%乙腈-0.46%乙酸铵-0.10% L-半胱氨酸;进样体积:100 µL;流速:1.0 mL/min。
1.3.3.2 原子荧光检测条件
载流:7% HCl溶液;氧化剂:1.0% K2S2O8+0.5% KOH;还原剂:2.0% KBH4+0.5% KOH;紫外消解仪:开;负高压:300 V;原子化器高度:10 mm;灯电流:30 mA;载气流量:400 mL/min;屏蔽气流量:900 mL/min;泵转速:80 r/min。
1.3.4 数学模型的确立与不确定度的分析
1.3.4.1 数学模型
根据测量的原理建立测量值的数学模型,进行不确定度来源的分析。本实验中汞形态分析的数学模型如下:
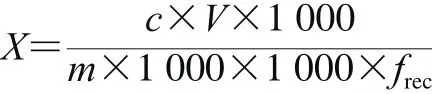
式中:X为试样中某组分的含量/(mg/kg);c为由标准曲线得到的试样中某组分的质量浓度/(μg/L);V为试样溶液的体积/mL;m为试样质量/g;frec为样品加标回收率/%。
1.3.4.2 不确定度分量的主要来源[11-17]
根据测量过程,该方法测定牛肝菌中无机汞、甲基汞、乙基汞不确定度的来源主要包括:标准品引入的不确定度、标准溶液的配制过程、标准工作曲线的拟合及样品前处理引入的不确定度等。
2 结果与分析
2.1 质量浓度引入的不确定度u(C)[18-21]
由质量浓度因素引入的标准不确定度,主要包括标准品浓度引入的不确定度、标准品称量和移取过程中引入的不确定度、标准溶液稀释过程中玻璃量器和移液器引入的不确定度、温度变动引入的不确定度、拟合标准曲线引入的不确定度。
2.1.1 标准品浓度引入的不确定度u1(C)
本实验所采用的标准品均购自国家标准物质中心,根据其所提供的标准物质证书,无机汞、甲基汞、乙基汞的扩展不确定度分别为:u(Cs(Hg2+))=±0.8%、u(Cs(CH3Hg+))=±2.9 µg/g、u(Cs(C2H5Hg+))=±2.8 µg/g;按B类评定取矩形分布,由标准品引入的相对不确定度分别为:
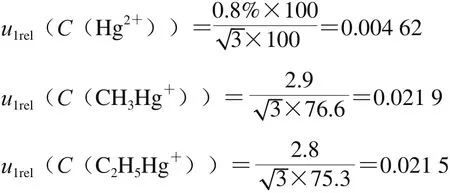
2.1.2 标准品称量和移取过程中引入的不确定度u2(m)
实验中分别称取甲基汞标准溶液130.55 mg、乙基汞标准溶液132.80 mg;用200 µL的移液器准确吸取100 µL的无机汞标准溶液;根据鉴定证书天平的最大允许误差为±0.05 mg,200 µL移液器的最大误差为±1.5%,按照矩形分布计算由称量标准品引入的相对不确定度分别为:
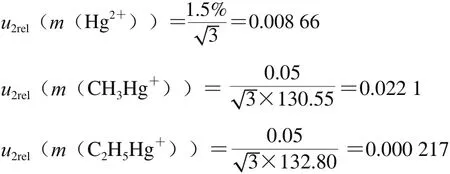
2.1.3 标准溶液稀释过程中玻璃量器和移液器引入的不确定度u3(V)
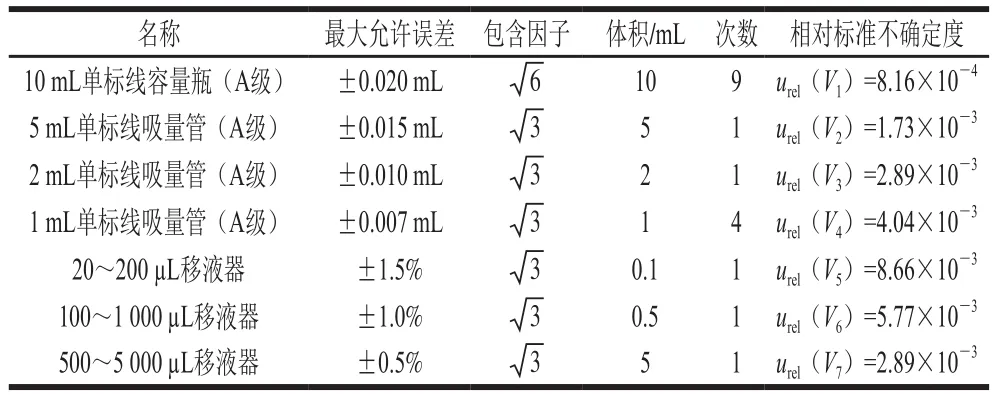
表1 标准溶液配制过程中玻璃量器和移液器引入的不确定度Table 1 Uncertainty resulting from the preparation of standard solution by volumetric flasks and pipettes
标准溶液的配制过程中所用的玻璃量器和移液器的最大允许误差,按照JJG 196—2006《常用玻璃量器检定规程》[22]和JJG 646—2006《移液器检定规程》[23]的要求确定。各玻璃量器和移液器的不确定度按B类不确定度评定,其中吸量管和移液器取矩形分布,容量瓶按三角分布计算[9],结果见表1。根据表1中的数据合成标准溶液稀释过程中玻璃量器与移液器引入的相对标准不确定度为:

2.1.4 标准溶液稀释过程中温度引入的不确定度u4(T)
标准溶液在稀释过程中的溶剂为纯水,各量具均在20 ℃的条件下进行检定,标准溶液配制室的温度控制在(20±5) ℃的范围内;由于玻璃量器的膨胀系数远小于液体的膨胀系数,可忽略不计,水在20 ℃的膨胀系数为2.1×10-4℃-1,取温度变化为均匀分布,据此计算的温度变化引入的不确定度见表2。
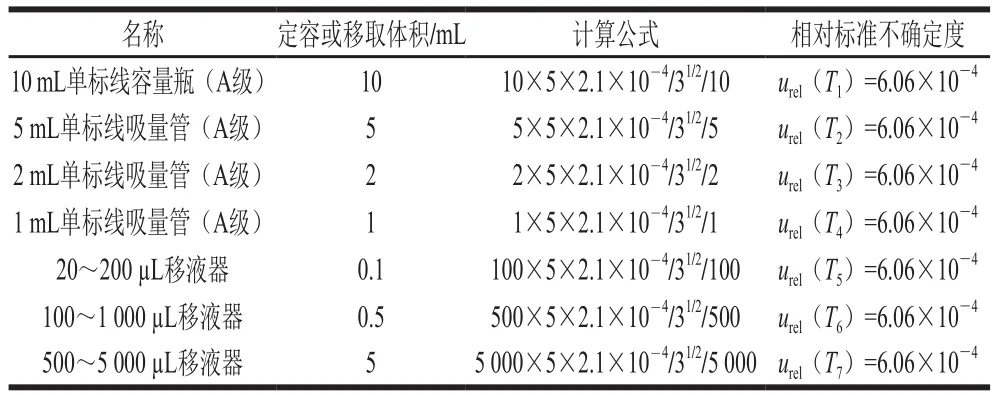
表2 标准溶液配制过程中温度变化引入的不确定度Table 2 Uncertainty resulting from the preparation of standard solution by temperature variation
根据表2中的数据标准溶液在配制过程中由温度变化引入的相对标准不确定度为:
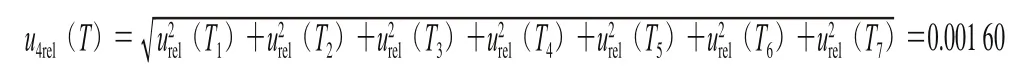
2.1.5 最小二乘法拟合标准曲线的不确定度u5(Cʹ)
通过对质量浓度分别为5、10、20、40、50 µg/L的无机汞、甲基汞、乙基汞的混合标准工作液进行测定,每个校准点测定2 次,采用最小二乘法拟合标准溶液的质量浓度与峰面积曲线,各数据结果详见表3;同时对一组阳性样品在拟合标准曲线的状态下进行两次重复测定,根据如下公式对标准曲线拟合引入的不确定度进行计算:
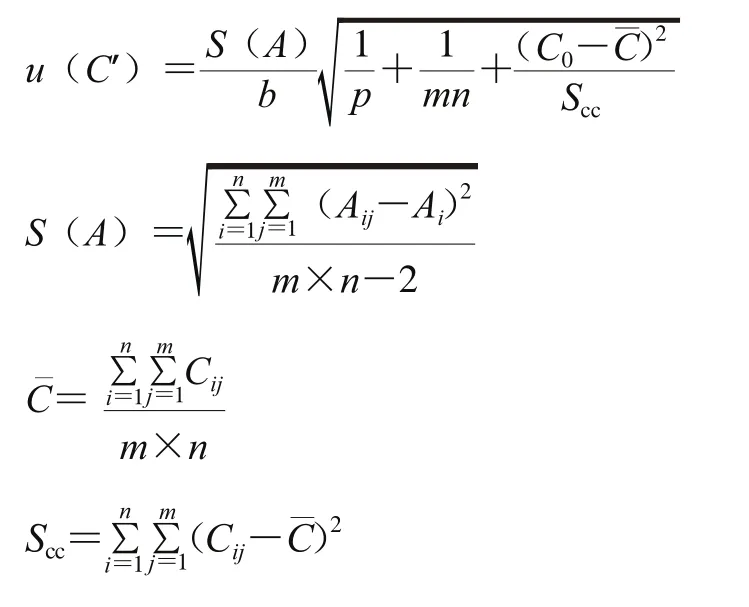
式中:b为校准曲线斜率;C0为阳性样品测定质量浓度的平均值;p为测试样品的次数;m为标准工作液的测定次数;n为标准溶液校准点的总数;为标准溶液各校准点Cij的质量浓度平均值;Aij为各质量浓度点测定的峰面积;Ai为由校准方程计算得到的各质量浓度点的峰面积;Cij为标准溶液各校准点的浓度。对阳性样品进行2次测定,其含量分别为:C0(Hg2+)=21.64 µg/L、C0(CH3Hg+)=10.12 µg/L、C0(C2H5Hg+)=15.17 µg/L。根据表3中的数据计算得到:Scc=3 000;由以上数据计算出标准曲线拟合的相对不确定度分别为:
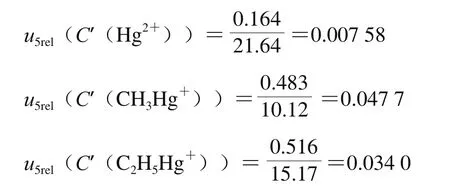
在样品的测定过程中由浓度引入的相对合成不确定度按如下公式计算:
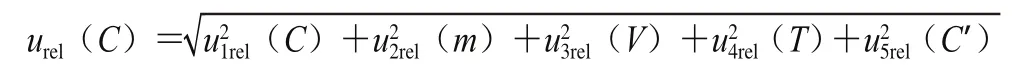
分别计算出urel(C(Hg2+))= 0.017 3;urel(C(CH3Hg+))=0.053 9;urel(C(C2H5Hg+))=0.042 0。

表3 校准曲线拟合数据及不确定度Table 3 Data for fitting calibration curve and uncertainty
2.2 样品前处理引入的不确定度[24-29]
2.2.1 试样质量称量引入的不确定度u(W)
在实验中称取0.25 g(精确到0.000 1 g)的试样,根据鉴定证书天平最大允许误差为±0.05 mg,按B类评定取矩形分布,由试样称量引入的相对不确定度为:
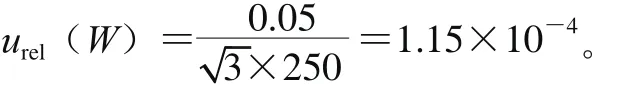
2.2.2 试样定容引入的不确定度u(Vʹ)
试样处理完成后采用10 mL的容量瓶进行定容,温度变化范围为(20±5)℃,其中10 mL A级单标线容量瓶的最大允许误差为±0.020 mL,由容量瓶和温度变化引入的不确定度分别如下:
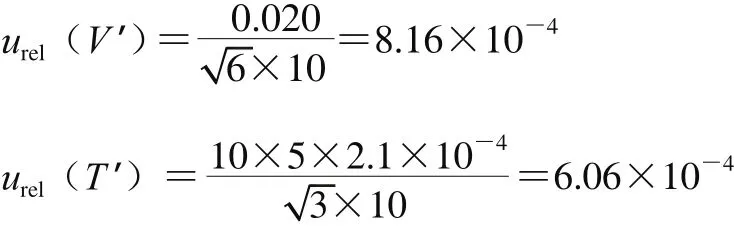
由试样定容过程引入的相对标准不确定度为:
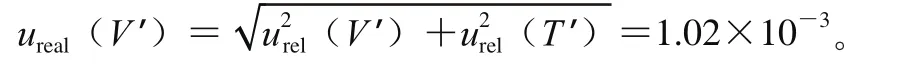
2.2.3 由样品不均匀性引入的不确定度u(f)
由于处于不同生长时期和处于同一生长时期的牛肝菌中不同组织部位对无机汞、甲基汞和乙基汞的富集作用及烷基化的能力差异较大[5],因此在不确定度评定中应包含由样品非均匀引入的不确定度分量。在本实验中通过充分混匀样品、加大样品的制样量,经过科学的取样和缩分及平行实验来保障试样的均匀性和检测结果的代表性。实验对同一阳性样品进行了7 组独立试样的平行实验结果见表4,同时按A类评定对其不确定度进行计算,计算公式如下:

根据此公式分别计算得到由样品非均匀性引入的相对标准不确定度为:urel(f(Hg2+))=0.016 7;urel(f(CH3Hg+))=0.029 3;urel(f(C2H5Hg+))=0.018 4。
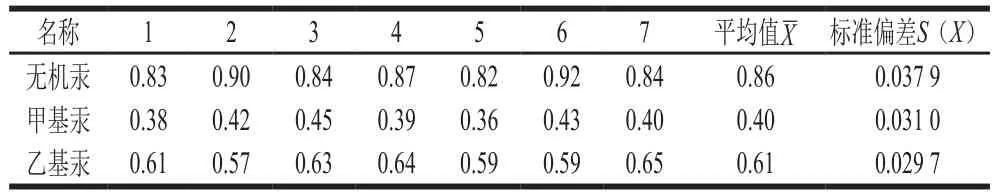
表4 样品中无机汞、甲基汞、乙基汞的测定结果Table 4 Determination results of inorganic mercury, methyl mercury and ethyl mercury in the samplemg/kg
2.2.4 提取效率引入的不确定度
在空白试样中添加7 组不同的混合标准溶液,考察回收率对不确定度的影响,按A类进行评定,由回收率引入的相对不确定度根据如下公式计算:;同时对回收率进行显著性检验,计算公式为:,结果见表5;查t检验临界值分布表(f = n-1=6)得双侧临界值t(0.05,6)为2.447。在本实验中t值均大于t(0.05,6),故实验中所得到的回收率与100%具有显著差异,因此必须在计算结果的公式中采用回收率因子R对结果进行修正。
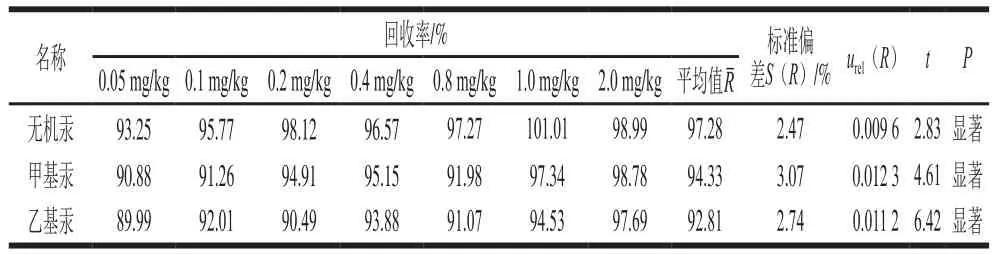
表5 无机汞、甲基汞、乙基汞的回收率和不确定度Table 5 Recoveries and uncertainties of inorganic mercury, methyl mercury and ethyl mercury
在样品前处理过程中各分量引入的相对标准不确定度按如下公式计算:
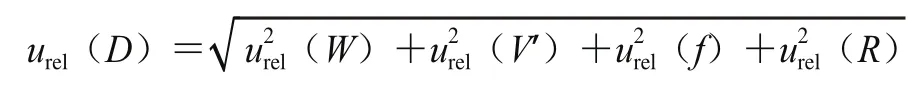
根据此公式分别计算得到由样品前处理过程中引入的相对标准不确定度为:urel(D(Hg2+))=0.019 3;urel(D(CH3Hg+))=0.031 8;urel(D(C2H5Hg+))=0.021 6。
2.3 高效液相色谱-原子荧光分析系统引入的不确定度u(E)
根据检定证书高效液相色谱-原子荧光分析系统的扩展不确定度u=5%,k=2,因此由分析仪器引入的不确定度为:
2.4 合成不确定度及扩展不确定度
2.4.1 合成标准不确定度
各不确定分量相互独立,相对合成标准不确定度计算公式为:
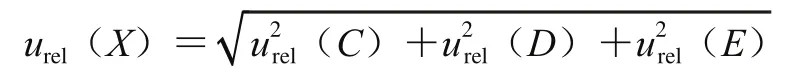
由此公式分别计算得到无机汞、甲基汞、乙基汞的相对合成标准不确定度为:urel((Hg2+))=0.036 0;urel(X(CH3Hg+))=0.067 4;urel(X(C2H5Hg+))=0.053 4;根据合成标准不确定度的计算公式uC(X)=urel(X)×,其中为表4中阳性样品经测定后按1.3.4.1节中的公式计算结果的平均值,分别计算得到无机汞、甲基汞、乙基汞的合成标准不确定度为:uC((Hg2+))=0.031 8;uC(X(CH3Hg+))=0.028 6;uC(X(C2H5Hg+))=0.035 1。
2.4.2 扩展不确定度
依据JJF 1135—2005《化学分析测量不确定度评定》[30],在95%的置信水平下,取包含因子k=2,扩展不确定度U=k×uC(X),据此得到的高效液相色谱-原子荧光联用法测定牛肝菌中的无机汞、甲基汞、乙基汞含量的结果见表6。

表6 不确定度评定结果Table 6 Uncertainty evaluation for the determination of inorganic mercury, methyl mercury and ethyl mercury
3 结 论
通过对牛肝菌中无机汞、甲基汞、乙基汞的测定过程中各分量因素引入的不确定度进行评定,结果表明:在无机汞的测定过程中对不确定度贡献最大的因素依次为仪器、浓度因素、样品不均匀性和样品提取效率,其中在浓度因素中主要受到标准曲线的拟合及体积因素的影响。在甲基汞和乙基汞的测定过程中不确定度的主要来源为:浓度因素、仪器、样品不均匀性以及样品提取效率引入的不确定度;其中在浓度因素中主要受到标准曲线的拟合及标准品纯度的影响。因此,在今后的实际检测过程中,通过保持仪器较高的灵敏度并按时进行检定、选择高纯度的标准品、科学制样与缩分、选择高精密度的量器、提高检验人员的熟练水平和操作的规范性等方法减小测量数据的不确定度,保障检测结果的准确性从而提高检测质量。
[1] ULLRICH S M, TANTON T W, ABDRASHITOVA S W. Mercury in the aquatic environment∶ a review of factors affecting methylation[J].Critical Reviews in Environmental Science and Technology, 2001,1(3)∶ 241-293. DOI∶10.1080/20016491089226.
[2] 陈邵鹏, 顾海东, 秦宏兵. 高效液相色谱-氢化物发生-原子荧光光谱联用技术测定水中的烷基汞[J]. 中国环境监测, 2012, 28(5): 79-82.
[3] BENDER M, LYMBERIDI-STTIMO E, RD G. New mercury treaty exposes health risks[J]. Journal of Public Health Policy, 2014, 35(1):1-13. DOI:10.1057/jphp.2013.39.
[4] 杨天伟, 张霁, FALANDYSZ J, 等. 云南常见牛肝菌属真菌中汞含量及食用安全评价[J]. 生态学杂志, 2015, 34(12): 3518-3525.DOI:10.13292/j.1000-4890.2015.0330.
[5] 毛永杨, 舒平, 赵浩军, 等. 高效液相色谱-原子荧光联用测定食用菌中无机汞、甲基汞、乙基汞[J]. 云南大学学报(自然科学版), 2016,38(3): 471-476. DOI:10.7540/j.ynu.20150697.
[6] 国家卫生和计划生育委员会. 食品中总汞及有机汞的测定: GB 5009.17—2014[S]. 北京: 中国标准出版社, 2014.
[7] 冯歆轶, 芦智远, 吴正昌, 等. ICP-AES法测定复合蛋白饮料中钠含量的不确定度评定[J]. 粮食与食品工业, 2015, 22(1): 93-96.DOI:10.3969/j.issn.1672-5026.2015.01.027.
[8] 霍晓敏. 气相色谱法对干海参中的六六六滴滴涕测量结果不确定度的评定[J]. 食品科学, 2013, 34(8): 224-248. DOI:10.7506/spkx1002-6630-201308053.
[9] 国家质量监督检验检疫总局. 测量不确定度评定与表示: JJF 1059.1—2012[S]. 北京: 中国计量出版社, 2012.
[10] 中国合格评定国家认可委员会. 化学分析中不确定度的评估指南:CNAS-GL06:2006[S]. 北京: 中国标准出版社, 2006.
[11] 王静, 顾文龙, 端礼钦. 禽肉中总汞测定的不确定度评定[J].安徽农业科学, 2015, 43(32): 186-187. DOI:10.3969/j.issn.0517-6611.2015.32.063.
[12] 兴丽, 王梅, 赵凤敏, 等. ICP-MS两种模式下测定亚麻籽中微量元素及其不确定度评定[J]. 光谱学与光谱分析, 2014, 34(1): 226-230.DOI:10.3964/j.issn.1000-0593(2014)01-0226-05.
[13] 张建辉, 张继红, 张丽, 等. ICP-MS法和石墨炉原子吸收法测定大米中镉含量不确定度评估的比较[J]. 食品科学, 2016, 37(18): 185-188.DOI:10.7506/spkx1002-6630-201618030.
[14] 孙玲玲, 宋金明, 于颖, 等. 微波消解-电感耦合等离子体发射光谱法测定牡蛎中锌的不确定度评定[J]. 食品科学, 2016, 37(16): 187-192.DOI:10.7506/spkx1002-6630-201616030.
[15] BANERJEE K, OULKAR D P, DASGUPTA S, et al. Validation and uncertainty analysis of a multi-residue method for pesticides in grapes using ethyl acetate extraction and liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A, 2007, 1173(2): 98-109.DOI:10.1016/j.chroma.2007.10.013.
[16] HASEGAWA H, SHINOHARA Y, HASHIMOTO T, et al. Prediction of measurement uncertainty in isotope dilution gas chromatography/mass spectrometry[J]. Journal of Chromatography A, 2006, 11363(2):226-230. DOI:10.1016/j.chroma.2006.09.073.
[17] 赵一霖, 李姗, 何霜, 等. 电感耦合等离子体质谱法测定水产品中16 种元素的不确定度评定[J]. 食品安全质量检测学报, 2016, 7(10):4156-4162.
[18] 许光, 杨波, 李爱李, 等. ICP-AES测定大豆中锰、铁、锌含量的不确定度评价[J]. 食品研究与开发, 2013, 34(9): 69-72. DOI:10.3969/j.issn.1005-6521.2013.09.019.
[19] 高端峰, 高孟朝, 凌睿, 等. ICP-MS测定淀粉铝含量的不确定度评定及改进方法[J]. 光谱学与光谱分析, 2016, 36(4): 1211-1216.DOI:10.3964/j.issn.1000-0593(2016)04-1211-06.
[20] 陆美斌, 李为喜, 李静梅, 等. 电感耦合等离子体质谱法测定谷物中砷和镉的不确定度评定[J]. 中国食品学报, 2014, 14(5): 180-185.
[21] 徐幸, 张晓鸣, 舒平, 等. 超高效液相色谱-稳定性同位素稀释质谱法测定米线中乌洛托品的不确定度评估[J]. 食品科学, 2015, 36(16):246-250. DOI:10.7506/spkx1002-6630-201516047.
[22] 国家质量监督检验检疫总局. 常用玻璃量器检定规程: JJG 196—2006[S]. 北京: 中国计量出版社, 2006.
[23] 国家质量监督检验检疫总局. 移液器检定规程: JJG 646—2006[S].北京: 中国计量出版社, 2006.
[24] WALORCZYK S. Validation and use of a QuEChRS-based gas chromatography-tandem mass spectrometric method for multiresidue pesticide analysis in blackcurrants including studies of matrix effects and estimation of measurement uncertainty[J]. Talanta, 2014, 120:106-113. DOI:10.1016/j.talanta.2013.11.087.
[25] JIMÉNEZ J J. Determination of aminopolycarboxylic acids in river water by solid-phase extraction on activated charcoal cartridges and gas chromatography with mass spectrometric detection. Method performance characteristics and estimation of the uncertainty[J].Analytica Chimica Acta, 2013, 770: 94-102. DOI:10.1016/j.aca.2013.01.060.
[26] 杨波, 段凤敏, 保志娟, 等. 微波消解-原子荧光光谱法测定烟草中汞的不确定度分析[J]. 计量与测试技术, 2016, 43(3): 90-92.DOI:10.15988/j.cnki.1004-6941.2016.03.042.
[27] 樊继鹏, 汪洋, 魏晓培, 等. ICP-MS法测定饮用水中铅砷镉的不确定度评定的研究[J]. 包装与食品机械, 2016, 34(3): 70-72.DOI:10.3969/j.issn.1005-1295.2016.03.016.
[28] 杜德贤, 林晓君. ICP-MS法测定白酒中铅及其不确定度[J]. 食品与发酵科技, 2016, 52(3): 77-80. DOI:10.3969/j.issn.1674-506X.2016.03-018.
[29] 舒平, 杨卫花, 徐幸. 气相色谱法-三重四级杆质谱联用法测定核桃油中酚类抗氧化剂的不确定度评估[J]. 食品科学, 2016, 37(6): 194-198. DOI:10.7506/spkx1002-6630-201606035.
[30] 国家质量监督检验检疫总局. 化学分析测量不确定度评定: JJF 1135—2005[S]. 北京: 中国计量出版社, 2005.
Uncertainty Evaluation of for Determining Inorganic Mercury, Methyl Mercury and Ethyl Mercury in Boletus by High Performance Liquid Chromatography Combined with Atomic Fluorescence Spectrometry
MAO Yongyang1, YANG Tong2, SU Tao1, LI Zhigao1, TIAN Jinlan1
(1. Food Inspection and Testing Institute of Dali, Dali 671000, China;2. Erhai Lake Conservation and Management Bureau of Dali, Dali 671000, China)
In this study, we identified the main sources of uncertainty by mathematical modeling and calculated the main uncertainty components and combined and expanded uncertainties for the determination of inorganic mercury, methyl mercury and ethyl mercury in Boletus by high performance liquid chromatography combined with atomic fluorescence spectrometry (HPLC-AFS). The results showed that the major factors of uncertainty were concentration, instrumental measurement, sample heterogeneity, and recovery. Moreover, the curve fitting was the major factor causing the uncertainty for concentration. This study may provide a guideline for uncertainty evaluation for determining inorganic mercury, methyl mercury and ethyl mercury in edible fungus by HPLC-AFS.
high performance liquid chromatography combined with atomic fluorescence spectrometry; mercury specie;uncertainty; Boletus
DOI∶10.7506/spkx1002-6630-201724044
O657.3
A
1002-6630(2017)24-0272-06
毛永杨, 杨桐, 苏涛, 等. 高效液相色谱-原子荧光光谱联用法测定牛肝菌中无机汞、甲基汞、乙基汞的不确定度评估[J].食品科学, 2017, 38(24): 272-277.
10.7506/spkx1002-6630-201724044. http://www.spkx.net.cn
MAO Yongyang, YANG Tong, SU Tao, et al. Uncertainty evaluation of for determining inorganic mercury, methyl mercury and ethyl mercury in Boletus by high performance liquid chromatography combined with atomic fluorescence spectrometry[J]. Food Science, 2017, 38(24)∶ 272-277. (in Chinese with English abstract) DOI∶10.7506/spkx1002-6630-201724044. http∶//www.spkx.net.cn
2016-12-08
云南省卫生厅科研项目(云卫[2014]DB005)
毛永杨(1985—),男,助理工程师,硕士,研究方向为食品安全质量检测。E-mail:maoyongyang@163.com
