普鲁士蓝及其衍生物中的钴、铁对其作为锂离子电池正极时比容量的影响
2017-11-24王二东王素力孙公权
姜 巍,王二东,孙 海,王素力,孙公权
普鲁士蓝及其衍生物中的钴、铁对其作为锂离子电池正极时比容量的影响
姜 巍1,2,王二东1,孙 海1,王素力1,孙公权1
(1中国科学院大连化学物理研究所,辽宁大连 116023;2中国科学院大学,北京 100039)
普鲁士蓝及其衍生物(以下简称PBAs)凭借其简单的制备工艺、优良的倍率性能、低廉的成本等优势成为一种具有潜力的碱金属离子和碱土金属离子电池正极材料。通过合成含有钴、铁的PBAs,借助X射线粉末衍射技术(XRD)、扫描电子显微技术(SEM)和电化学技术等表征测试手段获得其晶体结构、形貌和电化学行为,研究处于不同结构中的铁和钴之间相互影响的规律。结果表明,在“M1—N≡≡C—M2”结构中,通过改变不同过渡金属元素M2可对过渡金属元素M1的电化学活性有着显著影响。
普鲁士蓝;正极材料;锂离子电池
锂离子电池作为一种高效、清洁的电化学储能技术,在便携设备、电动汽车、规模储能等诸多领域得到了广泛的应用。然而现有锂离子电池的比能量、循环寿命和安全性等仍亟待进一步改进,以满足未来的应用需求。开发新型的正极材料成为其中的一条技术路线。PBAs因为其具有更加开放的金属有机骨架结构、低廉的成本和简单的制备工艺而作为锂离子电池[1-7]、钠离子电池[3, 6, 8-12]以及碱土金属离子电池[13-15]正极材料的选项之一而被关注。
在PBAs正极研究中,OKUBO等[1]探索并指出AMnFe(CN)6(A= K、Rb)不同条件下Fe-CN-Mn电子的离域和互变异构现象对锂离子可逆嵌入与迁出起到稳定作用;CUI等[14]利用共沉淀法制备KNiFe(CN)6和KCuFe(CN)6并考察了不同碱土金属离子的水溶液中,10 C(C=60 mA·h/g)倍率下获得60%以上的容量保持率;GOODENOUGH等[10]对一系列KMFe(CN)6(M为过渡金属)在钠离子电池体系中的应用进行研究,并利用晶体场理论对电荷转移机理进行了解释。
尽管研究者们对PBAs在不同电池体系中进行了广泛的研究,并且对PBAs发生电化学变化时过渡金属电子结构变化做出解释和探讨。但是,在以往的研究工作中却未考虑M1-CN-M2结构中M1和M2之间的相互影响所带来的正极材料比容量的变化。以KFeIIFeIII(CN)6(FeFePBA)、KCoIIFeIII(CN)6(CoFePBA)和KFeIICoIII(CN)6(FeCoPBA)为研究对象,利用物相、形貌表征、电化学分析和电池测试技术,探索和讨论PBAs中两种不同结构的金属在电化学行为中所起的作用以及对正极材料比容量的影响。
1 实 验
1.1 FeFePBA、CoFePBA和FeCoPBA的合成
FeFePBA的合成:利用还原-沉淀法[3]首先将10 mmol K3Fe(CN)6固体溶解于150 mL、0.1 mol/L的盐酸溶液中。在快速磁力搅拌作用下,80 ℃恒温回馏12 h。将墨绿色悬浊液进行减压过滤,并用4倍于悬浊液体积的去离子水清洗滤饼至滤液透明 且呈中性后,将滤饼转移至真空干燥箱并在80 ℃下真空干燥6 h以上,得到深绿色FeFePBA固体粉末。
CoFePBA和FeCoPBA的合成:利用共沉淀法[14]将3 mmol CoCl2·6H2O和1.5 mmol K3Fe(CN)6固体分别溶解于60 mL去离子水中,利用恒流泵将两种溶液以相同速率(约20 mL/h)加入到80 ℃快速磁力搅拌的30 mL去离子水中。进料完毕后,继续恒温搅拌至12 h。将悬浊液减压过滤后,用4倍于悬浊液体积的去离子水清洗滤饼,之后转移至真空干燥箱中,在80 ℃下真空干燥6 h,得到棕红色CoFePBA固体粉末。以上述相同方法利用FeCl2·4H2O和K3Co(CN)6合成得到土黄色FeCoPBA固体粉末。
1.2 材料表征
材料的物相表征是利用日本理学Miniflex600型X射线粉末衍射仪,在2为6°~90°间以5°/min扫描并收集数据。采用日本电子株式会社JSM- 7800F场发射扫描电子显微镜研究材料微观形貌。
1.3 电化学表征及电池充放电测试
将PBAs、super P导电碳和10%(质量分数) PVDF/NMP(-甲基吡咯烷酮)按照质量比8∶1∶1混合,滴加适量NMP后搅拌6 h,刮涂到铝箔上,120 ℃真空干燥10 h以上,裁剪成所需要的形状和尺寸作为正极(循环伏安测试中作为工作电极);锂片作为负极(循环伏安测试中作为辅助电极和参比电极);LiF6/DC-DEC-DMC(1∶1∶1)作为电解质溶液;陶瓷膜作为隔膜组装成CR2032纽扣电池。循环伏安测试使用上海辰华CHI760E电化学工作站,扫描电势范围为2.0~4.2 V,扫描速率为0.5 mV/s;充放电测试使用武汉蓝电CT2001A电池充放电测试系统,电压为2.0~4.2 V,恒电流充放电的电流大小为25 mA/g。
2 结果与讨论
2.1 材料的晶体结构
图1为FeFePBA、CoFePBA和FeCoPBA的XRD图。由XRD数据中(200)晶面对应的衍射峰位置的2值,借助布拉格方程计算进而得到立方晶系的PBA晶胞参数,对应如表1中的数据。
根据图1可知,FeFePBA、CoFePBA和FeCoPBA中的原子排布均属于立方晶系,三者虽然组成不同,合成方法有所差异,但晶体结构相同。根据表1中的计算结果知,3种PBAs晶体结构中最小立方体的棱长,即(200)晶面间距为10.25~10.35Å(1Å=1´10-10m),再考虑到PBAs骨架中离子或原子半径(表2),经过计算,可供锂离子通过的通道的边长不小于12.93Å,远大于锂离子的离子半径0.68Å[16],因此锂离子可以较容易地在这3种材料中进行嵌入/迁出,并且在材料中能够以较大的扩散速率迁移。
2.2 材料形貌
图2为FeFePBA、CoFePBA和FeCoPBA 的SEM照片。图2(a)和图2(c)表明FeFePBA颗粒主要呈均匀的立方体形状,尺寸分布较均匀(立方体颗粒的棱长集中于500 nm左右);图2(b)和图2(d)表明CoFePBA颗粒虽然主要呈立方体形状,但尺寸分布较不均匀(立方体颗粒棱长从100 nm到500 nm不等);图2(c)和图2(f)表明FeCoPBA主要形成“堆砌碎片”状的颗粒,可以观察到少量的立方体形状的棱角,高倍下观察也可看到立方结构形貌,不过目前在一些研究工作中看到可以通过在合成时添加一定量的聚乙烯吡咯烷酮(PVP)来制备具有类似图2(a)~2(e)形貌特征的FeCoPBA[18-19]。
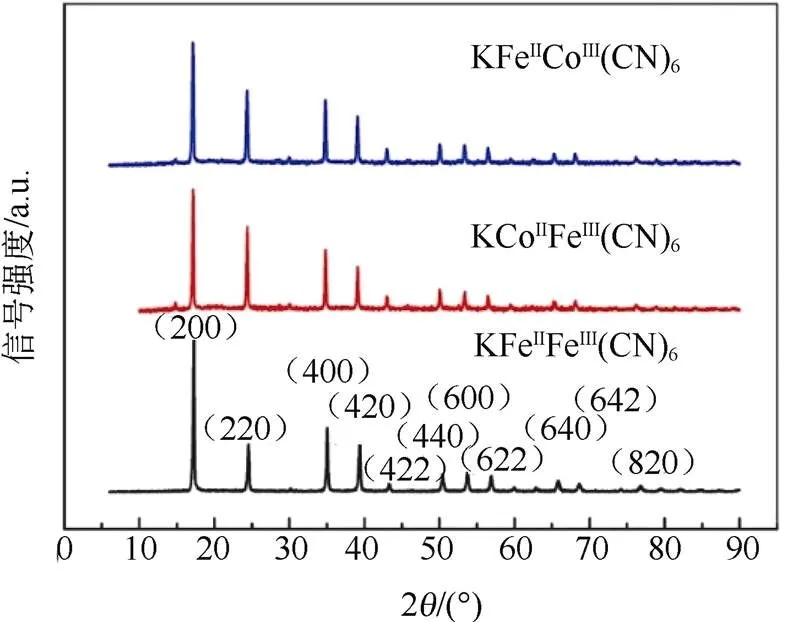
图1 FeFePBA、CoFePBA和FeCoPBA XRD图

表1 FeFePBA、CoFePBA和FeCoPBA (200)晶面2θ值和晶胞参数
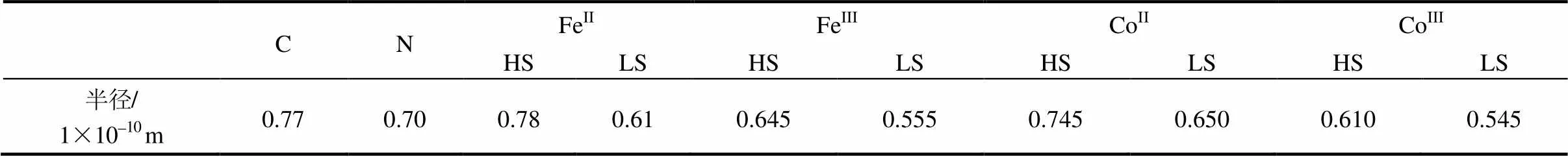
表2 不同元素的原子半径和离子半径[17]
图2(d)中还可以观察到由正八面体到立方体过渡的颗粒,而图2(a)和图2(d)仅出现立方体互相融合的颗粒,从而间接表明了FeFePBA生长机理可能为初次成核后,更倾向于小颗粒聚集并融合成大颗粒生长,而CoFePBA在初次成核后难以通过聚集再融合的途径,而是继续由小颗粒独立缓慢生长成大颗粒。

(a)FeFePBA (b)CoFePBA (c)FeCoPBA(d)FeFePBA (e)CoFePBA (f)FeCoPBA
图2 FeFePBA、CoFePBA和FeCoPBA的SEM照片
Fig.2 SEM images of FeFePBA、CoFePBA and FeCoPBA
2.3 电化学表征和充放电测试



图4(c)中并未出现任何显著的充放电平台,恰好与循环伏安曲线吻合。
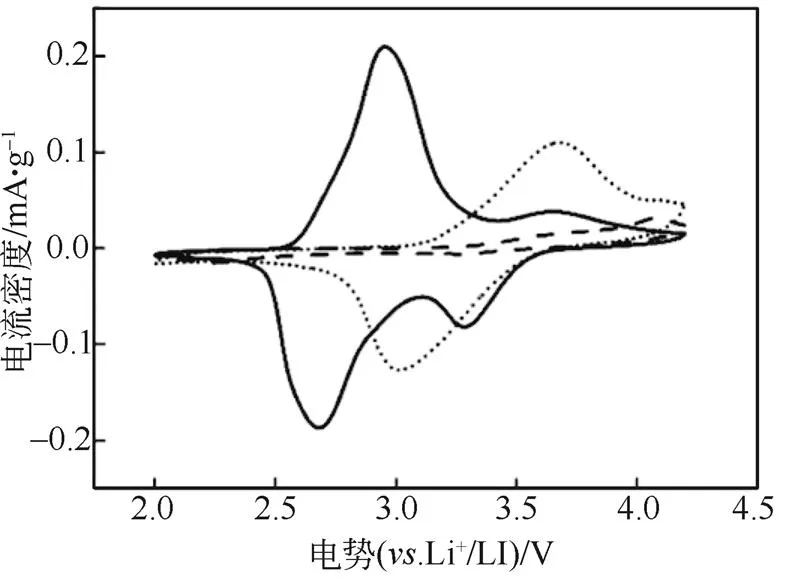
图3 FeFePBA(—)、CoFePBA(…)和FeCoPBA (- - -)循环伏安曲线

再次结合循环伏安曲线和充放电测试曲线可知,FeFePBA中的N-FeII和C-FeIII均能够在锂离子电池正极的工作电压范围内发生一定程度上可逆的氧化还原反应,从而自身拥有相对较高的比容量(约120 mA·h/g);然而CoFePBA与FeFePBA相比,仅将N-FeII换作N-CoII,而N-CoII并不能在锂离子电池正极工作电压下通过自身发生氧化还原反应贡献电极容量,导致其相较于CoFePBA在比容量上低了近90 mA·h/g,但就结果而言C-FeIII仍然能够一定程度上不受影响,保有自身所能贡献的约30 mA·h/g的比容量;最后FeCoPBA与FeFePBA相比,仅将C-FeIII换作C-CoIII,不但C-CoIII不能在上述条件下贡献容量,N-FeII结构同样也失去了贡献容量的能力。
表3为FeFePBA、CoFePBA、FeCoPBA与LiFePO4四种材料的理论能量密度对比。计算中我们假定所有在实验中观察到可变价金属均发生电氧化还原反应,同时假定材料的化学组成均严格与其分子式对应,FeFePBA、CoFePBA和FeCoPBA的理论电压是根据图3中测试得到的电氧化还原峰的电势值取平均值获得,LiFePO4的理论电压则由文献中查得。从表中数据对比中可以看出,FeFePBA材料的理论能量密度最高,并接近LiFePO4材料的理论能量密度,二者仅相差30.98 W·h/kg,若能在今后的研究工作中获得接近其理论能量密度的结果,则其将是一种具有潜力的替代LiFePO4的正极材料。

表3 FeFePBA、CoFePBA、FeCoPBA和LiFePO4的理论能量密度
表4列出了FeFePBA、CoFePBA和FeCoPBA三种材料比容量和能量密度与文献值相对比的情况。可以看出本工作与文献中同一种材料的性能仍有一定的差距,但考虑到本工作的PBAs材料本身由于化学组成、缺陷和形貌等与文献中有所不同,对电化学以及电池性能会造成不同程度的影响,进而造成比容量以及能量密度有所差别。至于化学组成、缺陷以及形貌等因素如何影响性能,可在以后的工作中深入细致探讨。但同时我们可以看出,即便是文献值,也与本工作所得结果规律相一致,这也进一步支持了我们的观点。

表4 FeFePBA、CoFePBA和FeCoPBA三种材料的比容量和能量密度
基于以上事实和总结的规律,我们认为PBAs [KM1IIM2III(CN)6]在作为锂离子电池正极材料测试时,M1和M2均可以通过自身发生氧化还原反应而贡献容量,但是两种结构中的金属元素是否发生反应可能是相互影响的。N-M1II发生氧化还原反应与否对C-M2III是否发生氧化还原反应影响不明显,反之C-M2III发生氧化还原反应与否对N-M1II是否发生氧化还原反应影响显著。在PBAs中,一方面,C-CoIII不仅自身呈现电化学惰性,而且对邻近的N-FeII电化学活性起到抑制作用,而C-FeIII虽然通过自身发生氧化还原反应而贡献的比容量较少,却可以促进邻近的N-FeII发生氧化还原反应而贡献容量;另一方面,无论是有电化学活性的N-FeII或无电化学活性的N-CoII,均无法显著地影响或改变C-CoIII和C-FeIII的电化学活性。C-M2III发挥着类似于“泵”的作用,当自身“运动”时,可以对其它部分起到促进作用,当自身“静止”时,也可以对其它部分起到抑制作用。
3 结 论
通过以PBAs中的FeFePBA、CoFePBA和FeCoPBA 为研究对象,借助物相表征、形貌表征、电化学表征以及充放电测试等多种手段,对组成相似、结构相同、但电化学行为大不相同的3种PBAs展开研究和讨论。在排除了由于材料结构或形貌导致锂离子嵌入/迁出难易程度对电化学行为的影响之后,结合电化学表征和充放电测试结果总结得到推论:在锂离子电池正极测试条件下,KM1IIM2III(CN)6中存在N-M1II和C-M2III两种结构,N-M1II的电化学行为对C-M2III的电化学行为无显著影响,而C-M2III的电化学行为却对N-M1II的电化学行为有着显著的影响。因此,在未来的正极材料选择或设计时,应当结合已有的资料,甄选具有促进作用的C-M2III结构,调变具有高比容量和高氧化还原电势的N-M1II结构,从而制备高比容量和高比能量的正极材料。
符 号 说 明
M(=1,2)——M1和M2分别表示PBAs中与N连接和与C连接的金属元素
——立方晶系晶胞常数
[1] OKUBO M, ASAKURA D, MIZUNO Y, et al. Switching redox-active sites by valence tautomerism in Prussian blue analogues AMn[Fe(CN)6]·H2O (A: K, Rb): Robust frameworks for reversible Li storage[J]. The Journal of Physical Chemistry Letters, 2010, 1: 2063-2071.
[2] IMANISHI N, MORIKAWA T, KONDO J, et al. Lithium intercalation behavior of iron cyanometallates[J]. Journal of Power Sources, 1999, (81/82): 530-534.
[3] WU X, SHAO M, WU C, et al. Low defect FeFe(CN)6framework as stable host material for high performance Li-ion batteries[J]. Acs Applied Materials & Interfaces, 2016, 8(36): 23706-23712.
[4] WEWSSELLS C D, PEDDADA S V, CUI Y, et al. The effect of insertion species on nanostructured open framework hexacyanoferrate battery electrodes[J]. Journal of the Electrochemical Society, 2011, 159(2): A98-A103.
[5] TOMOYUKI M, YUTAKA M. Thin film electrode of Prussian blue analogue for Li-ion battery[J]. Applied Physics Express, 2011, 4 (4): doi: 10.1143/APEX.4.047101.
[6] CHEN L, SHAO H, ZHOU X, et al. Water-mediated cation intercalation of open-framework indium hexacyanoferrate with high voltage and fast kinetics[J]. Nat. Commun., 2016, 7: 11982.
[7] IMANISHI N, MORIKAWA T, KONDO J, et al. Lithium intercalation behavior into iron cyanide complex as positive electrode of lithium secondary battery[J]. Journal of Power Sources, 1999, 79(2): 215-219.
[8] YOU Y, WU X L, GUO Y G, et al. High-quality Prussian blue crystals as superior cathode materials for room-temperature sodium-ion batteries[J]. Energy & Environmental Science, 2014, 7(5): 1643-1647.
[9] YUAN Y, WANG J, JIAO S, et al. Na2Co3[Fe(CN)6]2: A promising cathode material for lithium-ion and sodium-ion batteries[J]. Journal of Alloys and Compounds, 2016, 685: 344-349.
[10] LU Y, WANG L, CHENG J, et al. Prussian blue: A new framework of electrode materials for sodium batteries[J]. Chem. Commun., 2012, 48(52): 6544-6546.
[11] WANG L, SONG J, GOODENOUGH J B, et al. Rhombohedral Prussian white as cathode for rechargeable sodium-ion batteries[J]. Journal of the American Chemical Society, 2015, 137(7): 2548-2554.
[12] WANG L, LU Y, GOODENOUGH J B, et al. A superior low-cost cathode for a Na-ion battery[J]. Angewandte Chemie International Edition, 2013, 52(7): 1964-1967.
[13] MIZUNO Y, OKUBO M, YAMADA A, et al. Electrochemical Mg2+intercalation into a bimetallic CuFe Prussian blue analog in aqueous electrolytes[J]. Journal of Materials Chemistry A, 2013, 1(42): 13055-13059.
[14] WANG R Y, WESSELLS C D, CUI Y, et al. Highly reversible open framework nanoscale electrodes for divalent ion batteries[J]. Nano Letters, 2013, 13(11): 5748-5752.
[15] TOJO T, SUGIURA Y, SAKURAI Y, et al. Reversible calcium ion batteries using a dehydrated prussian blue analogue cathode[J]. Electrochimica Acta, 2016, 207: 22-27.
[16] LIANG Y L, YOO H D, YAO Y, et al. Interlayer-expanded molybdenum disulfide nanocomposites for electrochemical magnesium storage[J]. Nano Letters, 2015, 15: 2194-2202.
[17] GREENWOOD N N, EARNSHAW A. Chemistry of the elements[M]. 2nded. Oxford: Butterworth-Heinemann, 1997.
[18] HU M, NAFY L K, YAMAUCHI Y, et al. Size- and shape-controlled synthesis of Prussian blue nanoparticles by a polyvinylpyrrolidone- assisted crystallization process[J]. Cryst. Eng. Comm., 2012, 14: 3387.
[19] LIU J Y, LI X N, WANG J H. Zinc-modulated Fe-Co Prussian blue analogues with well-controlled morphologies for the efficient sorption of cesium[J]. Journal of Materials Chemistry A, 2017, 5: 3284-3292.
[20] GOODENOUGH J B, KIM Y. Challenges for rechargeable Li batteries[J]. Chemistry of Materials, 2010, 22(3): 587-603.
The effect of prussian blue and its analogues containing Fe and Co on specific capacity as cathode material of lithium-ion battery
JIANG Wei1,2, WANG Erdong1, SUN Hai1, WANG Suli1, SUN Gongquan1
(1Dalian Institute of Chemical Physics, Chinese Academy of Sciences, Dalian 116023, Liaoning, China;2University of Chinese Academy of Sciences, Beijing 100039, China)
Prussian blue and its analogues (PBAs) are considered as promising cathode materials of alkali metal-ion or alkaline earth metal-ion batteries due to their simple preparation process, high rate performance and low cost. Firstly, we prepared a series of PBAs containing Fe and Co, and then the crystal structure, morphology and electrochemical performance were characterized through XRD, SEM and electrochemical technologies. Finally, the interaction between Fe and Co in different structures was explored.The results suggested that in the structures of “M1—N≡≡C—M2”, by changing transition metal M1can notable influence the electrochemical activity of transition metal M2.
prussian blue; cathode material; Li-ion battery
10.12028/j.issn.2095-4239.2017.0029
O 646.541
A
2095-4239(2017)06-1280-06
2017-03-24;
2017-04-13。
中科院重点部署项目(KGBD-EW-P08)。
姜巍(1988—),男,硕士研究生,研究方向为新型二次电池,E-mail:jiangwei@dicp.ac.cn;
孙公权,研究员,研究方向为化学电源,E-mail:gqsun@dicp.ac.cn。
