离子液体在混合超级电容器中的应用进展
2017-11-24张之逸张超灿
张之逸,李 曦,张超灿
离子液体在混合超级电容器中的应用进展
张之逸,李 曦,张超灿
(武汉理工大学材料学院,湖北武汉 430070)
混合超级电容器具有高比功率、高比能量等优点,是一种极具潜力的储能装置,但其常用的溶液电解质或有机电解质分别存在电化学窗口较窄和易燃的缺点,限制了其应用范围。离子液体具有不可燃性、宽电化学窗口等特点,成为混合超级电容器用电解质的理想选择。本文回顾了近年来离子液体在混合超级电容器中的应用,介绍了离子液体单独作为电解质、混合电解质组分、固态电解质组分和电极组分在混合超级电容器中的应用,指出降低离子液体吸湿性与成本是未来应用于混合超级电容器方向上的研究重点。近年来由于对混合超级电容器与非对称超级电容器定义的理解出现偏差,造成了表述上的混乱,因此尝试对两者的概念进行了解释和区分。
离子液体;混合超级电容器;非对称超级电容器
随着经济的发展,人们对能源的消耗量大大提高,其中最主要的部分是石油的消耗。然而全球石油储量有限,这就需要人们转向风能、太阳能等新能源应用。新能源虽然环境友好且不会枯竭,但由于受到天气等因素的影响,难以持续供能,这就需要能源转换/储存装置来有效地储存这些间歇性的能源,因此,电池、超级电容器和燃料电池作为重要的能源转换/储存装置受到了日益广泛的关注[1-5]。
电容器由两块金属电极和之间夹着的一层绝缘电介质构成,其储存电容满足式(1)
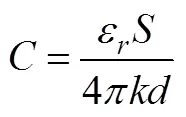
式中,ε为真空介电常数,为静电力常量,为电极板正对面积,为电极板间距。传统电容器由于只能在正、负电极表面处各积累一层电荷,因此电容较低。
以大比表面积的多孔碳为电极的超级电容器出现于1957年[6]。超级电容器的储能机理如图1(a)所示,通过电解质中阴、阳离子分别在电极/电解质界面通过吸附形成的电化学双电层(又称Helmholtz电层)储能,其电极储存电容满足式(2)
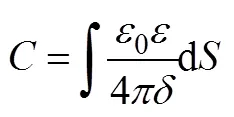
式中,0为真空介电常数,为电解质介电常数,为双电层厚度,为电极形成双电层部分的表面积。超级电容器的电极材料多为多孔碳、石墨烯、碳纳米管等具有极大比表面积的碳材料[7],因而具有远大于传统电容器的电极表面积,其双电层厚度也远小于传统电容器电极板间距,因此,超级电容器具有远超过传统电容器的比电容。
(a) (b) (c)
图1 超级电容器不同储能机理示意图:(a)赝电容器储能机理;(b)双电层超级电容器储能机理;(c)嵌入赝电容储能机理
Fig.1 Mechanism of different capacitors: (a) pseudocapacitor; (b) electric Double-layer capacitor(EDLC); (c) intercalation pseudocapacitance
1975年出现的赝电容器[8]机理如图1(b)所示。赝电容器主要通过电极表面快速且可逆的氧化还原反应储能,电极材料多为过渡金属氧化物和导电聚合物[9]。根据CONWAY的定义[10],赝电容电极虽然储能机理不同于超级电容器电极,但具有与其相同的电化学特征,即:在一定的电势范围内,其储存电荷量与电压变化呈线性关系。也就是说,赝电容电极具有电容特性。近年来,不断有新型锂离子电极材料被发现[11-14],这些电极材料在Li+的嵌入过程[图1(c)]中表现出了赝电容特性,通过这种机理产生的电容又被称为嵌入赝电容[15](intercalation pseudocapacitance)。嵌入赝电容通过离子在活性物质晶格间的嵌入/脱嵌储能,其机理与电池的嵌入/脱嵌机理十分类似,其区别在于,电池的嵌入/脱嵌过程受到电极活性物质晶格间离子扩散的限制,而嵌入赝电容则不受扩散过程的限制[16]。由于嵌入赝电容表现出了赝电容特性,可以将此类电极看作赝电容电极。赝电容器的电容主要来自电极表面的可逆氧化还原反应,其电极比表面积有限,因而双电层对电极电容的贡献不大,这是其与超级电容器的不同之处。如图2所示,混合超级电容器和非对称超级电容器是常被互换的两个概念,然而二者的定义并不完全相同。
非对称超级电容器是指两个电极为不同电容电极的电容器,如一个电极为超级电容器电极,另一个电极为赝电容电极[17]。混合超级电容器概念的第一次提出是在1995年[18],其两个电极分别为超级电容器电极和电池电极,从而具有介于超级电容器与电池之间的性能。可以看出,混合超级电容器和非对称超级电容器的区别在于:前者的两个电极分别表现出电容特性(超级电容器电极)和法拉第特性(电池电极),而后者两个电极均表现出电容特性。然而在现在的很多文献中,对于混合超级电容器和非对称超级电容器的定义十分混乱,这种错误的判断来源于将具有电池特性的电极错误地当作赝电容电极[19]。
赝电容电极与电池电极之间的区分,已由BROUSSE等[20]做出了清晰的解释。赝电容电极与电池电极可以通过相应电极的循环伏安曲线进行判断:赝电容电极的循环伏安曲线与超级电容器电极的十分类似,为接近矩形的形状,而电池电极的伏安循环曲线具有明显的氧化还原峰。
混合超级电容器不仅具备电池电极自身通过氧化还原反应储能的能力,还具备超级电容器电极比表面积高的优点。由于同时应用了两种储能机理,混合超级电容器不仅具有较高的循环性能,还具备高于超级电容器的比能量和比容量[21]。
离子液体(IL)是一类在接近室温时为液态的盐,由于其完全由阴阳离子组成,因此也被称为室温熔盐[22]。其具有蒸汽压低、不挥发、无色无味、离子电导率良好、化学稳定性强和宽电化学窗口等优点,且由于其阴阳离子能够根据需求而进行相应设计的特性,被广泛应用于电化学、合成等领域[23]。离子液体对多孔碳电极有较好的润湿性,可进入多孔碳电极的微孔内[24],有效地利用电极的高比表面积;另一方面,非对称超级电容器的电解质常需溶解特定的电化学活性金属盐,而离子液体也对金属盐有较好的溶解能力[25],因此,离子液体是非对称超级电容器体系电解质的理想选择。
本文综述了近年来离子液体在混合超级电容器中应用的研究进展。
1 离子液体作为液态电解质
超级电容器通常有较高的比功率,而比能量相对较低,因此在不降低比功率的前提下提高比能量成为了研究的重点[26]。由于比功率和比能量均取决于其工作电压的平方,提高超级电容器的工作电压就成了提高其比能量和比功率的关键[27]。
电解质作为超级电容器的组成部分,在很大程度上决定了电容器的工作电压,从而对超级电容器的性能产生了重要的影响。水溶液电解质和有机电解质是最常见的两类电解质,然而前者受水的分解电压影响,工作电压过低,且对多孔碳电极浸润性有限,后者虽然工作电压更高,但由于其有机溶剂易挥发、易燃烧等问题限制了其应用[28]。离子液体电解质由于其较高的工作电压和不挥发、化学稳定性强、浸润性好的特点,较好地弥补了以上两种电解质的不足之处。有报道指出,对于同样的碳电极,其在离子液体中的双电层电容要大于在有机溶剂中的电容[29]。
以具有法拉第氧化还原反应能力的电极与大比表面积碳材料双电层电容电极的混合超级电容器可以有效地提高电容器的比能量,在近年来引起了科研工作者的关注[30-32]。
1.1 离子液体作为镍基混合超级电容器电解质
LIU等[33]以镍基混合氧化物为正极、活性炭为负极,1-正丁基-3-甲基咪唑六氟磷酸盐(BMIMPF6)为电解质制备了最大工作电压为3 V的混合超级电容器。BMIMPF6是一种具有较高电导率和稳定电化学性能的离子液体,其作为电解质的应用,为该电容器提供了宽电化学窗口,提高了电容器的比功率和比能量,此外,由于BMIMPF6的低挥发性,使其得以长期浸润电极和隔膜,提高了电容器的稳定性。该电容器比功率和比能量分别为458 W/kg和50 W·h/kg,经过500次充放电循环后没有明显的电容损耗。可以看出其比功率和循环稳定性略有不足,说明以镍电极混合超级电容器仍存在改良的余地。
酞菁镍(NiPc)是一种典型的氧化还原物质,EGASHIRA等[34]将其负载于碳纳米管(CNT)上制备了NiPc/CNT负极,并以CNT为正极,1-乙基-3-甲基咪唑四氟硼酸盐(EMIMBF4)为电解质制备了一种新型的氧化还原电容器,同时制备了以1 mol/L四氟硼酸四乙基铵/碳酸丙烯酯溶液(Et4NBF4/PC)为电解质的电容器作为对比。其工作电压达2.5 V,比电容为7.3 F/g,高于Et4NBF4/PC的6.3 F/g。经过5000次循环后EMIMBF4和Et4NBF4/PC容量保持率分别为78%和53%。造成EMIMBF4电解质循环稳定性高于Et4NBF4/PC的原因是,长期充放电下NiPc在EMIMBF4中的溶解度小于Et4NBF4/PC,使得以EMIMBF4为电解质的电容器中NiPc能更紧密地负载于CNT上。尽管如此,以EMIMBF4为电解质的电容器循环稳定性仍然不高,这可能是因为离子液体本身性质导致金属氧化物电极在离子液体或离子液凝胶电解质中的循环稳定性远低于其在溶液电解质或有机电解质中[35]。
PARAVANNOOR等[36]设计了一种离子液体为电解质的NiO混合超级电容器。该电容器以NiO/碳纳米线复合物为正极,中孔碳为负极,一种典型的非质子型离子液体,1-乙基-3-甲基咪唑二氰胺盐(EMIMDCA)为电解质。经测试,其最大比能量和最大比功率为21 W·h/kg、8.3 kW/kg,经过2000次充放电循环后容量保持率为95%。
1.2 离子液体作为锰基混合超级电容器电解质

1.3 离子液体作为其它类型混合超级电容器电解质
Co(OH)2由于其大层间间距的多层结构,有利于电解质离子的快速扩散,且有较高的理论比电容,但由于电阻较高,限制了其作为电极材料的使用。CHENG等[39]通过将Co(OH)2修饰于石墨烯/碳纳米管(GN/CNT)复合材料上,有效地解决了这个问题。以GN/CNT管复合材料作为负极,将Co(OH)2纳米片修饰的GN/CNT作为正极,EMIMTFSI作为电解质制备了一种混合超级电容器。其最大工作电压为4 V,比电容高达310 F/g,最大比能量172 W·h/kg,最大比功率198 kW/kg。经过1500次充放电循环后,容量保持率为70%。
SUN等[40]首次证明了Fe2O3电极在离子液体中存在法拉第电化学反应,充放电过程中Fe2O3电极表面的反应见式(3)

为了进一步提高Fe2O3电极在离子液体中的比电容,该小组通过水热法将Fe2O3纳米颗粒负载于石墨烯纳米片上(Fe2O3@GNS)作为负极,活性炭(AC)或活性聚苯胺碳纳米棒(APDC)为正极、EMIMBF4为电解质制备了两种混合超级电容器。这两种电容器工作电压均可达4 V,电流密度0.1 A/g时以AC和APDC为负极的电容器比电容分别为57.1 F/g和79.6 F/g,最大比能量分别为118 W·h/kg和177 W·h/kg,且APDC电极的电容器在得到最大比功率8 kW/kg时比能量达62.4 W·h/kg,表明该电容器能同时提供较高的比能量和比功率。此外,在2000次充放电循环后Fe2O3@GNS//AC的容量保持率为81.5%,说明Fe2O3混合电容器具有较好的应用前景。
2 离子液体作为混合电解质组分
2.1 离子液体作为活性物质的溶剂
对于一些混合超级电容器体系,离子液体可作为溶剂溶解活性物质金属盐,以提供嵌入/脱嵌过程所需的离子。在这种情况下,使用离子液体作为溶剂,既避免了水溶液电化学窗口低的缺点,又避免了有机溶剂易燃的问题。
2006年ALESSANDRINI等[41]对-丁基--甲基吡咯烷双(三氟甲烷磺酰)亚胺盐/双三氟甲烷磺酰亚胺锂盐(PYR14TFSI/LiTFSI)混合电解质的性能进行了早期研究,结果表明由于离子液体的不挥发性和热稳定性,使得离子液体可以取代分子溶剂,和锂盐一起组成新型混合电解质,并应用于锂电池或超级电容器中。
ZAGHIB等[21]以多层Li4Ti5O12/石墨烯为正极,高比表面积碳为负极,1 mol/L LiFSI的EMIMFSI溶液为电解质制备了一种混合超级电容器,其经过20000次充放电循环后容量保持率为80%,其比能量为18 W·h/kg。
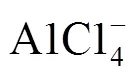
一般来说,混合超级电容器的两个电极为双电层电极和电池电极,分别为混合超级电容器提供高比功率和比能量。然而,两个电极均采用双电层电极,将氧化还原活性物质加入电解质中,使其在电极界面处发生法拉第氧化还原反应,也是一种构建混合超级电容器的思路。NAVALPOTRO等[44]分别以高比表面积(BET=2410 m2/g)的Pica碳和低比表面积(BET=240 m2/g)的Vulcan碳为电极制备了两组高性能的混合超级电容器,并以0.4 mol/L对苯醌(p-BQ)的PYR14TFSI溶液为氧化还原电解质。p-BQ在离子液体中的氧化还原反应见式(4)和式(5)
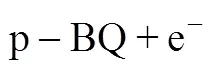
(5)
该电容器的储能分为两个部分:双电层的形成和电极-电解质界面处对苯醌的法拉第反应。p-BQ的加入,引入了法拉第反应,从而有效地提高了电容器的比电容。Pica碳电极具有更高的比表面积,其在p-BQ/PYR14TFSI电解质中的比电容也更高;而Vulcan碳电极更高的开孔率使得离子和p-BQ分子较易达到其电极区域,从而在高扫描速率下仍能保持较高的比电容。得到Vulcan碳电极混合超级电容器和Pica碳电极混合超级电容器最大比能量分别为10.3 W·h/kg和29.7 W·h/kg。由于使用了氧化还原电解质,本文中的混合超级电容器经过1000次充放电循环后,容量保持率仅为约50%,远低于其它混合超级电容器。尽管如此,经过1000次循环后比能量仍达4 W·h/kg,高于未添加p-BQ的同体系混合超级电容器。
2.2 离子液体作为有机电解质的共溶剂
离子液体具有不可燃、无毒、蒸汽压低等优点,却存在高黏度、高成本的缺点。通过将有机溶剂添加到离子液体中,可有效地降低其黏度并提升电导率等性能。虽然有机溶剂本身可燃性高,但有研究表明[45],在离子液体所占组分足够高的情况下,离子液体与有机电解质的混合物仍具有不可燃性。
ZHANG等[46]依次将CNT、Au纳米粒子、MnO2沉积于镍泡沫上作为正极,记作NF/CNT/Au/MnO2极,以活性炭作为负极,以BMIMPF6/DMF作为电解质,得到了混合超级电容器。向BMIMPF6电解质中加入适量DMF,可以削弱BMIMPF6分子间氢键和范德华力,从而有效地降低电解质的黏度和电阻,但过量加入DMF,则会降低BMIM+浓度,导致电容器性能下降。通过实验发现,BMIMPF6与DMF体积比为1∶1时电容器性能最佳。该MnO2混合超级电容器最大工作电压达3 V,最大比功率为20.4 kW/kg,最大比能量67.5 W·h/kg。将正极中Au分别替换为Pt或Pd,可以进一步提高该体系的比能量[27]。其中以NF/CNT/Pd/MnO2为正极的电容器性能最佳,其最大工作电压为3 V,最大比能量和最大比功率分别为78 W·h/kg和12.7 kW/kg。以上结果表明,采用BMIMPF6/DMF为混合电解质在MnO2混合超级电容器中有较好的应用前景。
K10是一种廉价的酸活化蒙脱石,其具有多层结构和高比表面积,且表面上存在大量羟基,在电化学能量储存装置中具有潜在的应用价值。MAITI等[47]以K10/多层碳纳米管/二氧化锰(KMC)复合材料为正极、活性炭为负极、1 mol/L Et4NBF4的乙腈(AN)溶液为电解质制备了混合超级电容器,该电容器工作电压可达2.7 V,比电容为48 F/g,比功率为1.98 kW/kg时有最大比能量171 W·h/kg,比能量为91.1 W·h/kg时有最大比功率96.4 kW/kg,表现出优良的倍率性能。能经过5000次充放电循环后容量保持率为85%。Et4NBF4中阳离子适中的离子尺寸(0.385 nm)使其能够扩散至K10的层间,增加层间间距,并与KMC表面的羟基相互作用形成双电层,增加了电容器的比电容。
由石墨烯片连接而成的三维(3D)石墨烯具有极高的比表面积、多孔结构、强力学性能、高电导率和优良电子转移能力等性能[48],是一种理想的电极材料。通过将其与纳米结构金属氧化物复合,可以有效地阻止石墨烯片的聚集,提高电极的比电 容[49]。ZHU等[50]将MnO2沉积在3D石墨烯上制备了3D石墨烯/MnO2复合材料,并将其作为正极,3D石墨烯为负极,2 mol/L EMIMBF4/AN为电解质,首次制备了以3D石墨烯/MnO2为电极、离子液体为电解质的混合超级电容器。工作电压可达3.5V,最大比能量68.4 W·h/kg,最大比功率8.79 kW/kg。在2 mol/L EMIMBF4/AN中正负极比电容分别可达236 F/g和150 F/g。由于MnO2在离子液体中稳定性不佳,1000次充放电循环后容量保持率仅为80%。
HU等[51]以rGO纸为负极,具有高Mn3O4负载量的Mn3O4/rGO(MG)复合纳米纸为正极,1 mol/L EMIMBF4的丙酮溶液为电解质,制备了一类性能优良的柔性混合超级电容器。EMIMBF4/丙酮为电解质的电容器的工作电压达3 V,在60°~180°弯曲角度时比电容约17 F/cm3,同时在弯曲角度变化时,比电容保持稳定,显示出较好的柔性,最大比能量0.0039 W·h/cm3,最大比功率10.95 W/cm3,6000次充放电循环后容量保持率95%。EMIMBF4离子半径较大,难以穿过Mn3O4八面体结构,因此氧化还原反应只能发生在Mn3O4的表面,导致EMIMBF4/丙酮为电解质的电容器比电容更低;另一方面,EMIMBF4较宽的电化学窗口又有利于提高电容器的比功率和比能量。
3 离子液体作为固态电解质组分
3.1 离子液体作为聚合物电解质组分
向电容器中引入锂掺杂的多孔碳电极可以有效提高电容器的比能量,这种电极通常在非水电解质中运行,而电极提供高比电容的前提是在水溶液电解质中运行[52]。通过构建锂电极|固态电解质|水溶液电解质|赝电容电极的结构,使混合超级电容器能同时得到赝电容电极和锂电极的优点[53]。
MAKINO等[54]开发了一种水稳定锂掺杂多层碳负极(LiC6),以聚环氧乙烯(PEO)-双三氟甲烷磺酰亚胺锂盐(LiTFSI)--甲基--丙基哌啶双三氟甲基磺酰亚胺盐(PP13TFSI)为固体电解质,1.0 mol/L Li2SO4或2.0 mol/L乙酸/乙酸锂(AcOH/AcOLi)为溶液电解质,活性炭或RuO2纳米片为正极构成了负极|固态电解质|溶液电解质|正极结构的混合超级电容器中。PP13TFSI的加入大大降低了电容器的ESR,增加了电导率,使得该电容器得以在25 ℃条件下性能与60 ℃条件下未添加PP13TFSI的电容器性能相当。以0.1 mol/L Li2SO4为液体电解质,活性炭为正极的混合超级电容器工作电压可达3.7 V,在经过3000次充放电循环后容量保持率为81%,负极ESR有所增加。以2.0 mol/L AcOH-AcOLi为液体电解质,RuO2纳米片为正极的混合超级电容器,在25 ℃时比容量为196 mA·h/g(-RuO2),比能量为625 W·h/kg(-RuO2)。
石墨烯量子点(GQDs)具有高比表面积,高电导率等特点,以其作为电极材料的微型电容器具有频率响应快、倍率性能高等优点[55]。SHEN等[56]以MnO2纳米片为正极,GQDs为负极,EMIMBF4- 20%(质量分数,下文同)PVDF-HFP(偏氟乙烯-六氟丙烯共聚物)离子液凝胶、EMIMTFSI-20% PVDF-HFP离子液凝胶、EMIMBF4-20% 气相二氧化硅纳米粉(FS)离子液凝胶、EMIMTFSI-3%、EMIMTFSI-4%、EMIMTFSI-5%、EMIMTFSI-6% FS离子液凝胶分别为电解质制备了一系列全固态微型电容器。这类固态微型电容器在微纳米器件供能、微型发电装置集成储存能量方面有潜在的应用前景。其中EMIMTFSI-4% FS为电解质的电容器电化学性能最佳,最大工作电压2.5 V,比电容0.81 mF/ cm2,比能量0.703 μW·h/cm2(此时比功率为 101.9 μW/cm2)。循环伏安测试中,即使在扫描速率高达2000 V/s时其循环伏安曲线仍接近矩形,表明以EMIMTFSI-FS为电解质的电容器具有极强的快速充放电能力和瞬时功率能力。
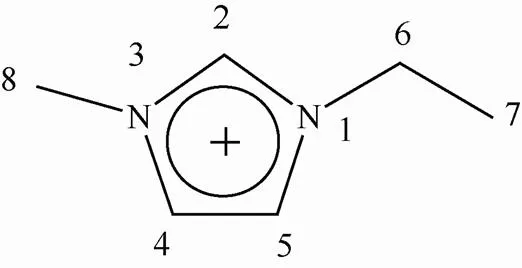
图3 EMIM+的结构
如图3所示,C(2)位置上的H较易形成氢键。FS表面存在大量羟基,使得C(2)-H和Si-OH之间形成了更多氢键,有利于凝胶的形成[57]。此外,氢键的取向性有利于破坏电荷对称性,增加离子液体的流动性,从而增强电容器的电化学性能。
3.2 离子液体作为二氧化硅电解质组分
SHEN等[58]制备了一种高效储能系统,基于储备丰富、环境友好的γ-FeOOH电极与EMIMTFSI离子液体电解质,且通过电化学石英晶体微天平(EQCM)、XPS等电化学测试研究了γ-FeOOH电极在EMIMTFSI电解质中的电荷储存机理。测试表明,该电极电荷储存可分为3部分:[EMIM]+在γ-FeOOH晶面间嵌入/脱嵌的储能、电极表面快速氧化还原反应的储能和几乎可以忽略不计的电极表面双电层储能。SHEN等[58]进一步制备了一种新型柔性固态超级电容器,以γ-FeOOH沉积于碳布作为电池电极,APDC涂覆于碳布作为双电层电容电极,纳米气相二氧化硅与EMIM-NTF2(4%)混合作为电解质,在高温下表现出优异的电化学性能。能随着温度变化而改变其比电容,且在200 ℃下比能量高达1.44 mW·h/cm3,比电容为115 mF/cm2。在经过2000次充放电循环后其容量保持率为80.5%,库仑效率高于90%。值得注意的是,该设备能在高于所有已知报道中最高的温度下工作,且在180 ℃下弯曲时表现出了高电容稳定性和力学耐久性。
4 离子液体在电极中的应用
离子液体不仅可以作为电解质应用于电化学装置中,也可以应用于导电聚合物的制备过程。其具有环境友好、可循环使用的特性,并且可以显著地改变聚合物的形态结构[59]。已有文献表明[60],使用与电容测试中相同的离子液体进行电化学聚合,可使得到的聚合物有较好的性能。
SUN等[61]采用水热法制备了三维多孔MnO2-rGO凝胶和IL-CNT-rGO凝胶自支撑电极,并分别为正负极,1 mol/L Na2SO4溶液为电解质制备了新型混合超级电容器,其最大工作电压为1.8 V、电流密度为1 A/g时比电容、比能量和比功率分别为57 F/g、25.6 W·h/kg和9.07 kW/kg。在循环10000次后容量保持率为90%。IL-CNT-rGO电极中离子液体BMIMBF4的存在,使得BMIMBF4咪唑环与rGO和CNT表面存在阳离子-π相互作用,防止了石墨烯的无序堆积和聚集,从而增加了IL-CNT-rGO的比表面积,提供了更多导电通道,有利于水溶液电解质中离子向石墨烯表面的传导,从而提高了该电容器的性能。
CHOI等[62]将IL同时作为正负极的组分,制备了一种高性能的柔性固态混合超级电容器。负极为离子液体功能化的改性石墨烯(IL-CMG)膜,正极为RuO2-IL-CMG复合膜,电解质为聚乙烯醇(PVA)-H2SO4凝胶电解质。制备CMG的过程中包括GO的剥落,而 BMIMBF4在GO剥落过程中起到稳定剂的作用。此外,BMIMBF4官能团在IL-CMG表面为RuO2纳米粒子的沉积提供了形核和生长的位置。正负电极都具有良好的力学性能:IL-CMG膜的拉伸模量为45 GPa,抗张强度为356 MPa,而RuO2-IL-CMG的拉伸模量为40 GPa,抗张强度为273 MPa。电容器的最大工作电压为1.8 V,比电容、最大比功率和最大比能量分别为175 F/g、6.8 kW/g和19.7 W·h/kg。该电容器有较高的机械强度和循环稳定性,因此先后在正常、扭曲、弯曲状态下进行充放电循环2000次后容量保持率仍高达95%。
5 展 望
离子液体已经成为了混合超级电容器的重要组成部分。BMIMBF4、EMIMPF6等离子液体已经作为混合超级电容器的电解质得到了广泛的应用,其较宽的电化学窗口有利于提高电容器的工作电压,从而提高其电化学性能,而其高化学稳定性和热稳定性又确保了电容器的安全性。将离子液体与有机溶剂或气相二氧化硅纳米粉等物质共用,形成了混合电解质和凝胶电解质,起到了提高电容器电化学性能,力学性能的作用。此外,在电极合成过程中引入离子液体,也可以起到提高电容器性能的作用。然而离子液体仍然存在吸湿性强和成本较高的问题,限制了其实际应用。一方面,离子液体电解质体系中水分的含量会显著影响电解质的性能,较强的吸湿性导致体系性能易受影响。另一方面,离子液体封装所采用的额外措施增加了使用成本,且合成所用的原料成本高昂。因此,解决这两个问题是未来离子液体应用于混合超级电容器体系的研究方向之一。
[1] HALL P J, BAIN E J. Energy-storage technologies and electricity generation[J]. Energy Policy, 2008, 36(12): 4352-4355.
[2] QU Q T, SHI Y, TIAN S, et al. A new cheap asymmetric aqueous supercapacitor: Activated carbon//NaMnO2[J]. Journal of Power Sources, 2009, 194(2):1222-1225.
[3] THOUNTHONG P, RAËL S, DAVAT B. Energy management of fuel cell/battery/supercapacitor hybrid power source for vehicle applications[J]. Journal of Power Sources, 2009, 193(1):376-385.
[4] LI W, JOÓS G, BÉLANGER J. Real-time simulation of a wind turbine generator coupled with a battery supercapacitor energy storage system[J]. IEEE Transactions on Industrial Electronics, 2010, 57(4): 1137-1145.
[5] DÍAZ-GONZÁLEZ F, SUMPER A, GOMIS-BELLMUNT O, et al. A review of energy storage technologies for wind power applications[J]. Renewable & Sustainable Energy Reviews, 2012, 16(4):2154-2171.
[6] BECKER H I. Low voltage electrolytic capacitor: US 2800616[P]. 1957-07-23.
[7] KÖTZ R, CARLEN M. Principles and applications of electrochemical capacitors[J]. Electrochimica Acta, 2000, 45(15/16): 2483-2498.
[8] CONWAY B E. Transition from `supercapacitor' to `battery' behavior in electrochemical energy storage[J]. Journal of the Electrochemical Society, 1991, 138(6):1539-1548.
[9] FRACKOWIAK E, BÉGUIN F. Carbon materials for the electrochemical storage of energy in capacitors[J]. Carbon, 2001, 39(6): 937-950.
[10] CONWAY B E. Electrochemical supercapacitors: Scientific fundamentals and technological applications[M]. Germany: Springer Science & Business Media, 2013.
[11] ZUKALOVA M, KALBAC M, KAVAN L, et al. Pseudocapacitive lithium storage in TiO2(B)[J]. Chemistry of Materials, 2005, 17(5): 1248-1255.
[12] WANG J, POLLEUX J, JAMES LIM A, et al. Pseudocapacitive contributions to electrochemical energy storage in TiO2(anatase) nanoparticles[J]. The Journal of Physical Chemistry C, 2007, 111(40): 14925-14931.
[13] BREZESINSKI T, WANG J, TOLBERT S H, et al. Ordered mesoporousa-MoO3with iso-oriented nanocrystalline walls for thin-film pseudocapacitors[J]. Nature Materials, 2010, 9(2): 146-151.
[14] AUGUSTYN V, SIMON P, DUNN B. Pseudocapacitive oxide materials for high-rate electrochemical energy storage[J]. Energy & Environmental Science, 2014, 7(5): 1597-1614.
[15] AUGUSTYN V, COME J, LOWE M A, et al. High-rate electrochemical energy storage through Li+intercalation pseudocapacitance[J]. Nature Materials, 2013, 12(6): 518-522.
[16] SATHIYA M, PRAKASH A S, RAMESHA K, et al. V2O5-anchored carbon nanotubes for enhanced electrochemical energy storage[J]. Journal of the American Chemical Society, 2011, 133(40): 16291-16299.
[17] SUMBOJA A, FOO C Y, WANG X, et al. Large areal mass, flexible and free-standing reduced graphene oxide/manganese dioxide paper for asymmetric supercapacitor device[J]. Advanced Materials, 2013, 25(20): 2809-2815.
[18] YOSHIDA A, AOKI I, NONAKA S, et al. Electric double layer capacitor: US 5450279[P]. 1995-09-12.
[19] HU G, TANG C, LI C, et al. The sol-gel-derived nickel-cobalt oxides with high supercapacitor performances[J]. Journal of the Electrochemical Society, 2011, 158(6): A695-A699.
[20] BROUSSE T, BÉLANGER D, LONG J W. To be or not to be pseudocapacitive?[J]. Journal of the Electrochemical Society, 2015, 162(5): A5185-A5189.
[21] ZAGHIB K, CHAREST P, GUERFI A, et al. HQ asymmetric super capacitor: Graphite-Li4Ti5O12/ionic liquid/carbon[J]. Ecs Transactions, 2007, 3(36): 89-93.
[22] SEDDON K R. Ionic liquids for clean technology[J]. Journal of Chemical Technology & Biotechnology, 1997, 68(4): 351-356
[23] CHANG J K, LEE M T, TSAI W T, et al. X-ray photoelectron spectroscopy andX-ray absorption spectroscopy studies on reversible insertion/desertion of dicyanamide anions into/from manganese oxide in ionic liquid[J]. Chemistry of Materials, 2009, 239(1):46-54.
[24] MERLET C, ROTENBERG B, MADDEN P A, et al. On the molecular origin of supercapacitance in nanoporous carbon electrodes[J]. Nature Materials, 2012, 11(4): 306-310.
[25] CHIAPPE C, MALVALDI M. Highly concentrated "solutions" of metal cations in ionic liquids: Current status and future challenges[J]. Physical Chemistry Chemical Physics, 2010, 12(37):11191-11196.
[26] LIU C, YU Z, NEFF D, et al. Graphene-based supercapacitor with an ultrahigh energy density[J]. Nano Letters, 2010, 10(12): 4863-4868.
[27] ZHAO D, ZHAO Y, ZHANG X, et al. Application of high-performance MnO2, nanocomposite electrodes in ionic liquid hybrid supercapacitors[J]. Materials Letters, 2013, 107(18): 115-118.
[28] 杨德志, 沈佳妮, 杨晓伟, 等. 石墨烯基超级电容器研究进展[J]. 储能科学与技术, 2014, 3(1): 1-8.
YANG Dezhi, SHEN Jiani, YANG Xiaowei, et al. Progress in graphene based supercapacitors[J]. Energy Storage Science and Technology, 2014, 3(1): 1-8.
[29] SHIRAISHI S, MIYAUCHI T, SASAKI R, et al. Electric double layer capacitance of activated carbon nanofibers in ionic liquid: EMIMBF4[J]. Electrochemistry, 2007, 75(8): 619-621.
[30] ZHAO X, JOHNSTON C, GRANT P S. A novel hybrid supercapacitor with a carbon nanotube cathode and an iron oxide/carbon nanotube composite anode[J]. Journal of Materials Chemistry, 2009, 19(46): 8755-8760.
[31] WANG X F, YOU Z, RUAN D B. A hybrid metal oxide supercapacitor in aqueous KOH electrolyte[J]. Chinese Journal of Chemistry, 2006, 24(9): 1126-1132.
[32] CHEN S, ZHU J, WU X, et al. Graphene oxide-MnO2nanocomposites for supercapacitors[J]. Acs Nano, 2010, 4(5): 2822-2830.
[33] LIU H, PING H, LI Z, et al. A novel nickel-based mixed rare-earth oxide/activated carbon supercapacitor using room temperature ionic liquid electrolyte[J]. Electrochimica Acta, 2006, 51(10): 1925-1931.
[34] EGASHIRA M, SAITO W, TOKITA M. Electrode properties of nickel phthalocyanine/carbon nanotube composite in ionic liquid electrolyte[J]. Electrochemistry, 2013, 81(10):783-786.
[35] MAYRAND-PROVENCHER L, ROCHEFORT D. Influence of the conductivity and viscosity of protic ionic liquids electrolytes on the pseudocapacitance of RuO2electrodes[J]. The Journal of Physical Chemistry C, 2009, 113(4): 1632-1639.
[36] PARAVANNOOR A, NAIR S V, PATTATHIL P, et al. High voltage supercapacitors based on carbon-grafted NiO nanowires interfaced with an aprotic ionic liquid[J]. Chemical Communications, 2015, 51(28): 6092-6095.
[37] MAITI S, PRAMANIK A, MAHANTY S. Influence of imidazolium-based ionic liquid electrolytes on the performance of nano-structured MnO2hollow spheres as electrochemical supercapacitor[J]. Rsc Advances, 2015, 5(52):41617-41626.
[38] RENNIE A J R, SANCHEZRAMIREZ N, TORRESI R M, et al. Ether-bond-containing ionic liquids as supercapacitor electrolytes[J]. Journal of Physical Chemistry Letters, 2013, 4(17): 2970-2974.
[39] CHENG Q, TANG J, SHINYA N, et al. Co(OH)2nanosheet-decorated graphene-CNT composite for supercapacitors of high energy density[J]. Science & Technology of Advanced Materials, 2014, 15(1):14206-14211.
[40] SUN S, LANG J, WANG R, et al. Identifying pseudocapacitance of Fe2O3in an ionic liquid and its application in asymmetric supercapacitors[J]. Journal of Materials Chemistry A, 2014, 2(35): 14550-14556.
[41] PASSERINI S, ALESSANDRINI F, APPETECCHI G B, et al. Ionic liquid based electrolytes for high energy electrochemical storage devices[J]. Ecs Transactions, 2006, 1(14): 67-71.
[42] LIN M C, GONG M, LU B, et al. An ultrafast rechargeable aluminium-ion battery[J]. Nature, 2015, 520(7547): 325-328.
[43] JIAO H, WANG J, TU J, et al. Aluminum-ion asymmetric supercapacitor incorporating carbon nanotubes and an ionic liquid electrolyte: Al/AlCl3-[EMIm] Cl/CNTs[J]. Energy Technology, 2016, 4(9): 1112-1118.
[44] NAVALPOTRO P, PALMA J, ANDERSON M, et al. High performance hybrid supercapacitors by using para-Benzoquinone ionic liquid redox electrolyte[J]. Journal of Power Sources, 2016, 306: 711-717.
[45] YANG B, LI C, ZHOU J, et al. Pyrrolidinium-based ionic liquid electrolyte with organic additive and LiTFSI for high-safety lithium-ion batteries[J]. Electrochimica Acta, 2014, 148: 39-45.
[46] ZHANG X, ZHAO D, ZHAO Y, et al. High performance asymmetric supercapacitor based on MnO2electrode in ionic liquid electrolyte[J]. J.Mater.Chem. A, 2013, 1(11):3706-3712.
[47] MAITI S, PRAMANIK A, CHATTOPADHYAY S, et al. Electrochemical energy storage in montmorillonite K10 clay based composite as supercapacitor using ionic liquid electrolyte[J]. Journal of Colloid & Interface Science, 2016, 464:73-82.
[48] LI C, SHI G. Three-dimensional graphene architectures[J]. Nanoscale, 2012, 4(18): 5549-5563.
[49] CHOI B G, YANG M, HONG W H, et al. 3D macroporous graphene frameworks for supercapacitors with high energy and power densities.[J]. Acs Nano, 2012, 6(5): 4020-4028.
[50] ZHU X, PENG Z, SHAN X, et al. Free-standing three-dimensional graphene/manganese oxide hybrids as binder-free electrode materials for energy storage applications[J]. Acs Applied Materials & Interfaces, 2014, 6(14): 11665-11674.
[51] HU Y, GUAN C, FENG G, et al. Flexible asymmetric supercapacitor based on structure-optimized Mn3O4/reduced graphene oxide nanohybrid paper with high energy and power density[J]. Advanced Functional Materials, 2015, 25(47): 7291-7299.
[52] CAO W J, ZHENG J P. Li-ion capacitors with carbon cathode and hard carbon/stabilized lithium metal powder anode electrodes[J]. Journal of Power Sources, 2012, 213(9): 180-185.
[53] MAKINO S, SHINOHARA Y, BAN T, et al. 4 V class aqueous hybrid electrochemical capacitor with battery-like capacity[J]. Rsc Advances, 2012, 2(32): 12144-12147.
[54] MAKINO S, YAMAMOTO R, SUGIMOTO S, et al. Room temperature performance of 4 V aqueous hybrid supercapacitor using multi-layered lithium-doped carbon negative electrode[J]. Journal of Power Sources, 2016, 326: 711-716.
[55] LIU W W, FENG Y Q, YAN X B, et al. Superior micro-supercapacitors based on graphene quantum dots[J]. Advanced Functional Materials, 2013, 23(33):4111-4122.
[56] SHEN B, LANG J, GUO R, et al. Engineering the electrochemical capacitive properties of microsupercapacitors based on graphene quantum dots/MnO2using ionic liquid gel electrolytes[J]. Acs Applied Materials & Interfaces, 2015, 7(45): 25378-25389.
[57] DONG Kun, ZHANG Suojiang, WANG Daxi, et al. Hydrogen bonds in imidazolium ionic liquids[J]. Journal of Physical Chemistry A, 2006, 110(110):9775-9782.
[58] SHEN B, GUO R, LANG J, et al. A high-temperature flexible supercapacitor based on pseudocapacitive behavior of FeOOH in an ionic liquid electrolyte[J]. Journal of Materials Chemistry A, 2016, 4(21):8316-8327.
[59] AHMAD S, DEEPA M, SINGH S. Electrochemical synthesis and surface characterization of poly(3,4-ethylenedioxythiophene) films grown in an ionic liquid.[J]. Embo Journal, 1994, 13(4):914-923.
[60] PRINGLE J M, FORSYTH M, MACFARLANE D R, et al. The influence of the monomer and the ionic liquid on the electrochemical preparation of polythiophene[J]. Polymer, 2005, 46(7):2047-2058.
[61] SUN Y, CHENG Y, HE K, et al. One-step synthesis of three-dimensional porous ionic liquid-carbon nanotube-graphene gel and MnO2-graphene gel as freestanding electrodes for asymmetric supercapacitor[J]. Rsc Advances, 2015, 5(14):10178-10186.
[62] CHOI B G, CHANG S J, KANG H W, et al. High performance of a solid-state flexible asymmetric supercapacitor based on graphene films[J]. Nanoscale, 2012, 4(16):4983-4988.
Progress in application of ionic liquids in hybrid supercapacitor
ZHANG Zhiyi, LI Xi, ZHANG Chaocan
(School of Materials Science and Engineering, Wuhan University of Technology, Wuhan 430070, Hubei, China)
Hybrid supercapacitors are energy-storage devices with great potential, they typically have high specific power, high cycle stability, high safety and relatively high specific energy, but the aqueous and organic electrolytes they use often suffer from drawbacks such as narrow electrochemical window and high flammability. In the meantime, the unique features of ionic liquids, such as low vapor pressure, non-flammability and wide electrochemical window make them ideal electrolytes for hybrid supercapacitors. This paper reviews the recent applications of ionic liquids in hybrid supercapacitors, including ionic liquids as pure electrolytes, components for mixture electrolytes, solid electrolytes and electrodes. Finally, it is pointed out that future research directions for ionic liquids in hybrid supercapacitor system is to improve its moisture stability and cutting down the cost of preparation. Due to the misunderstandings about the notion of hybrid supercapacitor and asymmetric supercapacitor, there has been many inappropriate descriptions about them. In this paper we try to explain the difference between the above-mentioned two kinds of supercapacitors.
ionic liquid; hybrid supercapacitor; asymmetric supercapacitor
10.12028/j.issn.2095-4239.2017.0034
TQ 028.8
A
2095-4239(2017)06-1208-09
2017-03-30;
2017-05-07。
国家自然科学基金项目(51273155)。
张之逸(1992—),男,硕士研究生,研究方向为铝离子混合超级电容器电解质,E-mail:zhangzy032@foxmail.com;
张超灿,教授,研究方向为功能高分子材料,E-mail:polymers@whut.edu.cn。
