基于非钠金属负极的有机钠离子电池研究进展
2017-11-24张慧敏张文峰文越华杨裕生
张慧敏,明 海,张文峰,文越华,杨裕生,明 军
基于非钠金属负极的有机钠离子电池研究进展
张慧敏1,2,3,明 海1,3,张文峰1,3,文越华1,3,杨裕生1,3,明 军4
(1防化研究院,北京 100191;2北京理工大学,北京 100081;3先进化学蓄电技术与材料北京市重点实验室,北京 100191;4中国科学院长春应用化学研究所,吉林长春 130022)
钠和锂元素具有相似的物化性质,且钠资源丰富、分布广泛、原料成本低廉,使得钠离子电池在大规模储能领域表现出极大的应用潜力。与水系钠离子电池相比,有机体系钠离子电池的电化学窗口宽(1.5~4.5 V)、能量密度较高(100~350 W·h/kg),受到了广泛的关注。目前有机系钠离子电池的研究工作多数是在半电池体系(以钠金属为对电极)中针对单一的正极或负极材料进行性能评价,但是金属钠,因为其过于活泼的化学性质会带来严重的安全问题,使其在液态有机体系中几乎不太可能作为商业负极来使用。为了贴近实际应用,构建以非钠金属负极为主的商业化有机钠离子电池体系意义重大。本文基于碳材料、钛基化合物、钠合金、过渡金属氧化物等非钠金属负极材料,并以它们为线索重点介绍一些性能较为突出的有机钠离子电池体系,并指出要实现钠离子电池的产业化,除了要开发高性能、低成本的正负极材料以外,深入研究正/负电极材料相互匹配问题、电解液和黏结剂的优化、隔膜改性等机理也至关重要。
钠离子电池;钠金属;负极材料;有机电解液;全电池
锂离子电池具有工作电压高、容量高、自放电小、功率性能好和循环寿命长等优点,因而被广泛应用于各种电子产品,但由于锂资源储量有限且分布不均,因此有必要开发其它廉价储能技术用于大规模储能以降低风光发电的成本。钠和锂元素具有近似的物化性质,且钠资源丰富、原料成本低廉;另外,钠与铝不会形成合金,钠离子电池的正负极集流体均可以使用成本低廉的铝箔,这些都使得钠离子电池成为非常有发展潜力的储能体系。另外考虑到Na+/Na的电化学当量(23.00)是Li+/Li的3倍还多(6.94),钠离子的半径(1.02 Å,1 Å=10-10m)比锂离子(0.76 Å)的大很多,由此使得钠离子电池的质量比能量和体积比能量都低于锂离子电池,虽然其在电动汽车上的应用优势不大,但作为规模储能电池用于电网的潜力巨大[1-3]。
目前,室温钠离子电池根据电解液的类型主要分为有机和水体系两类。水电解液体系的电化学窗口窄,水的热力学电化学窗口为1.23 V,即使考虑到动力学因素,水系钠离子电池的电压也不可能高于1.5 V,过低的电压窗口导致了其较低的能量密度(约40 W·h/kg)。而有机体系的工作电压范围一般为1.5~4.5 V,高电压区间意味着有机体系的钠离子电池具有比较高的能量密度(100~350 W·h/kg),确保了其高的性价比和良好的应用前景。此外,钠的离子半径(0.102 nm)比锂离子和质子大许多,在水溶液中的溶剂化离子半径更大(0.358 nm),使得钠离子在嵌入反应过程中容易造成晶体结构坍塌,影响电极材料的充放电循环稳定性;再加上许多钠盐化合物在水中的溶解度很大,或遇水容易分解,这些都限制了储钠材料的选择与水系钠离子电池的性能[4]。
相比之下,有机体系的钠离子电池不存在上述问题,在容量利用率和循环寿命方面也基本达到应用要求。如今大部分的钠离子电池的研究工作多数是以钠金属为对电极与正极或负极材料组成半电池体系对电极材料进行性能评价,而钠金属的使用存在严重的安全问题,使其在液态有机体系中几乎不太可能作为商业负极来使用。此外,由于钠金属作为对电极可以提供富足的钠离子和较低的电压平台,因此以钠金属作为对电极研究电极材料的电化学性能往往存在片面性。因此非钠金属负极的有机钠离子电池的研究需要引起重视,这是促进有机钠离子电池应用的关键一环。鉴于此,人们已开始了对非钠金属负极的有机体系钠离子电池进行研 究[5-6]。非钠金属负极材料主要包括碳材料、钛基化合物、钠合金、过渡金属氧化物等。碳基与钛基材料,虽然比容量较低,但循环过程中结构稳定,因而具有良好的循环稳定性。钠合金、过渡金属氧化物具有高的比容量,但可逆转化反应与合金化过程伴随巨大的体积变化,造成材料结构容易粉碎与坍塌,导致容量迅速衰减。因此,对非钠金属负极材料的研究迫在眉睫。另外,有机体系钠离子全电池的研究仍是新电池体系的一个前进和优化过程,在实际应用研究中仍存在许多问题,如低循环寿命、低库仑效率、正负极不匹配诱发的新型副反应等。本综述基于碳材料、钛基化合物、钠合金、过渡金属氧化物等非钠金属负极材料重点介绍近几年报道的有机钠离子电池体系,以分析钠离子全电池组装过程中的正负极选择/匹配机制、电解液或黏结剂优化、电极材料改性等对电池性能的影响,为钠离子全电池的应用发展提供科学借鉴。
1 非钠金属负极的有机钠离子全电池
1.1 碳基负极材料
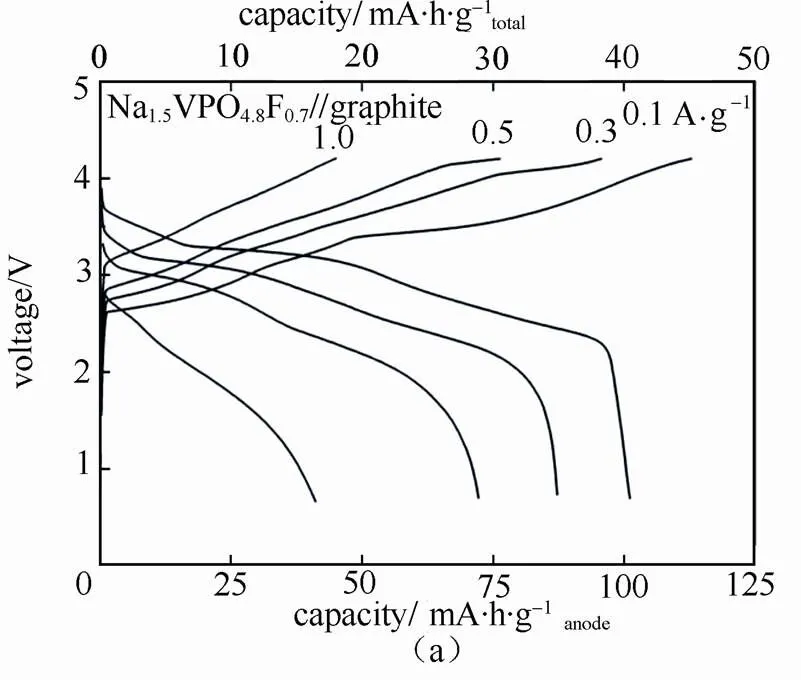
由于钠的离子半径比锂离子的约大30%,使得常规石墨作为钠离子电池负极材料的优势并不大。但鉴于石墨低成本、高化学稳定性、工艺成熟等特性,石墨仍是钠离子电池负极研究的热点。例如,WEN等[7]通过氧化和部分还原石墨的方法扩大石墨的层间距,其可逆容量在20 mA/g的电流密度下达284 mA·h/g,循环2000次后容量保持率仍有73.92%。后来ADELHELM等[8]利用溶剂(二甘醇二甲醚)共嵌入的方法使钠嵌入石墨中,储钠电位约为0.6 V,循环1000次后可逆比容量约为100 mA·h/g。在此基础上,KIM等[9]研究了不同链长的乙醚基电解液溶剂对石墨嵌钠行为的影响,将其与Na1.5VPO4.8F0.7正极组装成钠离子全电池,平均工作电压为2.92 V,该体系在0.5 A/g的电流密度下循环250次后容量保持率仍有70%,能量密度可达120 W·h/kg(基于所有电活性物质质量之和),如图1(a)~(b)所示。HAN等[10]还利用激光打孔的方法制备多孔柔性石墨膜,并以其为负极,以Na3V2(PO4)3为正极,利用Na-溶剂共插层的机理装配了钠离子全电池。该体系能量密度可达130.7 W·h/kg(基于所有电活性物质质量之和),在100 mA/g的电流密度下循环500次后容量保持率高达92%。
相较于石墨,硬碳的层间距较大且结构无序,可逆比容量较高,也已广泛应用于钠离子电池研究。2010年后,以硬碳作为负极,以过渡金属层状氧化物为正极的全电池研究也越来越多,电池的能量密度也获得显著提升。KOMABA等[11]报道了以硬碳为负极,以O3型Na[Ni1/2Mn1/2]O2为正极的钠离子全电池,电池的平均工作电压为3 V,容量达到200 mA·h/g(基于负极活性物质的质量),且该电池的倍率性能优异,即使电流密度高达300 mA/g,其容量也没有明显衰减,质量比能量为高比能石墨/ LiCoO2锂离子电池的60%。但是Na[Ni1/2Mn1/2]O2中锰元素不具备电化学活性,WANG等[12]用较轻的钛元素部分取代锰元素,利用简单的固相反应制备了O3型层状氧化物NaNi0.5Mn0.3Ti0.2O2,以该材料作为正极,以预嵌钠的硬碳为负极组装成钠离子全电池,可逆容量可达131 mA·h/g(基于正极活性物质的质量)。
类似的,KIM等[13]合成了正极Na[Ni1/3Fe1/3Mn1/3]O2,并以硬碳为负极、1 mol/L NaClO4的PC溶液为电解质溶液,组装得到的钠离子全电池容量保持率良好,75 mA/g的电流密度下循环150次后容量仍有100 mA·h/g,不过该正极材料在空气中不稳定,对水蒸气及二氧化碳比较敏感,不能长时间在空气中保存,所以在实际应用方面仍有一定的困难。2015年韩国汉阳大学的SUN课题组[14]合成了具有浓度梯度径向排列的多层柱状结构的正极材料Na[Ni0.75Co0.02Mn0.23]O2-Na[Ni0.58Co0.06Mn0.36]O2,并与负极硬碳装配成钠离子全电池,该全电池在15 mA/g的电流密度下的可逆容量为157 mA·h/g,稳定循环300次以上的容量保持率为80%,甚至在10 C(1500 mA/g)高倍率下的容量也能保持132.6 mA·h/g,平均工作电压为3.2 V。该钠离子全电池模型与商业化锂电池模型极其相似,正负极分别是层状氧化物和嵌入性硬碳,充分说明了钠离子电池的商业化应用前景。
对于O3相氧化物,Na+的脱出嵌入过程中会发生相变,从而导致循环不稳定。虽然可以通过控制电压进而限制容量以使循环稳定,但是O3相材料在空气中不稳定。胡勇胜等[15]提出了用无毒便宜的Cu元素代替层状氧化物中的Ni、Co元素,通过简单的固相共混法制备了在空气中稳定的正极O3-Na0.9[Cu0.22Fe0.30Mn0.48]O2,该材料的平均储钠电位约为3.2 V,可逆容量为100 mA·h/g。若采用硬碳负极,以0.8 mol/L NaPF6/EC∶DMC(1∶1体积比)作为电解液组装得到的钠离子全电池,工作电压为3.2 V,能量密度可达210 W·h/kg,即使是在6 C的高倍率下容量仍能达到初始容量的74%。该体系中的正负极材料均源于环境友好且价格低廉的元素,有着很好的实际应用前景。
为了进一步提高钠离子全电池的能量密度,YOSHIDA等[17]报道了P2-Na2/3[Ni1/3Mn2/3]O2,它的理论容量可以达到180 mA·h/g,平均储钠电位为3.5 V,且该材料在水中可以稳定存在,一定程度上可以降低电池成本。LI等[16]以单分散的硬碳微球为负极,以P2-Na2/3[Ni1/3Mn2/3]O2为正极,基于1 mol/L NaClO4的EC/DEC(1∶1,体积比)电解液组装成全电池,工作电压为3.5 V,其能量密度为200 W·h/kg,该全电池中负极活性物质的容量可达300 mA·h/g,循环150次后容量保持率为73%。但是当P2型氧化物中Na的含量低于0.33时,材料就会从P2型向O3型氧化物转变,从而导致材料的循环稳定性和倍率性能变差。
为了改善P2型层状氧化物的循环稳定性,2014年,YOSHIDA等[17]用Ti部分取代了Mn,合成了P2-型Na2/3Ni1/3Mn1/2Ti1/6O2正极材料,该材料的平均储钠电位为3.7 V,可逆容量达170 mA·h/g。以硬碳为负极,得到的全电池平均工作电压为3.7 V,能量密度高达300 W·h/kg,接近石墨/LiCoO2锂离子电池体系能量密度的80%。
为了进一步提高电极材料的稳定性,聚阴离子正极材料也受到了广泛关注。研究者采用聚阴离子型化合物作为正极,并以硬碳作为负极进行了钠离子全电池的研究。聚阴离子型化合物是指含有四面体或者是八面体的阴离子结构单元的化合物的总称。这些结构单元通过强共价键连成三维网络结构,使得聚阴离子型化合物正极材料具有和金属氧化物正极材料不同的晶相结构以及由结构决定的各种突出的性能,如较高的电压和结构稳定性。这类化合物主要包括NaMPO4(M 为过渡金属)、NaMPO4F、焦磷酸盐和NASICON钠离子超导体、普鲁士蓝化合物等[18]。
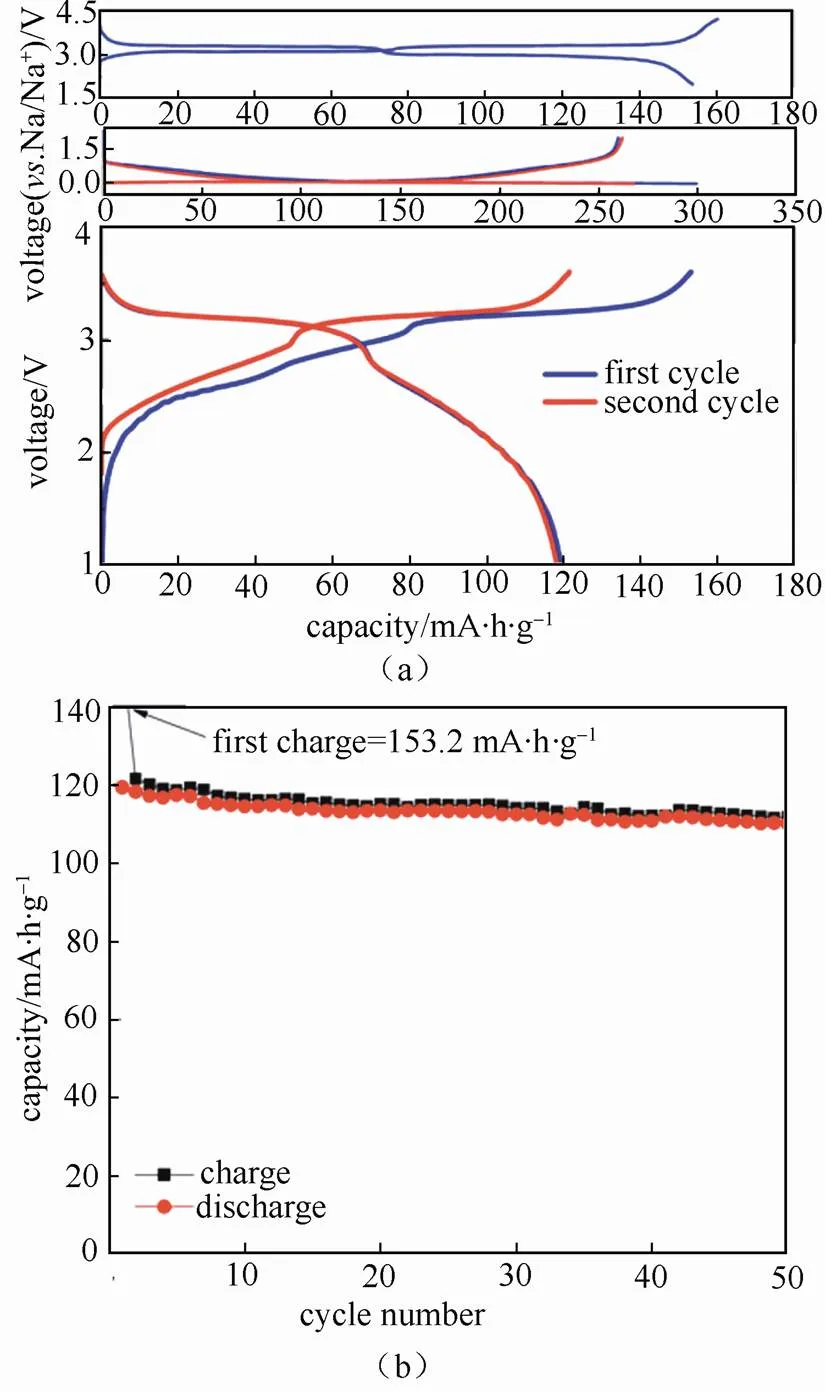
REN等[19]合成了3D网络结构的Na3V2(PO4)3,该材料的平均储钠电位高达3.4 V,倍率性能优异,在150 C的高倍率下容量仍有77 mA·h/g,以Na3V2(PO4)3为正极,硬碳作为负极组装得到的全电池,工作电压为3.3 V,能量密度高达350 W·h/kg。BARKER等[20]率先提出了以硬碳为负极,氟磷酸化合物NaV(PO4)F为正极,并以1 mol/L NaClO4的EC/DMC(质量比为2∶1)溶液为电解液,虽然组装成的钠离子全电池循环了30次之后容量保持率只为50%,但是其工作电压却达到3.7 V。NOSE 等[21]制备了一种新型的钠离子电池正极材料钴基磷酸焦磷酸盐Na4Co3(PO4)2P2O7,该材料具有3D开放离子通道,该材料的平均储钠电位高达4.5 V,容量可以达到95 mA·h/g,在70s内放电容量可达到80 mA·h/g。将其与硬碳负极构成的钠离子全电池工作电压为4.0 V,循环50次后容量保持率为93%,循环100次后容量保持率仍有83%,如图1(c)和1(d)所示,不过使用钴等元素比较昂贵,所以这类材料是否可以作为储能材料还有待深入研究。
另外,普鲁士蓝化合物是一类具有开放式框架结构的钠离子电池正极材料,这类材料拥有三维的钠离子嵌脱通道、高的理论容量、可调的氧化还原反应电位且容易合成,是一种极具应用潜力的钠离子电池正极材料。但其结晶水和配位水在高压下的分解会降低首次库仑效率,并且分解产物留在电解液中会对电池的循环稳定性产生不良影响。SONG等[22]研究了配合水对钠锰铁氰化物结构及电化学性能的影响,并以脱水钠锰铁氰化物Na2-MnHFC为正极,硬碳为负极得到电化学性能良好的钠离子全电池(图2),工作电压为3.5 V,合适的电流密度下电池的容量可以达到140 mA·h/g,甚至在2 C的倍率下容量仍可保持在96 mA·h/g。此外,由于受到合成条件等因素的影响,普鲁士蓝晶体内部很容易产生大量的晶格缺陷,不利于其结构的稳定性,所以普鲁士蓝化合物实用化仍面临着多方面的 挑战。
综上所述,以硬碳为负极组装成的钠离子全电池能量密度分布在200~300 W·h/kg(基于正极和负极的活性物质质量之和),一些体系的能量密度甚至能超过300 W·h/kg,可以与锂离子电池相匹敌。但是,硬碳作为负极,嵌钠行为主要集中在0 V附近,低的嵌钠平台在高倍率的条件下会由于钠金属的析出而形成钠枝晶,造成内部局部短路,从而出现安全问题。另外,碳材料的密度1.7 g/cm3也会造成钠离子全电池体系的体积比能量偏低,为了满足其应用需求,新型电解液以及添加剂的开发、固态电解质隔膜的应用等手段用以辅助改善钠离子电池的安全性也十分必要。
1.2 钛基化合物
四价钛元素在空气中可以稳定存在,且Ti4+/Ti3+的氧化还原电位处于0~2 V之间(. Na/Na+),不同结构中表现出的储钠电位不一样,合适的电位可以避免钠枝晶的形成,使得钛基化合物的安全性能高于硬碳,同时钛基化合物的倍率性能也优于碳,因此,Ti的氧化物作为钠离子电池的负极得到了广泛关注[23]。TiO2、Na2TiO2n+1、NaTi2(PO4)3是具有代表性的3类钠离子电池钛基负极材料。
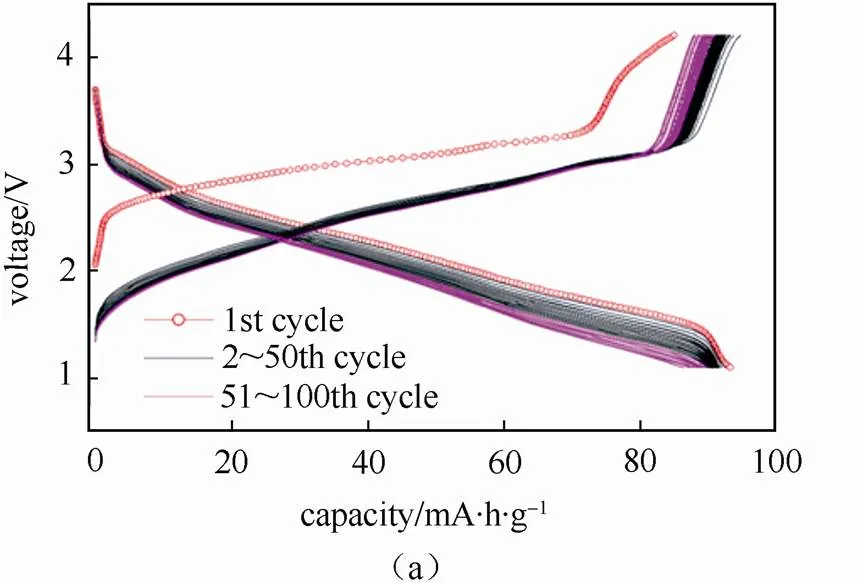
最常见的含钛化合物是TiO2,XIONG等[24]通过自组装的方法合成了无定形TiO2纳米管(TiO2NT),发现直径大于80 nm的TiO2NT才能够支持钠离子发生电化学循环,该电极循环15次后可逆容量仍有150 mA·h/g。并以此为负极,以Na1.0Li0.2Ni0.25Mn0.75O为正极,基于1 mol/L NaClO4的PC溶液为电解液组装成钠离子全电池,该电池平均工作电压为1.8 V,在11 mA/g的电流密度下放电容量约为80 mA·h/g,虽然钛基化合物电极的容量低于碳材料,但是其倍率性能优异:在11 C的高倍率下容量保持率仍能达到70%,如图3(a)所示。Na2TiO2n+1也可以写成Na2O·TiO2(=3~8),该类化合物具有单斜层状结构,在钠离子电池中,研究者对Na2Ti3O7(=3)及Na2Ti6O13(=6)的嵌钠行为研究较多。XU等[25]制备了碳包覆的Na2Ti3O7,该材料的首次充放电过程对应2个Na+的可逆脱嵌,容量可达177 mA·h/g,循环100次后容量仍可保持115 mA·h/g。若以Na2Ti3O7作为负极,Na0.80Li0.12Ni0.22Mn0.66O2作为正极组装成钠离子全电池,由于Na2Ti3O7的超低储钠电位(约为0.35 V,Ti4+/Ti3+),全电池工作电压高达3.1 V,可以与商用的锂离子电池相比拟,足以点亮一个2.5 V的LED灯泡,如图3(b)~(c)所示。该电池在0.1C倍率下循环25次后负极容量为105 mA·h/g,能量密度为100 W·h/kg(相对于正负极活性物质的质量之和),略低于锂离子电池,但由于Na不会与Al形成合金,所以Al可以作为集流体应用于钠离子电池的正负极,从而可进一步提高能量密度、降低成本。ZHANG等[26]利用Na2Ti3O7纳米管作为负极,VOPO4纳米片为正极,组装的全电池平均工作电压为2.9 V,能量密度高达220 W·h/kg(相对于正负极活性物质的质量之和),即使考虑到集流体、电解液质量等因素,预计该体系的实际能量密度仍可达到132 W·h/kg,可以与锂离子电池相媲美。Na2Ti6O13(=6)具有良好的倍率及循环性能,RUDOLA等[27]采用CTAB软模板法合成了具有优异倍率性能和循环稳定性的Na2Ti6O13纳米棒状材料,如图3(d)所示,在20 C的高倍率下循环5000次后容量保持率高达85%。以Na2Ti6O13纳米棒作为负极,Na3V2(PO4)2F3/C为正极,基于1mol/L NaClO4的EC∶PC(1∶1,体积比)基电解液,组装成平均工作电压为2.5 V的全电池,该体系在C/5的倍率下容量为42 mA·h/g(基于负极活性物质的质量),比容量较低但安全性好,适用于大规模储能领域。

IVANOVA等[28]根据锂离子电池负极Li4Ti5O12的储锂机理,以Li4Ti5O12为负极,P3-Na3/4Co1/3Ni1/3Mn1/3O2为正极、LiPF6的EC/DMC溶液为电解液组装成钠锂离子全电池,该电池的平均工作电压为2.35 V,可逆容量为100 mA·h/g。他还提出了该混合钠锂离子全电池的电化学反应机理,认为在开始的可逆循环中是锂离子和钠离子的同时脱嵌,而在后面的循环中锂离子的脱嵌占主导地位。这个体系的研究开启了钠锂离子混合全电池的研究。胡勇胜等[29]借鉴尖晶石结构Li4Ti5O12储钠机理,制备了无应变正极P2-Na0.66[Li0.22Ti0.78]O2,该材料最大的特点是其优异的循环稳定性,在2 C的倍率下循环1200次后容量保持率仍有75%。若以碳包覆的Na3V2(PO4)3作为正极,基于1 mol/L NaPF6的EC∶DEC(4∶6的体积比)为电解液组装成钠离子全电池,尽管未经任何优化,得到的电池电化学性能仍良好,如图4(a)~(b)所示。这类全电池对于加速室温长寿命钠离子电池的发展有着重要的价值。胡勇胜等[30]还以Na+和空位无序规律为基础,选择了离子半径相似的Ti4+和Cr3+,设计了P2-Na0.6[Cr0.6Ti0.4]O2层状材料。由于该材料在钠离子脱出的时候Cr的化合价可以由3+氧化到4+,在钠离子嵌入的时候Ti的化合价可以从4+还原到3+,这样就使得该材料可同时用作正负极材料。作为负极时,该材料的平均储钠电位为0.8 V,可逆比容量约为108 mA·h/g,对应0.4个Na+可逆脱嵌。作为正极时,该材料的平均储钠电位为3.5 V,可逆比容量约为74 mA·h/g,对应0.26个Na+的可逆脱嵌。该材料具有较好的倍率性能,利用其既作正极又作负极,基于0.8 mol/L NaPF6的EC/DEC(4∶6,体积比)电解液组装对称钠离子全电池。经测试,发现该电池12 C倍率下的容量是1 C倍率下的75%。1 C的倍率下的能量密度估算为82 W·h/kg,如图4(c)~(d)所示。该体系比较适合用于对功率性能、循环寿命和成本要求较高但对能量密度要求不太高的大规模储能。
虽然钛基负极材料具有高安全性、循环稳定、环境友好等优点,但钛基负极材料也存在导电性能差、容量较低等缺点,且多数钛基负极材料的储钠机理也不是很明确,这些都限制了钛基负极材料的进一步应用。鉴于此,研究者可以通过掺杂、包覆来提高其导电性能,也可以与高比容量的负极复合来提高其容量。此外,由于目前钛基化合物作为负极,以层状氧化物为正极组装成的全电池能量密度主要集中在250 W·h/kg以下,为了提高该体系的能量密度,对正负极匹配问题的研究也是至关重要的。

1.3 合金负极材料
合金类材料的比容量(质量比容量和体积比容量)较高,可有效提高电池的能量密度,因此钠合金得到了广泛的研究。Na可以与很多金属或半导体元素形成合金,主要集中在第IVA和VA族元素,N、P、As、Sb、Bi可以结合3个Na,Sn和Pb可以与3.75个Na发生合金反应。不过合金类材料在嵌钠过程中体积形变比较大,导致材料易粉化,合金材料颗粒聚集长大造成极片脱落,从而使电池循环性能变差。为了解决上述问题,科研人员主要采用如下几种方法:将合金材料分散在没有电化学活性的基质(如Fe、Cu、FeSi2、Al2O3、SiC等),这类方法可有效缓冲活性物质的体积膨胀,但是由于这些基质本身不具备电化学活性,所占比重不宜太大。另外也有人将合金材料分散到有电化学活性的基质中,利用两种元素活性电位的不同,当一种元素发生反应的时候,而另一种元素不参与反应,这样也可起到缓冲体积膨胀的作用(如Sn-Sb合金),或者利用合金反应和转换反应的不同步来缓冲体积膨胀(SnS、SnS2等)。当然也有研究者利用碳材料机械强度高、体积膨胀小、离子电导率好的优点将电极活性物质与碳材料复合来进行改性,或将材料纳米化而使其能承受更大的内应力,进而抑制材料的体积膨胀和粉碎脱落[31]。
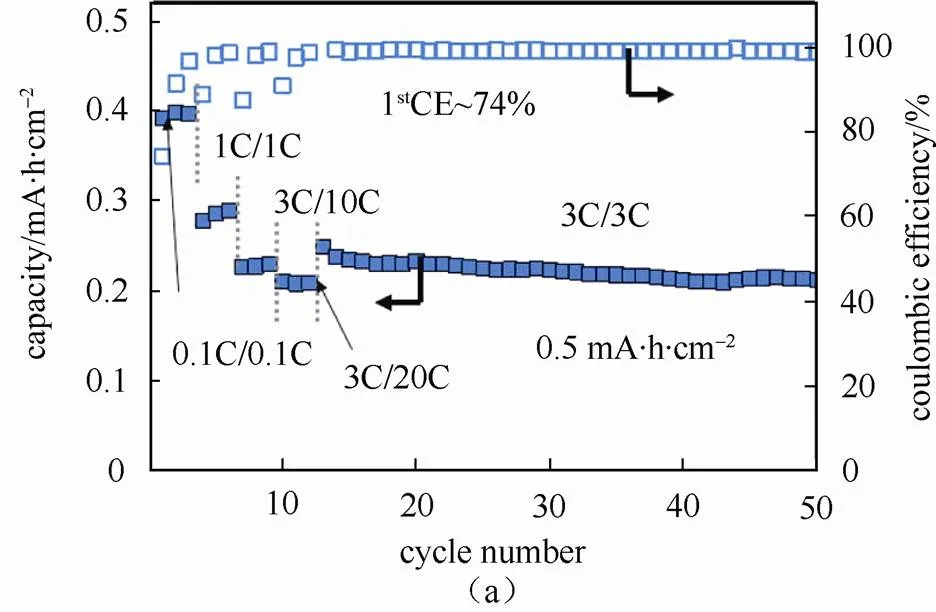
ZHAO等[32]将Sb和膨胀石墨进行复合得到的电极材料密度高达2.5 g/cm3,体积比容量为658 mA·h/cm3,是传统硬碳材料的2~3倍。将该电极材料作为负极、1mol/L NaPF6的EC(2% FEC,体积分数)溶液为电解液与正极材料钠锰铁氰化物(NMHFC)组装成钠离子全电池,其容量可达0.5 mA·h/cm2。该电池在3 C倍率下充电、20 C下放电的电压滞后与0.1 C倍率下充放电相比仅仅增加了600 mV,容量保持率还有50%,即使在3 C的倍率下循环40次仍有80%的容量保持率,表现出良好的倍率性能,可以与高功率锂离子电池相匹敌(图5)。
LIANG等[33]利用模板法制备得到了高度有序、间隔较大(190 nm)的一维Sb纳米棒状材料,以此材料作为负极可不添加黏结剂和添加剂,0.2 C的倍率下循环100次容量高达620mA·h/g,循环250次后容量仍能保持84%,在20 C的高倍率下可逆容量仍有557.7 mA·h/g。当与正极P2-Na2/3Ni1/3Mn2/3O2、1.0 mol/L NaClO4的EC/PC(体积比1 : 1,5%FEC)电解液组装成钠离子全电池,平均工作电压为2.9 V,循环110次后容量仍高达620 mA·h/g(保持率为94%,相对于Sb的质量),循环从110次增加至130次后电池的容量衰减到450 mA·h/g,这主要是因为Sb形貌的变化造成的,然而在0.5 A/g的高电流密度下循环至250次容量仍有334 mA·h/g。另外从能量比较图也可以发现,该体系的功率密度远高于商用锂离子电池,能量密度远高于电化学电容器,这些都使其在储能方面的应用成为可能(图6)。
为了改善合金负极材料的循环性能,很多人利用合金反应和转换反应的不同步来缓冲体积膨胀,如SnO和SnS的提出,但是在合金化的过程中还是会产生较大的体积膨胀。LU等[34]利用硬碳和还原氧化石墨烯来改性SnS(SnS/G+C),缓冲其在充放电过程因合金化产生的体积膨胀。同时以SnS/G+C作为负极,以Na3V2(PO4)2F3为正极,1.0 mol/L NaPF6的EC/DEC(体积比为1∶1)电解液组装成钠离子全电池,并与Na3V2(PO4)2F3//SnO体系作了对比,如图7(a)~(b)所示。Na3V2(PO4)2F3//SnO的首次库仑效率仅为29.5%(322/95 mA·h/g),Na3V2(PO4)2F3//SnS/G+C的首次库仑效率可以达到63.4%(504/319 mA·h/g)。SUN等[35]还利用棒状Bi2S3作为负极,Na3V2(PO4)3作为正极,组装成钠离子全电池,在100 mA/g的电流密度下容量为340 mA·h/g,但是该材料的体积膨胀比较严重。

LI等[36]通过向Sb中引入Mo缓冲Sb循环后的体积膨胀,并且利用碳进行包覆进一步降低由合金化产生的应力,得到的Mo3Sb7@C材料作为负极时,在0.2 C的倍率下容量可达400 mA·h/g,即使是在20 C的高倍率下容量仍可保持180 mA·h/g,并且在0.5 C的倍率下循环800次之后的容量保持率高达91.8%。其与Na3V2(PO4)3@C正极组成的全电池图7(c)~(d),平均工作电压为2.5 V,在0.2A/g的电流密度下,可逆容量高达320 mA·h/g(基于负极活性物质的质量),循环20次后容量保持率高达98%。

合金类材料的比容量较高,可以有效提高电池的能量密度,并且采用合金作为钠离子电池负极可以有效避免由钠单质产生的枝晶问题,因而可以提高钠离子电池的安全性、延长钠离子电池的使用寿命。合金材料作为钠离子电池的负极,如何抑制其体积膨胀,提高黏结剂的力学性能和导电性能也显得尤为重要。但是钠原子在材料中所占的体积是锂原子所占体积的2倍,而其体积能量密度却远远低于相应的锂合金,使得这种合金的应用在一定程度上受到了限制。
1.4 其它负极材料
过渡金属氧化物凭借其较高的容量已广泛作为锂离子电池负极材料进行研究,该类材料也可以作为钠离子电池的负极材料。除了上述几种常见的钠离子负极材料,意大利罗马大学的HASSOUN 等[37-38]研究了不同的氧化物(MCMB-CuO,MCMB-NiO,MCMB-Fe2O3)在钠离子电池中的电化学性能。OH[39]利用碳包覆的Fe3O4作为负极、层状的 Na[Ni0.25Fe0.5Mn0.25]O2作为正极、以NaClO4作为电解质、FEC和甲磺酸乙酯作为溶剂,组装钠离子全电池体系。该电池的工作电压约为2.4 V,循环100次后的容量保持率为82.8%。另外,MING等[40]也报道了多孔碳负载Fe3O4作为负极,Na2FeP2O7为正极的全铁系钠离子全电池,提出了一种基于铁基的环境友好可持续发展的钠电池。图8显示该电池的容量为93 mA·h/g,平均工作电压为2.28 V,循环100次后容量保持率为93.3%。该电池的能量密度可达到203 W·h/kg(相对于正极活性物质的质量)。HARIHARAN等[41]利用α-MoO3作为负极时首次嵌钠和脱钠容量高达771 mA·h/g和410 mA·h/g,且在0.2 C的倍率下循环500次后的容量保持率为55%。当以该材料为负极、以1.0 mol/L NaClO4的EC/PC(体积比1∶1)为电解液、Na3V2(PO4)3为正极组装的钠离子全电池,平均工作电压为1.4 V,放电容量约为164 mA·h/g。
从电化学角度说,单质磷(P)具有较小的原子量和较强的钠离子嵌入能力,其理论嵌钠容量可达2600 mA·h/g。在各种单质磷的同素异形体中,红磷是电子绝缘体,并不具备电化学活性,而正交结构的黑磷由于具有类似石墨的结构,且具有较大的层间距,目前研究较多。CHEN等[42]将黑磷、石墨化炭黑、多壁碳纳米管高能球磨合成了磷含量高达70%(质量分数)的纳米复合材料(BPC),BPC作为钠离子电池的负极首次库仑效率达到90%以上,在1.3 A/g的电流密度下循环100次容量还有1700 mA·h/g(基于黑磷的质量)。以该复合材料为负极,以Na0.66Ni0.26Zn0.07Mn0.67O2为正极,组装得到的全电池体系倍率性能优异,120 mA/g电流密度下容量可保持12 mA/g时的90%。受正极材料容量的限制,该体系的放电容量为92.1 mA·h/g,若与Na2/3Ni1/3Mn2/3O2匹配,可进一步提高全电池体系的容量和能量密度。磷基材料是一种容量较高的储钠材料,目前需要解决的问题主要是如何抑制钠离子嵌脱过程中材料的体积膨胀。


1.5 对称型钠离子全电池
现阶段大多数的钠离子全电池都是非对称的,但全对称的钒基、钛基钠离子全电池也已被提出。对称的钠离子全电池由于正负极有着相同的活性材料使得电池能承载一定程度的过充,缓冲一定的体积膨胀,并且可以极大地简化加工工艺,降低生产成本,所以对称型的钠离子全电池的研究也相当重要。
Na3V2(PO4)3表现出两个电压平台,分别在3.4 V和1.65 V,对应V3+/V4+和V2+/V3+的氧化还原电对,可同时作为钠离子电池的正负极。理论比容量为117.6 mA·h/g,能量密度为400 W·h/kg。LI等[47]利用Na3V2(PO4)3/C作为正负极、1 mol/L NaClO4/EC+DMC为电解液组装成钠离子全电池,还研究了乙炔黑(AC)、碳纳米管(CNT)、石墨(graphite)这3种不同碳基质对电池性能的影响。发现以Na3V2(PO4)3/AC为电极材料得到的全电池性能最好,该体系在1 C倍率下循环200次的容量保持率为80%,能量密度为185.5 W·h/kg,功率密度可达5000 W/kg(图10)。HUNG等[48]利用sp2杂化的碳包覆介孔Na3V2(PO4)3兼作正负极,研究了对称型Na3V2(PO4)3全电池的电化学性能,该体系倍率性能优异,在0.1 A/g的电流密度下循环100次后容量保持率仍高达92.2%。
Na3Ti2(PO4)3表现出两个电压平台,分别在2.1 V和0.4 V,对应Ti3+/Ti4+和Ti2+/Ti3+电对,SENGUTTUVAN等[49]利用其制备了全钛基钠离子电池,并证明了开发基于Ti2+/Ti3+的低电势电极材料的可能性。
不过很多对称型的钠离子全电池存在着循环稳定性差、能量密度低的缺点。GUO等[50]制备了O3-Na0.8Ni0.4Ti0.6O2,该材料拥有Ni4+/Ni2+(3.5 V)和Ti4+/Ti3+(0.7 V)两个氧化还原电对,基于该材料的正负极,以1 mol/L NaClO4的PC(2% FEC,体积分数)溶液为电解液进行电池组装,得到的钠离子全电池工作电压为2.8 V,可逆容量达85 mA·h/g,能量密度在0.2 C的倍率下为96 W·h/kg。该电池在1 C的倍率下循环150次后容量保持率为75%,如图11(a)~(b)所示。GUO等[51]还制备了双极性电极材料P2-Na0.66Ni0.17Co0.17Ti0.66O2,以其作为正负极,正极的电势高达3.74 V(. Na+/Na),负极的电势为0.69 V(. Na+/Na),基于该材料的对称全电池有着优异的电化学性能,工作电压约为3.10 V,循环100次后的容量保持率为94.8%,循环1000次后的容量保持率仍有75.9%,甚至在2 C的高倍率下容量也能保持65 mA·h/g。

图10 Na3V2(PO4)3/AC, Na3V2(PO4)3/CNT和Na3V2(PO4)3/graphite对称钠离子全电池的(a)倍率性能;(b)循环性能[47]
近年来,除了无机化合物,有机物在钠离子电池中也得到了人们的关注,主要是因为有机物来源广泛、价格低廉,且具有多电子转移反应和可调的电化学窗口等优点[52-54]。WANG等[55-56]通过“锅式”绿色反应制备了Na4C8H2O6,该材料可兼作正负极使用,分别对应烯醇基团在1.6~2.8V(Na2C8H2O6/ Na4C8H2O6)和羧基在0.1~1.8 V(Na4C8H2O6/ Na6C8H2O6)间的氧化还原反应。基于该材料的对称钠离子全电池平均工作电压为1.8 V,在0.1 C的倍率下循环100次后的容量保持率仍有76%,能量密度大约为65 W·h/kg,如图11(c)~(d)所示。不过作为电极材料,有机化合物有个比较严重的缺点就是它的导电性能比较差,从而导致倍率性能差,当倍率增加到0.2 C时电极就会出现明显的极化,同时伴随着工作电压和容量的降低,所以提高有机物导电性能是解决其实用化的关键。


表1 典型的钠离子全电池体系
① 基于负极活性物质的质量,② 相对于正负极活性物质的质量之和。
2 总结与展望
发展非钠金属体系的有机钠离子电池是高比能钠离子电池的首选,是其走向规模储能商业化应用的关键一步(表1总结了近年来典型的钠离子全电池体系)。但目前钠离子电池的能量和功率密度是制约其发展的瓶颈,主要根源在于目前缺乏同时具有高比容量和高倍率性能的正负极材料。并且钠离子全电池体系的研究理论体系还有待于进一步完善;为了提高其电化学性能和安全性,也应深入研究正/负电极相互匹配问题、电解液和黏结剂的优化、固态电解质、隔膜改性等。此外,作为规模储能电池除了追求高能量密度之外,其成本也是不得不考虑的因素;因此在设计钠离子全电池体系时,确保电池性能的同时优先选择含有Fe、Mn等资源丰富元素的电极材料。当然,随着固态电解质技术的发展,采用钠金属或者钠合金的全固态钠离子全电池也是未来高比能钠离子电池的一个发展方向。
[1] BARKER J, SAIDI M Y, SWOYER J L. A sodium-ion cell based on the fluorophosphate compound NaVPO4F[J]. Electrochemical and Solid-State Letters, 2003, 6(1): A1-A4.
[2] KIM S W, SEO D H, MA X, et al. Electrode materials for rechargeable sodium-ion batteries: Potential alternatives to current lithium-ion batteries[J]. Advanced Energy Materials, 2012, 2(7): 710-721.
[3] YABUUCHI N, KUBOTA K, DAHBI M, et al. Research development on sodium-ion batteries[J]. Chemical Reviews, 2014, 114(23): 11636-11682.
[4] 杨汉西, 钱江锋. 水溶液钠离子电池及其关键材料的研究进展[J]. 无机材料学报, 2013, 28(11): 1165-1171.
YANG H X, QIAN J F. Recent development of aqueous sodium ion batteries and their key materials[J]. Journal of Inorganic Materials, 2013, 28(11): 1165-1171.
[5] SHACKLETTE L W, JOW T R, TOWNSEND L. Rechargeable electrodes from sodium cobalt bronzes[J]. Journal of the Electrochemical Society, 1988, 135(11): 2669-2674.
[6] DESILVESTRO J, HAAS O. Metal oxide cathode materials for electrochemical energy storage: A review[J]. Journal of the Electrochemical Society, 1990, 137(1): 5C-22C.
[7] WEN Y, HE K, ZHU Y, et al. Expanded graphite as superior anode for sodium-ion batteries[J]. Nature Communications, 2014, 5: doi: 10.1038/ncomms5033.
[8] JACHE B, ADELHELM P. Use of graphite as a highly reversible electrode with superior cycle life for sodium-ion batteries by making use of Co-intercalation phenomena[J]. Angewandte Chemie International Edition, 2014, 53(38): 10169-10173.
[9] KIM H, HONG J, PARK Y U, et al. Sodium storage behavior in natural graphite using ether-based electrolyte systems[J]. Advanced Functional Materials, 2015, 25(4): 534-541.
[10] HAN P, HAN X, YAO J, et al. Flexible graphite film with laser drilling pores as novel integrated anode free of metal current collector for sodium ion battery[J]. Electrochemistry Communications, 2015, 61: 84-88.
[11] KOMABA S, MURATA W, ISHIKAWA T, et al. Electrochemical Na insertion and solid electrolyte interphase for hard-carbon electrodes and application to Na-ion batteries[J]. Advanced Functional Materials, 2011, 21(20): 3859-3867.
[12] WANG H, GU M, JIANG J, et al. An O3-type NaNi0.5Mn0.3Ti0.2O2compound as new cathode material for room-temperature sodium-ion batteries[J]. Journal of Power Sources, 2016, 327: 653-657.
[13] KIM D, LEE E, SLATER M, et al. Layered Na[Ni1/3Fe1/3Mn1/3]O2cathodes for Na-ion battery application[J]. Electrochemistry Communications, 2012, 18: 66-69.
[14] HWANG J Y, OH S M, MYUNG S T, et al. Radially aligned hierarchical columnar structure as a cathode material for high energy density sodium-ion batteries[J]. Nature Communications, 2015, 6: 6865.
[15] MU L, XU S, LI Y, et al. Prototype sodium-ion batteries using an air-stable and Co/Ni-free O3-layered metal oxide cathode[J]. Advanced Materials, 2015, 27(43): 6928-6933.
[16] LI Y, XU S, WU X, et al. Amorphous monodispersed hard carbon micro-spherules derived from biomass as a high performance negative electrode material for sodium-ion batteries[J]. Journal of Materials Chemistry A, 2015, 3(1): 71-77.
[17] YOSHIDA H, YABUUCHI N, KUBOTA K, et al. P2-type Na2/3N1/3Mn2/3-TiO2as a new positive electrode for higher energy Na-ion batteries[J]. Chemical Communications, 2014, 50(28): 3677-3680.
[18] 杨绍斌, 董伟, 沈丁, 等. 钠离子电池正极材料的研究进展[J]. 功能材料, 2015, 46(13): 13001-13006.
YANG S B, DONG W, SHEN D, et al. The research progress of cathode material for sodium-ion batteries[J]. Journal of Functional Materials, 2015, 46(13): 13001-13006.
[19] REN W, YAO X, NIU C, et al. Cathodic polarization suppressed sodium-ion full cell with a 3.3 V high-voltage[J]. Nano Energy, 2016, 28: 216-223.
[20] SLATER M D, KIM D, LEE E, et al. Sodium-ion batteries[J]. Advanced Functional Materials, 2013, 23(8): 947-958.
[21] NOSE M, NAKAYAMA H, NOBUHARA K, et al. Na4Co3(PO4)2P2O7: A novel storage material for sodium-ion batteries[J]. Journal of Power Sources, 2013, 234: 175-179.
[22] WANG L, SONG J, QIAO R, et al. Rhombohedral Prussian white as cathode for rechargeable sodium-ion batteries[J]. Journal of the American Chemical Society, 2015, 137(7): 2548-2554.
[23] 王跃生, 容晓晖, 徐淑银, 等. 室温钠离子储能电池电极材料研究进展[J]. 储能科学与技术, 2016, 5(3): 268-284.
WANG Y S, RONG X H, XU S Y, et al. Recent progress of electrode materials for room-temperature sodium-ion stationary batteries[J]. Energy Storage Science and Technology, 2016, 5(3): 268-284.
[24] XIONG H, SLATER M D, BALASUBRAMANIAN M, et al. Amorphous TiO2nanotube anode for rechargeable sodium ion batteries[J]. The Journal of Physical Chemistry Letters, 2011, 2(20): 2560-2565.
[25] XU J, MA C, BALASUBRAMANIAN M, et al. Understanding Na2Ti3O7as an ultra-low voltage anode material for a Na-ion battery[J]. Chemical Communications, 2014, 50(83): 12564-12567.
[26] LI H, PENG L, ZHU Y, et al. An advanced high-energy sodium ion full battery based on nanostructured Na2Ti3O7/VOPO4layered materials[J]. Energy & Environmental Science, 2016, 9(11): 3399-3405.
[27] RUDOLA A, SARAVANAN K, DEVARAJ S, et al. Na2Ti6O13: A potential anode for grid-storage sodium-ion batteries[J]. Chemical Communications, 2013, 49(67): 7451-7453.
[28] IVANOVA S, ZHECHEVA E, KUKEVA R, et al. Layered P3-NaCo1/3Ni1/3Mn1/3O2versus spinel Li4Ti5O12as a positive and a negative electrode in a full sodium-lithium cell[J]. Acs Applied Materials & Interfaces, 2016, 8(27): 17321-17333.
[29] WANG Y, YU X, XU S, et al. A zero-strain layered metal oxide as the negative electrode for long-life sodium-ion batteries[J]. Nature Communications, 2013, 4: doi: 10.1038/ncomms3365.
[30] WANG Y, XIAO R, HU Y S, et al. P2-Na0.6[Cr0.6Ti0.4]O2cation- disordered electrode for high-rate symmetric rechargeable sodium-ion batteries[J]. Nature Communications, 2015, 6: doi: 10.1038/ncomms7954.
[31] 杨旭. 高比容量锡基负极材料的合成与电化学储能性质的研究[D]. 长春: 吉林大学, 2016.
YANG X. Synthesis and electrochemical properties of tin-based high-capacity anode materials for energy storage[D]. Changchun: Jilin University, 2016.
[32] ZHAO X, VAIL S A, LU Y, et al. Antimony/graphitic carbon composite anode for high-performance sodium-ion batteries[J]. Acs Applied Materials & Interfaces, 2016, 8(22): 13871-13878.
[33] LIANG L, XU Y, WANG C, et al. Large-scale highly ordered Sb nanorod array anodes with high capacity and rate capability for sodium-ion batteries[J]. Energy & Environmental Science, 2015, 8(10): 2954-2962.
[34] LU Y C, MA C, ALVARADO J, et al. Improved electrochemical performance of tin-sulfide anodes for sodium-ion batteries[J]. Journal of Materials Chemistry A, 2015, 3(33): 16971-16977.
[35] SUN W, RUI X, ZHANG D, et al. Bismuth sulfide: A high-capacity anode for sodium-ion batteries[J]. Journal of Power Sources, 2016, 309: 135-140.
[36] LI W, HU C, ZHOU M, et al. Carbon-coated Mo3Sb7composite as anode material for sodium ion batteries with long cycle life[J]. Journal of Power Sources, 2016, 307: 173-180.
[37] HASA I, VERRELLI R, HASSOUN J. Transition metal oxide-carbon composites as conversion anodes for sodium-ion battery[J]. Electrochimica Acta, 2015, 173: 613-618.
[38] HASA I, HASSOUN J, SUN Y K, et al. Sodium-ion battery based on an electrochemically converted NaFePO4cathode and nanostructured tin-carbon anode[J]. ChemPhysChem, 2014, 15(10): 2152-2155.
[39] OH S M, MYUNG S T, YOON C S, et al. Advanced Na[Ni0.25Fe0.5Mn0.25]O2/C-Fe3O4sodium-ion batteries using EMS electrolyte for energy storage[J]. Nano Letters, 2014, 14(3): 1620-1626.
[40] MING J, MING H, YANG W, et al. A sustainable iron-based sodium ion battery of porous carbon-Fe3O4/Na2FeP2O7with high performance[J]. Rsc Advances, 2015, 5(12): 8793-8800.
[41] HARIHARAN S, SARAVANAN K, BALAYA P. α-MoO3: A high performance anode material for sodium-ion batteries[J]. Electrochemistry Communications, 2013, 31: 5-9.
[42] XU G L, CHEN Z, ZHONG G M, et al. Nanostructured black phosphorus/ketjenblack-multiwalled carbon nanotubes composite as high performance anode material for sodium-ion batteries[J]. Nano Letters, 2016, 16(6): 3955-3965.
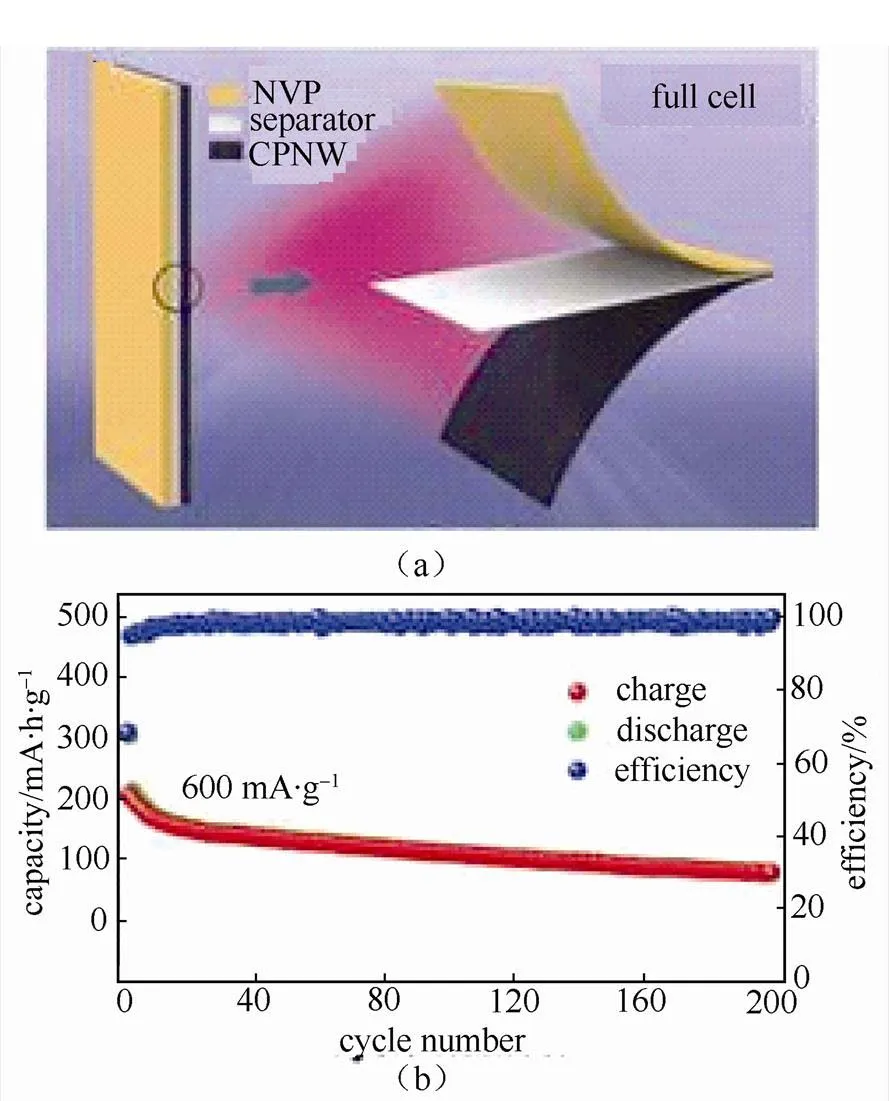
[43] FAN M, CHEN Y, XIE Y, et al. Half-cell and full-cell applications of highly stable and binder-free sodium ion batteries based on Cu3P nanowire anodes[J]. Advanced Functional Materials, 2016, 26(28): 5019-5027.
[44] ZHANG J, YIN Y X, GUO Y G. High-capacity Te anode confined in microporous carbon for long-life Na-ion batteries[J]. Acs Applied Materials & Interfaces, 2015, 7(50): 27838-27844.
[45] ZHANG K, PARK M, ZHOU L, et al. Cobalt-doped FeS2nanospheres with complete solid solubility as a high-performance anode material for sodium-ion batteries[J]. Angewandte Chemie International Edition, 2016, 55(41): 12822-12826.
[46] ZHANG K, PARK M, ZHOU L, et al. Urchin-like CoSe2as a high-performance anode material for sodium-ion batteries[J]. Advanced Functional Materials, 2016, 26(37): 6728-6735.
[47] LI S, DONG Y, XU L, et al. Effect of carbon matrix dimensions on the electrochemical properties of Na3V2(PO4)3nanograins for high-performance symmetric sodium-ion batteries[J]. Advanced Materials, 2014, 26(21): 3545-3553.
[48] HUNG T F, CHENG W J, CHANG W S, et al. Ascorbic acid-assisted synthesis of mesoporous sodium vanadium phosphate nanoparticles with highly sp2-coordinated carbon coatings as efficient cathode materials for rechargeable sodium-ion batteries[J]. Chemistry-A European Journal, 2016, 22(30): 10620-10626.
[49] SENGUTTUVAN P, ROUSSE G, ARROYO Y De DOMPABLO M E, et al. Low-potential sodium insertion in a NASICON-type structure through the Ti (III)/Ti (II) redox couple[J]. Journal of the American Chemical Society, 2013, 135(10): 3897-3903.
[50] GUO S, YU H, LIU P, et al. High-performance symmetric sodiumion batteries using a new, bipolar O3-type mateial, Na0.8Ni0.4Ti0.6O2[J]. Energy & Environmental Science, 2015, 8(4): 1237-1244.
[51] GUO S, LIU P, SUN Y, et al. A high-voltage and ultralong-life sodium full cell for stationary energy storage[J]. Angewandte Chemie International Edition, 2015, 54(40): 11701-11711
[52] ABOUIMRANE A, WENG W, ELTAYEB H, et al. Sodium insertion in carboxylate based materials and their application in 3.6 V full sodium cells[J]. Energy & Environmental Science, 2012, 5(11): 9632-9638.
[53] ZHAO L, ZHAO J, HU Y S, et al. Disodium terephthalate (Na2C8H4O4) as high performance anode material for low-cost room-temperature sodium-ion battery[J]. Advanced Energy Materials, 2012, 2(8): 962-965.
[54] WU X, JIN S, ZHANG Z, et al. Unraveling the storage mechanism in organic carbonyl electrodes for sodium-ion batteries[J]. Science Advances, 2015, 1(8): doi:10.1126/sciadv.1500330.
[55] WANG S, WANG L, ZHU Z, et al. All organic sodium-ion batteries with Na4C8H2O6[J]. Angewandte Chemie International Edition, 2014, 53(23): 5892-5896.
[56] WANG H, HU P, YANG J, et al. Renewable-juglone-based high- performance sodium-ion batteries[J]. Advanced Materials, 2015, 27(14): 2348-2354.
Non-aqueous sodium-ion batteries based on the anode of non-metallic sodium
ZHANG Huimin1,2,3, MING Hai1,3, ZHANG Wenfeng1,3, WEN Yuehua1,3, YANG Yusheng1,3, MING Jun4
(1Research Institute of Chemical Defense, Beijing 100191, China;2Beijing Institute of Technology, Beijing 100081, China;3Beijing Key Laboratory of Advanced Chemical Energy Storage Technology and Materials, Research Institute of Chemical Defense, Beijing 100191, China;4Changchun Institute of Applied Chemistry, Changchun 130022, Jilin, China)
Sodium element has similar physical and chemical properties with lithium, and sodium resource is abundant in the earth, so research interest on sodium ion batteries has rapidly increased recently, particularly for the grid energy storage. Compared with aqueous sodium-ion batteries, non-aqueous sodium-ion batteries have attracted more attention due to its wider electrochemical window (1.5~4.5 V) and higher energy density (100~350 W·h·kg-1). Generally, electrochemical performance of the non-aqueous sodium-ion batteries is evaluated using half cells with metallic sodium as a counter electrode. However, it may cause some potential safety risks when used metallic sodium in sodium-ion batteries, so research on non-aqueous sodium-ion batteries based on the anodes of non-metallic sodium deserves much more attention, which will promote the practical application of sodium-ion battery. Herein, we will introduce some typical sodium-ion batteries based on the anodes of non-metallic sodium, including carbon-based materials, Ti-based compounds, Na-alloys and transition metal oxides. In order to realize the commercialization of sodium-ion batteries, it is needed to explore new cathode and anode materials with better performance and low cost. In addition, mutual matching issues between cathode and anode, designing better electrolyte and binders and separator modification are also important in promoting the commercial applications of sodium-ion batteries in future.
sodium ion batteries; metallic sodium; negative electrode materials; organic electrolyte; full cell
10.12028/j.issn.2095-4239.2017.0045
TM 912
A
2095-4239(2017)06-1159-16
2017-04-13;
2017-05-15。
国家重点研发计划项目(2016YFB0901503)。
张慧敏(1989—),女,博士研究生,主要研究方向为高安全、长寿命和低成本钠基储能电池的基础科学问题,E-mail:zhanghuimin_ 506@126.com;
杨裕生,院士,E-mail:yangyush32@ 126.com。
