通络玉液汤对糖尿病大鼠大动脉内皮细胞保护作用的机制研究
2017-11-24杨丽军张山起李淑贞
胡 庆,杨丽军,张山起,李淑贞
通络玉液汤对糖尿病大鼠大动脉内皮细胞保护作用的机制研究
胡 庆1,杨丽军2,张山起3,李淑贞1
目的探讨通络玉液汤对糖尿病大鼠大动脉血管内皮细胞保护作用的机制。方法选取SD大鼠72只随机分为正常对照4周组、8周组;糖尿病4周组、8周组;通络玉液汤4周组、8周组。检测各组大鼠血清C-反应蛋白(CRP)、白介素-6(IL-6)、超氧化物歧化酶(SOD)水平。结果糖尿病4周组、8周组与对照组同时间点比较IL-6、CRP明显增高、SOD明显降低(Plt;0.01);通络玉液汤4周组、8周组与糖尿病组同时间点比较,IL-6、CRP明显减少、SOD明显增高(Plt;0.01)。结论通络玉液汤能明显改善糖尿病导致的大动脉血管内皮细胞损伤,其机制可能与其抑制血管内皮细胞的慢性炎症反应及清除自由基有关,与用药时间长短无关。
糖尿病;通络玉液汤;腹主动脉内皮细胞;C反应蛋白;白细胞介素6;超氧化物歧化酶
糖尿病是引起动脉粥样硬化的主要原因之一,据文献报道,40岁以上人群5年以上病程的2型糖尿病病人并发血管病变达90.8%,并发血管病的发病率是非糖尿病的20倍[1]。糖尿病血管病变,即在糖尿病状态下的血管重构,是糖尿病心脑血管并发症的主要病理学基础,其发病机制尚未完全明确,临床治疗无有效方法,本实验探讨通络玉液汤对糖尿病大鼠大动脉血管内皮细胞保护作用的机制。
1 材料与方法
1.1 实验材料
1.1.1 实验动物与分组 清洁级健康SD大鼠72只,体重170 g~190 g[购自天津军事医学科学院,编号:SCXX-(军)2009-003]。随机分为正常对照4周组、8周组;糖尿病4周组、8周组;通络玉液汤4周组、8周组,每组12只。
1.1.2 药物与试剂 通络玉液汤组方:生晒参8 g,生黄芪30 g,生山药20 g,麦冬15 g,知母10 g,花粉10 g,葛根10 g,五味子9 g,鸡内金6 g,丹参15 g,当归尾15 g,地龙8 g,60 kg人临床1日剂量。以上中药均购自沧州同仁堂药店。将所购中药饮片浸泡,水煎煮30 min,过滤;再加水煎煮30 min,过滤,两次滤液合并,并浓缩成100%液体(每毫升含原方生药1.7 g),4 ℃冰箱保存备用。
1.2 实验方法
1.2.1 动物模型建立 72只大鼠适应性饲养1周后,随机选取24只,其中12只作为4周对照组,另12只作为8周对照组,普通饲料喂养;其余48只作为造模组给予高糖高脂饲料(20%蔗糖、10%猪油、2.5%胆固醇和67.5%基础饲料)分笼喂养4周。第5周造模组大鼠禁食12 h,给予一次性腹腔注射链脲佐菌素(购自Sigma公司)30 mg/kg(STZ,将STZ溶于0.1 mol/L,pH4.4的柠檬酸缓冲液中,终浓度为2%,在冰水中进行,现配现用,5 min内用完)。注射72 h后采集尾尖血(禁食12 h),检测血糖,浓度gt;16.7 mmol/L确定为2型糖尿病模型;正常对照组仅给予等量枸橼酸钠缓冲液(pH4.4)腹腔注射。将符合2型糖尿病标准的大鼠,分笼继续原饲料喂养,自由饮水。6周后即成糖尿病血管病变模型,模型大鼠均以原饲料再继续喂养4周和8周。
1.2.2 药物干预 将血管病变模型大鼠分组后分别给予药物干预:通络玉液汤组灌服通络玉液汤,剂量为17 g/(kg·d);正常对照组和糖尿病组每日灌服相应剂量的生理盐水,每周根据大鼠体重以及饲料消耗来调整药物剂量。
1.2.3 指标检测 禁食12 h后,给予10%水合氯醛0.3 mL/100 g腹腔注射麻醉,于颈总动脉取血10 mL,6 mL用于检测血糖(GLU)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)。其余4 mL,静置、分离血清,ELISA法检测C-反应蛋白(C-reactive protein,CRP)、白介素-6(interleukin 6,IL-6)、超氧化物歧化酶(superoxide dismutase,SOD)。ELISA试剂盒购自上海建宁生物科技公司,实验严格按照试剂盒说明书操作。

2 结 果
2.1 各组大鼠血糖、血脂指标比较(见表1)


组别GLUTGHDL-CLDL-CTC对照4周组5.56±1.230.31±0.193.97±1.250.27±0.091.23±1.65对照8周组5.91±2.420.53±0.864.13±2.010.35±0.321.57±0.89糖尿病4周组18.57±3.191)3.33±1.211)1.11±0.361)7.03±2.154.14±2.711)糖尿病8周组21.94±5.562)2.64±0.922)0.97±0.232)6.71±2.366.36±1.872)通络玉液汤4周组8.58±2.493)0.82±0.263)2.63±0.853)2.67±0.833)1.74±0.92通络玉液汤8周组6.87±1.394)0.77±0.214)3.61±0.734)1.46±0.524)1.67±0.57 与对照组4周组比较,1)Plt;0.01;与对照组8周组比较,2)Plt;0.01;与糖尿病4周组比较,3)Plt;0.01;与糖尿病8周组比较,4)Plt;0.01。
2.2 各组血清CRP、IL-6和SOD比较 糖尿病4周组、8周组血清CRP、IL-6均明显高于对照组同时间点(Plt;0.01),SOD明显低于对照组同时间点(Plt;0.01);通络玉液汤4周组、8周组血清CRP、IL-6均明显低于糖尿病组同时间点(Plt;0.01),SOD高于糖尿病组同时间点(Plt;0.01)。详见表2。

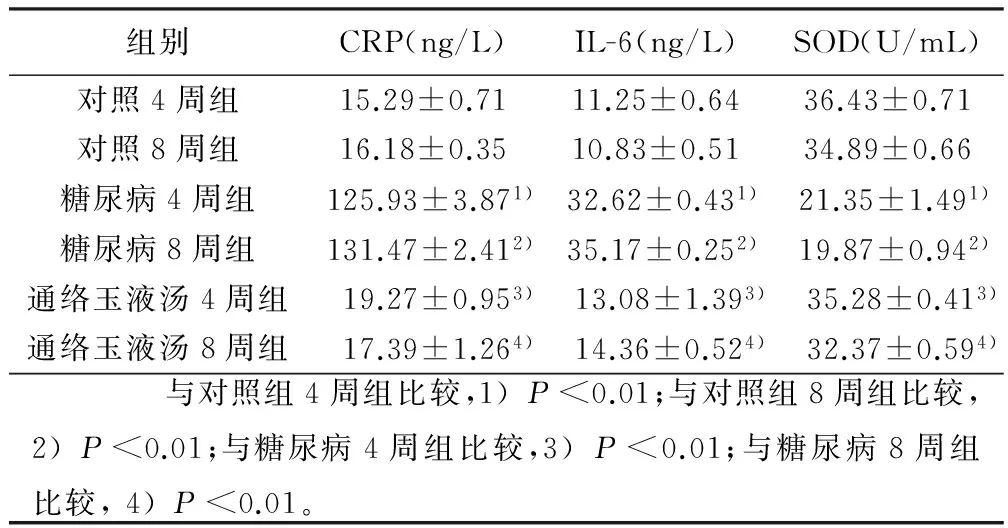
组别CRP(ng/L)IL-6(ng/L)SOD(U/mL)对照4周组15.29±0.7111.25±0.6436.43±0.71对照8周组16.18±0.3510.83±0.5134.89±0.66糖尿病4周组125.93±3.871)32.62±0.431)21.35±1.491)糖尿病8周组131.47±2.412)35.17±0.252)19.87±0.942)通络玉液汤4周组19.27±0.953)13.08±1.393)35.28±0.413)通络玉液汤8周组17.39±1.264)14.36±0.524)32.37±0.594) 与对照组4周组比较,1)Plt;0.01;与对照组8周组比较,2)Plt;0.01;与糖尿病4周组比较,3)Plt;0.01;与糖尿病8周组比较,4)Plt;0.01。
3 讨 论
既往报道发现,影响血管内皮功能因素较多[2-3],糖尿病状态下,持续高血糖引起血管内皮细胞功能紊乱,导致血管通透性增加、白细胞向内皮细胞的黏附增多,导致血管并发症的发生和发展[4-5]。导致内皮细胞功能紊乱的主要作用机制包括活性氧自由基的产生增加、激活炎症相关信号通路、促进一氧化氮(NO)降解、增加内皮素1(ET-1)含量等[6-7]。通络玉液汤改善糖尿病的代谢紊乱,恢复内皮细胞的正常功能。
通络玉液汤是在玉液汤和生脉散基础上加减化裁来,玉液汤记载于《医学衷中参西录》,由清代著名医家张锡纯创立,具益气滋阴、固肾止渴之功。现代广泛应用于糖尿病、高血压等疾病,但对糖尿病血管病变疗效较少报道。生脉散出自《医学启源》,是治疗气阴两虚证的常用方,用于治疗心血管病变等属于气阴两虚者。针对糖尿病血管病变气阴两虚,瘀血阻络病机,本实验利用通络玉液汤,行益气养阴、活血通络之功,达到治疗糖尿病血管内皮细胞损伤的目的。
血管内皮细胞内分泌功能强大,分泌多种活性物质如促炎因子CRP、IL-6、肿瘤坏死因子-α(TNF-α)、单核细胞趋化蛋白-1(MCP-1),抗炎因子NO、前列环素(PG)、血管细胞间黏附分子-1(VCAM-1)等[8]。正常情况下,这些因子维持在平衡状态,当血管内皮受损,其内分泌功能失调,可导致血管内皮炎性反应增强。
本实验高血糖导致炎性因子CRP、IL-6水平明显升高,SOD减少。CRP水平升高,抑制内皮细胞对NO及PG的释放,刺激ET-1及ET-1免疫样激活物释放,促进血管内皮增生[9]。IL-6是由平滑肌细胞、血管内皮细胞等产生的一种多功能细胞因子,可刺激血小板源生长因子(PDGF)分泌,PDGF可促进成纤维细胞、血管平滑肌细胞增殖,诱导成纤维细胞、巨噬细胞向血管内膜下游走、黏附损伤血管内皮[10],并使血管收缩,血压升高。高血压进一步导致血管紧张素Ⅱ通过与1型受体结合使还原型辅酶Ⅰ/还原型辅酶Ⅱ氧化酶活性增强,从而产生大量的超氧阴离子[11],而SOD减少,超氧阴离子增多,引起血管内皮细胞损伤加剧[12],启动粥样斑块的形成及发展,最终导致心血管疾病的发生。
通络玉液汤能明显减轻糖尿病的血管内皮细胞损伤,其机制可能是:①降低GLU、TC、TG、LDL-C、升高HDL-C,减少内皮细胞膜糖基化[13],减轻全身氧化应激状态和过亚硝酸盐形成损伤动脉的弹性蛋白,减轻LDL-C被巨噬细胞吞噬形成泡沫细胞,进而减轻动脉硬化[14];②提高SOD活性,减轻超氧阴离子对内皮细胞的损伤[15],增加内皮细胞生成[16];③减少CRP、IL-6分泌,减轻血管内皮细胞的炎症反应[17];④提高NO水平,NO是一种重要的内源性抗动脉粥样硬化介质,具有舒张血管、抑制血小板黏附和聚集、抑制白细胞黏附和迁移、减少氧自由基和氧化型低密度脂蛋白作用,减轻内皮细胞损伤[18]。
本实验通过检测通络玉液汤治疗大鼠血清CRP、IL-6、SOD变化,发现通络玉液汤对糖尿病大鼠动脉血管内皮细胞的保护作用,与减轻炎症反应和增强超氧化物歧化酶活性密切相关,但具体机制尚待进一步研究。
[1] 杨维娜,王璇,蓝茜,等.2型糖尿病并发周围血管病变的临床流行病学分析[J].西安交通大学学报(医学版),2013,34(1):73-76.
[2] Hopkins ND,Cuthbertson DJ,Kemp GJ,et al.Effects of 6 months glucagon-like peptide-1 receptor agonist treatment on endothelial function in type 2 diabetes mellitus patients[J].Diabetes 0bes Metab,2013,15(6):770-773.
[3] Torimoto K,kada Y,Mori H,et al.Low levels of 1,5 anhydro-D-glucitol are associated with vascuIar endothelial dysfunction in type 2 diabetes[J].Cardiovasc Diabetol,2014,13(4):98-99.
[4] Pigozzi F,Rizzo M,Fagnani F,et al.Endothelial(dys)function:the target of physical exercise for prevention and treatment of cardiovascular disease[J].J Sports Med Phys Fitness,2011,51(2):260-267.
[5] Jansson PA.Endothelial dysfunction in insulin resistance and type 2 diabetes[J].J Intern Med,2007,26(2):173-183.
[6] Liu J,Yan L,Niu R,et al.Protection effect of endomorphins on advanced glycation end products induced injury in endothelial cells[J].J Diabetes Res,2013,11(6):778-780.
[7] Zhuang X,Pang X,Zhang W,et al.Effects of zinc and manganese on advanced glycation end products(AGEs) formation and AGEs-mediated endothelial cell dysfunction[J].Life Sci,2012,90(3):131-139.
[8] 赵娜,马维红,苏赢,等.牛蒡根水提物对高血压大鼠血管内皮损伤的保护作用[J].天津医药,2015,34(1):42-45.
[9] Emilie C,Isabelle C,Kim T,et al.Estradiol inhibits vascular endothe lial cells pro- inflammatory activation induced by C-reactive protein[J].Mol Cell Biochem,2013,18(9):137-147.
[10] Okura T,Jotoku M,Irita J,et al.Association between cystatin C and inflammation in patients with essential hypertension [J].Clin Exp Nephrol,2010,14(6):584-588.
[11] 李萍,肖纯.病理学[M].北京:科学出版社,2012:201-203.
[12] 孟珊珊,赵庆杰,洪文,等.血糖水平对糖尿病大鼠脑缺血后血管新生的影响机制[J].卒中与神经疾病,2015,22(5):263-267.
[13] 贾晓炜,贾贺堂,唐发宽.临床干预血糖漂移对老年2型糖尿病患者血管内皮指标相关性分析[J].中华老年心脑血管病杂志,2015,17(4):361-364.
[14] 阮华玲,郭昆全,杨坤,等.2型糖尿病患者血糖波动与下肢血管病变的相关性[J].浙江临床医学,2015,17(9):1489-1491.
[15] 侯亮,刘雪平,侯训尧,等.氯沙坦对自发性高血压大鼠心脏血管紧张素转换酶2-血管紧张素(1~7)-MAS-ERK通路的影响[J].中华高血压杂志,2010,18(2):177-182.
[16] Selvakumar B,Hess DT,Goldschmidt-Clermont PJ,et al.Coregulation of constitutive nitric oxide synthases and NADPH oxidase by the small GTPase Rac[J].FEBS Lett,2008,58(2):2195-2202.
[17] 杨艳红,闫冬霞.辛伐他汀对高血压并颈动脉粥样硬化血管内皮功能的影响[J].中国实用神经疾病杂志,2010,13(5):78-79.
[18] 武云涛,张薇,田国祥,等.不同剂量辛伐他汀对冠状动脉粥样硬化症患者血管内皮细胞功能的影响[J].中国循证心血管医学杂志,2014,6(2):162-165.
2017-01-23)
(本文编辑 薛妮)
Protective Mechanism of Tongluo Yuye Decoction on Aortic Endothelial Cells of Diabetic Rats
Hu Qing, Yang Lijun, Zhang Shanqi, Li Shuzhen
Cangzhou Medical College, Cangzhou 061001, Hebei,China
Yang Lijun (Cangzhou Central Hospital, Cangzhou, Hebei,China)
Objective To investigate the protective mechanism of Tongluo Yuye decoction (TYD) on aortic endothelial cells of diabetic rats. Methods Seventy-two Sprague-Dawley (SD) rats were randomly divided into three groups: control group (4-week group, group A;8-week group, group B), diabetic group (4-week group, group C;8-week group, group D),and TYD group (4-week group, group E;8-week group,control group F). The levels of of serum C-reactive protein (CRP), interleukin-6 (IL-6),and superoxide dismutase (SOD) were measured and compared. Results Compared with control group,the level of SOD was decreased while the levels of IL-6,CRP were elevated significantly in diabetic group at the same time(Plt;0.01). Compared with diabetic group,the level of SOD was increased while the levels of IL-6,CRP were decreased significantly in TYD group at the same time(Plt;0.01). Conclusion TYD can obviously improve the damage of aortic endothelial cells caused by diabetes. The mechanism may be related to the inhibition of chronic inflammatory reaction of vascular endothelial cells and the clearance of free radicals.
diabetes;Tongluo Yuye decoction;abdominal aortic endothelial cells;C-reactive protein;interleukin-6;superoxide dismutase
R587.1 R285.5
A
10.3969/j.issn.1672-1349.2017.20.008
1672-1349(2017)20-2543-03
2015年沧州市科学技术研究与发展指导计划项目(No.151302098)
1.沧州医学高等专科学校(河北沧州 061001);2.河北省沧州市中心医院;3.沧州职业技术学院
杨丽军,E-mail:czyzhq@126.com
信息:胡庆,杨丽军,张山起,等.通络玉液汤对糖尿病大鼠大动脉内皮细胞保护作用的机制研究[J].中西医结合心脑血管病杂志,2017,15(20):2543-2545.
