化学题目中隐藏条件的辨识
2017-11-21张卡娃
◎张卡娃
化学题目中隐藏条件的辨识
◎张卡娃
解决化学问题,审题很关键,在审题过程中往往会因为忽视隐含条件而导致答非所问,所以加强隐含条件的辨识尤为重要,本文结合一些典型化学问题,分析了其中的隐含条件,仅供参考。
从隐含条件来说,它往往作为解决问题的关键信息存在,如果辨识不出来往往会出现答非所问的情况,所以解决带有隐含条件的化学问题,关键还是要学会辨识隐含条件。纵观历年来的高考化学题目,命题者往往有以下几种方式来设置隐藏条件。
限制隐含
有一类题目,题干中看似给出了很多已知条件,实质上确是一个陷阱,一旦不注意往往陷入复杂的计算当中,或是直接找不到解题的突破口。
例如:FeSO4和Fe2(SO4)3的混合物当中含硫a%,则含铁()
A、2a% B、3a%
C、1-2a% D、1-3a%
解析:该题目中,隐含的条件就在于S和O的比例(1:4,存在形式SO4),这一比例在题目中是一个固定的恒量,也是一个限制条件,找到它问题就迎刃而解。进一步从物理量层面考量,可知S原子质量为32,O原子质量为16,可知S和O的质量为1:2,进一步计算可得到Fe为1-3a%。
恒量隐含
例如,处于密闭状态下的铝和高锰酸钾混合物,经过充分加热,发现发生反应前后固体质量不变,试求铝和高锰酸钾恰当质量比。
解析:通过审题,提取关键信息可知,加热高锰酸钾会让发生分解,生成氧,而氧又可以和铝发生反应生成氧化铝。问题要求寻找铝和高锰酸钾的质量比(恰当),要保证反应前后固体质量不变,关键要使生成的氧气与消耗掉的氧气等质量。这是比较典型的将恒量隐含在生成物与反应物的质量关系中。只要能够将隐含的条件挖掘出来,该题目就会迎刃而解。
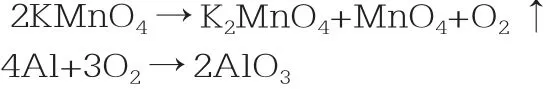
根据上述方程式,可知生成的氧气与消耗的氧气等质量,则铝和高锰酸钾的恰当质量比为9:79。
过程隐含
一些化学反应当中,既有显性的反应过程,也有隐藏的反应过程。命题者往往或利用这种情况,设置隐含条件,改变题目条件。
例如,一定温度下,容积为V的密闭容器中,充入amol NO2,发生以下反应:2NO2(g)↔N2O4(g)。达成平衡以后,再次充入amol NO2,比较原平衡和后续平衡,正确的选项是()
A、减小平均相对分子质量
B、压强比原来增加2倍
C、提高了NO2转化率
D、颜色变浅
解析:根据题目要求可知反应为可逆反应,基于此再现可逆反应的相关性质,当反应平衡,容器内各物质的量的百分含量不变,反应速率相同且不为零,各物质浓度不随时间变化。如果是气体那么混合气体的总压强或总物质的量或平均密度不随时间变化,平均质量不变,再次充入amol NO2,就相当于在原平衡状态下加压然后达到新的平衡状态,此时可判断向右平衡,然后采用排除法逐一排除可得答案为C。
实验事实隐含
一些考查实验的题目中,往往会对一些客观存在的实验事实进行隐藏,一旦出现这种状况,题目往往会变得比较复杂。
例如,实验室条件下,用氢还原CuO(mg),当出现大部分红色固体时,停止加热,量得固体质量n g,此时氢用量为w g,问生成水的质量()
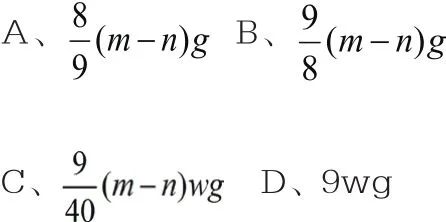
解析:题目考查氧化还原反应,题干中隐含着很多迷惑性的信息,乍一看题目给出的条件,好像比较简单,实质上却是陷阱。比如给定的氢气消耗量。如果这样去分析题目,就可能出现两个答案。这样就忽视了一个给定的限制条件——实验室条件下。要考虑到实验室条件下的实验事实——氢气的消耗量是要计算排除的空气、冷却的Cu和CuO三个部分,也就是说给定的w g氢,并不是实际用去的量,它就是一个陷阱。找准这一点才是解决问题的关键。所以氢还原CuO生成水和Cu,减少的固体的质量相当于水氧元素质量,所以答案为B。
可变条件隐含
所谓可变性的隐含条件,就是一些题目具有开放性,使得题目可变性大,会出现多个解。这种题目,就需要分类讨论,充分考虑可能隐含的可变条件。
例如:10mL容积的试管中充满氧气和二氧化氮的混合气体,试管倒立于水槽中,充分反应后,试管尚余1mLqiti ,试求,原混合气体的体积。
解析:该题目的可变性比较强,剩余的气体可能是氧气也可能是二氧化氮。题干没有明确给定剩余哪种气体,那么就需要分别寻找可能的隐含条件,即如果氧气过量,那么氧气就会剩余,此时体积为1mL。这种情况下分别计算可得出氧气体积为2.8mL,二氧化氮为7.2mL;如果二氧化氮过量,剩余的气体就是二氧化氮,体积同样是1mL,此时计算可得出氧气体积为1.4mL,二氧化氮为8.6mL。
物质性质隐含
例如,二氧化硫和硫化氢物质的量相等,在常温下的定容密闭容器中反应,待恢复常温后,分析容器内压强是原压强的多少()
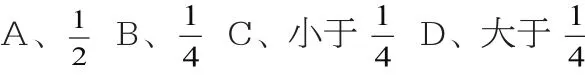
解析:在惯性思维下,容易单纯的考虑过量,按题目要求,本题需要先罗列方程式,分析反应物的物质的量,找出标准,寻找可能发生的变化。方程式为:SO2+2H2S→3S+2H2O,二氧化硫和硫化氢的比例为1:2,压强可视为0,假定两气体物质的量为2mol,待反应后二氧化硫剩余1mol,是原来的,可知压强为阿伏伽德罗定律)。此时就可能选择B,实质上就忽视了物质的溶解性,答案应该为C。
化学题目当中,隐含条件往往是解决问题的关键所在。在实际解决问题的过程中,必须认真审题,准确辨识出其中的隐含条件,才能准确解题,笔者分享了一些比较典型的题目,可作为参考。
(作者单位:湖南省长沙市第一中学)
