国产与进口血细胞处理机制备冰冻解冻去甘油红细胞的质量对比
2017-11-14时卉丽李玉秋李建民何路军
时卉丽,李玉秋,程 菲,李建民,何路军
(河北省血液中心质量法规处,河北 石家庄 050071)
国产与进口血细胞处理机制备冰冻解冻去甘油红细胞的质量对比
时卉丽,李玉秋,程 菲,李建民,何路军
(河北省血液中心质量法规处,河北 石家庄 050071)
目的通过对比国产智能红细胞洗涤机及配套耗材与美国ACP215血细胞处理机洗涤制备的效果,评价国产智能红细胞洗涤机的性能及应用可行性。方法抽取40袋全血,先甘油化,冰冻解冻后随机分为2组,实验组应用国产智能红细胞洗涤机制备冰冻解冻去甘油红细胞,对照组应用美国ACP215血细胞处理机洗涤制备,对制备的产品按照GB18469-2012版《全血及成分血质量要求》相关标准进行检测分析。结果2组血红蛋白含量、游离血红蛋白含量均符合国家标准要求,差异无统计学意义(P>0.05)。实验组甘油残留量、白细胞残留量高于对照组,差异有统计学意义(P<0.05),但均能达到国家标准要求。结论国产智能红细胞洗涤机制备的冰冻解冻去甘油红细胞产品指标符合国家相关标准;其耗材价格相对较低,维护相对方便,可以为血站节约成本,值得大力推广和应用。
红细胞;去甘油化;对比研究
10.3969/j.issn.1007-3205.2017.11.025
在我国,Rh(D)阴性献血者稀少,造成相应的血液品种库存严重不足,在临床稀有血型患者输血救治特别是大量失血患者抢救输血时,如何保障Rh(D)阴性血患者医疗急救用血是一个十分迫切的问题[1]。深低温冰冻保存可大幅度延长红细胞的体外存活时间和存活率[2],故国内许多血站均采取甘油化Rh阴性红细胞后,-80 ℃低温保存。美国FDA在上世纪80年代初批准冰冻保存红细胞的有效期为10年[3]。冰冻可延长红细胞的保存期,且具有可靠的质量,在经过洗涤后,红细胞的生理形态及生化特性均无明显改变,适合应用于稀有血型患者的输血治疗[4]。近些年,国内大多血站采用手工法和ACP215血细胞处理机对冰冻的红细胞进行解冻洗涤,但是传统的手工开放式洗涤法操作步骤相对复杂,制备时间较长,受人为因素影响较大[5]。我中心最早购置的美国ACP215血细胞处理机近几年也因为维修保养的不便以及进口耗材的昂贵、消费者多有怨言而利用度下降[6]。血细胞处理机的国产化正处于逐渐摸索投入使用阶段,其洗涤效果如何,是否符合质量要求标准,实际制备效果和产品质量有待探讨。我中心现试用一种新型国产智能红细胞洗涤机,本研究将其制备的冰冻解冻去甘油红细胞与美国ACP215血细胞处理机制备的产品质量进行比较,以评价其可行性,报告如下。
1 材 料 与 方 法
1.1 主要材料 去白悬浮红细胞(2 U/袋,由本中心提供),智能红细胞洗涤机(型号:ZHXD)配套耗材(成都佳颖),ACP215 血细胞处理机配套耗材(美国血液技术公司),无菌熔接片(日本泰尔茂公司),复方甘油溶液(石家庄四药有限公司),9% NaCl溶液(北京博得桑特输血技术公司),0.9%NaCl溶液(四川南格尔生物医学股份有限公司),甘油测定试剂(自制)。所有材料、试剂均在有效期内使用。
1.2 主要设备 智能红细胞洗涤机(型号:ZHXD),ACP215血细胞处理机,无菌接驳机(泰尔茂),血细胞计数仪(COULTER),765型分光光度计(上海精密科学仪器公司),-80 ℃低温冰箱(日本三洋SANYO),恒温水浴箱(上海发瑞仪器科技),全自动细菌培养仪(生物梅里埃)。
1.3 红细胞甘油化 随机抽取6 d内2~6 ℃保存的全血(400 mL/袋),制备成悬浮红细胞,放置于PVC血液保存袋内,用无菌接驳机接驳,其红细胞转移到空袋中。将血袋接驳于甘油化管路,再与甘油袋相连接。将浓度57%左右的甘油缓慢加入到去白悬浮红细胞中,边加边振荡,以使红细胞充分、均匀甘油化。室温静置30 min,离心去除多余的液体,将其置于-80 ℃低温冰箱保存。
1.4 红细胞去甘油化 将冰冻保存1年后的红细胞从-80 ℃低温冰箱中迅速取出,放入37 ℃恒温水浴箱(不断晃动至红细胞完全融化),解冻后随机分为2组,每组20袋。对照组用美国ACP215血细胞处理机及配套耗材(REF 235)洗涤,按照去甘油化程序相关操作规程[7]进行处理(运行程序已预先设定)。实验组用国产智能红细胞洗涤机,将已解冻的冰冻红细胞血袋与配套的去甘油化管路无菌接驳,放置在摇摆机上,启动机器,自检完成后选择去甘油化程序,安装耗材,连接洗液袋并打开所有管路夹子,开始自动洗涤。根据不同制备阶段加入相应的羟乙基淀粉和氯化钠溶液,为了保证红细胞渗透能力的稳定性,应在去甘油的洗涤过程中分别加入9%NaCl高渗溶液和0.9%NaCl等渗溶液,否则易促使红细胞发生形态、功能的改变,增加红细胞的破坏率。最后加入100 mL的红细胞保存液保存红细胞。2组分别记录洗涤制备时间,国产智能红细胞洗涤机用时50 min左右,ACP215血细胞处理机用时60 min左右。
1.5 质量检测 参照普通洗涤红细胞的要求称质量、留样,对样品进行无菌接种,在全自动细菌培养仪内培养观察7 d,应用COULTER AcT.5diff全自动血球计数仪检测红细胞的血红蛋白含量,用Trinder法进行体外溶血试验检测游离血红蛋白值,用Neubaue计数板检测残余白细胞数,用过碘酸钠滴定法测定甘油残余量[8-10]。
1.6 统计学方法 应用SPSS 16.0统计软件处理数据,计量资料比较采用独立样本的t检验。P<0.05为差异有统计学意义。
2 结 果
实验组白细胞残留量、甘油残留量均高于对照组,差异有统计学意义(P<0.05);2组血红蛋白含量、游离血红蛋白含量差异均无统计学意义(P>0.05)。见表1。

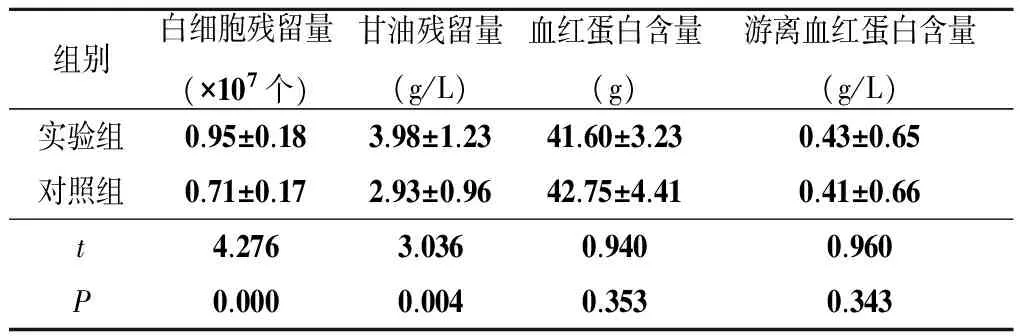
组别白细胞残留量(×107个)甘油残留量(g/L)血红蛋白含量(g)游离血红蛋白含量(g/L)实验组0.95±0.183.98±1.2341.60±3.230.43±0.65对照组0.71±0.172.93±0.9642.75±4.410.41±0.66t4.2763.0360.9400.960P0.0000.0040.3530.343
3 讨 论
众所周知,Rh(D)阴性血型是稀有血型,在Rh血型者中所占比率不到1%。而我国Rh (D)阴性血型者大约为0.59%,给临床急诊用血带来一定的困难,存在耽误患者抢救时机的风险。目前国内许多血站采取甘油化Rh阴性红细胞,于-80 ℃低温保存,保存期可达10年,且具备较好的保存质量,在临床输注前经过洗涤去甘油化后再应用于患者,是自身输血及稀有血型输血不可缺少的手段[11]。冷冻保存红细胞,既争取了抢救时间,又极大方便了临床用血,冰冻解冻去甘油红细胞是不可或缺的血液制品。目前这种红细胞制品在国内相当一部分血站仍沿用手工方法制备,工艺较繁琐,容易受离心机转速、温度等因素影响,且开放式制备存在被污染的安全隐患,对操作人员的技术要求也较高,整个添加过程受人为因素影响较大,操作稍有不慎将会直接影响到本类制品的质量,即对患者的用血安全造成威胁[12]。机器替代手工是近几年发展的方向,机器制备是有效保证血液质量的前提,探讨机器标准化制备冰冻红细胞,可减少人为误差,提高效率和产品质量。我国从1998年开始逐渐开展了机器洗涤红细胞技术,应用红细胞洗涤机制备出冰冻解冻去甘油红细胞,制备时间短,缩短了临床患者等待抢救的时间,减少了人工制备的劳动力及血液被污染的机会。但该技术的研发一直存在困难,很多公司生产的仪器并不能达到《全血及成分血质量要求》[13]相关标准,在仪器质量评估方面也存在很大空白[14]。
本研究实验组应用仪器是我中心新引进的一种国产智能红细胞洗涤机(型号:ZHXD),与美国较成熟的ACP215血细胞处理机进行对比研究,结果显示,2种机型制备的冰冻解冻去甘油红细胞的各项质量指标均符合国家标准,实验组白细胞残留量、甘油残留量虽高于对照组,但其他各项指标差异无统计学意义。表明国产智能红细胞洗涤机(型号:ZHXD)与美国ACP215血细胞处理机比较,其制备的冰冻解冻去甘油红细胞除有小部分的不足(白细胞、甘油残留量高),其余指标均无明显差异。目前有些大中城市的血液中心和中心血站应用的是美国进口的ACP215血细胞处理机,但该仪器价格昂贵,给患者带来一定的经济负担,故在国内广泛推广应用存在一定困难。
本研究结果显示,在甘油残留量方面国产机器略逊于进口机器,但无菌试验等各项指标均达到了国家标准的要求,其安全性和有效性是可靠的。有文献报道美国ACP215血细胞处理机的工序耗时为50~60 min[7]。而国产机器去甘油化进程要快于进口机器,符合冰冻解冻去甘油红细胞用于临床急救用血的要求;另一优势就是节省了资金成本,由于ACP215进口机器必须使用美方配套的一次性耗材,而这些耗材比国产的价格高好几倍,无形中增加了生产成本,致使许多血站不得不又重新拾起手工开放式洗涤法。国产智能红细胞洗涤机在洗涤标准达标的前提下,提高了洗涤速度,符合临床急救用血的迫切需求;另外,其配套耗材价格较低,为血站节约了成本,也能减轻患者的经济负担。本研究中国产机器的良好表现,有利于刺激国内更多生产厂家加入到国产红细胞洗涤机的自主研发行列。
FDA已经批准使用ACP215血细胞处理机制备去甘油红细胞,可于AS-3中保存2周。国内冯博等[15]尝试用MAP来延长产品的保存时间,观察其质量的变化情况。本研究结果显示国产智能红细胞洗涤机在洗涤后仍残留部分白细胞和其他细胞碎片,说明国产机器分离技术还不够成熟完善;甘油残存量相对较高,说明在去甘油化的过程中还存在需要继续完善的地方。但整体上已经符合国家标准,给我国从人工洗涤红细胞到机器洗涤带来重大变革。
综上所述,国产智能红细胞洗涤机具有我国的自主知识产权,在成本核算和机器的后期维护保养方面更具优势,开发和使用国产智能红细胞洗涤机及配套耗材势在必行,是实现血站自动化、标准化、规范化的必经之路,由人工制备转化为机器制备模式,应该有广阔的应用前景和市场价值,值得大力推广。
[1] 梁世艳,张支凤,李华领,等.Rh(D)阴性冰冻红细胞库的建立及临床应用[J].卫生职业教育,2012,30(22):134-135.
[2] 马庆,张嘉敏,李勤,等.深低温长期保存方法延缓红细胞衰老的研究[J].临床输血与检验,2013,15(2):112-115.
[3] 张玉华,徐雷,周虹,等.现代战争条件下美军野战输血保障情况分析与思考[J].军事医学,2014,38(6):474-477.
[4] 熊少欢,侯满意,李婉仪,等.RH(D)阴性冰冻红细胞质量及临床分析[J].现代医院,2015,15(11):66-67.
[5] 卢少芬,陈志忠,李洁敏,等.BBS 926全自动医用低速离心机制备冰冻解冻去甘油红细胞的质量评价[J].中国当代医药,2014,21(30):87-91.
[6] 梁艳.手工密闭式制备冰冻解冻去甘油红细胞的可行性研究[J].贵州医药,2016,40(6):592-593.
[7] 扬丽,张静,陈健.ACP215处理机制备冰冻解冻去甘油红细胞与手工制备的对比研究[J].临床输血与检验,2012,14(2):156-157.
[8] 冀慧,陈保民.两种方法测定解冻红细胞甘油残留量结果比较[J].中国输血杂志,2014,27(8):835-838.
[9] 夏红英,任芙蓉,陈小林,等.渗透压法检测冰冻解冻去甘油红细胞甘油残留量的可行性[J].北京医学,2015,37(6):588-591.
[10] 时卉丽,赵倩,杨凤霞,等.国产智能红细胞洗涤机及配套耗材制备冰冻解冻去甘油红细胞的质量观察[J].临床合理用药杂志,2016,9(22):168-169.
[11] 王林,唐玉清,闫晓鹏,等.冰冻亚型红细胞制备及使用的全程质量控制[J].中国医药科学,2014,4(17):136-138.
[12] 肖乐宇,任明臣,马振芳,等.机器法和手工法制备的冰冻解冻去甘油红细胞的质量比较[J].现代预防医学,2014,41(11):3201-3203.
[13] 中华人民共和国卫生部,中国国家标准化管理委员会.中华人民共和国国家标准GB18469-2012全血及成分血质量要求[S].北京:中国标准出版社,2012:8-9.
[14] 时卉丽,牛宏伟,杨凤霞,等.一种国产红细胞洗涤机的性能评价[J].中国医药导刊,2017,19(1):79-80.
[15] 冯博,段澜,龚晓燕,等.MAP液保存的冰冻解冻去甘油红细胞可保存天数的研究[J].中国输血杂志,2014,27(11):1170-1172.
·论著·
2017-07-24;
2017-08-24
河北省医学科学研究重点课题(20130134)
时卉丽(1978-),女,河北元氏人,河北省血液中心副主任医师,医学学士,从事血液质量安全、血站质量管理研究。
R331.122
B
1007-3205(2017)11-1344-04
(本文编辑:刘斯静)
