磺胺类抗生素与胞外聚合物作用的热化学机制
2017-11-07张程程吉芳英
王 静,张程程,吉芳英*,晏 鹏
磺胺类抗生素与胞外聚合物作用的热化学机制
王 静1,张程程2,吉芳英2*,晏 鹏3
(1.重庆建筑工程职业学院交通与市政工程系,重庆 400072;2.重庆大学三峡库区生态环境教育部重点实验室,重庆 400045;3.中国科学院重庆绿色智能技术研究院,重庆 400714)
本研究利用等温滴定微量热技术获得了胞外聚合物和磺胺类抗生素的相互作用的热力学参数,探索了其作用机制.结果表明,胞外蛋白和磺胺二甲基嘧啶(SMZ)强烈结合,结合过程由疏水相互作用驱动的熵作为主要驱动力.结合强度显著地受pH和离子强度的影响.在pH为6.8的近中性条件下,EPS和SMZ的结合反应最有利,且构象变化最大.离子强度对EPS和SMZ之间的相互作用有明显的影响.该研究的结果表明,活性污泥中存在的EPS对抗生素的迁移转化有显著影响.
胞外聚合物;等温滴定微量热;磺胺二甲基嘧啶;pH值;离子强度
磺胺类抗生素是现代医学中常用的一类人工合成的抗菌消炎药,因生产成本低、抗菌广谱等优势现已成为世界上应用最为广泛的抗生素之一[1-3].由于它们对微生物具有抑制效应,常规的活性污泥法对其去除效果非常有限,导致它们在污水厂出水中有残留,已在世界各地包括我国的污水处理厂出水中检出[4].
胞外聚合物(EPS),是由微生物在一定条件下分泌的高分子物质,覆盖在微生物细胞表面及填充在污泥絮体内部空隙中[5].EPS具有大量的活性官能团和疏水区域,有很强的吸附和络合污染物的能力[6-8].
磺胺类抗生素在污水处理厂的有效去除主要依赖于污泥絮体的吸附和生物降解[9-10],其中作为活性污泥主要成分的EPS对磺胺类抗生素的吸附具有重要的研究意义和价值,这引起了国内外污水处理领域相关学者的广泛关注[11].目前,通常采用化学分析法结合吸附模型的方式研究EPS与磺胺类抗生素的相互作用[12].但是,该方法具有耗时、精度低、灵敏度低等缺点,极大的阻碍了对其相互作用机制的认识.等温滴定微量热法是近年来发展起来的一种直接测量生物分子结合过程中的放热或者吸热的技术,在单次实验中即可提供一系列有关分子相互作用的完整信息[13].等温滴定微量热法与常规分析方法相比具有灵敏度高、精度高、快速、免标记、无损、原位等特点.本研究运用等温滴定微量热法探讨EPS模拟物与磺胺类抗生素的结合程度,以及离子强度和pH值对结合程度的影响.从热力学的角度深入探讨EPS与磺胺类抗生素间的相互作用机制,明晰EPS在磺胺类抗生素去除过程中所起的作用,揭示磺胺类抗生素去除过程中的干扰因素和影响规律,为磺胺类抗生素在活性污泥系统中的高效去除提供理论依据.
1 材料与方法
1.1 仪器与材料
牛血清白蛋白、葡聚糖、腐殖酸钠、磺胺二甲基嘧啶(SMZ),试剂均为分析纯.枯草芽孢杆菌菌种(ATCC6633,广州省微生物菌种保藏中心).酵母浸粉、蛋白胨均购于北京奥博星生物技术有限责任公司.
ITC200型等温滴定微量热仪,DW-86L386型超低温冰箱,Virtis BT4KXL型冷冻干燥机.
1.2 实验方法
1.2.1 细菌培养与EPS 提取冷冻干燥的枯草芽孢杆菌菌种,于灭活培养基(5g/L酵母浸粉,10g/L蛋白胨,5g/L NaCl)中在30℃下培养24h,随后取1~2mL转移至250mL灭活培养基中,培养40h(30℃),然后提取EPS.将细胞悬浮液分装于50mL离心管中离心(5000,4℃,20min),去除上清液,小心清洗剩余球团1~2次,后加入去离子水将球团冲洗下来至烧杯或锥形瓶超声(功率40%,时间3min×2次),将悬浮液转移至离心管,在4℃(7800~ 8000)离心50min,上清液即为EPS.经0.45μm滤膜过滤,而后冷冻干燥,于–40℃保存备用.
1.2.2 EPS模拟物与SMZ结合实验 EPS的主要组成物质为蛋白质和多糖,腐殖质,通常以牛血清白蛋白(BSA)、葡聚糖(Glucan)和腐殖酸钠(HA-Na)为EPS组分中的蛋白、多糖和腐殖质类物质的模拟物[14-16].所有溶液均用PBS缓冲液(1mmol/L, pH 6.8)配制.等温滴定的主体牛血清白蛋白(BSA)、葡聚糖和HA-Na浓度均为5g/L,配体SMZ浓度为0.5g/L.所有的溶液在滴定前进样过程中真空脱气,以防出现气泡干扰热量检测.
1.2.3 环境因素实验 采用磷酸盐缓冲体系调节pH值为5.7、6.8和8.0的缓冲液(1mmol/L).用NaCl调节离子强度分别为5mmol/L、50mmol/L和500mmol/L的 IS 1、IS 2 和IS 3溶剂.不同pH值和离子条件下主体EPS的浓度为5g/L,配体SMZ的浓度为0.5g/L,用ITC-200测定反应中吸收和放出的热量.
1.2.4 等温滴定微量热法 反应体积: 0.2mmol/L,进样针容积为40μL,反应温度:20℃;总注射次数: 19次;参照功率:5μCal/s;搅拌器转速:1000r/min.磺胺二甲基嘧啶溶液和PBS缓冲液分别滴定EPS模拟物,其中缓冲液滴定EPS模拟物为实验对照,用于扣除反应过程中的稀释热量.数据用Origin 7.0进行拟合分析得到结合化学计量数(),结合常数()和焓变(Δ).
2 结果与讨论
2.1 EPS组分对结合反应的影响
对EPS模拟物与SMZ的结合反应进行ITC检测,热谱图见图1,获得的结合参数见表1.由图1可知,SMZ与BSA和HA-Na结合的每一次滴定有明显的负峰出现,表明相互作用均是放热过程;而与葡聚糖的滴定反应热谱图中,每一次滴定基本出现正峰,第二滴的峰面积为0.57313μcals,低于1μcals,且每滴的热量变化微弱,表明SMZ与EPS中多糖模拟物葡聚糖的结合十分微弱.
SMZ与BSA和HA-Na非线性拟合出的热力参数、推导得到的吉布斯自由能变Δ及熵变Δ如表1所示.SMZ与BSA和HA-Na结合的吉布斯自由能变Δ和Δ皆为负值,表明均为典型的可自发进行的放热反应.SMZ与BSA的结合化学计量数为0.865sites,是SMZ与HA-Na的结合化学计量数(0.176sites)的近5倍; SMZ与BSA结合的结合常数比与HA-Na结合的结合常数略小1个数量级,表明EPS中的蛋白模拟物BSA较腐殖质模拟物HA-Na与SMZ的结合容量更大,但后者的复合物更稳定.SMZ与BSA结合过程中的熵变Δ< 0,|Δ|>|TΔ|,表明结合后体系构象变化受到限制[17],BSA与SMZ的结合是以氢键和范德华力为主要作用力的焓驱动过程.而SMZ与HA-Na结合过程中的熵变Δ> 0,|Δ|<|TΔ|,说明体系的无序度增加[18],反应主要是以疏水性相互作用为主要驱动力的熵驱动过程[19].
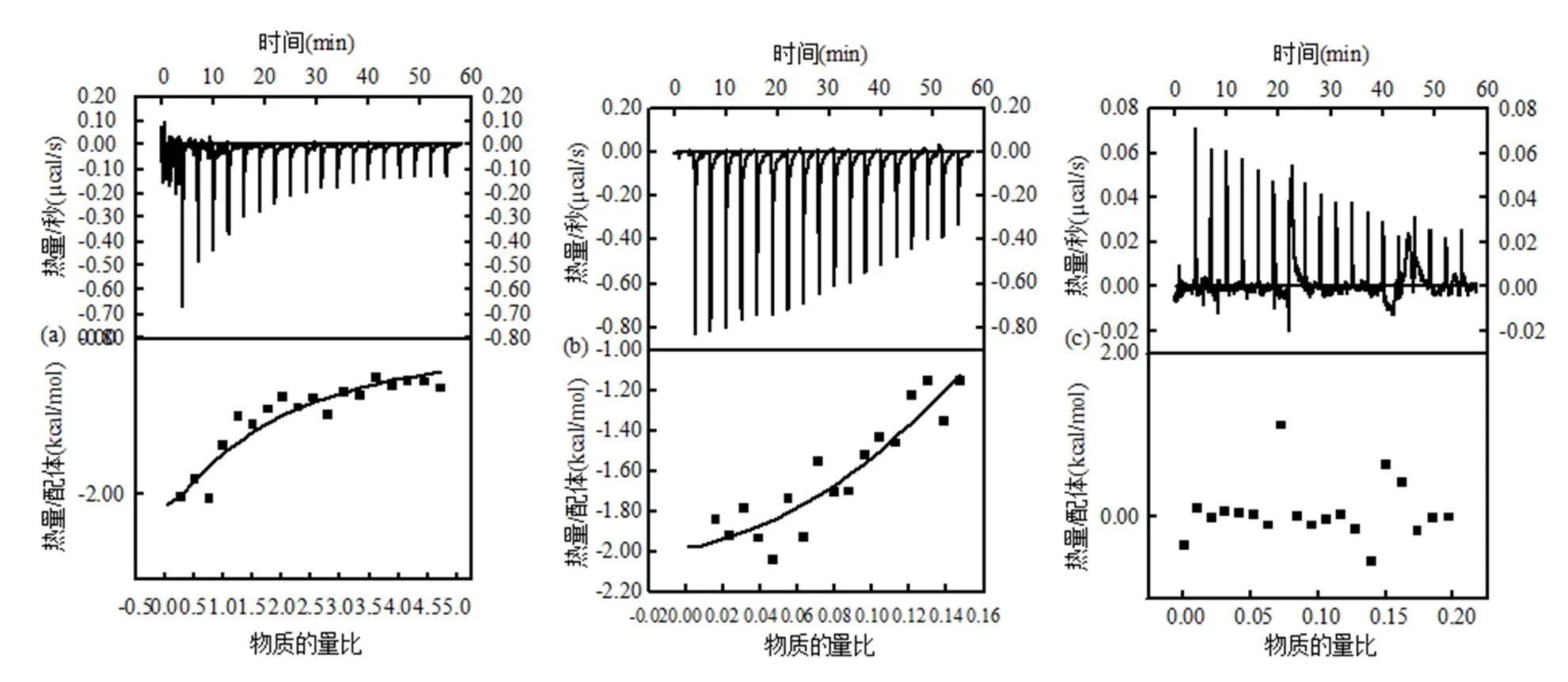
图1 SMZ与EPS模拟物结合的热谱图和非线性拟合
a- SMZ to BSA,b- SMZ to HA-Na,c- SMZ to Glucan
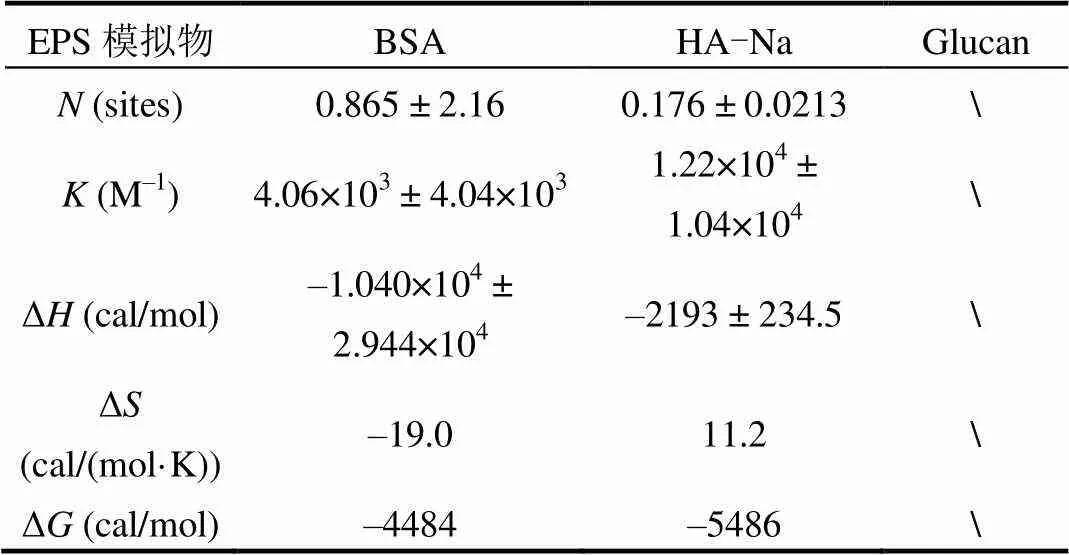
表1 SMZ与EPS模拟物的反应热力学参数
2.2 pH、离子强度对结合反应的影响
不同pH条件下EPS分别与SMZ的滴定反应的热谱图及非线性拟合图分别如图2所示.热谱图均有典型的负峰,表明EPS与SMZ的结合在不同pH条件下均为放热反应.EPS与SMZ在接近中性条件时结合放出的热量相对酸性和碱性条件下较小,拟合曲线斜率较低.由表2中EPS与SMZ结合的热力学参数可知,不同pH条件下,吉布斯自由能变Δ均小于零,且–ΔpH6.8>– ΔpH8.0>–ΔpH5.7,表明EPS与SMZ的结合反应在热力学上是有利的自发反应,在pH 6.8时反应在热力学上最为有利;结合常数的大小顺序为:pH6.8>pH8.0>pH5.7,且pH6.8高出一个数量级,表明EPS-SMZ结合物在近中性条件下稳定性最好;EPS与SMZ结合过程中反映构象变化的熵变Δ均大于零,大小顺序为ΔpH6.8>ΔpH8.0>ΔpH5.7,表明体系的无序度均增加[18],且在近中性条件时体系构象变化最大;由|Δ|<|TΔ|,表明EPS与SMZ的结合反应是以疏水性相互作用为主要驱动力的熵驱动过程[19],不同pH条件下EPS与SMZ结合的化学计量数变化不大且均接近1sites,皆略大于与EPS的蛋白类模拟物BSA与SMZ的结合化学计量数(0.865sites),表明EPS中的蛋白类物质在结合SMZ的过程中发挥着重要作用.由此可知,EPS与SMZ的结合化学计量比受到溶液pH的影响程度不大,但在近中性条件pH 6.8时,EPS与SMZ的结合反应热力学上最为有利,构象变化最大,EPS-SMZ结合物稳定性最高.
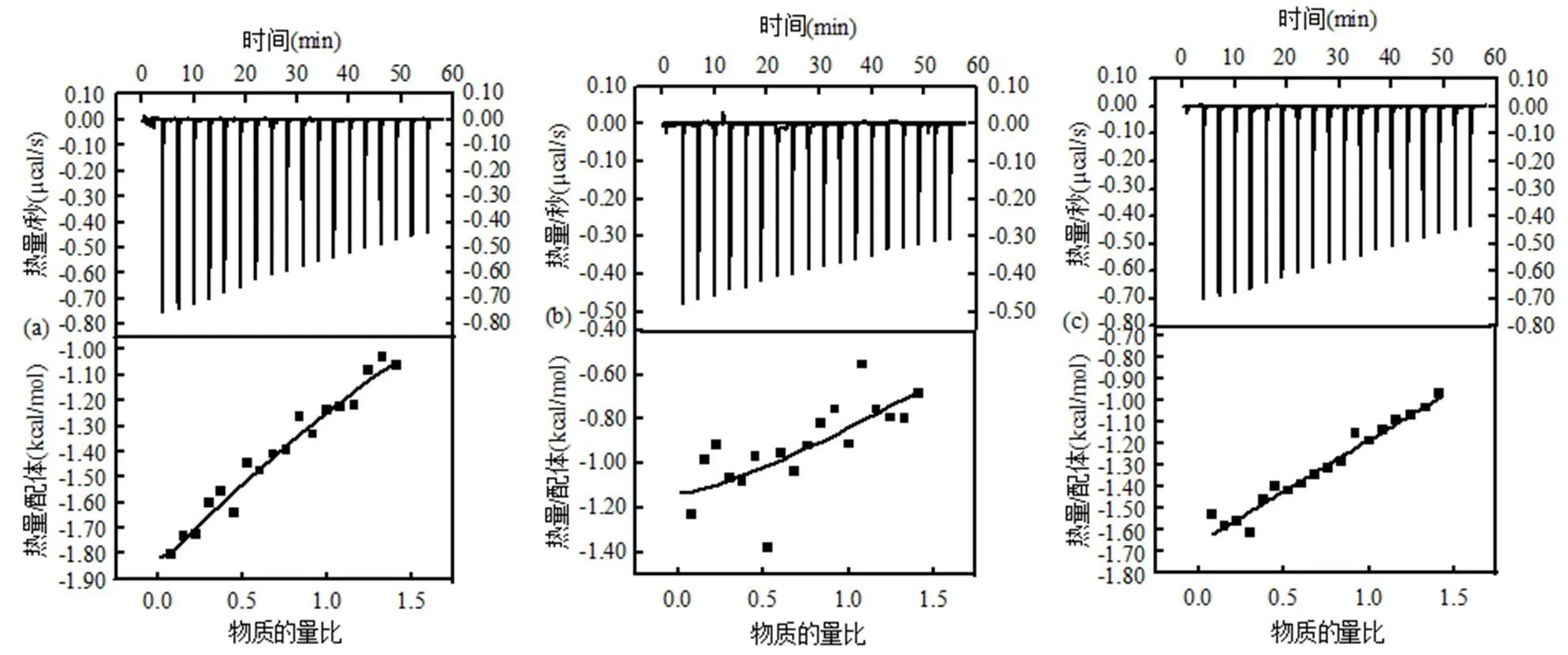
图2 不同pH下对SMZ与EPS结合的热谱图及其非线性拟合
a- pH 5.7,b- pH 6.8,c- pH 8.0
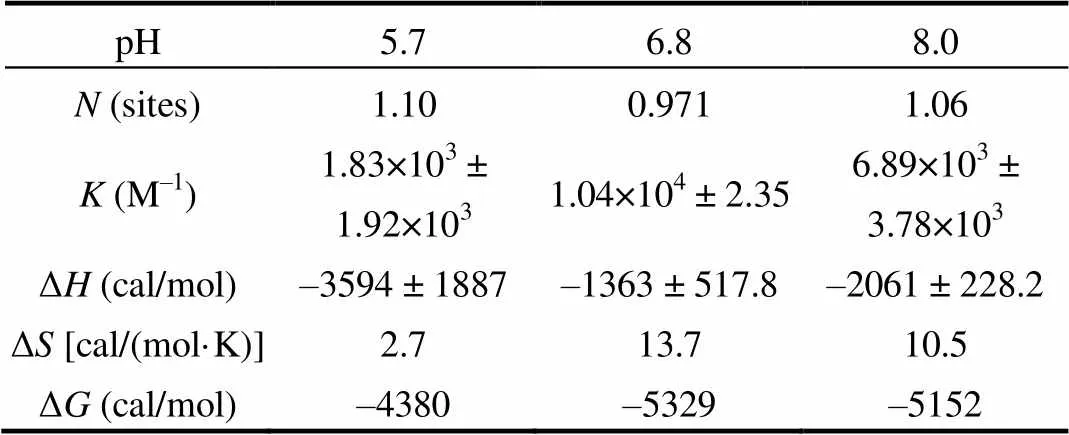
表2 不同pH下SMZ与EPS反应的热力学参数
不同离子强度(IS)下EPS与SMZ滴定反应的热谱图及非线性拟合图分别如图3所示.从图3可以看出,离子强度IS 1(5mmol/L)和IS 3(500mmol/L)条件下,EPS和SMZ反应的热谱图均出现典型的负峰,表明在低离子强度和高离子强度下的结合均为放热反应;而在IS 2(50mmol/L)条件下,EPS与SMZ反应的热谱图均为正峰,表明该条件下的结合反应为吸热反应.
据表3,各离子强度下EPS与SMZ结合的吉布斯自由能变Δ均为负,表明反应均是热力学上有利的自发过程.在离子强度为5mmol/L时,Δ为–4.10´104cal/(mol×K),表明EPS与SMZ在该条件下的结合中体系有序度大幅增加,结合化学计量数极小.在离子强度为50mmol/L时,Δ(1555 ± 394.0) cal/mol为正,表明在该条件下的反应是一个吸热过程.由式知,负焓变和正熵变有利于热力学的自发反应,在溶液离子强度50mmol/L时,Δ> 0,Δ> 0,表明该反应是一个由熵驱动的过程;离子强度500mmol/L时,Δ< 0,Δ> 0,表明在高离子强度下,EPS与SMZ的结合反应是一个由焓熵共同驱动的过程,但|Δ|<|TΔ|,表明结合反应主要是以疏水性相互作用为主要驱动力的熵驱动过程[17].对比离子强度分别为5mmol/L、50mmol/L及500mmol/L条件下EPS与SMZ结合的热力学参数大小,发现离子强度5mmol/L时,EPS与SMZ结合微弱;IS在50mmol/L和500mmol/L之间,溶液离子强度越高,EPS与SMZ的结合常数和负吉布斯自由能变–Δ越大,表明高离子强度下EPS与SMZ的结合更易自发进行,且EPS-SMZ结合物更稳定;但焓变绝对值|Δ|、熵变Δ和结合化学计量数越小,表明高离子强度不利于EPS与SMZ的大量结合.综上表明,EPS与SMZ的相互作用受离子强度影响显著,过低和过高离子强度均不利于二者的结合.
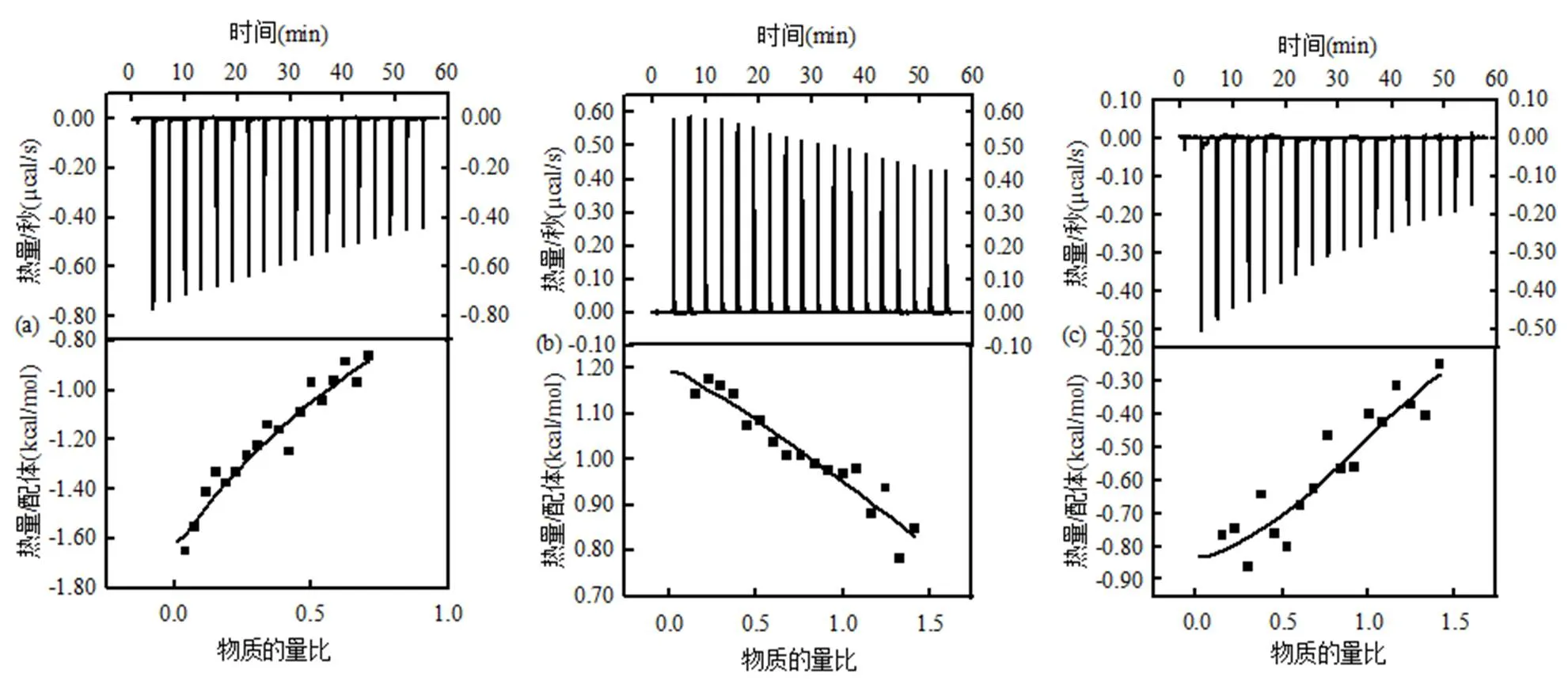
图3 不同离子强度下对SMZ与EPS结合的热谱图及其非线性拟合
a-5mmol/L,b-50mmol/L,c-500mmol/L

表3 不同离子强度下SMZ与EPS反应热力学参数
3 结论
3.1 SMZ与BSA的结合化学计量数为0.865sites,结合是以氢键和范德华力为主要作用力的焓驱动过程;SMZ与HA-Na的结合化学计量数为0.176sites,结合是以疏水性相互作用为主要驱动力的熵驱动过程.SMZ与葡聚糖无明显结合.因此在活性污泥系统中,SMZ的去除过程EPS的蛋白类物质发挥着重要作用,EPS与SMZ的结合是以疏水性相互作用为主要驱动力的熵驱动过程.
3.2 pH对EPS与SMZ结合化学计量数的影响较小,但在中性条件时,EPS与SMZ的结合反应在热力学上最为有利,体系构象变化最大,且EPS-SMZ结合物稳定性最高.
3.3 离子强度对EPS与SMZ的相互作用具有显著影响EPS与SMZ在离子强度5mmol/L时,结合微弱;在50mmol/L和500mmol/L之间,离子强度越高,EPS与SMZ的结合更易自发进行,且复合物更稳定,但结合化学计量数较小.
[1] Thiele-Bruhn S. Pharmaceutical antibiotic compounds in soils a review [J]. Journal of Plant Nutrition and Soil Science, 2003,166:145-167.
[2] Zhou Q, PENG D P, Wang Y L, et al. A novel hapten and monoclonal-based enzyme-linked immunosorbent assay for sulfonamides in edible animal tissues [J]. Food Chemistry, 2014,154:52-62.
[3] Chen Y S, Schwack W. Rapid and selective determination of multi-sulfonamides by high-performance thin layer chromatography coupled to fluorescent densitometry and electrospray ionization mass detection [J]. Journal of Chromatography A, 2014,1331:108-116.
[4] Heberer T. Occurrence,fate,and removal of pharmaceutical residues in the aquatic environment: a review of re-cent research data [J]. Toxicology Letters, 2002,131:5-17.
[5] 赵 健,杨晓凡,周福来,等.固相萃取/高效液相色谱/串联质谱法测定磺胺类抗生素 [J]. 中国给水排水, 2012,28(14):98-101.
[6] Badireddy A R, Chellam S, Gassman P L,et al. Role of extracellular polymeric substances in bioflocculation of activated sludge microorganisms under glucose-controlled conditions [J]. Water Research, 2010,44:4505-4516.
[7] Ueshima M, Ginn Brian R, Haack Elizabeth A,et al. Cd adsorption onto Pseudomonas putida in the presence and absence of extracellular polymeric substances [J]. Geochimica Et Cosmochimica Acta, 2008,72:5885-5895.
[8] Guibaud G, Comte S, Bordas F,et al. Comparison of the complexation potential of extracellular polymeric substances (EPS), extracted from activated sludges and produced by pure bacteria strains, for cadmium, lead and nickel [J]. Chemosphere, 2005,59:629-638.
[9] D’Abzac P, Bordas F, Van Hullebusch E,et al. Effects of extraction procedures on metal binding properties of extracellular polymeric substances (EPS) from anaerobic granular sludges [J]. Colloids and Surfaces B-Biointerfaces, 2010,80:161-168.
[10] Martin J, Camacho-Munoz D, Santos J,et al. Occurrence of pharmaceutical compounds in wastewater and sludge from wastewater treatment plants: Removal and ecotoxicological impact of wastewater discharges and sludge disposal [J]. Journal of Hazardous Materials, 2012,239:40-47.
[11] Radjenovic J, Petrovic M, Barcelo D. Fate and distribution of pharmaceuticals in wastewater and sewage sludge of the conventional activated sludge (CAS) and advanced membrane bioreactor (MBR) treatment [J]. Water Research, 2009,43(3): 831-841.
[12] Xu J, Sheng G P, Ma Y, et al. Roles of extracellular polymeric substances (EPS) in the migration and removal of sulfamethazine in activated sludge system [J]. Water Research, 2013,47:5298- 5306.
[13] 周 洁,玉延华,胡 炜,等.圆二色与等温滴定微量热技术检测3种微量元素与人血清白蛋白的结合[J]. 基因组学与应用生物学, 2014,33(2):413-417.
[14] Frank B P, Belfort G. Polysaccharides and sticky membrane surfaces: critical ionic effects [J]. Journal of Membrane Science, 2003,212:205-212.
[15] Ye Y, Le Clech P, Chen V, et al. Fouling mechanisms of alginate solutions as model extracellular polymeric substances [J]. Desalination, 2004,175:7-20.
[16] Priyananda P, Chen V. Flux decline during ultrafiltration of protein-fatty acid mixture [J]. Journal of Membrane Science, 2006,273:58-67.
[17] Mrinmoy D, YOU C C, Srivastava S,et al.Biomimetic interactions of proteins with functionalized nanoparticles: A thermodynamic study [J]. Journal of the American Chemical Society, 2007,129:10747-10753.
[18] Xu J, Sheng G P, Ma Y,et al.Roles of extracellular polymeric substances (EPS) in the migration and removal of sulfamethazine in activated sludge system [J]. Water Research, 2013,47:5298- 5306.
[19] Ross P D, Subramabian S. Thermodynamics of protein association reactions - forces contributing to stability [J]. Biochemistry, 1981,20:3096-3102.
Thermochemical mechanism of the interaction between sulfamethazineantibiotics and extracellular polymers.
WANG Jing1, ZHANG Cheng-cheng2, JI Fang-ying2*, YAN Peng3
(1.Department of Traffic and Municipal Engineering, Chongqing Jianzhu College, Chongqing 400072, China;2.Key Laboratory of the Three Gorges Reservoir Region’s Eco-Environments, Ministry of Education, Chongqing University, Chongqing 400045, China;3.Chongqing Institute of Green and Intelligent Technology, Chinese Academy of Sciences, Chongqing 400714, China)., 2017,37(10):3758~3763
Thermodynamic parameters of interactions between extracelluar polymeric substances (EPS) and sulfamethazine antibiotics were investigated by isothermal titration calorimetry (ITC) in this study. Results showed that extracellular proteins strongly combined with sulfamethazine (SMZ), and the binding process depended on entropy driven by the hydrophobic interaction as the main driving force. The binding was significantly affected by pH and ionic strength. The binding of EPS and SMZ and the conformational change was the most favorable and the maximal, respectively, at the condition of pH 6.8. The ionic strength had a significant effect on the interaction between EPS and SMZ. The results implied that EPS contained in activated sludge may had a significant influence on the fate of antibiotics in water environment.
extracelluar polymeric substances;isothermal titration calorimetry (ITC);sulfamethazine;pH;ionic strength
X703
A
1000-6923(2017)10-3758-06
王 静(1985-),女,四川乐山人,硕士,讲师,主要从事水污染控制技术研究.发表论文10篇.
2017-03-30
国家水体污染控制与治理重大科技专项(2013ZX07315- 001-02);重庆市建设科技计划项目(城科字2015第1-32号);重庆市教委科学技术研究项目(:KJ1504207);重庆建筑工程职业学院青年基金项目.
* 责任作者, 教授, jfy@cqu.edu.cn
