医疗器械溶血性能评价方法-NIH法的直接接触法和间接接触法比较
2017-11-06乔春霞屈秋锦赵增琳侯丽杨婧董秀丽
乔春霞 屈秋锦 赵增琳 侯丽 杨婧 董秀丽
1 国家食品药品监督管理局济南医疗器械质量监督检验中心;山东省医疗器械生物学评价重点实验室 (山东 济南 250101)2 山东恒信检测技术开发中心 (山东 济南 250101)
医疗器械溶血性能评价方法-NIH法的直接接触法和间接接触法比较
乔春霞1屈秋锦2赵增琳2侯丽1杨婧2董秀丽2
1 国家食品药品监督管理局济南医疗器械质量监督检验中心;山东省医疗器械生物学评价重点实验室 (山东 济南 250101)2 山东恒信检测技术开发中心 (山东 济南 250101)
根据ISO/TC194WG9的要求进行溶血比对(Round robin)试验。采用NIH(National Institutes of Health,美国国立卫生研究院)直接接触法和间接接触法测定了5种材料的溶血性能,结果显示聚乙烯、丁腈手套、#1橡胶和#2橡胶的溶血等级判定结果在两种方法是一致的,但是丁腈手套的两种方法的溶血率值有显著差异。乳胶手套的溶血率和判定结果不一致。作者分析了这些不一致产生的原因,为医疗器械或材料的溶血性能检测提出了一些建议,为新标准的发布和实施提供数据支持。
医疗器械 溶血性能 NIH方法
医疗器械本身或使用不当可能会导致溶血的发生,从而为临床带来一些不利的影响,因此评价医疗器械的溶血性能是很有意义的筛选试验。国际标准ISO 10993-4:2017(E)[1]中列出了三种试验方法供选择,分别是ASTM(American Society for Testing and Materials,美国材料与试验协会)F756-08[2]、NIH[3]和MHLW[4](日本劳动健康福利局)发布的关于溶血的方法。国内的标准有GB/T14233.2-2005[5]和GB/T16175-2008[6]等。GB/T14233.2-2005和GB/T16175-2008的方法相似,其与NIH法也是基本一致的。在这些关于NIH方法的标准中只是推荐采用直接法,本文根据ISO/TC194WG9进行溶血比对(Round robin)试验的要求,将NIH间接法与NIH直接法进行比较,探讨NIH间接法在医疗器械溶血性能检测中的可行性,为新标准制定提供数据支持。
1.资料与方法
1.1 临床资料
材料:材料有5种,分别是a:聚乙烯,b:丁腈手套,c:乳胶手套,d:#1橡胶,e:#2橡胶。
仪器设备:主要有分光光度计,水浴摇床和离心机。
1.2 方法
1.2.1 样品制备
严格按照表1列出的样品大小切割试验样品,每个试验样品平行3管,分别置于20mm×150mm玻璃试管中。
直接接触法:每支试管中各加入10mL生理盐水。同时制备阴性对照和阳性对照,分别加入10mL生理盐水和0.1%碳酸钠。制备1管空白管,加入10mL生理盐水。
间接接触法:每支试管中加入11mL生理盐水。阴性对照、阳性对照和空白管制备方法同直接接触法。将所有试管置于(37±2)˚C水浴中,60r/min振荡孵育(72±2)h。将孵育后各管中的浸提液移出10mL至新的玻璃试管中。
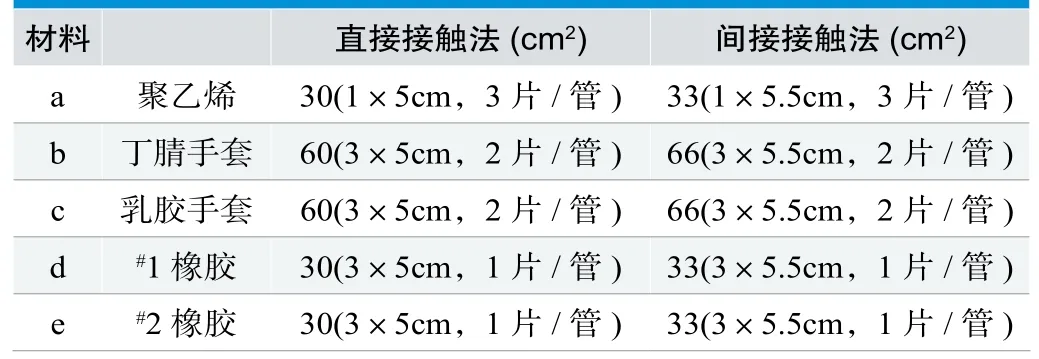
表1. 试验样品
1.2.2 兔血制备
新西兰白兔3只,每只抽取颈静脉血5mL,置于0.109M/3.2%枸橼酸钠抗凝的采血管中,混合得到15mL血液。取8mL,加入10mL生理盐水中混匀,得到稀释的兔血。
取10mL0.1%的碳酸钠置于玻璃试管中,加入稀释的兔血0.2mL。545nm条件下,用生理盐水调0,立即测定混合物的吸光度。本试验要求吸光度在0.90~1.00(透过率在10%~13%)稀释的兔血才能用于试验。
1.2.3 与血液接触
将按照3.1制备的所有试管置于(37±2)˚C水浴中孵育30min后加入3.2制备的稀释兔血0.2mL,空白管除外。将所有试管置于(37±2)˚C水浴中孵育(60±5)min。
1.2.4 结果测定
孵育结束后,所有试管中液体被移入到离心管中,500g离心5min。用空白管液体调0,545nm测定各管上清液的吸光度值。阳性对照管的吸光度值应大于0.90,否则应重新进行试验。
1.2.5 计算溶血率
按下列公式,计算得出a-e每个试验样品每管的溶血率值:
溶血率(%)=(T–Navg)/(Pavg–Navg)×100
T=每管试验样品OD值

表2. NIH法溶血结果判定
N=3管阴性对照平均OD值
P=3管阳性对照平均OD值
1.2.6 判定标准
计算每个试验样品3管溶血率的平均值按表2进行结果判定。
1.3 统计学分析
分别计算每周试验结果及3周试验结果的±s,对各个试验样品的试验结果(溶血率)的统计学分析采用方差分析,P<0.05表示具有统计学差异。
2.结果
2.1 实验3次结果比较
由表3可以看出,直接接触法的样品a、d和e的溶血率均小于5%,根据溶血等级判定为不溶血。样品b和c的溶血率均高于5%,根据溶血等级判定为溶血,但样品b的3次结果差异较明显。间接接触法的样品b溶血率为100%,具有溶血活性。样品a、c、d和e的溶血率均低于5%,判定为不溶血,5种试验样品3次结果判定一致。
2.2 直接接触法和间接接触法结果比较
由表4可以看出,样品b和c在直接接触法和间接接触法的结果上有统计学差异,而样品a、d和e的差异不显著。
3.讨论
NIH方法在医疗器械溶血检测中因为其操作的简便性,应用最为广泛。本次研究主要是对NIH直接接触法的重复性、间接接触法的重复性以及直接接触法和间接接触法之间的一致性进行研究,为制定医疗器械材料介导的溶血试验方法行业标准提供数据支持。
为了比较间接接触法和直接接触法之间的一致性,间接接触法选用与直接接触法相同的浸提比例和浸提温度。试验样品b在直接接触法3周试验中的重复性较差,考虑可能的原因是由于手套比较柔软,且试验时切割的样品比较大容易折叠在一起或容易紧贴管壁。
虽然试验样品b的直接接触法和间接接触法的溶血等级判定在同一个级别,但间接接触法的溶血率显著高于直接接触法,说明经过72 h的孵育,样品中能影响红细胞的物质充分释放至浸提液中,而直接接触法因为样品与浸提介质之间的接触时间只有90min,所以浸提出的有害物质较少。试验样品c直接接触法的溶血率显著高于间接接触法,两种方法的溶血性能不在同一级别,样品c是乳胶手套,质地较柔软,样品制备成3cm×5cm大小的长方形,没有尖锐的可以损伤红细胞的边角,因此溶血的发生与样品物理性状无关[7]。试验样品c在直接接触法检测时出现溶血现象的原因可能是某种物质存在与样品表面,直接与红细胞接触导致红细胞膜破损,释放血红蛋白。但是这种物质可能不溶于水,不会释放入浸提液中,所以间接接触法不会导致红细胞膜损伤。
综合分析结果,间接接触法的重复性要优于直接接触,但是两种方法检测结果的一致性不能一概而论。同时进行直接接触法和间接接触法试验,对一种未知医疗器械或材料的溶血性能检测是最好的选择。本次研究只是将NIH方法两种方法进行比较,得到的数据有限,下一步还将进行NIH方法、ASTM方法和MHLW方法之间的一致性问题,同时考虑兔血和人血对溶血性能的影响,为三种方法和结果的互换性提供依据。
[1] ISO 10993-4:2017 (E).Biological evaluation of medical devices -- Part 4:Selection of tests for interactions with blood[S].2017.
[2] ASTM F 756-08.Standard Practice for Assessment of Hemolytic Properties of Materials[Z].Astm,2008.
[3] Evaluation of hemodialyzers and dialysis membranes.Report of a Study Group for the Artificial Kidney-Chronic Uremia Program NIAMDD-1977.Chapter two.In vitro characterization of hemodialyzers[J].Artif Organs 1977,1(2):59-77.
[4] MHLW Notification by Director,OMDE,Yakushokuki-hatsu 0301 No.20,March 1,2012,Basic Principles of Biological Safety Evaluation Required for Application for Approval to Market Medical Devices[Z].2012.
[5] GB/T 14233.2-2005 Infusion,transfusion,injection equipment for medical use -Part2:Biological test methods [医用输液、输血医用输液、输血、注射器具检验方法第2 部分:生物学试验方法] [S].2005.
[6] GB/T 16175-1996,Organic silicone material for medical use — Biological evaluation test methods[S].1996.
[7] 孙皎,刘义荣,钱云芳.生物材料试样形状对溶血率的影响[J].口腔材料器械杂志,1993,2(2):17.
Comparison of Direct Contact Method and Indirect Contact Method for Evaluation of Hemolytic Performance of Medical Device-NIH Method
QIAO Chun-xia1QU Qiu-jin2ZHAO Zeng-lin2HOU Li1YANG Jing2DONG Xiu-li2
1 Jinan Quality Supevision and Inspection Center for Medical Device, CFDA; Shandong Provincial Key Laboratory of Biological Evaluation for Medical Devices (Shandong Jinan 250101)2 Shandong Hengxin Testing Technology Development Center (Shandong Jinan 250101)
1006-6586(2017)17-0042-02
R197.39
A
2017-07-12
表4. 直接接触法和间接接触法结果比较(±s,%)

表4. 直接接触法和间接接触法结果比较(±s,%)
*直接接触法与间接接触法相比,P<0.01
试验样品 溶血率直接接触法 间接接触法a 0.53±0.4 1.50±1.5 b 61.97±31.6 104.51±7.5*c 19.48±2.1 1.08±1.6*d 0.40±0.5 0.38±1.0 e 0.14±0.6 0.30±0.7
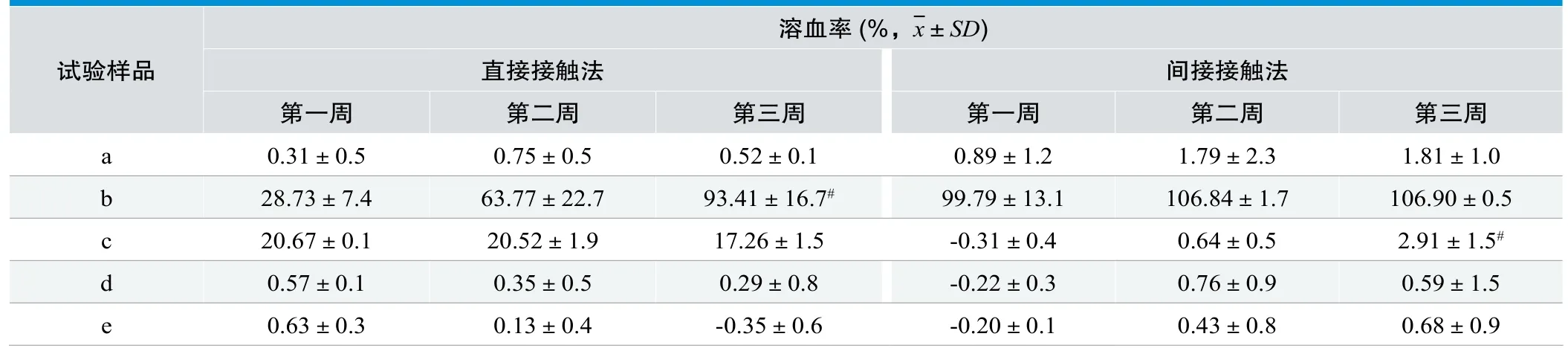
表3. 试验3次结果比较
