CH3CONH2/ZnCl2低共熔溶剂脱除模拟油中的硫化物
2017-11-02毛春峰赵荣祥李秀萍尹云智
毛春峰, 赵荣祥, 李秀萍, 刘 天, 张 哲, 尹云智, 张 磊
(1.辽宁石油化工大学 化学化工与环境学部,辽宁 抚顺 113001; 2.营口市食品安全检验检测中心,辽宁 营口 115004; 3.中国石油抚顺石化公司,辽宁 抚顺 113008)
CH3CONH2/ZnCl2低共熔溶剂脱除模拟油中的硫化物
毛春峰1, 赵荣祥1, 李秀萍1, 刘 天2, 张 哲3, 尹云智3, 张 磊3
(1.辽宁石油化工大学 化学化工与环境学部,辽宁 抚顺 113001; 2.营口市食品安全检验检测中心,辽宁 营口 115004; 3.中国石油抚顺石化公司,辽宁 抚顺 113008)
在110 ℃下,加热搅拌乙酰胺和氯化锌混合物制备了CH3CONH2/ZnCl2低共熔溶剂,对其结构进行了电喷雾电离质谱分析、红外分析和黏度分析。以CH3CONH2/ZnCl2作为萃取剂和催化剂,H2O2作为氧化剂,氧化脱除模拟油中的噻吩硫化物。对n(ZnCl2)/n(CH3CONH2)、n(H2O2)/n(S)、反应温度、剂油体积比和不同硫化物对脱硫率的影响进行了考察。在模拟油体积5 mL、n(ZnCl2)/n(CH3CONH2)=0.4、n(H2O2)/n(S)=8、剂油体积比1∶3、反应温度70 ℃、反应时间200 min的最佳条件下,二苯并噻吩的脱除率达到87.12%。经过5次循环之后,脱硫率略有降低。
氯化锌; 乙酰胺; 低共熔溶剂; 氧化; 脱硫
近些年,随着汽车工业的迅猛发展,汽车尾气排放造成的环境污染也日益加剧,雾霾、酸雨等恶劣的天气随之产生[1]。许多国家对油品中硫含量进行了严格的限制,欧洲在2005年将汽油中的硫质量分数限制为50 μg/g,2007年进一步要求汽油中的硫质量分数低于10 μg/g。美国和日本也相继出台硫质量分数低于10 μg/g的低硫汽油标准。中国也逐渐与世界接轨,自2017年1月起逐渐实施汽柴油国Ⅴ标准[2]。
目前,工业上采用传统的加氢技术来脱除汽柴油中的硫化物,但是该脱硫方法对于噻吩类硫化物效果较差[3],为了提升脱硫率,必须提高反应温度和反应压力或者使用活性更高的加氢催化剂[4-5]。这些措施必然会增加设备的运营成本,进而导致油价的上涨。由于以上原因,一些非加氢脱硫例如氧化脱硫、萃取脱硫和生物脱硫等已经引起人们的广泛关注[6-9]。其中,氧化脱硫由于反应条件温和、设备及操作费用低、脱硫效率高等优点成为学界研究的热点。在氧化脱硫体系中双氧水是应用最多的氧化剂,相比于KMnO4、NO2等[10-12],它的副产物只有水,是更加绿色的氧化剂[13]。
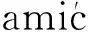
丛晓波[30]采用CH3CONH2和ZnCl2为原料经简单的加热搅拌合成了CH3CONH2/ZnCl2型低共熔溶剂,室温下为液态,其熔点远低于CH3CONH2(78 ℃)和ZnCl2(2 930 ℃),同时具有合成反应时间短、合成过程简单、原料比较低廉等优点。本研究合成了CH3CONH2/ZnCl2低共熔溶剂,以其为萃取剂和催化剂,H2O2用作氧化剂对模拟油中的二苯并噻吩进行氧化脱硫研究,分别对n(ZnCl2)/n(CH3CONH2)、反应温度、n(H2O2)/n(S)、剂油体积比和硫化物对脱硫效果的影响进行了考察,对低共熔溶剂循化利用以及反应机理进行了探讨。
1 实验部分
1.1 试剂与仪器
H2O2(质量分数为30%)、正辛烷、二苯并噻吩(纯度98%,阿拉丁试剂)、苯并噻吩(纯度97%,阿拉丁试剂)、噻吩(纯度99.8%,阿拉丁试剂)、ZnCl2(分析纯)、CH3CONH2(分析纯)、CCl4(纯度99%),以上试剂来自国药集团化学试剂有限公司。硫质量分数的分析采用WK-2D 型微库仑综合分析仪(江苏江分电分析仪器有限公司)。采用Nicolet公司NEXUS670 型红外光谱仪进行傅里叶变换红外光谱(FT-IR) 测定,KBr压片,4 000~400 cm-1扫描。采用Waters Acquity UPLC Premier XE公司的电喷雾质谱仪进行电离质谱分析。
1.2 低共熔溶剂的合成
称取一定量的ZnCl2和CH3CONH2于100 mL的锥形瓶中,在110 ℃下搅拌至澄清溶液,即可得到CH3CONH2·0.4ZnCl2低共熔溶剂,其合成机理如式(1)所示。
(1)
1.3 低共熔溶剂的氧化脱硫方法
称取1.437 g 二苯并噻吩(DBT)、1.047 g苯并噻吩(BT)和0.656 g 噻吩(TH),分别溶解到500 mL的正辛烷中,形成硫质量分数为500 μg/g的模拟油,量取5 mL模拟油、1.67 mLCH3CONH2·0.4ZnCl2低共熔溶剂及一定体积的H2O2加入到锥形瓶(带有回流装置)中,在一定温度下进行磁力搅拌,静止分层后,每20 min吸取一次上层的油相,通过WK-2D微库仑测定硫质量分数,计算脱硫率η:
η=(a-b)/a×100%
(2)
式中,a为反应前油品中硫质量分数;b为反应后油品中的硫质量分数;η为油品中硫化物的脱除率。
2 结果与讨论
2.1 低共熔溶剂的结构表征
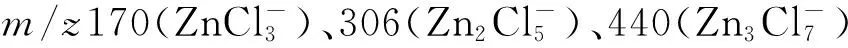

图1 CH3CONH2·0.4ZnCl2 电喷雾质谱
2.1.2 低共熔溶剂的红外分析 图2为CH3CONH2·0.4ZnCl2、ZnCl2以及CH3CONH2的红外图谱。从图2可以看出,在CH3CONH2的红外谱图中1 685、1 151 cm-1分别对应羰基峰和C—C伸缩振动峰;在CH3CONH2与ZnCl2形成低共熔溶剂后其相应的羰基吸收峰由1 685 cm-1向1 656 cm-1的方向移动,而C—C伸缩峰则由1 151 cm-1移动到1 128 cm-1附近,同时可以看到在3 300~3 600 cm-1形成了较强的宽峰,表明ZnCl2与CH3CONH2形成了分子间氢键[30]。氢键的形成使电子云密度平均化,伸缩振动频率降低。综合以上分析可以证实,CH3CONH2/ZnCl2低共熔溶剂已经形成。
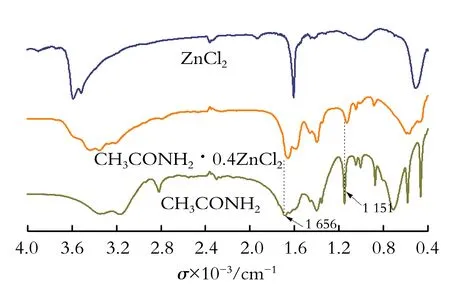
图2 ZnCl2、CH3CONH2·0.4ZnCl2和CH3CONH2的红外图谱
2.1.3 低共熔溶剂的黏度 在不同温度下应用旋转黏度计对CH3CONH2·0.4ZnCl2进行黏度测定,结果见图3。从图3可以看出,CH3CONH2·0.4ZnCl2在50、60、70、80 ℃的黏度依次为900.0、185.0、80.5、54.0 mPa·s。由此可知,低共熔溶剂的黏度随温度升高而降低。
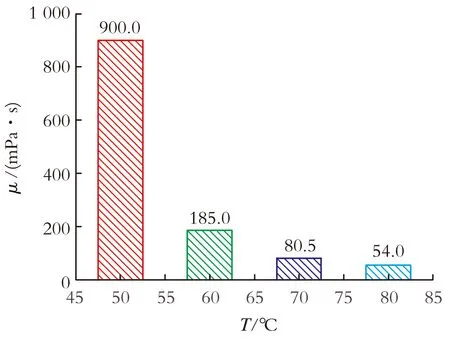
图3 不同温度下CH3CONH2·0.4ZnCl2黏度
2.2 氧化脱硫反应条件的优化
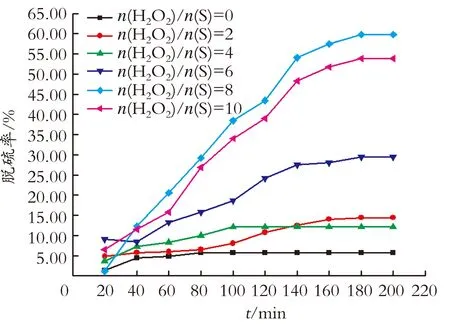
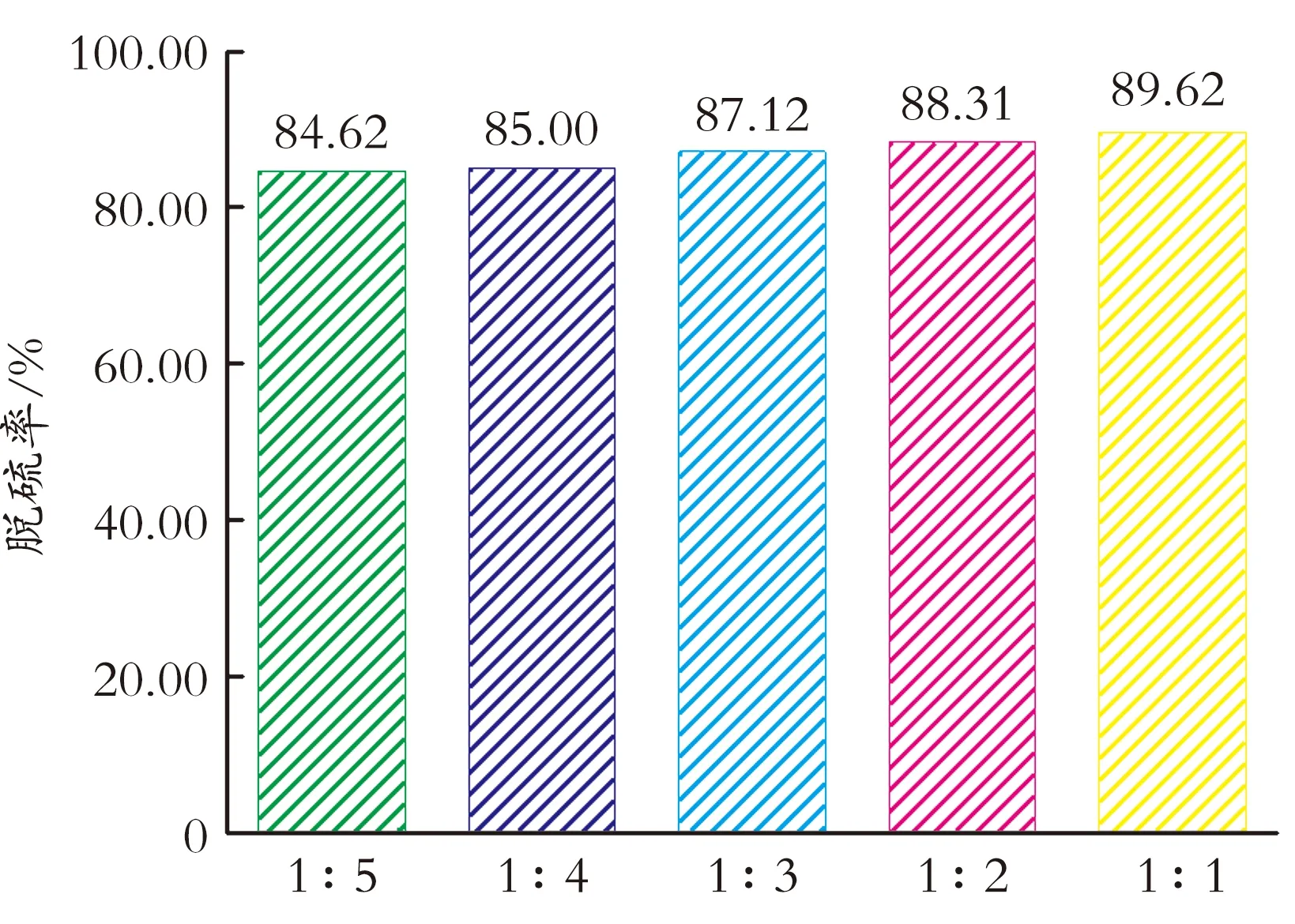
2.2.1n(ZnCl2)/n(CH3CONH2) ZnCl2作为路易斯酸,其含量直接影响低共熔溶剂的酸性。实验按n(ZnCl2)/n(CH3CONH2)合成了6种不同的低共熔溶剂:CH3CONH2·0.1ZnCl2、CH3CONH2·0.2ZnCl2、CH3CONH2·0.3ZnCl2、CH3CONH2·0.4ZnCl2、CH3CONH2·0.5ZnCl2、CH3CONH2·ZnCl2。其酸性顺序为CH3CONH2·0.1ZnCl2 图4 n(ZnCl2)/n(CH3CONH2)对脱硫效果的影响 2.2.2n(H2O2)/n(S) 在H2O2-CH3CONH2·0.4ZnCl2的氧化脱硫系统里,研究了n(H2O2)/n(S)对脱硫效果影响,在模拟油体积为5 mL、剂油体积比为1∶5、反应温度为50 ℃条件下,考察n(H2O2)/n(S)对脱硫效果的影响,结果见图5。从图5可以看出,当不加入H2O2时,其氧化脱硫率仅为5.77%,其原因是此时低共熔溶剂仅具有萃取能力。当n(H2O2)/n(S)从2增加到8时,其脱硫率由14.42%增加到59.81%,由于二苯并噻吩砜(DBTO2)的极性比二苯并噻吩高,与低共熔溶剂相似相溶,二苯并噻吩砜能够更好地溶解到低共熔溶剂中,进而从油品中除去。由氧化脱硫过程的化学计量比可知,1 mol的二苯并噻吩每消耗2 mol的H2O2可以获得1 mol相应的二苯并噻吩砜,然而,n(H2O2)/n(S)=8时的脱硫率远远高于n(H2O2)/n(S)=2时的14.42%,这是因为在氧化脱硫过程中,一些H2O2出现了分解,需要额外的H2O2将DBT氧化成DBTO2[32]。当n(H2O2)/n(S)继续由8增加到10时,其脱硫率由59.81%下降到53.85%,这是因为H2O2的量增加到一定程度时, 其分解为氧气的副反应速率也随着增加,氧源有效利用率下降[33],此外过多的H2O2会稀释离子液体相,降低离子液体的萃取脱硫能力[34]。因此,最佳的n(H2O2)/n(S)=8。 图5 n(H2O2)/n(S)对脱硫效果的影响 2.2.3 反应温度 在模拟油体积为5 mL、n(H2O2)/n(S)=8、剂油体积比为1∶5条件下,考察反应温度对脱硫效果的影响,结果见图6。 图6 反应温度对脱硫效果的影响 从图6可以看出,随着反应温度由50 ℃升高到70 ℃,脱硫率相应地从59.81%升高到84.62%,在此氧化脱硫体系中温度的影响体现在两个方面:一方面,提高反应温度可以提高催化剂的活性;另一方面,提高反应温度可以降低低共熔溶剂的黏度。黏度下降有利于提高传质速率[35],低共熔溶剂的黏度随温度的升高而降低,这将有助于油品中的硫化物从油相进入到离子液体相中[36],然而,当反应温度继续由70 ℃升高到80 ℃时,其脱硫率略有下降。这是因为过高的温度会使过氧化氢的分解速率加快[37]。综上分析,最佳的反应温度为70 ℃。 2.2.4 剂油体积比 低共熔溶剂在该氧化脱硫系统中既是萃取剂也是催化剂。然而,以更少的低共熔溶剂用量来获得更高的脱硫效果是实现工业化生产的前提。在模拟油体积为5 mL、n(H2O2)/n(S)=8、反应温度为70 ℃的条件下,考察剂油体积比对脱硫效果的影响,结果见图7。从图7可以看出,当剂油体积比由1∶5升高到1∶3时,在200 min内其对应的氧化脱硫率由84.62%升高到87.12%。然而,当剂油体积比继续增加到1∶1时,其氧化脱硫率略有上升(89.62%)。考虑到离子液体的成本,最佳剂油体积比为1∶3。 图7 剂油体积比对脱硫效果的影响 在实际油品中,硫的种类极其繁多,为了验证该氧化脱硫体系对不同种类硫的脱硫效果,在最优的反应条件下(模拟油体积5 mL、n(H2O2)/n(S)=8、剂油体积比1∶3、反应温度70 ℃),考察了苯并噻吩和噻吩的脱除效果,并与二苯并噻吩进行了对比,结果见图8。 从图8可以看出,在低共熔溶剂脱硫体系中苯并噻吩和噻吩的脱除率仅为31.12%和10.42%,远低于二苯并噻吩的87.12%。这种脱硫效果的差异与不同硫化物硫原子上的电子云密度密切相关,电子云密度越大,脱硫效果越好。由文献[38]可知,其电子云密度顺序为5.758(DBT)> 5.739(BT)>5.696(TH)。 图8 硫化物类型对脱硫率的影响 氧化脱硫实验完成后,采用分液漏斗回收下层低共熔溶剂相,旋转蒸发仪除去低共熔溶剂相中的水,等体积的CCl4对低共熔溶剂相进行反萃取3次,真空干燥箱进行干燥后得到回收的低共熔溶剂,加入新鲜的H2O2和模拟油在最优条件下(模拟油体积5 mL、n(H2O2)/n(S)=8、剂油体积比1∶3、反应温度70 ℃、反应时间200 min)进行氧化脱硫实验,结果见表1。由表1可知,低共熔溶剂循环使用5次后,其脱硫率下降到85.49%。脱硫率下降原因:一方面,低共熔溶剂在回收过程中有损失;另一方面,回收的低共熔溶剂中含有二苯并噻吩砜等杂质,对脱硫效果产生影响[39]。 表1 CH3CONH2·0.4ZnCl2的循环利用 为了获得氧化产物的结构信息,在70 ℃下采用旋转蒸发仪除去低共熔溶剂相中的水,用CCl4(V(CCl4)/V(IL)=2∶1)进行反萃取,在室温下搅拌45 min,静止24 h,使用旋转蒸发仪将CCl4蒸出,得到白色晶体即为氧化产物。将DBT与回收的白色晶体分别进行红外表征,结果见图9。 图9 DBT及其反应产物的红外图谱 从图9可以看出,白色晶体在1 047、1 288、1 166 cm-1处有3个红外吸收峰,通过文献[40-41]可知,DBTO2在1 047、1 288、1 166 cm-1处也有3个红外吸收峰,由此可以证实该白色晶体即为DBTO2。 CH3CONH2/ZnCl2低共熔溶剂和H2O2共同组成的低共熔溶剂相与含有二苯并噻吩的模拟油形成两相。CH3CONH2/ZnCl2低共熔溶剂具有催化和萃取的双重作用:一方面,由于CH3CONH2/ZnCl2可以与油相中硫化物形成稳定的氢键而具有很强的萃取功能,能够将模拟油中的二苯并噻吩萃取到低共熔溶剂相中;另一方面,CH3CONH2/ZnCl2低共熔溶剂具有催化功能。Y.Nie等[42]证实了FeCl3或者 ZnCl2型路易斯酸型低共熔溶剂能够促进H2O2产生具有强氧化性的羟基自由基。羟基自由基可以将低共熔溶剂相中的二苯并噻吩氧化成二苯并噻吩砜(DBTO2)。由于浓度的差异,油相中的二苯并噻吩可以连续不断地被萃取到低共熔溶剂相中发生氧化脱硫反应,直到H2O2消耗完全为止。具体的氧化脱硫机理如式(3)所示。 (3) 在110 ℃下,搅拌CH3CONH2和ZnCl2的混合物合成了CH3CONH2/ZnCl2低共熔溶剂。通过电喷雾电离质谱和红外光谱可以确认ZnCl2可以和CH3CONH2形成稳定的氢键。该氢键的形成可有效降低混合物的熔点。使用CH3CONH2/ZnCl2作为萃取剂和催化剂,质量分数为30% H2O2作为氧化剂的氧化脱除模拟油中的DBT。在70 ℃下,n(H2O2)/n(S)=8和剂油体积比为1∶3时,200 min其氧化脱硫率可以高达87.12%。低共熔溶剂可以重复使用5次,活性仅略微下降。 [1] Yang R T, Hernández-Maldonado A J, Yang F H. Desulfurization of transportation fuels with zeolites under ambient conditions[J]. Science, 2003, 301(5629):79-81. [2] 董楠. 国五排放标准给企业和市场缓冲时间[J]. 轻型汽车技术, 2016(3):1. [3] Lü H, Gao J, Jiang Z, et al. Ultra-deep desulfurization of diesel by selective oxidation with [C18H37n(CH3)3]4[H2NaPW10O36] catalyst assembled in emulsion droplets[J]. Journal of Catalysis, 2006, 239(2):369-375. [4] Oyama S T, Zhao H, Freund H J, et al. Unprecedented selectivity to the direct desulfurization(DDS) pathway in a highly active FeNi bimetallic phosphide catalyst[J]. Journal of Catalysis, 2012, 285(1):1-5. [5] Mondal S, Hangun-Balkir Y, Alexandrova L, et al. Oxidation of sulfur components in diesel fuel using Fe-TAML© catalysts and hydrogen peroxide[J]. Catalysis Today, 2006, 116(4):554-561. [6] Moaseri E, Shahsavand A, Bazubandi B. Microwave-assisted oxidative desulfurization of sour natural gas condensate via combination of sulfuric and nitric acids[J]. Energy & Fuels, 2014, 28(2):825-831. [7] Shen C, Wang Y J, Xu J H, et al. Synthesis of TS-1 on porous glass beads for catalytic oxidative desulfurization[J]. Chemical Engineering Journal, 2015, 259:552-561. [8] Amaral R A, Habert A C, Borges C P. Activated carbon polyurethane membrane for a model fuel desulfurization by pervaporation[J]. Materials Letters, 2014, 137:468-470. [9] Zhou M, Meng W, Li Y, et al. Extractive and catalytic oxidative desulfurization of gasoline by methyltrioxorhenium in ionic liquids[J]. Energy & Fuels, 2013, 28(1):516-521. [10] Lv Q, Li G, Sun H. Synthesis of hierarchical TS-1 with convenient separation and the application for the oxidative desulfurization of bulky and small reactants[J]. Fuel, 2014, 130:70-75. [11] Wang X, Chen W, Song Y F. Directional self-assembly of exfoliated layered europium hydroxide nanosheets and Na9EuW10O36· 32H2O for Application in Desulfurization[J]. European Journal of Inorganic Chemistry, 2014, 2014(17):2779-2786. [12] Zhang J, Wang A, Wang Y, et al. Heterogeneous oxidative desulfurization of diesel oil by hydrogen peroxide:Catalysis of an amphipathic hybrid material supported on SiO2[J]. Chemical Engineering Journal, 2014, 245:65-70. [13] 蔡永宏,贺建勋, 邹煜, 等.杂多酸季铵盐催化氧化脱除模拟汽油中苯并噻吩[J].西北大学学报(自然科学版), 2011, 41(4):628-632. [14] Nie Y, Li C, Sun A, et al. Extractive desulfurization of gasoline using imidazolium-based phosphoric ionic liquids[J]. Energy & Fuels, 2006, 20(5):2083-2087. [15] Abbott A P, Capper G, Davies D L, et al. Novel solvent properties of choline chloride/urea mixtures[J]. Chemical Communications, 2003(1):70-71. [16] Zhang Q, Vigier K D O, Royer S, et al. Deep eutectic solvents:Syntheses, properties and applications[J]. Chemical Society Reviews, 2012, 41(21):7108-7146. [17] Wu S H, Caparanga A R, Leron R B, et al. Vapor pressure of aqueous choline chloride-based deep eutectic solvents(ethaline, glyceline, maline and reline) at 30-70 ℃[J]. Thermochimica Acta, 2012, 544:1-5. [18] Carriazo D, Serrano M C, Gutiérrez M C, et al. Deep-eutectic solvents playing multiple roles in the synthesis of polymers and related materials[J]. Chemical Society Reviews, 2012, 41(14):4996-5014. [19] del Monte F, Carriazo D, Serrano M C, et al. Deep eutectic solvents in polymerizations:A greener alternative to conventional syntheses[J]. Chem. Sus. Chem., 2014, 7(4):999-1009. [20] Smith E L, Abbott A P, Ryder K S. Deep eutectic solvents(DESs) and their applications[J]. Chemical Reviews, 2014, 114(21):11060-11082. [21] Corma A, Garcia H. Lewis acids:From conventional homogeneous to green homogeneous and heterogeneous catalysis[J]. Chemical Reviews, 2003, 103(11):4307-4366. [22] Li Z, Jia Z, Luan Y, et al. Ionic liquids for synthesis of inorganic nanomaterials[J]. Current Opinion in Solid State and Materials Science, 2008, 12(1):1-8. [24] Mokhtar W N A W, Bakar W A W A, Ali R, et al. Deep desulfurization of model diesel by extraction with N, N-dimethylformamide:Optimization by Box-Behnken design[J]. Journal of the Taiwan Institute of Chemical Engineers, 2014, 45(4):1542-1548. [25] Li F, Liu Y, Sun Z, et al. Deep extractive desulfurization of gasoline withxEt3NHCl·FeCl3ionic Liquids[J]. Energy & Fuels, 2010, 24(8):4285-4289. [26] Gano Z S, Mjalli F S, Al-Wahaibi T, et al. The novel application of hydrated metal halide(SnCl2·2H2O)-based deep eutectic solvent for the extractive desulfurization of liquid fuels[J]. International Journal of Chemical Engineering and Applications, 2015, 6(5):367-371. [27] Wang X, Jiang W, Zhu W, et al. A simple and cost-effective extractive desulfurization process with novel deep eutectic solvents[J]. RSC Advances, 2016, 6(36):30345-30352. [28] Chen X, Guo H, Abdeltawab A A, et al. Brønsted-Lewis acidic ionic liquids and application in oxidative desulfurization of diesel fuel[J]. Energy & Fuels, 2015, 29(5):2998-3003. [29] Yin J, Wang J, Li Z, et al. Deep desulfurization of fuels based on an oxidation/extraction process with acidic deep eutectic solvents[J]. Green Chemistry, 2015, 17(9):4552-4559. [30] 丛晓波. 离子液体的制备及性质研究[D]. 昆明:昆明理工大学, 2011. [31] Jiang Y, Zhu W, Li H, et al. Oxidative desulfurization of fuels catalyzed by fenton-like ionic liquids at room temperature[J]. Chem. Sus. Chem., 2011, 4(3):399-403. [32] Gao H, Guo C, Xing J, et al. Extraction and oxidative desulfurization of diesel fuel catalyzed by a Brønsted acidic ionic liquid at room temperature[J]. Green Chemistry, 2010, 12(7):1220-1224. [33] 张存, 王洪娟, 刘涛, 等. 模拟油品氧化脱硫及反应动力学研究[J]. 燃料化学学报, 2011, 39(8):611-614. [34] 李宇慧,冯丽娟,王景刚,等. MoO3/Al2O3介孔催化剂在柴油氧化脱硫中的应用[J]. 石油学报(石油加工), 2011, 27(6):878-83. [35] Wang Y Y, Sun H, Li J, et al. Application of Et3NHCl-AlCl3ionic liquid as an initiator in cationic copolymerization of 1, 3-pentadiene with styrene[J]. Chinese Chemical Letters, 2006, 17(1):117-120. [36] Asumana C, Yu G, Li X, et al. Extractive desulfurization of fuel oils with low-viscosity dicyanamide-based ionic liquids[J]. Green Chemistry, 2010, 12(11):2030-2037. [37] Zhang W, Xu K, Zhang Q, et al. Oxidative desulfurization of dibenzothiophene catalyzed by ionic liquid [BMIm]HSO4[J]. Industrial & Engineering Chemistry Research, 2010, 49(22):11760-11763. [39] Zhang W, Ding Y, Gong J, et al. Oxidative desulfurization of dibenzothiophene catalyzed by carboxyl-functionalized ionic liquid [cmmim] BF4[J]. Journal of Fuel Chemistry and Technology, 2012, 40(5):626-629. [40] Otsuki S, Nonaka T, Takashima N, et al. Oxidative desulfurization of light gas oil and vacuum gas oil by oxidation and solvent extraction[J]. Energy & Fuels, 2000, 14(6):1232-1239. [41] Li C, Jiang Z, Gao J, et al. Ultra-deep desulfurization of diesel:Oxidation with a recoverable catalyst assembled in emulsion[J]. Chemistry-A European Journal, 2004, 10(9):2277-2280. [42] Nie Y, Gong X, Gao H S, et al. Simultaneous desulfurization and denitrogen of liquid fuels using two functionalized group ionic liquids[J]. Science China Chemistry, 2014, 57(12):1766-1773. Removal of Sulfides from Simulated Oil by CH3CONH2/ZnCl2Deep Eutectic Solvent Mao Chunfeng1, Zhao Rongxiang1, Li Xiuping1, Liu Tian2, Zhang Zhe3, Yin Yunzhi3, Zhang Lei3 (1.CollegeofChemistry,ChemicalEngineeringandEnvironmentalEngineering,LiaoningShihuaUniversity,FushunLiaoning113001,China; 2.YingkouFoodSafetyInspectionandTestingCenter,YingkouLiaoning115004,China; 3.PetroChinaFushunPetrochemicalCompany,FushunLiaoning113008,China) CH3CONH2/ZnCl2type deep eutectic solvent was prepared by heating the mixture of acetic acid amide and zinc chloride at 110 ℃. The structure was analyzed by electrospray ionization mass spectrometry, infrared analysis and viscosity analysis. CH3CONH2/ZnCl2was used as extraction agent and catalyst, and H2O2was used as oxidant to remove thiophene sulfide in simulated oil. The effects ofn(ZnCl2)/n(CH3CONH2),n(H2O2)/n(S), reaction temperature, agent oil volume ratio and different sulfides on desulfurization rate were investigated. The results indicated that under the optimum conditions of 5 mL oil volume,n(ZnCl2)/n(CH3CONH2)=0.4,n(H2O2)/n(S)=8, agent oil volume ratio 1∶3, reaction temperature 70 ℃ and reaction time 200 min, the removal rate of two thiophene was 87.12%. After 5 cycles, the desulfurization rate decreased slightly. Zinc chloride; Acetamide; Deep eutectic solvent; Oxidation; Desulfurization 1672-6952(2017)05-0001-07 投稿网址:http://journal.lnpu.edu.cn 2016-10-11 2017-05-25 辽宁省博士科研启动基金项目(201501105)。 毛春峰(1988-),男,硕士研究生,从事油品脱硫研究;E-mail:maochunfeng555@163.com。 赵荣祥(1971-),男,博士,副教授,从事油品脱硫研究;E-mail:zylhzrx@126.com。 TE624 A 10.3969/j.issn.1672-6952.2017.05.001 (编辑 宋官龙)

2.3 不同硫化物对脱硫效果的影响

2.4 低共熔溶剂的循环使用

2.5 氧化产物的红外表征

2.6 氧化脱硫机理

3 结 论
