尿酸酶自组装空心纳米微球体外稳定性
2017-11-01胡雪原晏子俊周云莉张景勍
邓 雪, 胡雪原, 何 丹, 晏子俊, 周云莉, 张景勍
(重庆医科大学 药学院,重庆 400016)
尿酸酶自组装空心纳米微球体外稳定性
邓 雪, 胡雪原, 何 丹, 晏子俊, 周云莉, 张景勍*
(重庆医科大学 药学院,重庆 400016)
制备载尿酸酶(Uricase,UOX)聚乙二醇-透明质酸(Hyaluronic acid-graft-poly(ethylene glycol),HA-g-PEG)/羟丙基-β-环糊精(Hydroxypropyl-beta-cyclodextrin,HPCD)自组装空心纳米微球(HA-g-PEG/HPCD self-assembly hollow spheres encapsulated uricase,UHPHD),并研究其体外稳定性。制备UHPHD,并测定其包封率、粒径及Zeta电位。再分别从最适温度、最适pH、热稳定性、贮存稳定性、酸碱稳定性和抗胰蛋白酶水解能力初步考察游离UOX和UHPHD的差异。结果:UHPHD的包封率为(62.17±2.94)%,粒径和Zeta电位分别为(299.60±13.05)nm和(-45.10±2.75)mV。UHPHD和UOX最适温度均为40℃,最适pH均为8.5。体外稳定性结果显示,UHPHD的体外稳定性明显高于UOX。
尿酸酶;稳定性;自组装空心纳米微球
尿酸是机体嘌呤代谢的终产物,经肾脏随尿液排出体外。尿酸及其盐类在水中溶解度很低,在某些病理情况下,由于嘌呤代谢紊乱,血液中尿酸积累过多,会导致高尿酸血症,继而引发痛风综合症[1]。尿酸酶(Uricase,UOX)能够催化尿酸氧化生成尿囊素、过氧化氢和二氧化碳[2]。UOX专一性强,催化效率高,能够在短时间内有效降低患者体内的尿酸水平[3]。20世纪90年代,尿酸酶已作为治疗痛风的药物首先在欧洲上市。但是作为一种外源性的蛋白质,UOX存在着易被体内酶水解,稳定性低、半衰期短等蛋白质药物的共同缺点,更严重的是它还存在着抗原性较强,易产生过敏反应等问题,因此大大限制了其临床使用[4]。
自组装空心纳米微球是一种新型的药物载体。Ha等[5]人将L-天冬酰胺酶包载于海藻酸钠-聚乙二醇/α-CD形成的空心纳米囊中。由于形成的囊膜具有半渗透性,酶的底物和催化产物能顺利通过囊膜,而酶不能自由通过从而提高了酶的稳定性、拓宽了酶的最适温度和最适pH。为了克服UOX的缺点,扩大其临床应用,作者以聚乙二醇-透明质酸(Hyaluronic acid-graft-poly ethylene glycol,HA-g-PEG)/羟 丙 基 -β-环 糊 精 (Hydroxypropyl-betacyclodextrin,HPCD)为载体,自组装形成空心纳米微球(HA-g-PEG/HPCD self-assembly hollow spheres encapsulated uricase,UHPHD), 并 着 重 考 察 了UHPHD的体外稳定性,为临床用药提供实验依据。
1 材料与方法
1.1 材料与仪器
UOX:美国Sigma公司;尿酸:英国 Alfa Aesar公司;羟丙基-β-环糊精:武汉国邦达医药化工有限公司;乙醚为分析纯。
AB204S电子分析天平:瑞士Mettler Toledo仪器公司;RE 52 AA旋转蒸发器:上海亚荣生化仪器厂;TGL-16B台式高速离心机:上海安亭科学仪器厂;SHZ-D(Ⅲ)型循环水式真空泵:巩义市予华仪器有限责任公司;UV-7504 PC型紫外分光光度计:上海欣茂仪器有限公司;ZS90型激光粒度电位仪:英国马尔文公司;PHS-3C型pH计:上海精密科学仪器有限公司;KQ-2200B型水浴型超声仪:江苏昆山市超声仪器有限责任公司;Sephadex G-200层析柱:上海楷洋生物技术有限公司。
1.2 试验方法
1.2.1 UHPHD的制备 采用Meng等[6]的方法制备UHPHD。先配制1.0%的HA-g-PEG溶液和6.0%的HPCD溶液;将一定量的UOX加入到2 mL的HA-g-PEG溶液中,缓慢溶解;然后将2 mL含有UOX的HA-g-PEG溶液缓慢滴加入6 mL的HPCD溶液中。开始滴加时,溶液变轻微的浑浊,表明开始有空心纳米球形成,继续在10℃条件下磁力搅拌2 h,即得 UHPHD。
1.2.2 UHPHD的包封率的测定 按照参考文献报道方法,采用凝胶柱分离-考马斯亮蓝法[7]测定包封率。吸取0.5 mL的UHPHD,上Sephadex G-200层析柱,用pH 8.5的Bicine-NaOH缓冲液以1 mL/min流速洗脱分离UHPHD和UOX。接收UHPHD部分,取其中100 μL,加入乙醚破乳后,再加入考马斯亮蓝,在595 nm波长处测定吸收度值(AUHPHD)。以同法处理的未过柱的UHPHD,同法测定吸收度值(A总)。包封率(%)=AUHPHD/A总×100%,重复3次。
1.2.3 UHPHD的粒径和Zeta电位的测定 取少量UHPHD混悬液,以1∶10比例稀释3倍后,在25℃下用激光粒度电位仪测定UHPHD的粒径和Zeta电位。
1.2.4 UHPHD和UOX最适温度和最适pH的测定将尿酸溶于50 mmol/L硼酸-硼砂(pH 8.5)缓冲液中,分别于20~70℃的水浴中预热10 min后,在25℃下按照Zhou等[8]方法测定UHPHD和UOX的活性,绘制温度-活性曲线图。在硼酸缓冲体系中分别配制pH 6.5~9.5的尿酸溶液,分别在最适温度条件下预热10 min后测定UHPHD和UOX的活性,绘制pH-活性曲线图。
1.2.5 UHPHD和UOX热稳定性的测定 分别取UHPHD和UOX各2 mL,置于55℃的水浴中,在第0、1、2、3、4、5 小时取 200 μL,测定 UHPHD 和 UOX的活性,结果以活性保留百分数进行计算。
1.2.6 UHPHD和UOX贮存稳定性的测定 将UHPHD和UOX(UOX的质量浓度为0.1 mg/mL)避光密封贮存于 4 ℃条件下, 分别于第 0、1、2、4、7、10、14、20、28天取出, 测定 UHPHD 和 UOX 的活性,结果以活性保留百分数进行计算。
1.2.7 UHPHD和UOX酸碱稳定性的测定 分别取UHPHD和UOX(UOX的质量浓度为0.3 mg/mL)100 μL, 加入 pH 5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5的缓冲液稀释3倍,置于40℃水浴中放置40 min,取出测定UHPHD和UOX的活性。以UHPHD在pH 8.5时的酸碱稳定性测定结果为100%,计算其余各点的相对活性。
1.2.8 UHPHD和UOX抗胰蛋白酶水解能力的测定 分别取1 mL UHPHD和UOX(UOX质量浓度为0.2 mg/mL),加入等体积0.2 mg/mL胰蛋白酶溶液混合,然后置于 37 ℃水浴中,在 0、10、20、30、40、50、60 min分别取出,测定UHPHD和UOX的活性,结果以活性保留百分数进行计算。
2 结果与讨论
2.1 UHPHD的包封率、粒径及Zeta电位
制备3批UHPHD,经检测,平均包封率为(62.17±2.94)%,平均粒径为(299.60±13.05)nm,Zeta电位为(-45.10±2.75)mV。UHPHD的粒径分布和电位见图1。

图1 UHPHD的粒径分布图和zeta电位分布图Fig.1 Size distribution profiles and zeta potential profiles of UHPHD
2.2 UHPHD和UOX的最适温度
UHPHD和UOX的最适温度均为40℃,如图2所示。结果显示,UHPHD在20~70℃ 时活性均高于UOX,其中40℃时UHPHD活性是UOX的116.31%。
2.3 UHPHD和UOX的最适pH值
pH测定结果见图3。UHPHD和UOX的pH从5.0到8.5时,活性逐渐升高,从pH 8.5到pH 9.5时活性逐渐降低,故UHPHD和UOX的最适pH值为8.5。此时,UHPHD活性是UOX的1.4倍。在pH 5.0~9.5范围内,UHPHD的活性均高于游离UOX,表明UHPHD能明显提高UOX的活性。
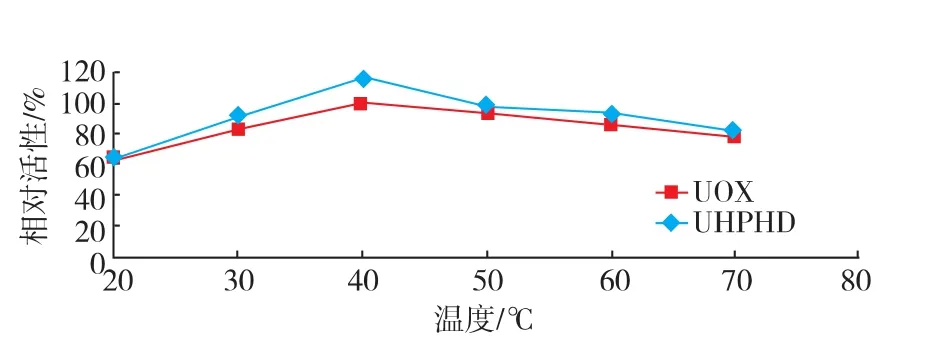
图2 UHPHD和游离UOX的最适温度(n=3)Fig.2 Optimal temperature of UHPHD and free UOX,(n=3)
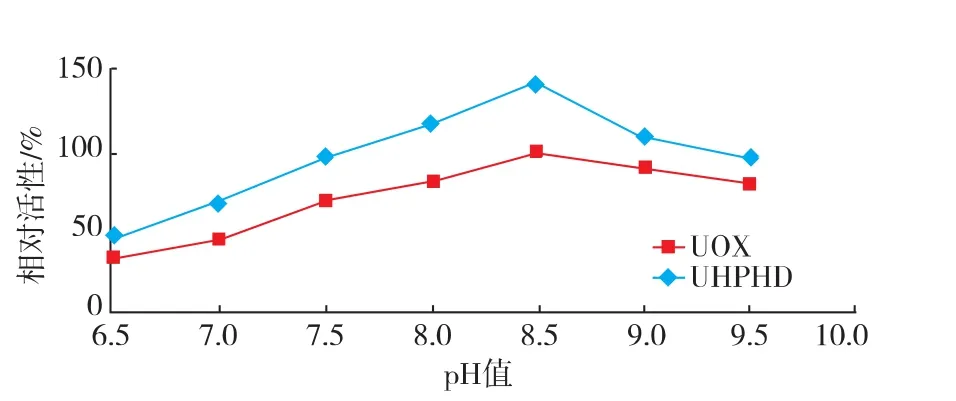
图3UHPHD和游离UOX的最适pH(n=3)Fig.3 Optimal pH of UHPHD and free UOX(n=3)
2.4 UHPHD和UOX热稳定性的测定
UHPHD和UOX的热稳定性测定结果见图4,UHPHD在55℃水浴中放置5 h后,酶活性仍保持为80%以上,而UOX在相同的条件下,活性由100%下降到16.76%。3 h时,UOX活性下降到50%以下,而UHPHD酶活性仍保留为85.31%。
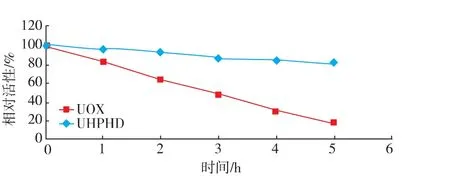
图4 UHPHD和游离UOX的热稳定性(n=3)Fig.4 Thermal stabilities of UHPHD and free UOX(n=3)
2.5 UHPHD和UOX贮存稳定性的测定
UHPHD和UOX的贮存稳定性测定的结果见图5。在4℃避光密封贮存条件下,UHPHD的稳定性明显优于UOX。当游离UOX在第28天活性保留值降至23.72%时,UHPHD仍保留有57.78%的活性;UHPHD在第10天时活性保留值为81.66%时,游离UOX则低于50%。综上,UHPHD有更好的贮存稳定性。

图5 4℃条件下UHPHD和UOX贮存稳定性的测定(n=3)Fig.5 Storage stabilities of UHPHD and free UOX incubated at 4 ℃(n=3)
2.6 UHPHD和UOX酸碱稳定性的测定
UHPHD和UOX的酸碱稳定性测定结果见图6。结果显示,在pH 5.0~9.5中,UHPHD活性保留最小值为55.64%,游离UOX活性保留最大值仅为66.77%,最小值为20.47%。在此pH范围内,UHPHD活性保留值均高于UOX。表明UHPHD较游离UOX有更好的耐溶液酸碱变化的能力。
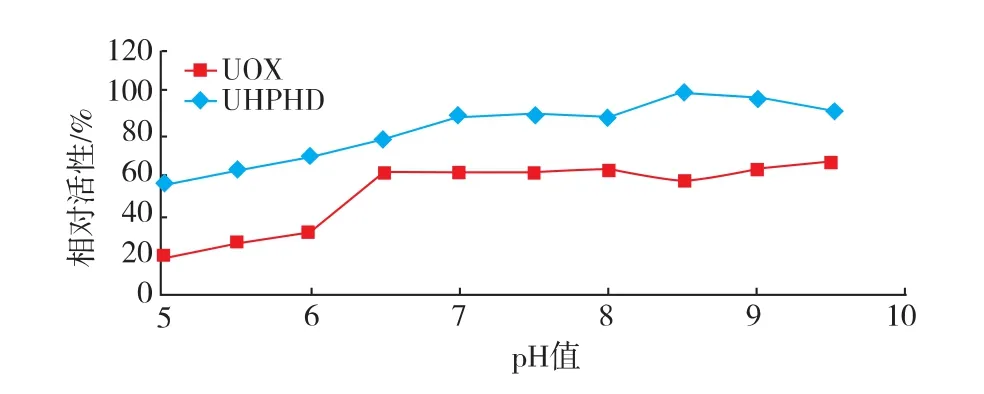
图6 UHPHD和UOX酸碱稳定性的测定(n=3)Fig.6 pH stabilities of UHPHD and free UOX(n=3)
2.7 UHPHD和UOX抗胰蛋白酶水解能力的测定
UHPHD和UOX的抗胰蛋白酶水解能力测定见图7。UOX的酶活性快速下降,在60 min时,活性仅保留了10.33%,几乎丧失活性。相反,UHPHD活性仍保留在50%以上,表明UHPHD相比于UOX有更好的抗酶解能力。
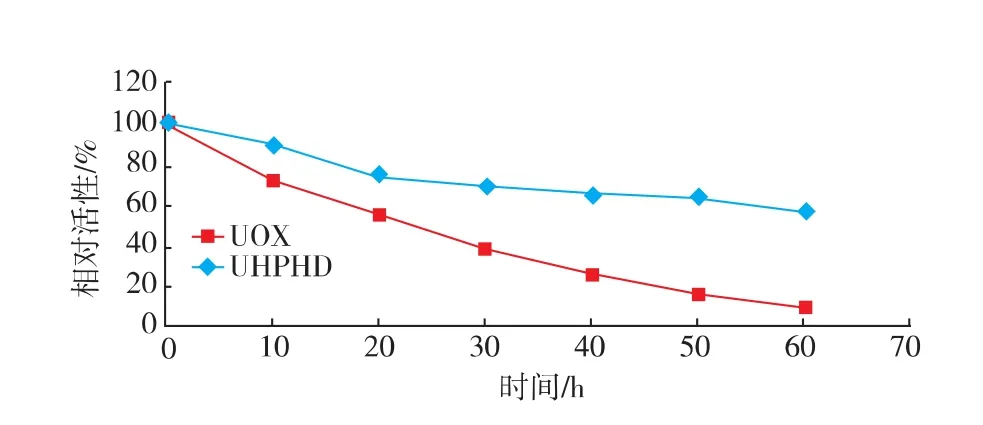
图7UHPHD和UOX抗胰蛋白酶水解能力的测定Fig.7 Proteolytic stabilities of UHPHD and free UOX
3 结语
本研究表明,UOX热稳定性、贮存稳定性、酸碱稳定性和抗胰蛋白酶水解能力均明显低于UHPHD,其原因可能是酶蛋白中的反应基团或者蛋白质中的一些高级结构直接暴露于外部环境中。过高或者过低的温度、过酸或者过碱的环境、贮存时间的延长以及胰蛋白酶的水解使得酶分子的内部结构和性质改变,导致酶活力的降低甚至丧失。据报道,Li等[9]将葡萄糖氧化酶包裹于羧甲基魔芋苷葡聚糖-聚乙二醇/α-环糊精自组装形成的纳米球中,提高了葡萄糖氧化酶的稳定性,且载体膜具有半渗透性及生物相容性。作者制备的HA-g-PEG/HPCD自组装空心纳米微球是一种新型的药物载体,将UOX包裹于HA-g-PEG/HPCD自组装空心纳米微球后,由于载体对酶蛋白具有一定的保护作用,降低了外界环境变化引起的酶分子构象改变的几率,因而使得酶的稳定性获得了提高。
作者从热稳定性、贮存稳定性、酸碱稳定性和抗胰蛋白酶水解能力方面分别对UHPHD和UOX的体外稳定性进行了研究,丰富了UOX的研究内容,也为UHPHD的体内研究奠定了良好的基础。由本研究可看出,UHPHD有提高UOX体外稳定性的优点。
[1]NANDA P,BABU P E.Isolation,screening and production studies of uricase producing bacteria from poultry sources[J].Prep Biochem Biotechnol,2014,44(8):811-821.
[2]SUPRIYA D,BEEDKAR C N,RAGINI G,et al.Comparative structural modeling and docking studies of uricase:possible implication in enzyme supplementation therapy for hyperuricemic disorders[J].Comput Biol Med,2012,42(6):657-666.
[3]BOMALASKI J S,HOLTSBERG F W,ENSOR C M,et al.Uricase formulated with polyethylene glycol (uricase-PEG 20):biochemical rationale and preclinical studies[J].J Rheumatol,2002,29(9):1942-1949.
[4]GUO Yuan,TIAN Fa,GAO Xiangdong.Effect ofPEGylation on properties ofuricase[J].Pharmaceutical Biotechnology,2011,18(6):488-491.(in Chinese)
[5]HA W,MENG X W,LI Q,et al.Self-assembly hollow nanosphere for enzyme encapsulation[J].Soft Matter,2010,6(7):1405-1408.
[6]MENG X W,HA W,CHENG C,et al.Hollow nanospheres based on the self-assembly of alginate-graft-poly (ethylene glycol)and α-cyclodextrin[J].Langmuir,2011,27(23):14401-14407.
[7]TAN Q,ZHANG J,WANG N,et al.Uricase from Bacillus fastidious loaded in alkaline enzymosomes:enhanced biochemical and pharmacological characteristics in hypouricemic rats[J].Eur J Pharm Biopharm,2012,82(1):43-48.
[8]ZHOU Y L,YANG L,WU J Y,et al.Primarily study on pharmacokinetics of uricase in uricase-catalase liposome[J].Chinese Journal of Hospital Pharmacy,2014,34(21):1805-1808.(in Chinese)
[9]LI Q,XIA B,MICKEY B,et al.Self-assembly of carboxymethyl konjac glucomannan-g-poly(ethyleneglycol) and cyclodextrin to biocompatible hollow nanospheres for glucose oxidase encapsulation[J].Carbohydrate Polymers,2011,86(10):120-126.
会议名称(中文):第九届中国工业生物技术发展高峰论坛
所属学科:生物技术与生物工程
开始日期:2017-11-06
结束日期:2017-11-08
所在城市:天津市 和平区
主办单位:中国科学院科技促进发展局、中国生物工程学会
承办单位:中国科学院天津工业生物技术研究所、中科育成(天津)科技发展有限公司
联系人:吴崇明
联系电话:022-24828776
E-MAIL:biocap@tib.cas.cn
会议网站:http://www.cas.cn/xs/201707/t20170710_4608053.shtml
会议背景介绍:“中国工业生物技术发展高峰论坛”是中国科学院科技促进发展局联合国家发改委高技术产业司、科技部中国生物技术发展中心、中国生物工程学会等部门和单位共同精心打造的国内唯一集政府、企业、科研、教育、金融等元素为一体的工业生物技术领域品牌盛会。“中国生物工业投资大会”由中国科学院天津工业生物技术研究所策划发起,国内首个生物工业领域以资本、技术、产业为核心的专业性、商务型投资会议,为促进工业生物技术领域“技术、产业、资本”深度融合搭建崭新平台。 2017年,中国工业生物技术发展高峰论坛专注深耕工业生物技术领域第十年,将与中国生物工业投资大会合并召开,力求办成特色互补、效应倍增的行业盛会!
“第九届中国工业生物技术发展高峰论坛暨第二届中国生物工业投资大会”将组织“技术创新”和“项目路演”、“企业展览”三大板块内容,着重探讨工业生物技术领域“合成生物技术”、“酶工程与生物催化”、“细胞工厂”、“生物计算与设计”、“高通量筛选装备与技术”等议题,并甄选处于不同阶段的优秀生物工业项目进行路演,发布《中国工业生物技术白皮书暨中国生物工业投资分析报告2017》,还将设立“年度创新先锋奖”、“年度科技转化奖”及“年度绿色企业奖”等奖项,同时开展小组讨论、一对一洽谈等活动。大会将采取多种组织形式,加强互动交流,欢迎在线注册报名参会!
In Vitro Stability of Uricase Self-Assembly Hollow Nanospheres
DENG Xue, HU Xueyuan, HE Dan, YAN Zijun, ZHOU Yunli, ZHANG Jingqing*
(College of Pharmacy,Chongqing Medical University,Chongqing 400016,China)
To prepare the self-assembly hollow nanospheres of hyaluronic acid-graft-poly(ethylene glycol)(HA-g-PEG)and hydroxypropyl-beta-cyclodextrin (HPCD)containing uricase (U HPCD)and study their stability in vitro.UHPCD were prepared and the entrapment efficiency,size and zeta potential of UHPCD were detected.The optimum temperature,optimum pH,thermal stability,storage stability,pH stabilities and proteolytic stabilities of UOX and UHPHD were measured.The entrapment efficiency of UHPHD was(62.17±2.94)%.The average particle size was(299.60±13.05)nm,and the zeta potential was (-45.10±2.75) mV.The optimal temperatures for UHPHD and U0X were 40 ℃ ,the optimal pH values were 8.5.UHPHD significantly enhanced the stability of free UOX in vitro.
uricase,stability,self-assembly hollow nanosphere
R 944.9
A
1673—1689(2017)09—0933—05
2015-04-14
国家自然科学基金项目(30973645);重庆市首批高等学校优秀人才资助计划项目(渝教人(2009)2号文件)。
*通信作者:张景勍(1973—),女,重庆市人,理学博士,教授,博士研究生导师,主要从事药物新剂型与新技术方面的研究。E-mail:zjqrae01@163.com
邓雪,胡雪原,何丹,等.尿酸酶自组装空心纳米微球体外稳定性[J].食品与生物技术学报,2017,36(09):933-937.
