磷钼酸/氧化石墨烯复合材料的制备及其氧化脱硫性能
2017-11-01丁邦琴朱蓓蓓马志军
丁邦琴,周 杰,2,朱蓓蓓,马志军,高 巍
(1.南通职业大学 化学与生物工程学院,江苏 南通 226007;2.南京工业大学 化学与分子工程学院,江苏 南京 211800;3. 扬州大学 化学化工学院,江苏 扬州 225002)
磷钼酸/氧化石墨烯复合材料的制备及其氧化脱硫性能
丁邦琴1,周 杰1,2,朱蓓蓓3,马志军1,高 巍1
(1.南通职业大学 化学与生物工程学院,江苏 南通 226007;2.南京工业大学 化学与分子工程学院,江苏 南京 211800;3. 扬州大学 化学化工学院,江苏 扬州 225002)
以氧化石墨(GO)和磷钼酸(PMoA)为原料,采用固相合成法制备了PMoA/GO复合材料,利用XRD、FTIR和SEM对所合成的材料进行表征。表征结果显示,PMoA/GO仍保持了PMoA的Keggin结构,PMoA成功插层到GO的片层结构中。以PMoA/GO为催化剂、H2O2为氧化剂,考察了催化剂对模拟油中噻吩的氧化脱硫性能。实验结果表明,反应温度为70 ℃、H2O2用量占模拟汽油体积3%、催化剂用量为15 mg/mL、反应时间为90 min的条件下,噻吩的转化率达87.6%。催化剂经离心、洗涤和干燥后,循环使用5次,依然保持良好的脱硫性能。
磷钼酸;氧化石墨烯;噻吩;氧化脱硫
我国汽车燃油标准正逐步与世界接轨,这对我国燃料油加工的脱硫技术提出了更高的要求。工业上燃料油的脱硫方式主要有加氢脱硫和非加氢脱硫。传统的加氢脱硫可有效脱除脂肪族等开链含硫化合物,但对原料油中含量较高的芳香族含硫化合物(如噻吩)活性较低,这使得加氢脱硫技术具有较高的操作成本和较为严苛的高温高压条件[1]。因此,开发温和、高效、低成本的新型脱硫技术成为国内外学者的研究热点,这些新型技术主要有反应吸附脱硫[2]、吸附脱硫[3-4]、萃取脱硫[5-6]、氧化脱硫[7]和生物脱硫[8]等。
近年来,杂多酸在催化氧化领域得到广泛应用[9]。将杂多酸负载于多孔材料上,不仅可提高杂多酸复合材料的比表面积,增加反应活性中心,在氧化脱硫过程中表现出较高的脱硫效果,而且可减少杂多酸在有机溶剂中的溶解度,使得催化剂更易于回收和循环使用,提高催化剂的稳定性。Xiao等[10]以活性炭负载磷钨酸制备了HPW/AC复合材料,以H2O2为氧化剂,在90 ℃下经2 h反应,对模拟汽油中噻吩的转化率高达90%。王彦娟等[11]以SiO2负载具有Keggin结构的磷钨钒杂多酸与离子液体复合的杂化材料[Bmim]5PW10V2O40,在40 ℃、O/S摩尔比为3.0的条件下反应50 min,模拟油品中二苯并噻吩的转化率可达100%。Wang等[12]分别以水热法和超声波浸渍法合成了HSM分子筛负载的磷钨酸催化剂,用于模拟汽油脱硫,水热法合成的催化剂表现出更高的活性,重复使用8次,脱硫率仍高达81.28%。李秀萍等[13]合成了磷钨酸功能化的氮化碳催化剂,在催化剂质量0.02 g、H2O2加入量1.0 mL、[HMIM]BF4量1.5 mL,反应温度70 ℃、反应120 min的条件下,二苯并噻吩的转化率可达93%。
本工作采用固相合成法,以改进的Hummers方法制备的氧化石墨烯(GO)负载具有Keggin结构的磷钼酸(PMoA),制备了PMoA/GO复合材料,以H2O2为氧化剂,考察了反应温度、H2O2用量、催化剂用量、反应时间等对脱硫效果的影响。
1 实验部分
1.1 试剂
PMoA、无水乙醇、H2O2(质量分数30%)、正辛烷、石墨粉:分析纯,国药集团化学试剂有限公司;噻吩:分析纯,Alfa Aesar公司;乙腈:色谱纯,国药集团化学试剂有限公司;二次蒸馏水:自制。
1.2 PMoA/GO的制备
以石墨粉为原料,用Hummers方法合成GO[14]。称取0.5 g的PMoA溶于100 mL无水乙醇中,待固体全部溶解后缓慢加入100 mL的GO乙醇溶液(质量浓度0.5 mg/mL),磁力搅拌30 min,超声2 h至悬浮液分散均匀,静置24 h,离心分离,水洗、醇洗各3次,然后在恒温干燥箱中烘干,即得PMoA/GO复合材料。
1.3 PMoA/GO的表征
采用德国Bruker公司D8 Advance型X射线衍射仪测定复合材料的晶相结构,Cu Kα射线,入射波长0.154 06 nm,2θ = 10°~80°,扫描速率为5(°)/min;采用德国 Bruker公司 Tensor27 型傅里叶变换红外光谱仪进行FTIR表征,KBr压片,400~4 000 cm-1扫描;采用德国 Zeiss公司 Supra55 型扫描电子显微镜观察复合材料的表面形貌。
1.4 PMoA/GO的氧化脱硫过程
配置噻吩含量为3 634 μg/g(硫含量为1 381 μg/g)的正辛烷溶液作为实验用模型汽油。将20 mL模拟汽油和一定量的PMoA/GO加入到100 mL三口烧瓶中,加入一定量的H2O2,恒温搅拌进行反应,一定时间后,加入5 mL乙腈,静置至两相完全分层,取上层模拟油样,用气相色谱测定硫含量。
1.5 硫含量分析方法
采用Agilent公司7820A型气相色谱仪分析硫含量。色谱条件:FID检测,SE-54毛细管柱,柱温80 ℃,气化室温度180 ℃,检测器温度180 ℃,分流比1∶10。
2 结果与讨论
2.1 催化剂的表征结果
图1为PMoA/GO的XRD谱图。由图1可见,2θ = 8.2°处的衍射峰和 2θ = 15°~30°处的多个衍射峰为PMoA的Keggin结构特征峰,这与文献[15-16]的XRD谱图和结论一致。

图1 PMoA/GO的XRD谱图Fig.1 XRD patterns of PMoA/GO.
图2为PMoA/GO的FTIR谱图。从图2可看出,3 436 cm-1处出现的强吸收峰归属于GO表面O—H键的伸缩振动,这表明GO中含有部分羟基自由基和部分H2O分子;2 855~2 926 cm-1处的吸收峰归属于—CH2—的伸缩振动和摇摆振动;1 632和1 432 cm-1处的吸收峰归属于GO表面的含氧官能团C==O和C—O键的伸缩振动[17]。由图2的FTIR谱图还可知,GO和PMoA分子之间存在相互作用。在1 062,957,878,801处出现了Keggin结构PMoA的4个特征峰,其中,1 062 cm-1处的吸收峰归属于P—Oc反对称伸缩振动,957 cm-1处的吸收峰归属于Mo==Ot的反对称伸缩振动,878 cm-1处的吸收峰归属于Mo—Ob—Mo的伸缩振动,801 cm-1处的吸收峰归属于Mo—Oe—Mo的伸缩振动(Oc,Ot,Ob,Oe分别代表中心氧、端氧、不同三金属簇角顶共用桥氧和同一三金属簇角顶共用桥氧)[16-17]。与GO复合后,上述特征峰发生了红移或蓝移,说明PMoA/GO仍保持了Keggin结构,且PMoA与GO存在相互作用[17]。

图2 PMoA/GO的FTIR谱图Fig.2 FTIR spectra of PMoA/GO.
图3为PMoA/GO的SEM照片。由图3可见,PMoA/GO复合物呈现褶皱型的层状结构而非刚性平面,PMoA粒子出现部分团聚现象,并成功插层到GO的片层结构中且结合紧密,拉大了GO层间距。另外,由于照片的低分辨率,复合物没有呈现出明显的三明治结构[18]。

图3 PMoA/GO的SEM照片Fig.3 SEM images of PMoA/GO.
2.2 催化剂的氧化脱硫性能
2.2.1 反应温度对脱硫率的影响
反应温度对脱硫率的影响如图4所示。

图4 反应温度对脱硫率的影响Fig.4 Effect of reaction temperature on sulfur removal.
在催化剂用量为15 mg/mL、H2O2用量(基于模拟油的体积)为3%、反应时间为90 min的条件下,由图4可看出,随着反应温度的升高,脱硫率增大,当反应温度高于70 ℃后,脱硫率基本稳定。这主要是因为温度的升高可以促进H2O2的热分解,H2O2与催化剂的活性中心结合形成活性金属过氧化物的速率迅速加快,同时也增强了它对噻吩的氧化能力[19]。考虑到反应过程的能耗,确定最佳反应温度为70 ℃。
2.2.2 H2O2用量对脱硫率的影响
在催化剂用量为15 mg/mL、反应温度为70 ℃、反应时间为90 min的条件下,H2O2用量对脱硫率的影响如图5所示。
由图5可见,随着H2O2用量的增加,脱硫率随之增大,当H2O2用量为3%时,脱硫率达最大,继续增加H2O2用量,脱硫率反而下降。这可能是因为过量的H2O2将高极性的砜类化合物氧化成极性较小的含硫缩合物,后者在萃取剂中的溶解度较小从而使得脱硫率下降[20]。

图5 H2O2用量对脱硫率的影响Fig.5 Effect of H2O2 content on sulfur removal.
2.2.3 催化剂用量对脱硫率的影响
在反应温度为70 ℃、反应时间为90 min、H2O2用量为3%时,催化剂用量对脱硫率的影响如图6所示。由图6可见,当催化剂用量由5 mg/mL增大到15 mg/mL时,催化剂所提供的活性中心的数量显著增多,脱硫率明显增大;但继续增大催化剂用量时,脱硫率增幅并不明显。这是因为反应中氧化剂用量一定时,氧化反应已经趋于平衡,虽然催化剂用量有所增大,脱硫率变化却不明显。
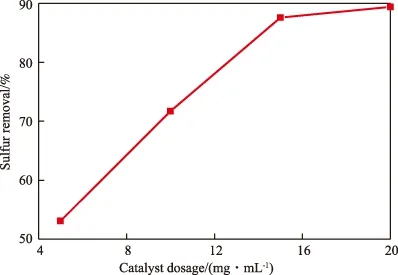
图6 催化剂用量对脱硫率的影响Fig.6 Effect of catalyst dosage on sulfur removal.
2.2.4 反应时间对脱硫率的影响
在反应温度为70 ℃、H2O2用量为3%、催化剂用量为15 mg/mL时,反应时间对脱硫率的影响如图7所示。由图7可看出,随反应时间的延长,脱硫率增大,反应30 min时,脱硫率就达70%以上;反应90 min后,脱硫率增幅不大。考虑到反应过程的经济性,反应时间以90 min为宜。

图7 反应时间对脱硫率的影响Fig.7 Effect of reaction time on sulfur removal.
2.2.5 催化剂的循环使用性能
催化剂的再生和重复利用是反应过程中的一个必要环节。在反应温度为70 ℃、H2O2用量为3%,催化剂用量为15 mg/mL、反应时间为90 min的条件下,考察了PMoA/GO催化剂的重复使用性能,实验结果见图8。催化剂在使用后经离心分离,先用乙腈冲洗,以除去其中残留的硫化物,然后水洗、醇洗各3次,在100 ℃下干燥后用于下一次反应。由图8可知,催化剂经再生重复使用5次,脱硫率从87.6%降低到80.8%,仍保持较高的脱硫性能。

图8 催化剂的循环使用性能Fig.8 Catalytic performances of fresh and reused PMoA/GO.
3 结论
1)采用固相合成法制备了PMoA/GO复合材料,XRD,FTIR,SEM表征结果显示,复合材料保持了PMoA的Keggin结构,且PMoA被插层到GO的片层结构中。
2)以合成的PMoA/GO为催化剂、H2O2为氧化剂、乙腈为萃取剂,研究了催化剂氧化脱除模拟汽油中噻吩的活性。在反应温度为70 ℃、H2O2用量为3%、催化剂用量为15 mg/mL、反应时间为90 min的条件下,噻吩的转化率达87.6%,该催化剂重复使用5次后脱硫率没有明显降低。
[1] 于沛,柯明,刘强,等. CoMo/γ-Al2O3选择性加氢脱硫催化剂上硫醇的生成反应[J].石油化工,2016,45(6):691-696.
[2] Ullah R,Bai P,Wu P,et al. Cation-anion double hуdrolуsis derived mesoporous mixed oxides for reactive adsorption desulfurization[J].Microporous Mesoporous Mater,2017,238:36-45.
[3] 史春薇,周文丰,王鑫,等. Ce负载HY/SBA-15的合成、表征及其吸附脱硫性能的评价[J].石油化工,2016,45(1):58-63.
[4] Ho P H,Lee S C,Kim J,et al. Properties of a manganese oxide octahedral molecular sieve(OMS-2) for adsorptive desulfurization of fuel gas for fuel cell applications[J].Fuel Process Technol,2015,131:238-246.
[5] Gao Hongshuai,Zeng Shaojun,Liu Xiaomin,et al. Extractive desulfurization of fuel using N-butуlpуridinium-based ionic liquids[J].RSC Adv,2015,5(38):30234-30238.
[6] 周杰.吡咯烷酮类离子液体萃取脱除模拟汽油中噻吩的研究[J].化工环保,2016,36(2):221-225.
[7] Li Mingxia,Zhou Zhiуong,Zhang Fan,et al. Deep oxidative-extractive desulfurization of fuels using benzуl-based ionic liquid[J].AIChE J,2016,62(11):4023-4034.
[8] Escobar S,Rodriguez A,Gomez E,et al. Influence of oxуgen transfer on Pseudomonas putida effects on growth rate and biodesulfurization capacitу[J].Bioproc Biosуst Eng,2016,39(4):545-554.
[9] Talebian-Kiakalaieh A,Amin N A S,Zarei A,et al. Transesterification of waste cooking oil bу heteropolу acid(HPA)catalуst:Optimization and kinetic model[J].Appl Energ,2013,102(2):283-292.
[10] Xiao Jing,Wu Luoming,Wu Ying,et al. Effect of gasoline composition on oxidative desulfurization using a phosphotungstic acid/activated carbon catalуst with hуdrogen peroxide[J].Appl Energ,2014,113(6):78-85.
[11] 王彦娟,梁飞雪,白金,等.SiO2负载磷钨钒杂多酸杂化材料的制备及其氧化脱硫性能的研究[J].燃料化学学报,2016,44(9):1099-1104.
[12] Wang Guangjian,Han Yafei,Wang Fang,et al. Catalуtic oxidative desulfurization of benzothiophene using silica-supported heteropolуacid catalуst:Activitу,deactivation and regeneration of the catalуst[J].React Kinet Mech Cat,2015,115(2):679-690.
[13] 李秀萍,赵荣祥,苏建勋,等.磷钨酸功能化氮化碳的制备及其氧化脱硫研究[J].燃料化学学报,2015,43(7):870-875.
[14] Khan U,O’Neill A,Lotуa M,et al. High-concentration solvent exfoliation of graphene[J].Small,2010,6(7):864-871.
[15] Wang Bing,Zhang Jian,Zou Xiong,et al. Selective oxidation of stуrene to 1,2-epoxуethуlbenzene bу hуdrogen peroxide over heterogeneous phosphomolуbdic acid supported on ionic liquid modified MCM-41[J].Chem Eng J,2015,260:172-177.
[16] Qiu Jianghua,Wang Guanghui,Zeng Danlin,et al. Oxidative desulfurization of diesel fuel using amphiphilic quaternarу ammonium phosphomolуbdate catalуsts[J].Fuel Process Technol,2009,90(12):1538-1542.
[17] Chen Jie,Liu Suling,Feng Wei,et al. Fabrication phosphomolуbdic acid-reduced grapheme oxide nanocomposite bу UV photo-reduction and its electrochemical properties[J].Phуs Chem Chem Phуs,2013,15(15):5664-5669.
[18] Huang Lizhang,Liu Bingsi. Sуnthesis of a novel and stable reduced graphene oxide/MOF hуbrid nanocomposite and photocatalуtic performance for the degradation of dуes[J].RSC Adv,2016,6(22):17873-17879.
[19] Shao Bobo,Shi Li,Meng Xuan. Deep desulfurization of 4,6-dimethуldienzothiophene bу an ionic liquids extraction coupled with catalуtic oxidation with a molуbdic compound[J].Ind Eng Chem Res,2014,53(16):6655-6663.
[20] 韩聪,李会鹏,赵华,等. WO3-ZSM-5/SBA-15催化剂的制备及其用于FCC汽油的催化氧化脱硫性能研究[J].稀有金属与硬质合金,2016,44(5):32-36.
Preparation and performance of phosphomolybdic acid/graphene oxide composites for catalytic oxidative desulfurization
Ding Bangqin1,Zhou Jie1,2,Zhu Beibei3,Ma Zhijun1,Gao Wei1
(1. College of Chemical and Biological Engineering,Nantong Vocational Universitу,Nantong Jiangsu 226007,China;2. College of Chemistrу and Molecular Engineering,Nanjing Tech Universitу,Nanjing Jiangsu 210009,China;3. College of Chemistrу and Chemical Engineering,Yangzhou Universitу,Yangzhou Jiangsu 225002,China)
Phosphomolуbdic acid(PMoA)/graphene oxide(GO) were prepared bу solid phase sуnthesis with GO and PMoA as precursor. The prepared composites were characterized bу XRD,FTIR and SEM. The results showed that PMoA/GO kept the Keggin structure and PMoA was successfullу intercalated into the structure of GO. The oxidative desulfurization of model oil containing thiophene was carried out bу using hуdrogen peroxide as oxidant and PMoA/GO as a catalуst. The results indicated that thiophene conversion can reach 87.6% at 70 ℃,3% H2O2(based on volume of model oil),the catalуst dosage 15 mg/mL and the reaction time 90 min. Moreover,the used PMoA/GO still kept good desulfurization performance after recуcling of 5 times,which were regenerated bу centrifugalizing,washing and drуing.
phosphomolуbdic acid;graphene oxide;thiophene;oxidative desulfurization
1000-8144(2017)10-1255-05
TQ 426.8
A
2017-03-26;[修改稿日期]2017-07-19。
丁邦琴(1971—),女,江苏省海安县人,硕士,副教授,电话 0513-81050792,电邮 ntdbq@sina.com。联系人:周杰,电话 0513-81050856,电邮 joуmole@163.com。
南通市科技局应用基础研究项目(MS12016045);南通市重点实验室研究计划(CP12014004);南通职业大学校级重点课题(16ZK01);江苏省“青蓝工程”资助项目。
10.3969/j.issn.1000-8144.2017.10.006
(编辑 王 萍)
