不同锌铝比水滑石的合成及其吸附脱除水中邻苯二甲酸性能
2017-11-01杨盈利闫新龙胡晓燕
杨盈利 闫新龙 胡晓燕 周 敏
不同锌铝比水滑石的合成及其吸附脱除水中邻苯二甲酸性能
杨盈利 闫新龙*胡晓燕 周 敏
(中国矿业大学化工学院,煤炭加工与高效洁净利用教育部重点实验室,徐州 221116)
采用共沉淀法合成一系列具有不同锌铝比的水滑石,并利用X射线衍射(XRD)、扫描电镜(SEM)、热重(TG)、氮气吸脱附及电感耦合等离子体质谱(ICP-MS)等表征手段对其结构与组成进行了测试。将上述水滑石材料用于吸附脱除水中邻苯二甲酸污染物,考察了不同锌铝比水滑石吸附邻苯二甲酸性能的差异。结果表明,在较低锌铝比时,随着水滑石锌铝比的增加,其对邻苯二甲酸的吸附量逐渐增大;当锌铝比较大时(>6),随着锌铝比的增加,水滑石的吸附量基本保持不变。进一步选取锌铝比为6的水滑石,分别对其吸附邻苯二甲酸的动力学和热力学进行了研究,发现其吸附等温线和吸附动力学数据分别符合Freundlich等温吸附模型和准二级动力学模型,且循环吸附性能较好。
水滑石(LDH);锌铝比;吸附分离;邻苯二甲酸;吸附动力学;吸附热力学
邻苯二甲酸酯类化合物作为常见的塑化剂,是一类环境内分泌干扰物,被广泛应用于玩具、医用材料、食品包装材料、农药、化妆品等多种产品的生产中,其分布广泛,很容易从塑料中迁移出来进入水环境中,且由于降解代谢慢,容易在水体中富集,已造成严重的水污染问题[1-3]。邻苯二甲酸是多种邻苯二甲酸酯(如邻苯二甲酸二甲酯、邻苯二甲酸二乙酯、邻苯二甲酸二丁酯等)的主要分解产物,在各大水系中广泛存在[4]。因此,邻苯二甲酸的有效脱除已逐渐成为污水处理过程的主要目标。通常,水中邻苯二甲酸的去除方法有生物降解法、吸附分离法、沉降法等。其中,吸附分离法具有操作简单、能耗低、适用范围广等优点,具有广泛的应用前景,而其关键则是吸附剂的选择与开发。
常见的吸附剂有活性炭[5-6]、氧化铝[7]、金属有机骨架材料(MOFs)[8]、生物质类[9]等。其中,活性炭具有发达的孔隙结构和较大的表面积,可对邻苯二甲酸进行吸附,但活性炭孔径分布较宽,吸附选择性较差[10-11]。氧化铝吸附剂结构中含有大量的毛细孔道,表面积大且活性高,可用作吸附剂,但氧化铝表面具有亲水性,与有机物质之间的作用力较弱,难以达到较好的吸附效果[12]。MOFs具有孔隙发达、结构可调等优点,在其结构中引入官能团也可增加吸附位点,但由于其稳定性较差、成本较高等,尚未大规模应用[13-14]。生物质类作为吸附剂虽成本较低,但吸附脱除较长链酯的过程复杂且耗时[10]。因此,开发寻找一种高效、廉价的吸附剂至关重要。
阴离子粘土是一类阴离子层状化合物,又称类水滑石类化合物,通常由带正电荷的金属阳离子和层间平衡阴离子构成,其表达式一般为[M2+1-xM3+x(OH)2]2+An-x/n·m H2O,M2+、M3+代表二价、三价金属离子(M2+:Mg2+、Zn2+、Mn2+、Co2+、Ni2+、Cd2+等,M3+:Al3+、Fe3+、Cr3+、Ga3+等),x 代表三价金属离子的个数,An-表示层间阴离子(CO32-、SO42-、NO3-、Cl-、OH-等),m 是水的数量。水滑石具有类似水镁石Mg(OH)2型正八面体结构,类水镁石Mg(OH)2层中的M2+部分被M3+取代,形成M2+与M3+位于中心,-OH位于顶点的复合氢氧化物八面体结构[15-18]。由于水滑石具有特殊的层状结构及层间阴离子的可交换性,可被广泛应用于吸附分离领域[19-20]。张璐虹等[21]采用水热法合成出不同镁铝比率的水滑石,并探究镁铝比率对Mg-Al LDH吸附甲基橙性能的影响。在最优实验条件下,当镁铝比率为2.5时,水滑石对甲基橙的吸附性能最佳,吸附量可达 83.33 mg·g-1。 王龙等[22]研究了 Mg/Al水滑石对3种邻苯二甲酸酯(DMP、DEHP和DnOP)的动力学吸附和热力学吸附,发现吸附剂对3种邻苯二甲酸酯的吸附动力学过程均符合准二级动力学模型;不同温度下,吸附等温线分别符合Langmuir和Freundlich吸附等温模型,吸附主要以表面物理吸附为主。3种邻苯二甲酸酯(DMP、DEH和DnOP)的最大吸附容量分别达23.1、3.9和8.9 mg·g-1。Li等[23]将具有不同内层阴离子(Cl-、NO3-、CO32-)的 Mg-Al LDH作为吸附剂,考察了其对有机农药草甘膦的吸附性能,结果表明,在Ce=1.0 mmol·L-1时,内层阴离子为Cl-的Mg-Al LDH吸附量最大,达1.3 mmol·g-1,且吸附量随着层间电荷(nMg/nAl)密度的增加而增大。上述结果表明,水滑石对某些有机物具有较好的吸附效果,但将其用作吸附剂脱除水中邻苯二甲酸尚鲜见报道。
同时,由于合成LDHs的方法较多,如共沉淀法、水热合成法、尿素水解法、溶胶-凝胶法等,其中共沉淀法是最常用的方法,而在合成过程中,金属离子的比率对产物的结构及吸附性能都有较大的影响[17,24-25]。因此,本文采用共沉淀法合成了一系列具有不同锌铝比的水滑石,研究了不同锌铝投料比对所合成水滑石结构与组成的影响,考察了所合成水滑石吸附脱除水中邻苯二甲酸的性能,包括了吸附动力学和吸附等温线的研究等。
1 实验部分
1.1 实验试剂
实验室所用试剂硝酸铝(Al(NO)3·9H2O)、硝酸锌(Zn(NO3)2·6H2O)、氢氧化钠(NaOH)和纳米氧化锌、氨水和盐酸(HCl)均来自于国药集团化学试剂有限公司,邻苯二甲酸(H2-PA)由TCI公司提供,上述试剂均为分析纯,使用前未经纯化;实验用水为去离子水。
1.2 样品合成
锌铝水滑石的合成:采用共沉淀法合成具有不同锌铝比的Zn-Al LDH样品,首先,分别将一定量的 Zn(NO3)2·6H2O 和 Al(NO3)3·9H2O 加入去离子水中,搅拌混合,形成金属离子浓度为0.15 mol·L-1的溶液,然后用氢氧化钠(2 mol·L-1)调节溶液的pH值,使之保持在~7.5。最后,将上述溶液移入三口烧瓶,并在70℃水浴加热24 h,待溶液冷却后通过离心、洗涤收集样品,并在70℃烘干。所得到的7个样品分别标记为x-Zn-Al LDH,x表示投料锌铝物质的量之比(x=2、3、4、5、6、7、8)。
ZnAl2O4的合成:以 Zn(NO3)2·6H2O 和 Al(NO3)3·9H2O为原料,首先配成离子浓度为1 mol·L-1的溶液,其中锌铝离子的物质的量之比为1∶2,然后在搅拌过程中,用氨水调节pH=12,生成白色胶状物,离心收集、干燥,最后在1 000℃下煅烧。
1.3 测试与表征
X射线衍射(XRD)测试采用德国布鲁克(BRUKER)D8 ADVANCE型号的X射线衍射仪,Cu靶,Kα辐射,电压40 kV,电流 30 mA,扫描速度:0.2°·min-1,采样间隔 0.019 450°。LDHs中锌铝元素含量是将合成的LDHs通过盐酸处理后,用电感耦合等离子体质谱仪(ICP-MS 7900)分析得到。采用扫描电镜(FEI Quanta 400 FEG)分析样品的表观形貌。用德国耐驰公司生产的STA 449F5热重分析仪对样品进行热重分析,升温速率为10℃·min-1,载气为 Ar气,流量为 100 cm3·min-1。 在进行 N2吸附-脱附等温线测试之前,将样品于100℃的温度下进行脱气处理,用康塔IQ2吸附仪在77 K下测量,总孔体积以相对压力为0.99的条件下吸附液氮的体积计算得到,微孔体积采用t-plot法计算,介孔体积为总孔体积与微孔体积之差。
1.4 吸附实验
吸附热力学测试:配置不同初始浓度的邻苯二甲酸溶液,将5 mg真空干燥过的吸附剂加入50 mL一定浓度的邻苯二甲酸溶液中,搅拌混合,在20℃下保持24 h。然后用0.22 m聚四氟乙烯膜过滤器将溶液进行过滤,并用紫外分光光度计 (北京普析TU-1810)检测吸附后溶液中吸附质的浓度。
吸附动力学测试:将50 mL浓度为100 mg·L-1的邻苯二甲酸溶液与5 mg真空干燥过的吸附剂混合并不断搅拌,保持温度为20℃,每隔一定时间,取一定量的溶液用0.22 m聚四氟乙烯膜过滤器过滤,然后用紫外分光光度计测量溶液中吸附质的浓度。
吸附剂对溶液中吸附质的吸附量计算公式如下:

C0、Ce分别为起始和吸附平衡后溶液中吸附质的质量浓度(mg·L-1);V为溶液体积(L);m 为吸附剂质量(g)。
2 结果与讨论
2.1 样品组成与结构性质表征
2.1.1 ICP、XRD和形貌分析
ICP定量分析结果表明,Zn-Al LDHs系列样品的实际锌铝比比合成中的投料比低,其值分别为1.89、2.87、3.41、3.93、4.50、6.15 和 7.83。 所合成 Zn-Al LDHs样品的XRD图如图1所示,所有Zn-Al LDHs样品在低衍射角度(2θ≈10°、20°)均有相对强度较大的特征衍射峰,峰形尖锐且较宽,分别归属于(003)、(006)晶面对应的衍射峰。在高衍射角度(2θ≈30°、34°、60°),特征衍射峰的强度较弱,分别归属于(009)、(101)、(110)晶面衍射峰。 晶胞参数 a表示晶体内层结构中金属离子之间的平均距离、c表示3 倍的(003)晶面距离 a=2d(110),c=3d(003),Zn-Al LDHs层中阳离子与羟基之间键的强度和方向会影响晶胞参数[26]。对比7个样品可以发现:随着锌铝比的增加,a值略有增加,这是由于锌离子半径(0.74 nm)比铝离子(0.51 nm)半径大。同时,也可看出,随着锌铝比的增加,Zn-Al LDHs样品的特征衍射峰强度逐渐减弱,这是由于样品中杂质含量增加的缘故。在较高锌铝比时,杂质ZnO、ZnAl2O4相的特征衍射峰逐渐显示出来,且随锌铝比的增加峰强度变大[27-28]。
Zn-Al LDH的形貌如图2所示,Zn-Al LDH样品均呈层状结构,在较低锌铝比时,样品表面光滑。随着锌铝比的增加,样品表面粗糙程度逐渐增加,出现较小的剥落状颗粒,这可能是由于晶体表面逐渐出现ZnO相和ZnAl2O4相所导致的[29],该结论与上述XRD结果一致。
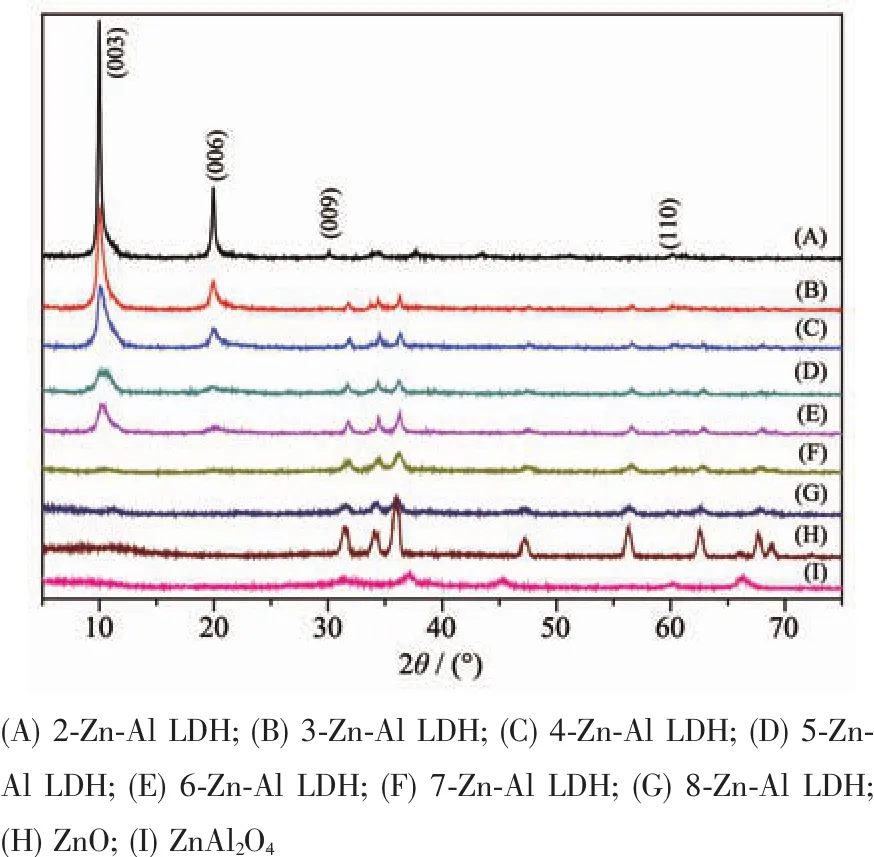
图1 不同锌铝比LDH样品及ZnO和ZnAl2O4的XRD图Fig.1 XRD patterns of LDH samples with different n Zn/n Al molar ratios and ZnO,ZnAl2O4

图2 不同锌铝比LDH样品和ZnO的SEM图片Fig.2 SEM micrographs of LDH samples with different n Zn/n Al molar ratios and ZnO
2.1.2 热重分析
不同锌铝比LDH样品的热重曲线如图3所示,所合成Zn-Al LDH样品表现出类似的失重趋势,可分为三部分:200℃之前的失重,主要是由于吸附在水滑石表面和层间的水分子脱除所导致的;在200~300℃之间,类镁石层脱羟基产生失重;在300~500 ℃水滑石层间离子 (NO3-、OH-、CO32-) 被分解,层状结构被破坏,导致失重[30-31];500℃之后没有明显的失重现象。计算200~500℃之间7个不同锌铝比LDH样品的失重,分别为22.90%、22.91%、21.77%、17.46%、14.54%、13.30%和 8.61%, 可以看出,随着锌铝比的增加,样品失重百分比逐渐减少,这是由于锌铝比的增加,ZnO相和ZnAl2O4相的含量增加,而ZnO和ZnAl2O4在200~500℃之间失重较小,从而使得Zn-Al LDH的失重百分比减小[32-33]。
2.1.3 氮气(N2)吸脱附和多孔性能
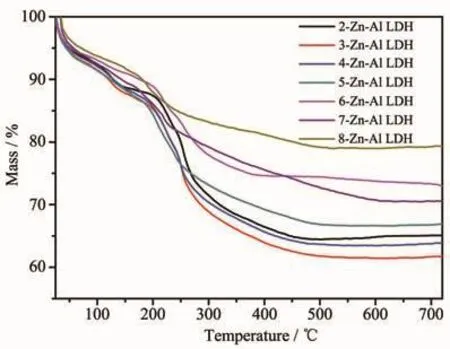
图3 不同锌铝比LDH样品的热重曲线Fig.3 TGA curves of LDH samples with different n Zn/n Al molar ratios
Zn-Al LDH的孔隙结构通过氮气吸脱附来表征,吸附等温线如图4所示。所有Zn-Al LDH的氮气吸脱附等温线均属于Ⅳ类型并有滞后回环,说明所合成的材料具有介孔结构[34]。这主要是由于LDH的层间颗粒所形成的。锌铝比为2时,所合成Zn-Al LDH的表面积和孔容均为最小。在较低锌铝比时,随着锌铝比的增加,Zn-Al LDH的表面积逐渐增大(表1),这是由于杂质的出现,导致LDH层与层之间面对面聚集的几率减小,从而导致孔隙结构增加,表面积增大[35]。在锌铝比为6时,Zn-Al LDH的BET表面积和总孔体积达到最大,分别为126 m2·g-1和 0.24 cm3·g-1。进一步增加锌铝比,Zn-Al LDH的BET表面积和总孔体积下降,这可能由于锌铝比过大,导致样品中生成的水滑石含量减少,而杂质组分为致密结构,孔隙不发达,因此,导致样品表面积和孔容减小。
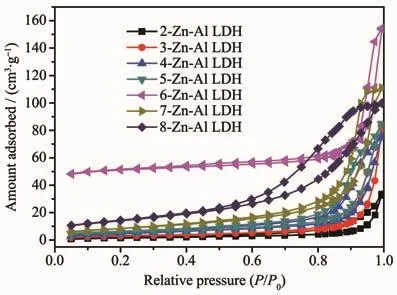
图4 不同锌铝比LDH样品的氮气吸脱附等温线Fig.4 N2 adsorption-desorption isotherm of LDH samples with different n Zn/n Al molar ratios

表1 不同锌铝比LDH样品的结构及孔隙性质Table 1 Textural properties of LDH samples with different n Zn/n Al molar ratios
2.2 吸附邻苯二甲酸
2.2.1 不同锌铝比水滑石吸附性能对比
将上述不同锌铝比的水滑石用作吸附剂,在初始浓度为100 mg·L-1的邻苯二甲酸溶液中吸附24 h后,其吸附量如图5所示。可以看出,在较低锌铝比时,随着水滑石锌铝比的增加,其吸附量逐渐增大;当锌铝比增加到6,继续增大锌铝比,样品的吸附量变化极小。水滑石对邻苯二甲酸的吸附量最高约为480 mg·g-1,远高于文献中报道的活性炭(249 mg·g-1)、MOFs(187 mg·g-1)[36]及吸附树脂(约 120 mg·g-1)[37]等。
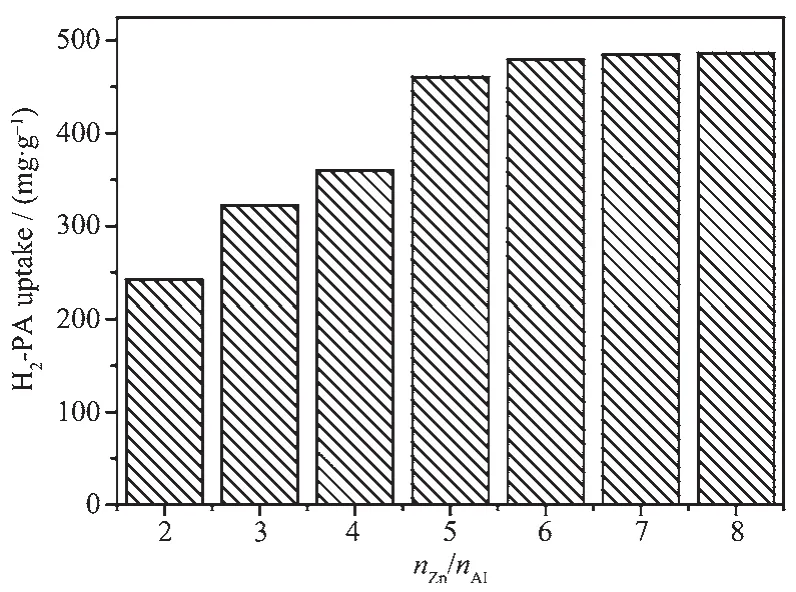
图5 不同锌铝比LDH样品对邻苯二甲酸的吸附量Fig.5 H2-PA removal capacity of LDH samples with different n Zn/n Al molar ratios
2.2.2 吸附动力学研究
选取6-Zn-Al LDH样品,对吸附性能进行进一步研究,在20℃的温度下测试样品吸附时间与吸附量的关系,结果如图6所示,在初始阶段,随着吸附时间的增加,样品的吸附量快速增大,说明在初始吸附阶段,邻苯二甲酸与Zn-Al LDH上的吸附位点快速结合。当吸附时间为270 min时,吸附量达到最大,再增加吸附时间,样品的吸附量变化较小,说明吸附过程已经达到饱和。

图6 不同吸附时间6-Zn-Al LDH样品对邻苯二甲酸的吸附量Fig.6 Adsorption capacity of 6-Zn-Al LDH sample with different adsorption time
将所得数据分别用准一级动力学方程和准二级动力学方程[38-39]进行拟合,拟合结果如图7和表2所示。
准一级动力学方程:
Ln(qe-qt)=Lnqe-k1t
准二级动力学方程:
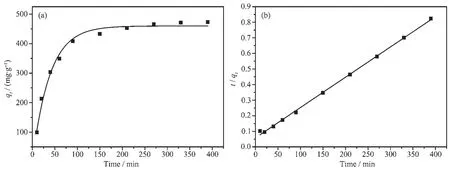
图7 6-Zn-Al LDH样品吸附邻苯二甲酸的准一级动力学拟合(a)和准二级动力学拟合(b)Fig.7 Pseudo-first order kinetic(a)and pseudo-second order kinetic(b)for H2-PA adsorption onto the 6-Zn-Al LDH sample

表2 6-Zn-Al LDH样品吸附邻苯二甲酸的动力学拟合参数Table 2 Kinetics parameters of adsorption H 2-PA onto the 6-Zn-Al LDH sample
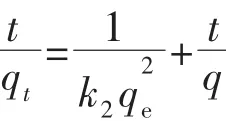
其中,qe(mg·g-1)为吸附平衡时6-Zn-Al LDH对邻苯二甲酸的吸附量;qt(mg·g-1)为时间t时6-Zn-Al LDH对邻苯二甲酸的吸附量;k1(min-1)、k2(g·mg-1·min-1)分别为准一级动力学和准二级动力学速率常数。
从拟合的结果可以看出,一级动力学方程模拟的相关系数(R2=0.987)小于二级动力学方程的相关系数(R2=0.999)。这表明准二级动力学方程比准一级动力学方程能更好地描述LDH对邻苯二甲酸的吸附。
内扩散模型又称为Weber-Morris动力学模型,方程为qt=kw,mt0.5+C。qt:时间t时的吸附量,C:涉及到厚度、边界层的常数,kw,m:内扩散率常数。
分别以qt和t0.5为纵坐标和横坐标作图 (图8),由斜率和截距可求出内扩散模型速率常数kw,m和与边界层厚度相关的常数C。内扩散模型模拟得到的不是条直线且不通过原点,说明吸附过程不是由粒子内部扩散单独控制,还受粒子外部扩散及其他因素影响[40-41]。在10~90 min之间,吸附速率较快,以外扩散为主,邻苯二甲酸从溶液主体迅速扩散到6-Zn-Al LDH表面上,并与吸附位紧密结合发生吸附行为;在90~270 min之间,主要发生内扩散,邻苯二甲酸从6-Zn-Al LDH表面向层间或孔道内扩散进行吸附;在270 min之后,吸附速率减慢,吸附逐渐趋于饱和。
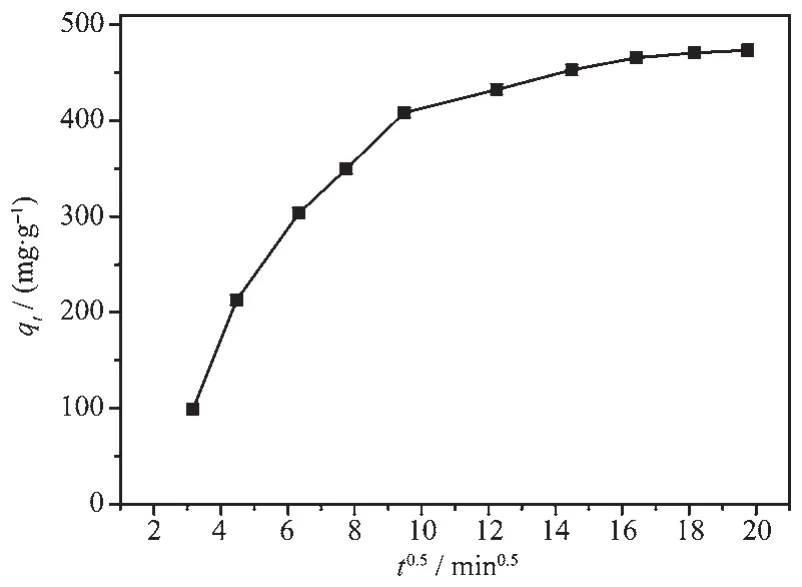
图8 6-Zn-Al LDH样品吸附邻苯二甲酸的内扩散模拟曲线Fig.8 Curve of internal diffusion simulation of adsorption H2-PA onto the 6-Zn-Al LDH sample
2.2.3 吸附热力学研究
图9所示为6-Zn-Al LDH对邻苯二甲酸的吸附等温线,可以看出,随着初始浓度的增加,6-Zn-Al LDH的饱和吸附量也逐渐变大。分别用Langmuir等温吸附模型和Freundlich等温吸附模型[42-43]对6-Zn-Al LDH吸附邻苯二甲酸的热力学吸附过程进行拟合,拟合结果如表3所示。比较结果发现,Langmuir等温吸附模型的线性相关系数为R2=0.776,远小于Freundlich等温吸附模型的线性相关系数(R2=0.988)。因此,样品6-Zn-Al LDH对邻苯二甲酸的热力学吸附过程更符合Freundlich等温吸附模型。
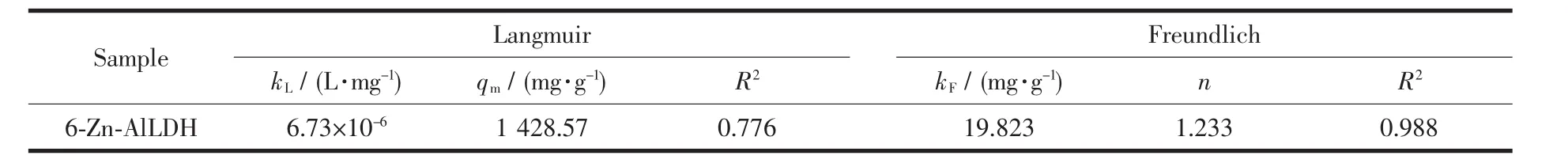
表3 6-Zn-Al LDH吸附邻苯二甲酸的Langmuir和Freundlich等温曲线参数Table 3 Langmuir and Freundlich isotherm parameters for H 2-PA adsorption onto the 6-Zn-Al LDH sample
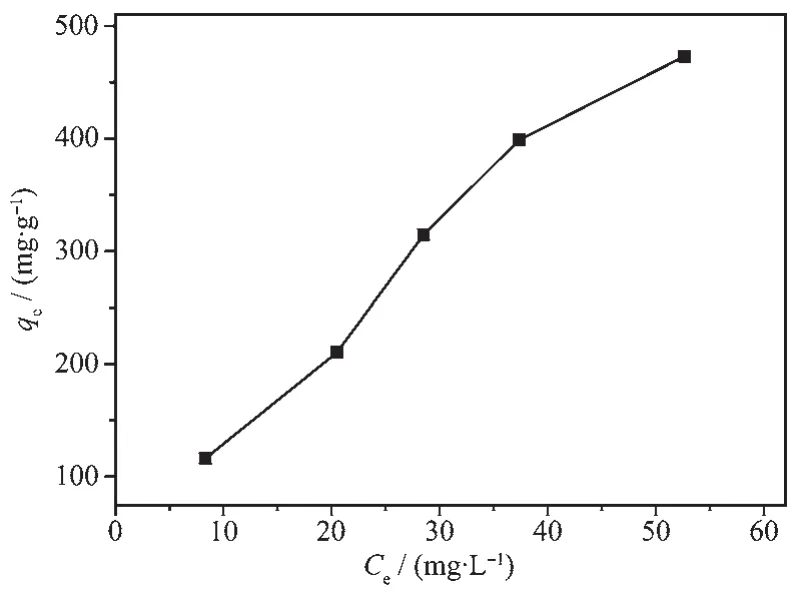
图9 邻苯二甲酸在6-Zn-Al LDH样品上的吸附等温线Fig.9 Adsorption isotherm of H2-PA on 6-Zn-Al LDH sample
2.2.4 吸附机理探讨
在吸附过程中,Zn-Al LDH本身呈碱性,而邻苯二甲酸为酸性。因此,酸-碱作用有利于邻苯二甲酸的吸附。此外,Zn-Al LDH颗粒表面带正电荷,而邻苯二甲酸在溶液中易水解形成阴离子,与Zn-Al LDH产生静电吸附作用,从而被吸附[36,44]。因此,纯的水滑石对邻苯二甲酸的吸附量较高。
此外,由图5和表1可知,在锌铝比为2~5时,Zn-Al LDH样品对邻苯二甲酸的吸附量随锌铝比的增加而增大。考虑到随着锌铝比的增加,样品中杂质ZnO和 ZnAl2O4量的增大,因此,为了考察杂质的存在对水滑石吸附量的影响,在相同条件下测试了分析纯ZnO和制备的ZnAl2O4对邻苯二甲酸的吸附性能。结果表明,ZnAl2O4对邻苯二甲酸的吸附量极小(27.9 mg·g-1),而纳米 ZnO(见图 2)的吸附量较高,约为 450 mg·g-1,略低于 6-Zn-Al LDH。可以得出,随锌铝比的增加,水滑石吸附量的增大有以下两方面的原因:(1)随锌铝比的增加,水滑石的表面积增大,与邻苯二甲酸的接触面积增加,吸附量提高。(2)随锌铝比的增加,水滑石中氧化锌的含量增加,而氧化锌对邻苯二甲酸的吸附量较高,导致吸附量的增大。而在较高锌铝比时(6~8),随锌铝比的增加,水滑石的吸附量变化较小。这可能是因为随着锌铝比的增加,水滑石中氧化锌含量增加,从而增加了吸附剂单位面积的吸附位点。因此,虽然随锌铝比的增加,水滑石表面积减小,但单位面积氧化锌含量增多,所以,吸附量随锌铝比变化较小。
2.2.5 Zn-Al LDH的循环利用
6-Zn-Al LDH吸附邻苯二甲酸后,将样品回收并用低浓度氢氧化钠(0.02 mol·L-1)进行脱附处理,洗涤干燥后,测试水滑石的循环再生性能。图10为不同循环再生次数时,6-Zn-Al LDH对邻苯二甲酸的吸附量。从图中可以发现,经过3次循环再生后,6-Zn-Al LDH对邻苯二甲酸仍保持较好的吸附性能,吸附量可达到初次吸附的80%以上,这说明Zn-Al LDH是一种可重复使用且循环性能良好的吸附材料。
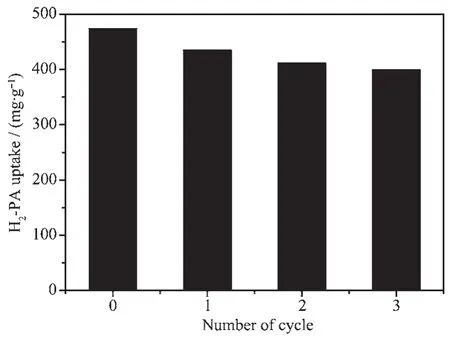
图10 循环再生次数对邻苯二甲酸吸附量的影响Fig.10 Effect of regeneration time on adsorption
3结 论
本文以共沉淀法成功合成了一系列不同锌铝比的Zn-Al LDH,并研究了锌铝比对LDH的形貌结构、组成和吸附邻苯二甲酸性能的影响。在较低锌铝比时,LDH的结晶度及纯度较高,随着锌铝比的增加,杂质ZnO、ZnAl2O4相的含量逐渐增加,样品BET表面积和总孔体积也逐渐增加,在锌铝比为6时,Zn-Al LDH的BET表面积和总孔体积达到最大,分别为 126 m2·g-1和 0.24 cm3·g-1。 进一步增加锌铝比,Zn-Al LDH的BET表面积和总孔体积减小。将Zn-Al LDH用作吸附剂吸脱附除水中的邻苯二甲酸,结果表明,所制备Zn-Al LDH样品均对邻苯二甲酸有较强的吸附能力,随着锌铝比的增加,LDH对邻苯二甲酸的吸附量逐渐变大,当锌铝比为6时,吸附量可达约480 mg·g-1,继续增大锌铝比,样品的吸附量不再增加。进一步对6-Zn-Al LDH吸附邻苯二甲酸的动力学和热力学过程进行了研究,结果表明,吸附动力学过程更好地符合准二级动力学模型;吸附热力学过程与Freundlich等温吸附模型更吻合。6-Zn-Al LDH在循环利用3次以后,吸附量仍可达到初次吸附的80%以上,是一种循环性能较好的吸附材料。
[1]Charles A S,Dennis R P,Thomas F P,et al.Chemosphere,1997,35(4):667-749
[2]Susanne J,Jörgen E,Anna L,et al.Water Res.,2003,37:609-617
[3]Mahmoud M,JoséR U,Raúl OP,et al.J.Environ.Manage.,2012,109:164-178
[4]CHEN Bo(陈波),LIN Jian-Guo(林建国),CHEN Qing(陈清),Envirinmental Science and Management(环境科学与管理),2009,34(2):71-75
[5]NafaâA,Lotfi M.Sep.Purif.Technol.,2004,38:233-239
[6]JoséD M D,Mahmoud M A D,JoséR U,et al.J.Colloid Interface Sci.,2012,369:358-365
[7]CHENG Xu-Ze(陈旭泽),WU Jia-Wei(伍佳伟),QIU Cai-Ying(邱彩英),et al.Chemistry&Bioengineering(化学与生物工程),2016,33(1):57-59
[8]LI Xiao-Juan(李小娟),HE Chang-Fa(何长发),HUANG Bin(黄斌),et al.Chemical Industry and Engineering Progress(化工进展),2016,35(2):586-594
[9]Chan H W,Lau T C,Ang PO,et al.J.Appl.Phycol.,2004,16:263-274
[10]Markéta J,Roman S.J.Environ.Manage.,2012,94:13-24
[11]Ayranci E,Bayram E.J.Hazard.Mater.,2005,122:147-153
[12]Li J D,Shi Y L,Cai Y Q,et al.Chem.Eng.J.,2008,140:214-220
[13]Yan X L,Yang Y L,Wang C,et al.J.Sol-Gel Sci.Technol.,2016,60:523-530
[14]Wang C,Yan X L,Hu X Y,et al.J.Mol.Liq.,2016,223:427-430
[15]Richetta M,Digiamberardino L,Mattoccia A,et al.Surf.Interface Anal.,2016,48:514-518
[16]Liu JQ,Song JY,Xiao H D,et al.Powder Technol.,2014,253:41-45
[17]Kloprogge J T,Hickey L,Frost R L.J.Solid State Chem.,2004,177:4047-4057
[18]Mascolo G,Mascolo M C.Microporous Mesoporous Mater.,2015,214:246-248
[19]Peligro F R,Pavlovic I,Rojas R,et al.Chem.Eng.J.,2016,306:1035-1040
[20]Inacio J,Taviot-Gueho C,Forano C,et al.Appl.Clay Sci.,2001,18:255-264
[21]ZHANG Lu-Hong(张璐虹),TANG You-Gen(唐有根),ZHANG Li(张丽),et al.Journal of Functional Materials(功能材料),2012,18(43):2469-2472
[22]WANG Long(王 龙),GAO Xu(高 旭),GUO Jin-Song(郭 劲松),et al.Journal of Chongqing University(重庆大学学报),2011,5(11):2537-2541
[23]Li F,Wang Y F,Yang Q Z,et al.J.Hazard.Mater.,2005,125(1/2/3):89-95
[24]Frederick L T,Godwin A A,Ray L F.Appl.Surf.Sci.,2016,383:200-213
[25]Li R H,Wang J J,Zhou B Y,et al.Sci.Total Environ.,2016,559:121-129
[26]Tzompantzi F,Mantilla A,Baňuelos F,et al.Top.Catal.,2011,54:257-263
[27]Abdullah A A A,Abidin Z T,Mohd Z B H,et al.J.Solid State Chem.,2012,191:271-278
[28]Seftel E M,Popovici E,Mertens M,et al.Microporous Mesoporous Mater.,2008,113:296-304
[29]Kingshuk D,Somnath D,Amitava P.J.Colloid Interface Sci.,2012,366:8-36
[30]Huang JH,Yang Z H,Wang R J,et al.J.Mater.Chem.A,2015,3:7429-7436
[31]SONG Guo-Jun(宋国君),SUN Linag-Dong(孙良栋),LI Pei-Yao(李培耀),et al.Materials Review(材料导报),2008,22(1):53-57
[32]Didier T,Olivier L,Bernard C,et al.Microporous Mesoporous Mater.,2005,80:213-220
[33]Tatjana V,Andreas R,Jonjaua R,et al.J.Therm.Anal.Calorim.,2012,110:227-233
[34]WANG Lan(王澜),GE Sheng-Song(葛圣松),SHAO Qian(邵谦),et al.Chinese J.Inorg.Chem.(无机化学学报),2016,32(11):1896-1904
[35]Benito P,Labajos F M,Rocha J,et al.Microporous Mesoporous Mater.,2006,94:148-158
[36]Nazmul A K,Beom K J,Zubair H,et al.J.Hazard.Mater.,2015,282:194-200
[37]LIU Zong-Tang(刘总堂),SUN Yu-Feng(孙玉凤),YANG Shang-Shang(杨珊珊),et al.Ion Exchange and Adsorption(离子交换与吸附),2013,29(1):51-57
[38]Shahwan T.J.Environ.Chem.Eng.,2014,2:1001-1006
[39]Ho Y S,McKay G.Process Biochem.,1999,34:451-465
[40]YUE Qin-Yan(岳钦艳),XIE Jian-Kun(解建坤),GAO Bao-Yue(高宝玉),et al.Acta Scientiae Circumstantiae(环境科学学报),2007,27(9):1431-1438
[41]SUN Xiao-Li(孙小莉),ZENG Qing-Xuan(曾庆轩),FENG Chang-Gen(冯长根).Acta Phys.-Chim.Sin.(物理化学学报),2009,25(10):1951-1957
[42]WANG Long(王 龙),GAO Xu(高 旭),GUO Jin-Song(郭 劲松),et al.Journal of Chongqing University(重庆大学学报),2010,33(7):91-96
[43]SUN Yuan-Yuan(孙媛媛),ZENG Xi-Bai(曾希柏),BAI Ling-Yu(白玲玉).Acta Scientiae Circumstantiae(环境科学学报),2011,31(70):1377-1385
[44]NI Zhe-Ming(倪哲明),WANG Qiao-Qiao(王巧巧),YAO Ping(姚萍).Acta Chim.Sinica(化学学报),2011,69(5):529-535
Zn/Al Hydrotalcite with Different nZn/nAlMolar Ratios:Synthesis and Phthalic Acid Adsorption Behaviour
Zn-Al layered double hydroxides(LDHs)with different Zn/Al molar ratios were prepare by co-precipitation method in this work.The structure and composition were investigated using X-ray diffraction(XRD),scanning electron microscope (SEM),thermogravimetric (TG),N2adsorption-desorption and inductively coupled plasma mass spectrometry (ICP-MS).The adsorption properties of as-prepared Zn/Al hydrotalcites for phthalic acid removal from water were investigated and compared.Results show that the adsorption capacity increased with the increasing of Zn/Al molar ratios at low Zn/Al molar ratios for hydrotalcites.Further increasing the nZn/nAlmolar ratios(>6),the adsorption capacity shows little change.Among those hydrotalcites,one sample with the highest adsorption capacity was selected and its adsorption kinetic and isotherm was further investigated.The adsorption equilibrium data were well described by Freundlich isotherm model and the kinetics followed a pseudo-second order kinetic equation/mechanism.In addition,the hydrotalcite can be reused at least 3 cycles without significant loss of adsorption capacity.
hydrotalcite;Zn/Al molar ratios;adsorption and separation;phthalic acid;adsorption kinetics;adsorption thermodynamics
O614.24+1;O614.3+1
A
1001-4861(2017)10-1748-09
10.11862/CJIC.2017.232
YANGYing-Li YAN Xin-Long*HU Xiao-Yan ZHOU Min
(School of Chemical Engineering&Technology,Key Laboratory of Coal Processing and Efficient Utilization,Ministry of Education,China University of Mining and Technology,Xuzhou,Jiangsu 221116,China)
2017-04-12。收修改稿日期:2017-08-30。
国家自然科学基金(No.21606252,21506247),江苏省自然科学基金(No.BK20140182),江苏高校优势学科建设工程和中国矿业大学研究生教育教学改革研究与实践项目资助。
*通信联系人。 E-mail:yanxl@cumt.edu.cn
