反相微乳液交联法制备葡聚糖水凝胶微球的粒径调控
2017-10-20张稳韩晓东于坤苏红莹贾庆明陕绍云
张稳,韩晓东,于坤,苏红莹,贾庆明,陕绍云
反相微乳液交联法制备葡聚糖水凝胶微球的粒径调控
张稳,韩晓东,于坤,苏红莹,贾庆明,陕绍云
(昆明理工大学化学工程学院,云南昆明 650500)
基于天然高分子的水凝胶微球因具有良好的生物相容性,作为生物材料得到了广泛应用。本文采用反相微乳液交联技术制备了一系列葡聚糖水凝胶微球,并探讨了反相微乳液体系中表面活性剂的亲水亲油平衡值(HLB值)、乳化方式、水油相体积比()、水相与表面活性剂的摩尔比(0)等因素对该葡聚糖水凝胶微球形貌及粒径的影响情况。结果表明:采用环己烷(CYH)/Span 80-Tween 80/醛基化葡聚糖(Dex-CHO)乳液体系制备所得葡聚糖水凝胶微球的粒径在400nm~70μm之间可调;相对于机械搅拌乳化,超声波乳化条件下获得的凝胶微球具有更小的粒径,且当复配乳化剂(Tween 80)/(Span 80)=0.10、HLB值=5.27、=1/6时,获得的凝胶微球粒径最小(约422nm);葡聚糖凝胶微球的粒径随着0值的增加呈现增大趋势。该葡聚糖水凝胶微球粒径可控,是一类天然高分子水凝胶,有望作为载体材料应用于生物医学领域。
葡聚糖;水凝胶微球;反相微乳液;粒径调控
基于天然高分子材料的水凝胶因具有优良的生物安全性,作为生物材料得到了广泛的应用。葡聚糖是一种来源丰富的天然多糖材料,作为一种生物材料应用具有良好的生物相容性,而且具有容易获取、与药物亲和能力强,其长链上的活性基团极易进行修饰得到具有反应活性的葡聚糖衍生物,能通过不同方式进行交联形成水凝胶网络等特点[1-3],因此,是制备天然高分子水凝胶并作为生物材料应用的优良聚合物。水凝胶微球的形貌及粒径是影响其性能及应用的重要因素,特别是作为药物、蛋白质、疫苗等环境敏感型分子的载体系统时对其粒径有一定的要求[4],因此控制水凝胶微球的粒径大小并根据应用领域对其粒径进行调控在水凝胶微球的制备方法中显得尤为重要[5]。微乳液法是目前常用于微/纳米材料制备的一种方法。其中,反相微乳液交联是在反相微乳液聚合的基础上发展起来的,其首先应用于高分子领域。它是以油包水(W/O)型反相微乳液作为微反应器,通过交联剂对修饰了活性反应基团的水溶性聚合物进行交联,获得稳定的凝胶状纳米网络[6-8],该法具有通过改变微乳液结构参数、调节微观结构来控制水凝胶微球的粒径、形貌的特点,并且反应条件简单。微乳液是一种热力学稳定体系,它的制备与优化是反相微乳液交联的基础,建立稳定的反相微乳液体系,对于研究反相微乳液交联法制备水凝胶微球至关重要。水凝胶粒子的纳米尺度是其性质和功能的基础,此法为获得尺度均一可控的纳米水凝胶提供了新的思路和手 段[9-11]。通过绿色简单的反相微乳液交联法制备的天然高分子葡聚糖水凝胶微球有望作为载体材料应用于生物医学领域。
葡聚糖的反相微乳液由醛基化葡聚糖单体水、油相、表面活性剂等构成。乳化剂种类及HLB值、乳化方式、水油相体积比()、水与表面活性剂的摩尔比(0)等因素是影响着微乳液结构的重要因素,进而影响葡聚糖水凝胶微球的粒径。本文采用Shah法把油相(环己烷)、表面活性剂(Span 80/Tween 80)混合均匀,然后向体系中加入水相,在一定配比范围内体系呈半透明,即形成微乳 液[12-13]。研究者们也曾用环己烷(CYH)/Span 80-Tween 80/水相组成的微乳液体系制备出了多种纳米材料[14-16]。本文在微乳液的基础上采用环己烷(CYH)/Span 80-Tween 80/醛基化葡聚糖(Dex-CHO)反相微乳液体系用于葡聚糖水凝胶微球的制备。通过扫描电子显微镜(SEM)、动态激光光散射仪(DLS)进行分析,系统地研究影响葡聚糖水凝胶微球形貌和粒径大小的因素,确定了反相微乳液体系的优化配方,为进一步制备不同粒径的葡聚糖水凝胶微球奠定了基础。
1 实验
1.1 试剂与仪器
葡聚糖(Dextran,分子量w=40000,Aladdin化学公司);高碘酸钠(NaIO4,99.0%,Aladdin化学公司);Span 80(AR,SIGMA);Tween 80(AR,SIGMA-ALDRICH);乙二胺[C2H4(NH2)2, AR,≥99.0%,天津市风船化学试剂科技有限公司];环己烷(C6H12,AR,天津市风船化学试剂科技有限公司);实验用水为陶氏水处理设备工程有限公司生产的型号为TS-DI-10L/H设备产出的超纯水。
葡聚糖水凝胶微球的的粒径和形貌采用TESCAN公司的VEGA3 SBH型号扫描电子显微镜进行表征,测试前把分散于水溶液中的水凝胶微球滴在单晶硅上,室温干燥后,对样品进行喷金处理。采用动态激光光散射仪(DLS,英国Mastersizer 2000)对水凝胶微球在水溶液中的粒径分布进行 测定。
1.2 葡聚糖水凝胶微球的制备
以非离子型Span 80-Tween 80复配表面活性剂为乳化剂,环己烷为连续相,制备反相微乳液(0值为0.1969×10–3~1.575×10–3)。首先将适量的Tween 80-Span 80(质量比0.05~0.2)溶解于连续相环己烷中,配成一定浓度Span 80-Tween 80/环己烷溶液,搅拌3min,使其充分溶解;机械搅拌或超声条件下,将配制好的浓度为75mg/mL的醛基化葡聚糖水溶液(醛基化葡聚糖通过高碘酸钠氧化葡聚糖获得)1mL缓慢滴入该溶解了乳化剂的环己烷溶液中,充分乳化形成稳定的反相微乳液;再向获得的反相微乳液中滴入—NH2/—CHO的摩尔比为0.52的乙二胺溶液,室温、搅拌条件下反应20h。所得溶液通过离心收集沉淀,沉淀物用乙醇反复洗5~6次,去除乳化剂,得到葡聚糖水凝胶微球,并分散于去离子水中保存。本文在相同条件下采用单一Span 80作为乳化剂制备葡聚糖水凝胶微球,与采用复配表面活性剂乳液体系制备的葡聚糖水凝胶微球进行了对比。
2 结果与讨论
2.1 复配表面活性剂的HLB值对水凝胶微球粒径的影响
亲油性的Span 80(HLB=4.3)和亲水性的Tween 80(HLB=15)比例不同会影响混合乳化剂的HLB值和体系形成微乳液的类型,进而影响水凝胶微球的粒径和形貌。因此,实验测定交联温度25℃条件下,固定各组分的量,仅改变复配乳化剂中Span 80和Tween 80质量比时,油相环己烷、复配乳化剂混合体系在机械乳化条件下对水凝胶微球粒径和形貌的影响,结果见图1。实验中采用的Span 80/Tween 80复配体系的HLB值以及获得的凝胶微球的粒径大小如表1所示。
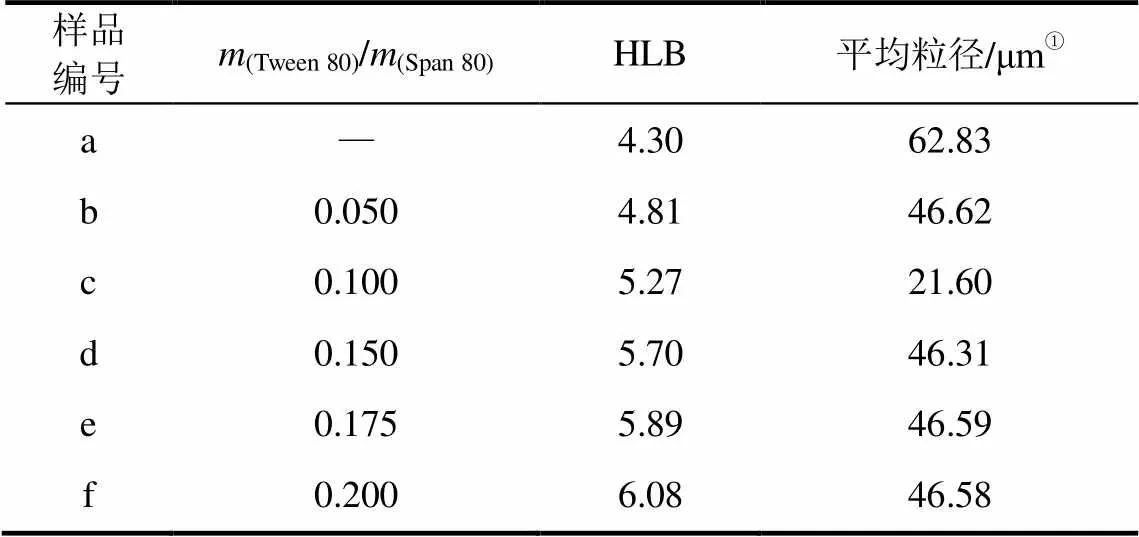
表1 复配表面活性剂的亲水亲油平衡值对水凝胶微球粒径的影响
① 平均粒径是采用DLS在水中测量所得。
从图1及表1中可以看出:使用单一Span 80作为乳化剂获得的葡聚糖凝胶微球[图1(a)]粒径较大(62.83μm),而使用Span 80/Tween 80复配体系制备的凝胶微球[图1(b)~图1(f)]粒径相对较小;且随着表面活性剂复配体系HLB值在可调范围内增加,获得的葡聚糖凝胶微球的粒径呈现先减小后增大并基本保持不变的趋势。从图中可看出所得的微球粒径范围20~63μm,该体系存在一个最佳HLB值约为5.27,获得的凝胶微球具有最小的粒径(21.60μm),且在这个HLB值附近所得微球粒径相对较小。以单一Span 80为乳化剂制备的葡聚糖凝胶微球为较大的圆球形颗粒,微球表面光滑,粒径分布较宽;而以Span 80/Tween 80复配体系(HLB=5.27)为乳化剂制备的凝胶微球具有更小的粒径,且粒径分布更为均匀,平均粒径分布在20 μm左右,相对于单一表面活性剂所制备的微球,尺寸明显减小。
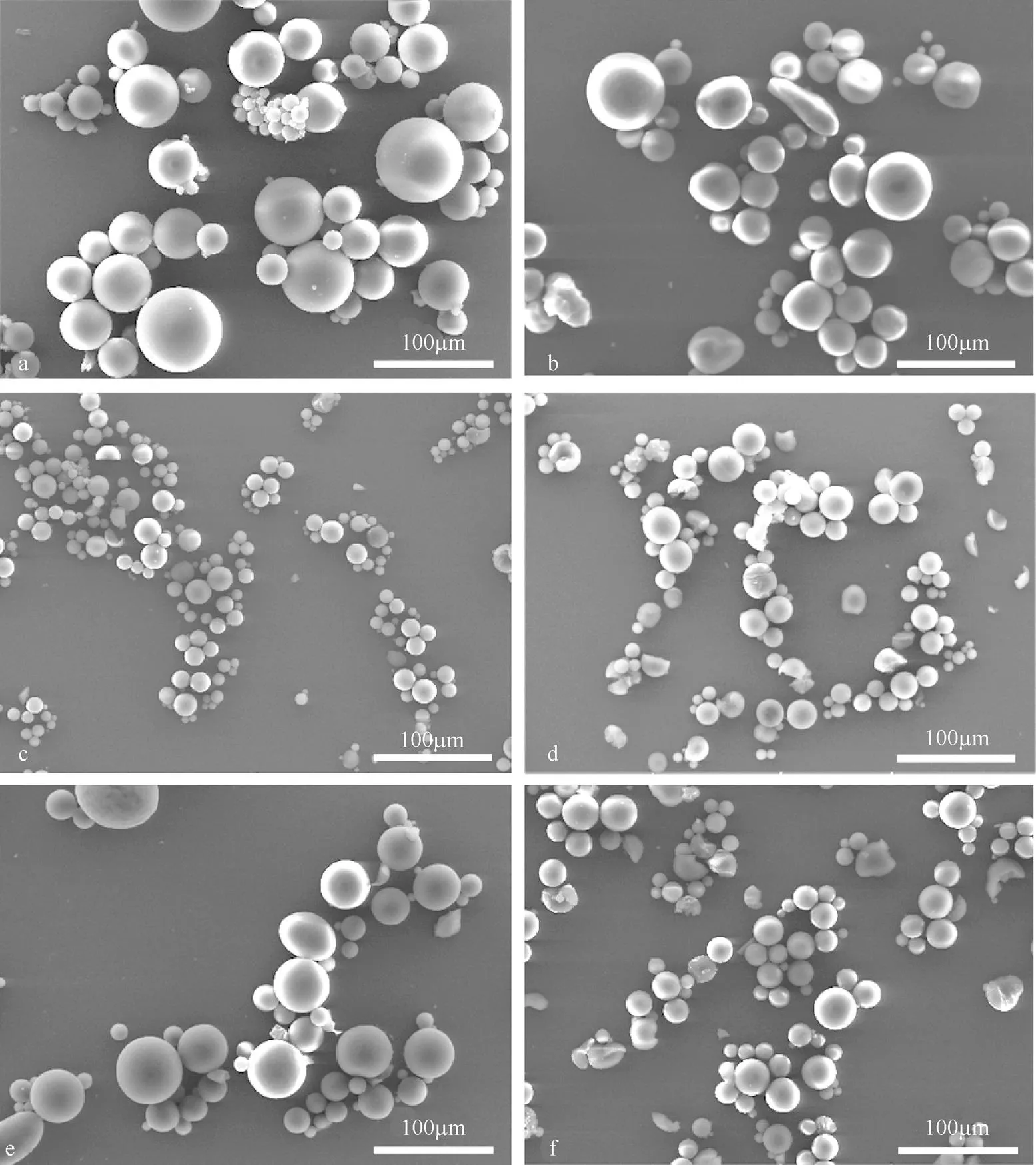
图1 不同质量比的表面活性剂(HLB值)所制备的葡聚糖水凝胶微球的SEM照片
(图中a~f为样品编号,同表1)
实验结果表明,在其他条件不变的情况下复配表面活性剂较之单一表面活性剂得到的乳状液更稳定。使用亲水表面活性剂与亲油表面活性剂复配后粒径明显减小且分布范围变窄,这是由于单一表面活性剂在体系中溶解度较低,两者复配后,彼此的亲水基团和亲油基团相互配合,从而相互有增溶作用。复配表面活性剂可能更多地降低了表面张力,有利于乳化过程的进行。更重要的是复配表面活性剂在界面层中分子能较紧密的排列,可在液珠表面形成混合液晶的中间相,在表面上复配表面活性剂组分之间可形成分子复合物。这些可使界面层的膜强度增加,增强乳状液对聚并的稳定性[13]。因此油溶性的表面活性剂Span 80与水溶性的表面活性剂Tween 80共同使用可使乳状液的稳定性大为提高,有利于微球的形成。表面活性剂Span 80/Tween 80复配比例的不同导致HLB值的变化,而HLB值与表面活性剂的结构、油相组成、温度、盐类型及结构又密切相关[17-19],是影响葡聚糖水凝胶微球形貌和粒径变化的因素,该因素影响力的大小由组成该体系的成分决定。
2.2 乳化方式对水凝胶微球粒径的影响
反相微乳液是油、水、表面活性剂按照一定的比例混合形成的透明或半透明的热力学稳定性体系,分散相质点在10~100nm之间,黏度小,流动性强,具有超低界面张力,增溶量大,应用广泛。乳状液作为多相分散体系,乳状液的制备是将大块的分散相变成0.5~2.5μm的液滴,将产生很大的界面积。在较高油水界面张力时,因为很大的界面积则需要较大的能量,这些能量的输入不能够靠简单摇动或搅拌完成。纳米乳液是非平衡体系,它的形成需要外加能量对其做功,其方式有摇荡、射流、搅动、流动、超声波振动等,利用这些方式乳化之后,可制备粒径更小的纳米粒子。而微乳液的形成本不需要外加功,主要依靠体系中各组分的匹配而自发乳化,但在这种条件下制备出的水凝胶微球呈微米级,对其在生物医药、化学分离等领域的应用有一定的限制。因此本文在其他条件均不变的情况下,仅改变形成稳定反相微乳液的乳化方式(机械乳化和超声乳化),探讨这两种乳化方式对葡聚糖水凝胶微球粒径的影响,结果见图2。
由图2可以看出,不同的乳化方式下形成的葡聚糖水凝胶微球的粒径差异很明显。机械乳化条件下形成的微球粒径在20μm左右,而超声乳化获得的微球粒径更小达600nm左右。机械乳化只是通过普通的搅拌剪切力促进微乳液颗粒的分散得到一定粒度分布的普通乳状液;超声乳化则依靠超声传播时介质分子受声波能量的振动而发生纵波方向上的弹性振动,从而引发一系列机械效应、空化效应及碎裂效应,这些效应的综合作用促使水相“喷发”进入油介质中,形成小液滴。另外,超声波的应用会产生声波的空穴,即一个简单的声波会使微泡形成,随后微泡有破裂或塌陷。某一个微泡的破裂会导致局部极度湍流,这种湍流微爆可作为一个有效的方法将分散在介质中的大液滴破裂为亚微尺寸[20-21]。
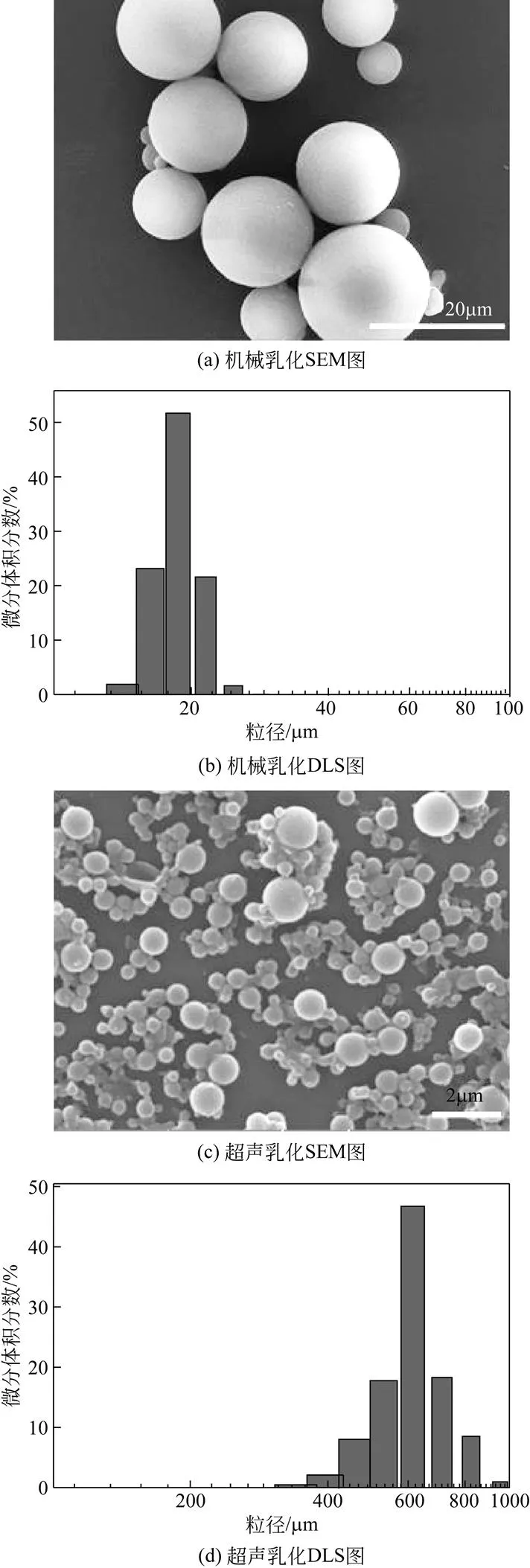
图2 不同乳化方式制备的葡聚糖水凝胶微球的SEM图及DLS图
2.3 水相与油相体积比对水凝胶微球形貌和粒径的影响
通过将表面活性剂溶解于油相中,再向油相中加入水相制备W/O型反相微乳液。加入水相的初期实际是从反相胶束到W/O型微乳液,随着水相的体积分数增加,合并在一起形成双连续或层状结构,而具有表面活性剂层状胶束特点的层状结构的形成对微乳液的形成起着重要作用[22]。当HLB=5.27、(Tween 80)/(Span 80)=0.1、超声乳化条件下时,水相与油相的体积比分别取1/4、1/6、1/8、1/10、1/12,对葡聚糖水凝胶微球形貌和粒径的影响如表2和图3所示。
可以看出从1/4降至1/10的范围内,即随体系中环己烷体积的增加,制备的葡聚糖水凝胶微球的粒径呈现先减小后增大而后基本保持不变的趋势。加入水相氧化葡聚糖溶液的初期,实际上是从反胶束到W/O型微乳液,随着体系中氧化葡聚糖体积分数的增加(油相体积分数较小),形成双连续或层状结构,在这种情况下形成的水凝胶微球如图3(a)所示,微球粒径稍大且粘结严重;当体系中氧化葡聚糖的体积分数达到乳状液转换点EIP(emulsion inversion point)附近时,体系中表面活性剂浓度可使得油相环己烷完全增溶,导致了单分散、亚微米大小的液滴形成,此情况下形成的微球如图3(c)、图3(e)所示,微球粒径较小且分散性相对较好;当体系中氧化葡聚糖的体积分数超过EIP点时,增加体系中油相环己烷的体积会使双连续或层状结构分解为更大的油滴,继续再加入环己烷并不改变油已经在液滴形成阶段所形成的液滴尺寸,此情况下所形成的水凝胶微球如图3(g)、图3(i)所示。此体系中HLB=5.27、(Tween 80)/(Span 80)=0.1、超声乳化条件下水油相体积比为1/6时效果最佳。
2.4 水相与表面活性剂的物质的量比0对水凝胶微球粒径的影响
微乳液合成纳米粒子的过程是通过水核的互相碰撞、物质交换来实现。因而,体系的动力学性质是影响粒子大小的重要因素[23]。在微乳液体系中,水是通过表面活性剂而分散于油相的,体系中水相与表面活性剂的摩尔比0以水(W)与表面活性剂(S)的相对含量来表示,即0=[W]/[S]。水与表面活性剂的摩尔比0的变化将直接影响到微乳液液滴水核半径大小,从而影响到纳米颗粒的大 小[24]。实验固定其他条件均不变,采用超声乳化探讨水相与表面活性剂的摩尔比0(0.1969×10–3~1.575×10–3)对葡聚糖水凝胶微球粒径的影响结果见图4及表3。
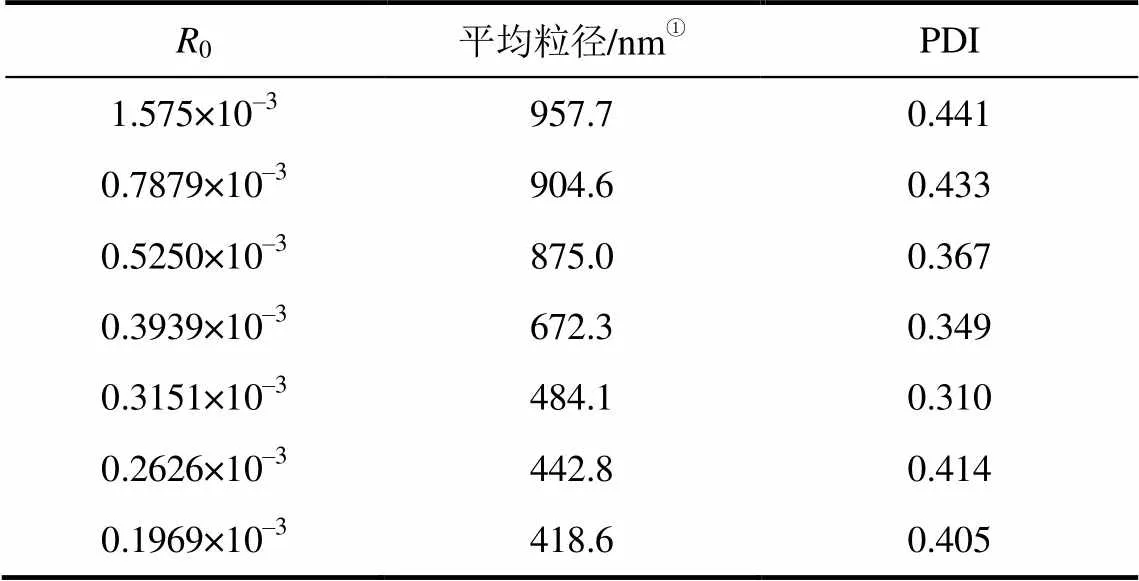
表3 R0对水凝胶微球粒径的影响
①平均粒径是采用DLS在水中测量所得。
从图4及表3中可以看出,随着水相与表面活性剂的物质的量比0的增加,葡聚糖水凝胶微球的粒径呈现增大趋势。在水凝胶微球的合成过程中,有机相中单分散的水核不断扩散、发生碰撞,水核的碰撞是非弹性碰撞,将导致水核间互相粘结并形成较大液滴。但由于表面活性剂的存在,水核间的这种粘结是不稳定的,聚结的大液滴又会相互分离,重新形成小的水核。这种聚合与分离是个动态过程,使水核的平均直径和数目不随时间发生变化。在反相微乳液体系中,反应物被限定于水滴内部,反应的发生是通过水滴的碰撞、聚结、物质交换与化学反应等步骤实现的,反应产物存在于大小均匀的水核当中。当产物粒子的大小接近水核的大小时,表面活性剂分子所形成的界面膜附着于产物粒子的表面,限制了产物粒子的进一步生长,使合成的粒子大小、形貌与水核的大小和形状一致[25-26]。当0较小时,水核在体系中所占比例较低,水核分散度高,体系的流动性好,液滴相互碰撞的概率较低,同时,发生物质交换后的粘结水核发生分离的趋势显著,使产物粒子不容易长大和团聚所形成的葡聚糖水凝胶微球的粒径较小。随着0的提高,体系中水的浓度增大,水核在体系中所占比例提高,体系的流动性也随之变差,两液滴相互碰撞的概率增大,而发生物质交换后的粘结水核发生分离的动力减弱,从而增大了反应器的平均尺寸,使产物粒子的平均直径变大。
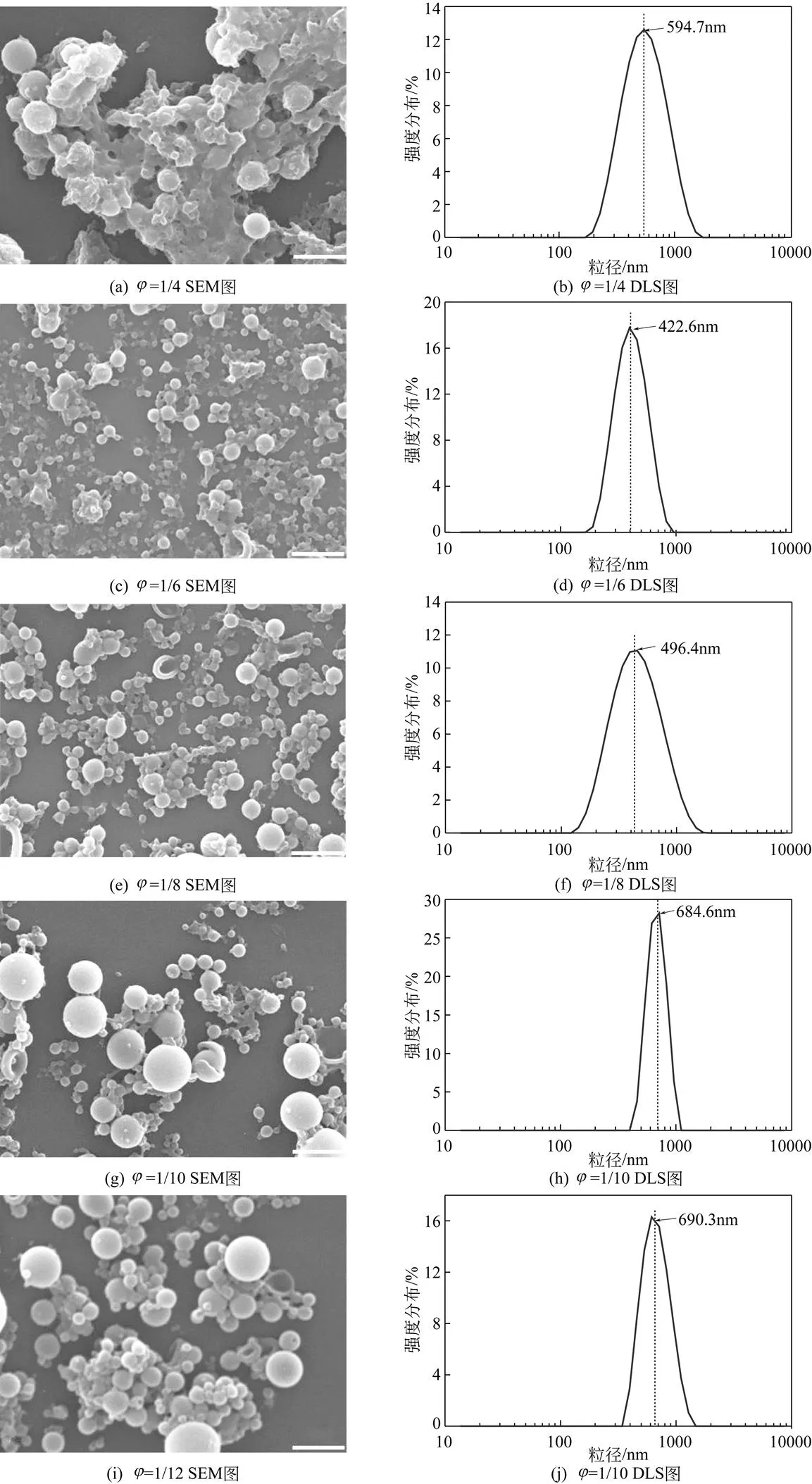
图3 不同水油相体积比φ下制备的葡聚糖水凝胶微球的SEM图及DLS图
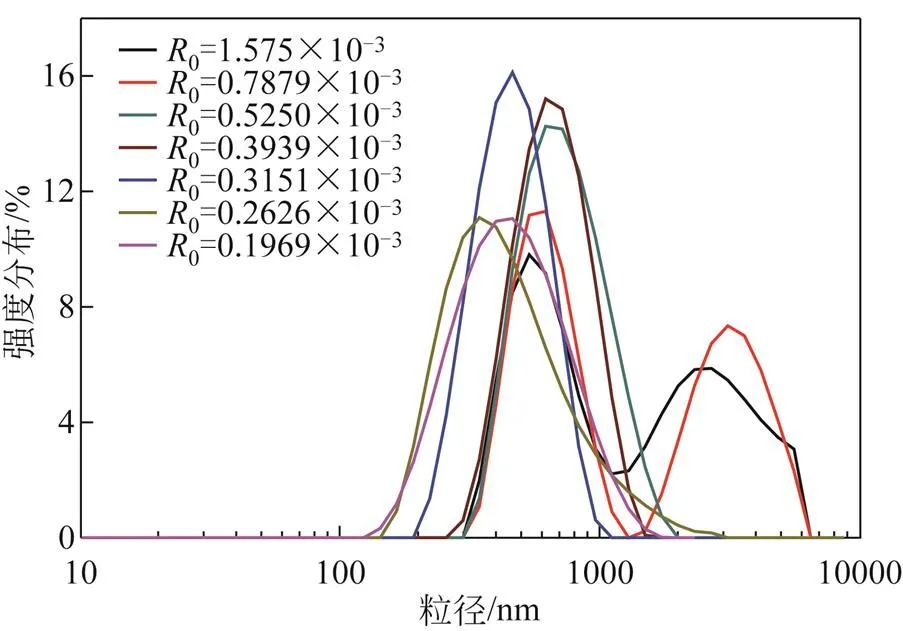
图4 水相与表面活性剂不同摩尔比R0下制备葡聚糖水凝胶微球的DLS图
3 结论
本文通过反相微乳液交联法,以天然高分子葡聚糖为材料基础,乙二胺为交联剂,在室温条件下制备了一系列粒径分布在400nm~70μm的水凝胶微球。通过对制备葡聚糖水凝胶微球影响因素的探索得到了环己烷(CYH)/Span 80-Tween 80/醛基化葡聚糖(Dex-CHO)微乳液的优化体系,确定当体系复配乳化剂(Tween 80)/(Span 80)=0.10,HLB值为5.27,水油相体积比为1/6时获得的葡聚糖凝胶微球具有较好的分散性和稳定性;相对于机械搅拌乳化,超声波乳化方式可使葡聚糖水凝胶微球的粒径实现由微米级向纳米级的跨度,且随着水相与表面活性剂的摩尔比0增加,微球粒径呈现增大趋势。微乳液体系的影响因素较多,对其进行系统研究较复杂,仍需要广大学者不断进行探索和改进。
[1] LIU Y,CHAN-PARK M B. A biomimetic hydrogel based on methacrylated dextran-graft-lysine and gelatin for 3D smooth muscle cell culture[J]. Biomaterials,2010,31(6):1158-1170.
[2] NGUYEN K,DANG P N,AISBERG E. Functionalized,biodegradable hydrogels for control over sustained and localized siRNA delivery to incorporated and surrounding cells[J]. Actabiomaterialia,2013,9(1):4487-4495.
[3] SUN G,SHEN Y I,KUSUMA S,et al. Functional neovascularization of biodegradable dextran hydrogels with multiple angiogenic growth factors[J]. Biomaterials,2011,32(1):95-106.
[4] RIBEIRO M P,MORDAGO P I,MIGUEL S P,et al. Dextran-based hydrogel containing chitosan microparticles loaded with growth factors to be used in wound healing[J]. Materials Science and Engineering:C,2013,33(5):2958-2966.
[5] NAKABAYASHI K,AMEMIYA F,FUCHIGAMI T,et al. Highly clear and transparent nanoemulsion preparation under surfactant-free conditions using tandem acoustic emulsification[J]. Chemical Communications,2011,47(20):5765-5767.
[6] HAMZAH M Y,ISA N M,NAPIA L M A. Preparation and characterization of polyethylene glycol diacrylatemicrogels using electron beam radiation[C]//AIP Conference Proceedings,2014:141-144.
[7] MARIA A C,STEFANIA C,SETTIMIO P,et al. Dextran-based hydrogel microspheres obtained in w/o emulsion:preparation,characterisation andstudies[J]. Journal of Microencapsulation,2014,31(5):440-7.
[8] KABANOV A V,VINOGRADOY S V. Nanogels as pharmaceutical carriers:finite networks of infinite capabilities[J]. Angewandte Chemie International Edition,2008,48(48):5418-29.
[9] 张稳,韩晓东,苏红莹,等. 反相微乳液法制备纳米凝胶的研究进展[J]. 高分子材料科学与工程,2016,32(9):178-183.
ZHANG Wen,HAN Xiaodong,SU Hongying,et al. Progress in synthesis of nanogels by inverse microemulsion[J]. Polymeric Materials Science and Engineering,2016,32(9):178-183.
[10] MA X,CHEN Y,QIAN J,et al. Controllable synthesis of spherical hydroxyapatite nanoparticles using inverse microemulsion method[J]. Materials Chemistry and Physics,2016,183:220-229.
[11] WU X,YU G,LUO C,et al. Synthesis and evaluation of a nanoglobular dendrimer 5-aminosalicylic acid conjugate with a hydrolysable Schiff base spacer for treating retinal degeneration[J]. ACS Nano,2014,8(1):153-161.
[12] SHAH P,BHALODIA D,SHELAT P. Nanoemulsion:a pharmaceutical review[J]. Systematic Reviews in Pharmacy,2010,1(1):24-32.
[13] 王军. 乳化与微乳化技术[M]. 北京:化学工业出版社,2012:53-72.
WANG Jun. Emulsification and microemulsion technology[M]. Beijing:Chemical Industry Press,2012:53-72.
[14] SU H Y,JIA Q M,SHAN S Y. Synthesis and characterization of Schiff base contained dextran microgels in water-in-oil inverse microemulsion[J]. Carbohydrate Polymers,2016,152:156-162.
[15] 谭雪梅,万涛,胡俊燕,等. 聚合物智能纳米凝胶的反相微乳液聚合法合成与性能[J]. 高分子材料科学与工程,2014,30(5):20-24.
TAN X M,WAN T,HU J Y,et al. Synthesis and performance of polymeric intelligent nanogels prepared by inverse microemulsion polymerization[J]. Polymeric Materials Science & Engineering,2014,30(5):20-24.
[16] CHENG G,MI L,CAO Z,et al. Functionalizable and ultrastable zwitterionicnanogels[J]. Langmuir the ACS Journal of Surfaces & Colloids,2010,26(10):6883-6886.
[17] ESQUENA J,SOLANS C. Influence of the HLB parameter of nonionic surfactants on normal and reversed-phase thin layer chromatography[J]. Colloids & Surfaces A Physicochemical & Engineering Aspects,2001,189(1-3):85-92.
[18] KRISTER H,BO J,BENGT K,et al. Surfactants and polymers in aqueous solution[M].2nd ed. New York:John Wiley & Sons,Ltd.,2003.
[19] El-DIN M R N,KHAMIS E A. Corrosion inhibition efficiency,electrochemical and quantum chemical studies of some new nonionic surfactants for carbon steel in acidic media[J]. Journal of Surfactants and Detergents,2014,17(4):795-805.
[20] KITTIPOOMWONG P,NARASINGH M. Emulsification of water and pyrolysis oil[J]. Energy Procedia,2015,79:752-758.
[21] KOBAYASHI D,HIWATASHI R,ASAKURA Y,et al. Effects of operational conditions on preparation of oil in water emulsion using ultrasound[J]. Physics Procedia,2015,70:1043-1047.
[22] CARVER M T,CANDAU F,FITCH R M. Effect of solution components on the termination mechanism in acrylamide microemulsion polymerizations[J]. Journal of Polymer Science Part A:Polymer Chemistry,1989,27(7):2179-2188.
[23] ZARUR A J,YING J Y. Reverse microemulsion synthesis of nanostructured complex oxides for catalytic combustion[J]. Nature,2000,403(6765):65-67.
[24] QIU S,DONG J,CHEN G. Preparation of Cu nanoparticles from water-in-oil microemulsions[J]. Journal of Colloid & Interface Science,1999,216(2):230-234.
[25] SCHULMAN J H,STOECKENIUS W,PRINCE L M. Mechanism of formation and structure of micro emulsions by electron microscopy[J]. Journal of Physical Chemistry,1958,63(10):1677-1680.
[26] ZARUR A J,YING J Y. Reverse microemulsion synthesis of nanostructured complex oxides for catalytic combustion[J]. Nature,2000,403(6765):65-67.
Synthesis and size control of dextran hydrogel microparticles using the inverse microemulsion technique
ZHANG Wen,HAN Xiaodong,YU Kun,SU Hongying,JIA Qingming,SHAN Shaoyun
(Department of Chemical Engineering,Kunming University of Science and Technology,Kunming 650500, Yunnan,China)
Hydrogel microparticles(microgel)based on natural polymers have been widely used as biomaterials due to their excellent biocompatibility. In this study,a series of dextran microgel were prepared using the inverse microemulsion technique. And,effects of the HLB value,emulsification method,volume ratio of water to oil(),molar ratio of water to emulsifier(0)on the morphology,and particle size of the dextran microgel were investigated. The results indicated that dextran microgels with particle size from 400nm to 70μm could be prepared with the CYH/Span 80-Tween 80/Dex-CHO emulsion system. Microgels prepared under ultrasonic had smaller particle size than that prepared under mechanical agitation. Dextran microgel with relatively small diameter at ~422nm was obtained with(Tween 80)/(Span 80)=0.10,HLB=5.27,=1/6. In addition,the particle size of the dextran microgel increased with the increase of the0value.The dextran hydrogel microparticles based on the natural dextran with controllable particle size can be used as promising carrier materials for biomedical applications.
dextran;hydrogel microparticles;inverse microemulsion;particle size control
TQ314.255
A
1000–6613(2017)10–3807–08
10.16085/j.issn.1000-6613.2017-0256
2017-02-22;
2017-04-20。
国家自然科学基金(51503090)及昆明理工大学自然科学基金(14118713)项目。
张稳(1989—),女,硕士研究生。E-mail:1076546068 @qq.com。
苏红莹,博士,讲师,从事纳米生物材料研究。E-mail:hongyingsu@kmust.edu.cn。
