溶剂萃取-树脂吸附联合脱除盐湖老卤中的微量硼
2017-10-20王雄刘明言宋军超
王雄,刘明言,宋军超
溶剂萃取-树脂吸附联合脱除盐湖老卤中的微量硼
王雄1,刘明言1,2,宋军超1
(1天津大学化工学院,天津化学化工协同创新中心(天津),天津 300350;2化学工程联合国家重点实验室(天津大学),天津 300350)
采用溶剂萃取-树脂吸附联合的方法对青海盐湖卤水中的硼进行了提取和脱除。研究了pH、相比和萃取级数对萃取过程的影响,讨论了萃取后卤水的pH和树脂用量等对吸附过程的影响,考察了D564树脂的吸附等温线和吸附动力学特性,并对反萃和洗脱过程进行了优化。研究结果表明:萃取过程中卤水pH为2时,萃取效果最佳,相比和萃取级数增加至3后继续增加相比和萃取级数对进一步降低卤水中硼浓度的作用并不明显;吸附过程中卤水的pH最佳值为7,吸附动力学数据符合准二级动力学模型,吸附等温线数据符合Langmuir等温吸附模型;当树脂用量为6g/(100mL卤水)时,可直接将一级萃取后卤水中的硼浓度降低至1.0mg/L以下;建议使用0.1mol/L的NaOH溶液作反萃剂,0.5mol/L的HCl溶液作洗脱剂。
溶剂萃取;吸附;硼酸;盐湖卤水
硼及其化合物由于其特殊的物理化学性能而成为轻工、冶金、机械和医药等工业领域的重要原料,具有“工业味精”的美誉[1]。我国盐湖卤水中富含钾、钠、镁、锂、硼等多种元素,具有巨大的经济利用价值。盐湖卤水在提钾后浓缩酸化沉硼,使大部分硼元素以硼酸形式析出,余下的低硼高镁锂卤水溶液(简称老卤)可用于生产氯化镁、氢氧化镁和碳酸镁等产品。但是,老卤中剩余的硼浓度如果仍然较高(如1mg/L以上),将会显著影响后续碳酸锂等产品的质量[2]。因此,如果采用适当的提硼方法,进一步降低老卤中的硼浓度,使之达到1mg/L以下,不仅可以提高后续锂镁等产品的质量,而且对盐湖资源的综合利用也具有十分重要的 意义。
目前用于卤水提硼的方法主要有酸化法、溶剂萃取法和吸附法等。酸化法[3]通过卤水中的硼与盐酸或硫酸等的反应,生成硼酸,利用硼酸在饱和盐溶液中溶解度低的特点使其结晶析出,从而实现硼和卤水中其他成分的分离。这种方法具有操作简单、设备投资小的优点,但是对硼的分离效率低且消耗较大量的酸。溶剂萃取法通常采用一元醇、二元醇和混合醇等为萃取剂[4],利用醇和硼酸会发生酯化反应的特点,将硼萃取到萃取剂有机相中,以达到和水相其他成分分离的目的。研究表明,异辛醇[5]、2-乙基-1,3己二醇[6]、2,2,5-三甲基-1,3-己二 醇[7]以及一元醇和二元醇等组成的混合醇萃取 剂[8]均对硼具有较好的萃取效果。吸附法因操作简单、易于设计、成本较低等优点,而被广泛应用于低品位海水和卤水中硼的提取和分离。常用的硼吸附剂有:无机矿物和黏土[9]、有机-无机杂化材料[10]以及含功能基团的硼特效树脂等[11-14]。其中,硼特效树脂因其再生简单、机械强度高和对硼有高选择性等特点更加适合在盐湖卤水中的实际应用。LIU等[11]和肖湘等[12]分别考察了D564树脂在硼酸溶液和盐湖卤水中对硼的吸附性能,结果表明,该树脂对硼有较好的吸附性能和循环稳定性。萃取法和吸附法在硼的提取分离方面具有广阔的应用前景,但是,萃取法一般适用于硼浓度较高体系中硼的提取,而不适用于除去溶液中的低浓度或微量的 硼[15]。硼选择性树脂[11-14]对硼的吸附容量较低,更适用于对低浓度硼的分离。单一的萃取法和吸附法都难以有效地将老卤中的较低浓度的硼降低到1mg/L以下,但是,将萃取法和吸附法加以联合使用,则可以使两种方法的优势得到互补,用于盐湖老卤中硼元素的深度提取。因此,刘明言等[16]发明了盐湖老卤中硼元素的溶剂萃取-树脂吸附联合提取新方法。
本文针对青海盐湖资源的特点,采用溶剂萃 取-树脂吸附联合提取方法,对盐湖老卤中的硼元素进行了深度提取研究。首先采用正癸醇、磷酸三丁酯、异辛醇、2-乙基-1,3己二醇和航空煤油等组成萃取剂,考察了pH、相比、萃取级数等对硼萃取过程的影响以及NaOH溶液浓度对反萃过程的影响;之后,采用D564树脂对萃取后的老卤进一步进行吸附分离研究,探讨了老卤的pH和树脂用量等因素对吸附过程的影响,研究了硼的吸附等温线和吸附动力学特性,并对树脂的洗脱过程进行了研究。研究结果可以为溶剂萃取-树脂吸附联合提硼新方法的工业应用提供基础指导。
1 实验材料和方法
1.1 实验材料
实验所用原料是盐湖卤水浓缩酸化沉硼后的卤水,即盐湖老卤,由青海中信国安科技发展有限公司提供,其部分化学组成和性质如表1所示。萃取剂由正癸醇、磷酸三丁酯、异辛醇、2-乙基-1,3己二醇和航空煤油组成,其中航空煤油为工业级,其他试剂为分析纯。所用盐酸、氢氧化钠、甘露醇、硼酸、甲亚胺-H、柠檬酸、冰乙酸和乙酸铵等试剂为分析纯。所用D564树脂购置于郑州勤实科技有限公司。
1.2 实验及数据处理和分析方法
1.2.1 溶剂萃取及反萃实验
(1)萃取剂组成 将一元醇正癸醇和异辛醇、二元醇2-乙基-1,3-己二醇,以及磷酸三丁酯和稀释剂航空煤油按照典型体积比30∶13∶5∶2∶50混合配制成萃取剂储存于广口瓶中备用。
(2)硼的萃取及反萃 用NaOH溶液调节老卤的pH到给定值,按照实验所需老卤和萃取剂的相比(3∶4、1∶1、1∶2、1∶3、1∶4)量取盐湖老卤和萃取剂于烧杯中。采用机械搅拌的方法,在室温下搅拌20min后,将混合液移入分液漏斗静置分层。取下层水相,测量其中硼的浓度。通过物料衡算可计算出萃取相中硼的浓度。硼萃取的分配系数为在给定温度下,硼在萃取相中的浓度与在萃余相中的浓度之比,如式(1)。

表1 盐湖老卤的化学组成和物性
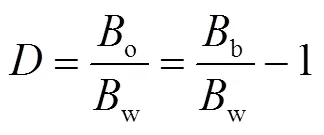
萃取率是硼在萃取相的含量与硼的总含量之比,如式(2)。
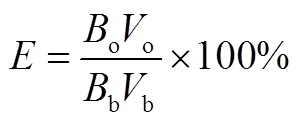
硼酸酯能在碱性条件下有效地水解,因此本文采用不同浓度的NaOH溶液作为反萃剂。按照相比1∶3称取萃取相与NaOH溶液于烧杯中,机械搅拌30min后将混合液移入分液漏斗中,静置一段时间后取下层水相,测量其中硼的含量。反萃取率为 反萃剂中硼的含量与萃取相中硼的含量之比, 如式(3)。
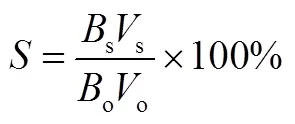
1.2.2 树脂吸附与洗脱实验
(1)树脂预处理 树脂的预处理依据国标规定的方法进行[17]。称取50g树脂,用去离子水浸泡24h,洗去树脂内的杂质。然后,移入8倍树脂体积的1mol/L盐酸溶液中,磁力搅拌30min,再用去离子水洗涤至中性。再移入8倍树脂体积的1mol/L氢氧化钠溶液中,磁力搅拌30min,用去离子水洗涤至中性。重复以上步骤3次后将树脂储存于蒸馏水中备用。
(2)pH对吸附的影响 用0.1mol/L的NaOH溶液和HCl溶液调节原始酸度下单级萃取后卤水的pH范围为1~7;称取0.1g树脂与10mL卤水于离心管中,置于摇床上,在室温下振荡12h,后取上层卤水测定硼含量,硼的吸附率按式(4)计算。
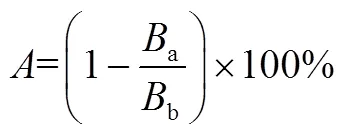
(3)树脂用量对吸附的影响 用0.1mol/L的NaOH溶液和HCl溶液调节原始酸度下单级萃取后的卤水和相比为3时单级萃取后卤水的pH范围为1~7;称取0.1~0.8g树脂和10mL卤水于离心管中,置于摇床上,在室温下震荡12h,后取卤水测量其中的硼含量。
(4)树脂的洗脱 用一定浓度的HCl和NaOH溶液作为洗脱剂,称取一定体积的洗脱剂与1g吸附后的树脂于烧杯中搅拌30min,然后测量上层洗脱剂清液中的硼含量。洗脱率为洗脱剂中硼的量与树脂吸附的硼的量之比,如式(5)。

(5)吸附动力学及吸附平衡实验 吸附动力学实验的测定采用间歇吸附方式,在298K温度下进行。实验采用浓度为100mg/L,pH调节为1~7的硼酸溶液100mL,置于恒温水浴锅中机械搅拌,加入2g D564树脂,并测定不同时间溶液中硼的浓度。吸附平衡实验取100mL硼浓度范围在50~300mg/L、pH为1~7的硼酸溶液于烧杯中,加入2g树脂,在298K温度下磁力搅拌12h,后测量溶液中硼的浓度。
吸附动力学采用Lagergren准一级速率方程[18]和准二级速率方程[19]进行拟合,其线性形式如式(6)、式(7)所示。吸附平衡采用Langmuir等温吸附模型[20]和Freundlich等温吸附模型[21]描述,其线性形式如式(8)、式(9)所示。
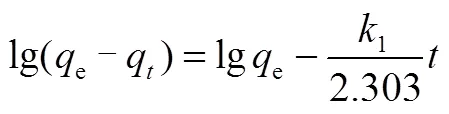
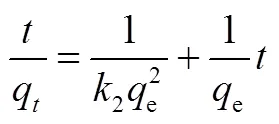

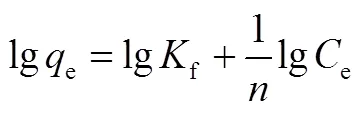
1.2.3 硼含量的测定方法
采用甘露醇-碱滴定法和甲亚胺-H酸紫外分光光度法测定溶液中的硼含量[22]。
2 结果与讨论
2.1 溶剂萃取和反萃过程
2.1.1 溶剂萃取过程
(1)卤水pH对萃取效果的影响 实验测得了不同初始pH条件下,萃取剂对卤水中硼的萃取效果,结果如图1所示。在原老卤初始酸度的基础上,逐渐增加溶液的pH,分配系数先是平缓地增加, 在pH为2时,达到最大值61.05,此时萃取剂对硼的萃取率为98.38%;当pH大于2以后,分配系数急剧下降,在pH为5时,分配系数已处于较低的水平,此时萃取剂对硼的萃取率为68.4%。由此 可以看出,较低的pH更利于萃取剂对硼酸的萃取,而较高的pH则会抑制萃取剂的萃取效果。这与不同pH溶液中硼的存在形式有关。硼在溶液中的存在形式主要受硼浓度和溶液pH的影响。本实验中所用的盐湖老卤中的硼浓度较高,在较低的pH下,卤水中的硼主要以中性分子B(OH)3的形式存在,而随着溶液pH的增加,一部分B(OH)3会转换为B(OH)4–、B3O3(OH)4–、B4O5(OH)42–和B5O6(OH)4–等形式[23]。而醇类萃取剂萃取硼酸的本质是依靠醇与中性的B(OH)3发生络合反应,因此卤水pH升高会导致中性B(OH)3所占比例减少,不利于萃取过程的进行[6, 24]。
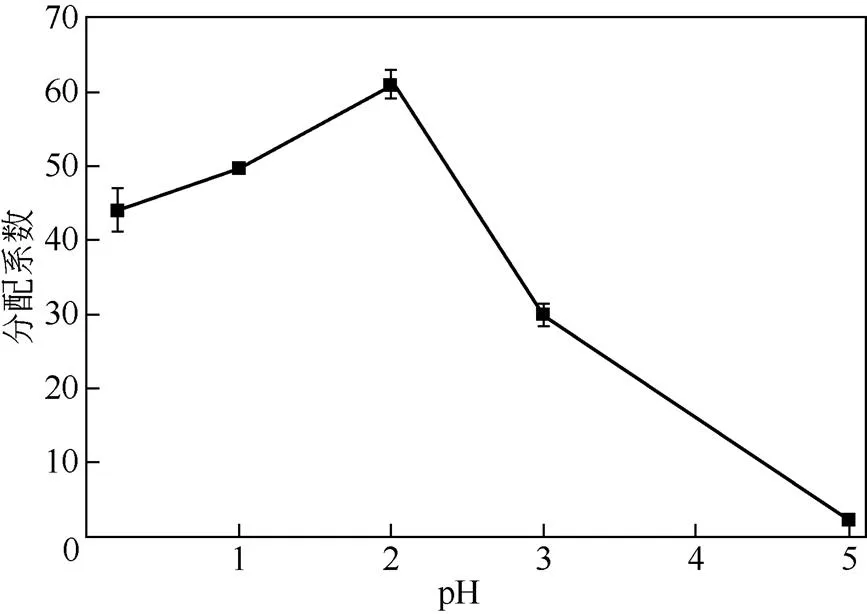
图1 卤水pH对分配系数的影响
(2)相比对萃取结果的影响 萃取时有机相和水相的体积比(O/A)称为相比,工业上称为流比。相比是影响萃取剂萃取效率的又一重要因素。本实验考察了在老卤原始酸度下,相比分别为3∶4、1∶1、2∶1、3∶1、4∶1时,萃取剂对硼的萃取效果,结果如图2所示。随着相比O/A的增加,硼的萃取率呈增加的趋势,在相比为4时,萃取率达到最大值99.04%。但在相比增大到2以后,萃取率的增加趋势变得平缓。相比为3时卤水中剩余硼浓度为28mg/L,此时硼浓度不会随着相比的增加而进一步明显降低。增加相比虽然一定程度上增加了萃取剂对硼的萃取效率,但同时也增加了萃取过程中萃取剂的用量,造成萃取剂成本变高,还会导致后续的反萃过程成本的相应增加,且增加相比无法有效地将硼的浓度进一步降低。
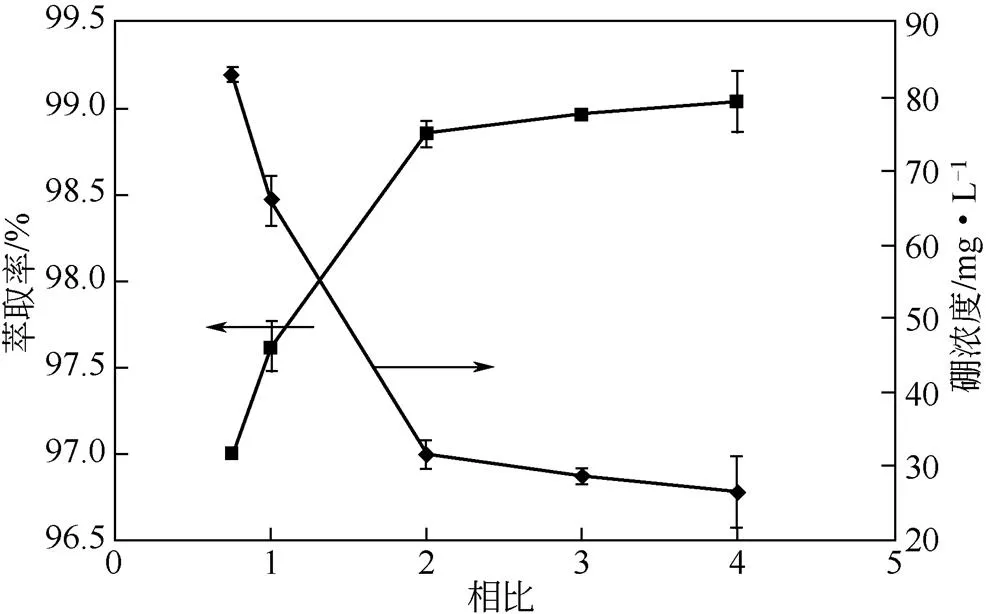
图2 相比对萃取率及硼浓度的影响
(3)萃取级数对萃取结果的影响 一般情况下,一级萃取通常不能达到充分的分离、提纯和富集的目的,需对盐湖卤水进行多级萃取,以提高萃取分离的效果。因此,本研究在相比为1,老卤在原始酸度条件下进行了多级错流萃取实验,结果如图3所示。由图3可以看出,随着萃取级数的增加,萃余相中硼的浓度逐渐减小,累积的萃取率逐渐增大。在三级萃取后,硼浓度的降低趋势和萃取率增加趋势明显减小。经三级萃取,萃余相中硼浓度降低到大约25mg/L,在此基础上进一步增加萃取级数不能有效降低硼浓度并会导致萃取剂用量的增加。但是,为了保证卤水后续碳酸锂等产品的质量,应采取其他分离方法进一步降低卤水中硼的浓度至1.0mg/L。
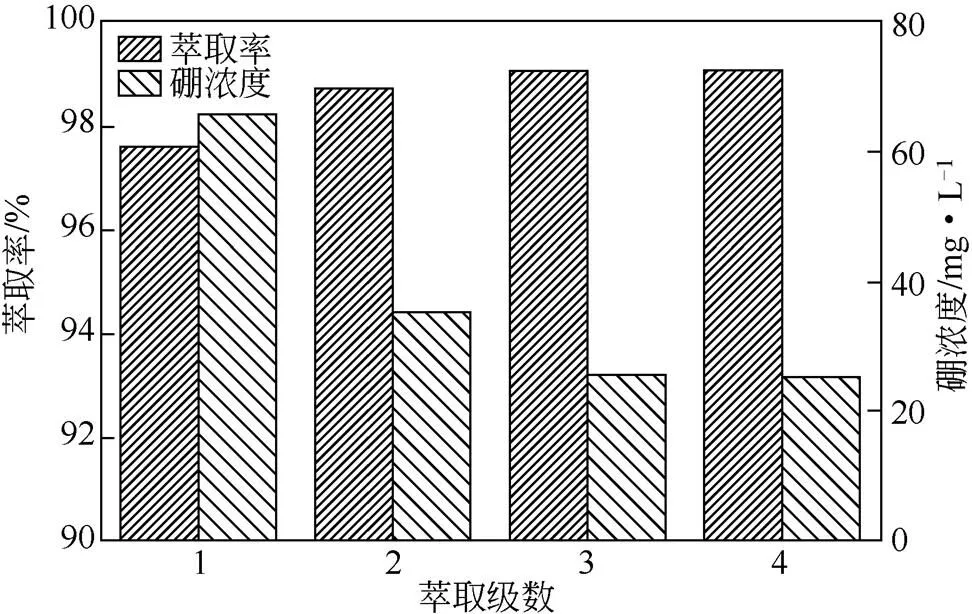
图3 不同萃取级数下萃取率及萃余相中硼的浓度
(4)对萃取过程中萃取剂的溶解损失及锂的损失的考察 为进一步评价萃取剂的应用性能,考察了萃取剂在水中的溶解损失以及萃取过程中锂的损失。萃取剂的溶解损失实验采用蒸馏水代替盐湖老卤,与萃取剂按体积比1∶1混合后,机械搅拌20min,后测量水相中水的含量。锂的损失通过测量一级萃取前后盐湖老卤中锂的浓度获得。结果表明,水相中水的含量约为99.3%,折算成萃取剂的溶解损失为0.8%,锂元素在一级萃取后的损失约为3.5%。
2.1.2 反萃
(1)NaOH浓度对反萃结果的影响 图4所示为不同浓度的NaOH溶液对萃取有机相中硼的反萃效果。从图4可以看出,硼的反萃取率随着NaOH浓度的增加而增加,并在NaOH浓度为0.2mol/L时达到92.12%,但继续增加NaOH的浓度,反萃率基本保持不变。此外,在反萃过程中当NaOH的浓度大于0.1mol/L后,反萃过程的乳化现象变得较为明显。所以,为了避免出现乳化现象,影响反萃操作的正常进行,选取浓度为0.1mol/L的NaOH溶液作为反萃剂较为适宜。在反萃的过程中,萃取剂中的表面活性物质、固体微粒和水相的酸碱度都可能诱发乳化的产生。本实验中使用的盐湖老卤中含有大量的Mg2+,在萃取的过程中部分Mg2+可能进入了有机相中,而随着反萃剂碱性的增强,Mg2+与NaOH反应生成Mg(OH)2颗粒,从而诱发了乳化现象的 产生。
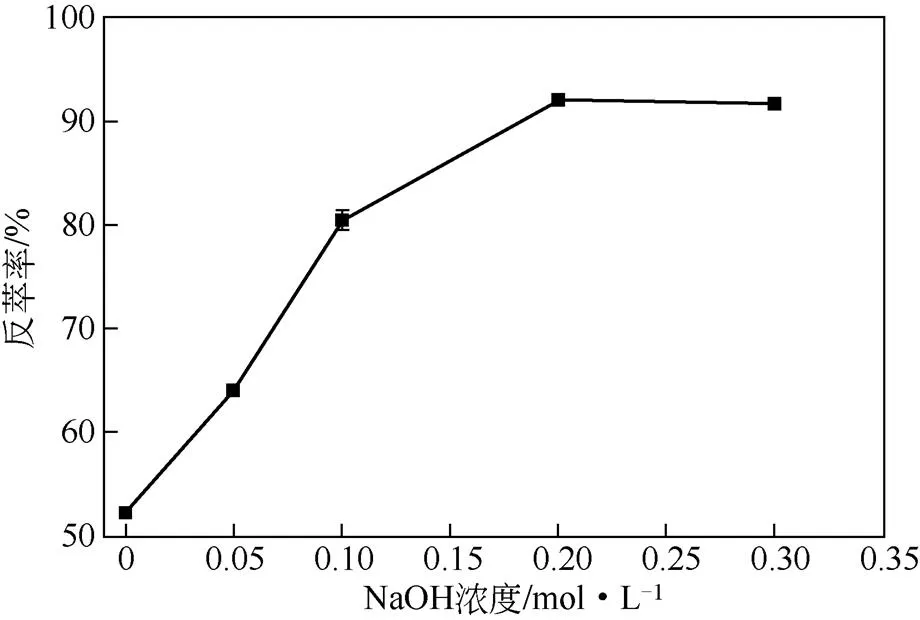
图4 NaOH浓度对反萃率的影响
(2)反萃级数对反萃结果的影响 在相比(O/A)为1∶3,并且NaOH水溶液的浓度为0.1mol/L的条件下,对萃取相进行多级错流反萃,结果如图5所示。当反萃级数为2时,累积反萃率达到99.02%。当反萃级数为3时,累积反萃率已接近100%。
2.2 树脂吸附与洗脱
为将卤水中硼的浓度进一步降低至1mg/L,在萃取的基础上,采用D564树脂对萃取后的盐湖卤水中的硼进行吸附分离。
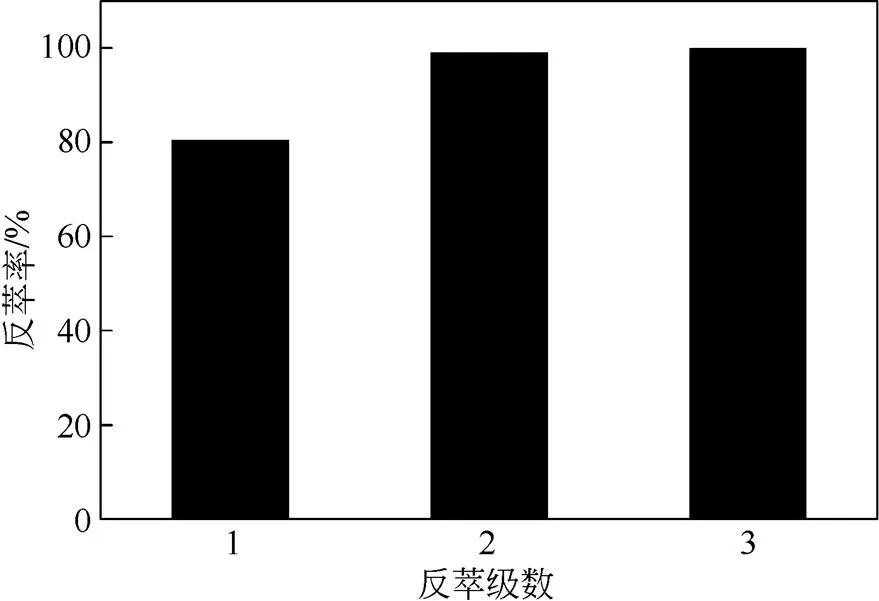
图5 不同级数下累积反萃取率
2.2.1 树脂吸附
(1)卤水pH对吸附过程的影响 溶液pH对吸附剂的吸附效果影响较大,是吸附过程优化的重要参数。因为实验中所用卤水中含有大量的Mg2+,碱性条件下会生成Mg(OH)2沉淀,所以本实验中只调节卤水的pH在1.0~7.0范围内,考察pH对硼吸附结果的影响,结果如图6所示。从图6可以看出,树脂对硼吸附率随着溶液pH的增加而增加,说明增加溶液pH有利于D564树脂对硼的吸附。这与不同pH下硼在溶液中的存在形式不同有关。研究表明,当溶液中的硼酸浓度低于0.025mol/L时,硼酸分子之间不发生聚合,硼只以B(OH)3和B(OH)4–两种形式存在,每种形式所占比例由溶液pH决定。硼酸的解离常数pa为9.24,当溶液pH低于这一值时,硼主要以B(OH)3形式存在;随着pH的升高,B(OH)4–的含量会相应增加[25]。D564树脂中的官能团是典型的顺位二醇结构,这种结构对B(OH)4–的亲和性要高于B(OH)3[11, 26],所以随着pH的升高,卤水中B(OH)4–浓度增加,并与树脂的二醇结构反应生成稳定的络合物,树脂对硼的吸附量也相应增加。因此,调节萃取后卤水的pH为7,将更有利于后续的吸附过程。
(2)树脂用量对吸附过程的影响 如前文所述,在萃取过程中,相比为3时卤水中的硼浓度降低为28mg/L,当萃取级数为3时,卤水中硼浓度降低为25mg/L,在此基础上继续增加相比和萃取级数硼浓度几乎保持不变。因为相比和萃取级数都为3条件下,卤水中硼剩余浓度接近,因此,本文仅考察了硼剩余浓度分别为65mg/L(相比为1时一级萃取后的盐湖老卤)和28mg/L(相比为3时一级萃取后的盐湖老卤)时,树脂用量对硼去除效果的影响,结果如图7所示。在不同硼初始浓度下,硼浓度随着树脂用量的增加呈下降的趋势,且当树脂用量小于或等于2g/(100mL卤水)时,下降迅速,之后下降趋势变得平缓。当树脂用量为6g/(100mL卤水)时,盐湖卤水中硼浓度分别由65mg/L和28mg/L下降为0.91mg/L和0.86mg/L,而继续增加树脂用量,硼浓度的下降便不再明显。因此,综合考虑萃取阶段萃取剂的消耗量和吸附阶段树脂的消耗量,直接对一级萃取后的盐湖老卤采取适当用量的树脂吸附较为适宜。
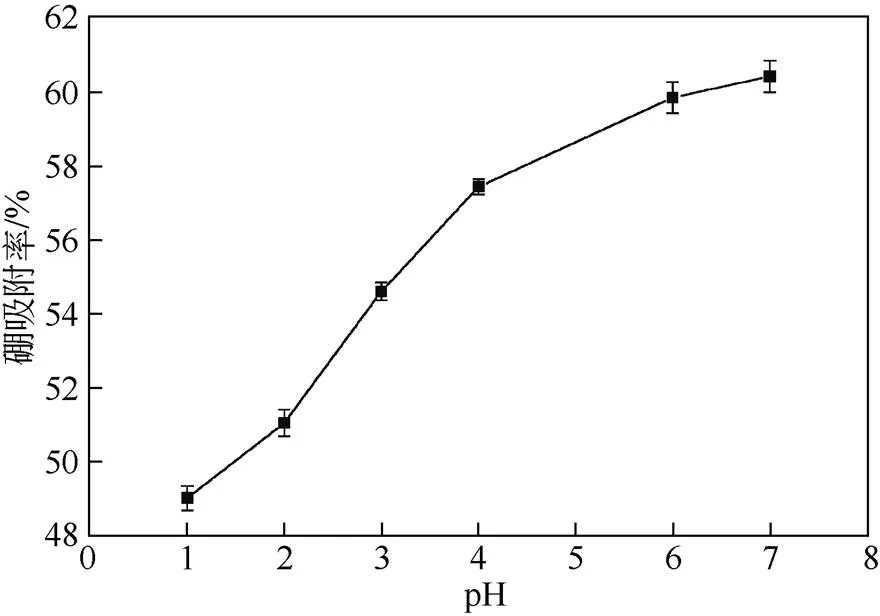
图6 pH对树脂吸附过程的影响
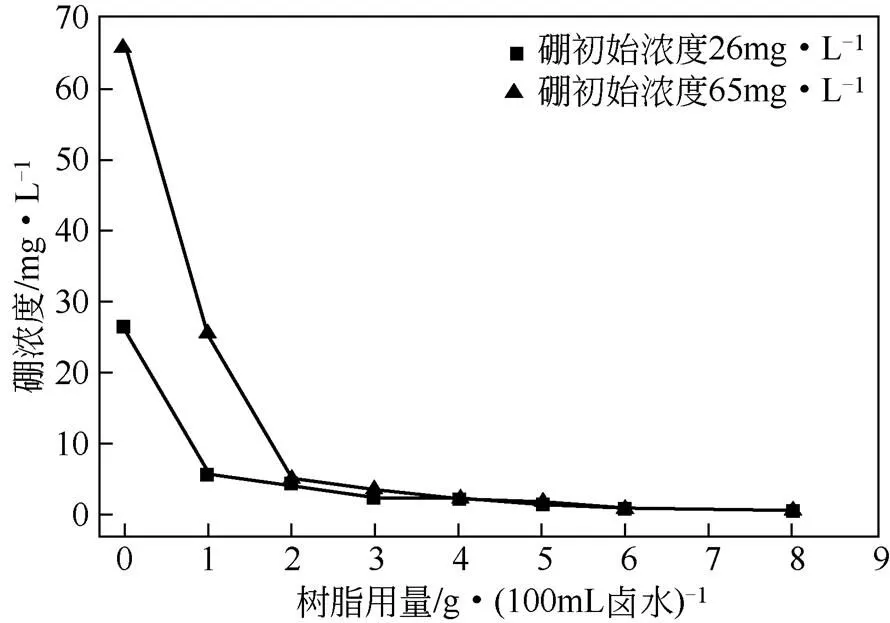
图7 不同硼初始浓度下树脂用量对吸附效果的影响
(3)树脂的吸附动力学及吸附等温线 吸附接触时间对树脂吸附量的影响如图8所示,在吸附的初始阶段树脂的吸附量随着吸附时间的增长而迅速增加,但随着时间的继续增长,吸附量增加的趋势变得平缓,当时间超过10h后,吸附量基本上不再发生改变,即吸附已达到了平衡。为了进一步研究树脂吸附硼的动力学过程,分别采用Lagergren准一级动力学方程和准二级动力学方程对动力学吸附数据进行了拟合,拟合结果和由模型计算得到的相关参数如图8和表2所示。在这两种吸附动力学模型中,准二级动力学模型对实验数据的拟合程度更好(2>0.999),说明吸附的速率控制步骤可能是化学吸附。而准一级动力学模型得到的相关系数2为0.923。由准二级速率方程得到的理论平衡吸附量为5.26mg/g,这与实验值也更加接近。LIU等[11]的研究也表明D564树脂对硼的吸附动力学更加符合准二级动力学方程。
不同硼初始浓度(100~300mg/L)下吸附剂对硼的吸附量如图9所示。随着硼初始浓度的升高,吸附剂对硼的吸附容量逐渐增加;当硼初始浓度增加到200mg/L后,曲线的走势偏于平坦,即吸附已接近饱和。为了进一步确定吸附等温线的类型,分别采用Langmuir吸附等温线方程和Freundlich吸附等温线方程,对吸附平衡实验数据进行拟合,拟合结果和由方程计算得到的相关参数如图9和表3所示。其中,Langmuir方程得到树脂对硼的最大吸附量0为8.06mg/g,而实验中得到的树脂对硼的平衡吸附量为7.92mg/g,二者非常接近。由Freundlich 方程得到参数和f的值分别为8.33和4.47。在整个研究的浓度范围内,Langmuir方程对实验数据拟合结果的相关性(2=0.999)要明显好于Freundlich方程(2=0.791)。因此,D564树脂对硼的吸附平衡行为更符合Langmuir等温吸附模型,也表明该吸附过程与单分子层吸附相一致。此外根据文献报道,D564树脂对硼的吸附等温线为H2型,表明该吸附过程为化学吸附[11]。
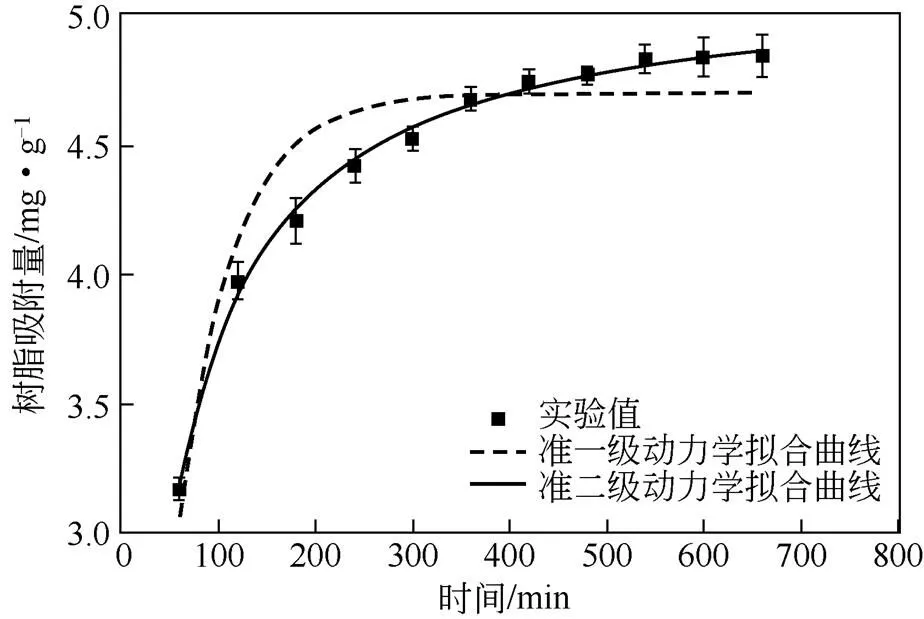
图8 D564树脂吸附动力学及拟合结果
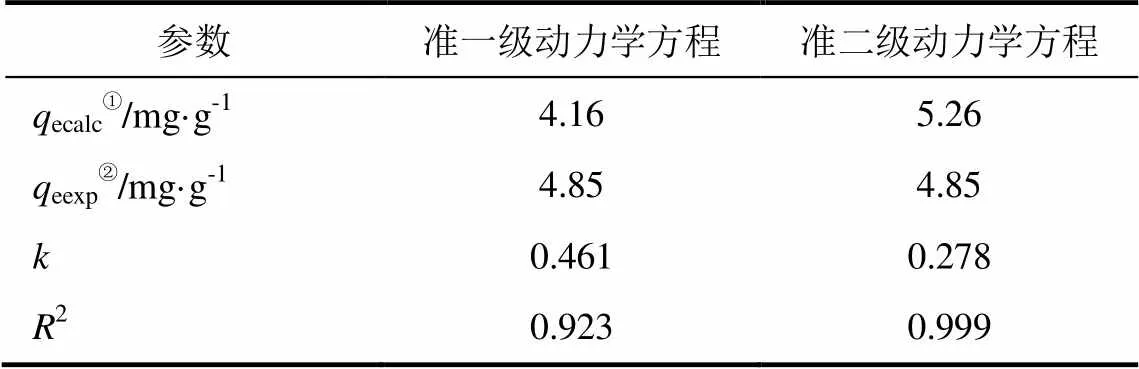
表2 D564树脂的准一级、准二级动力学方程参数值
①ecalc为饱和吸附容量的计算值;②eexp为饱和吸附容量的实验值。
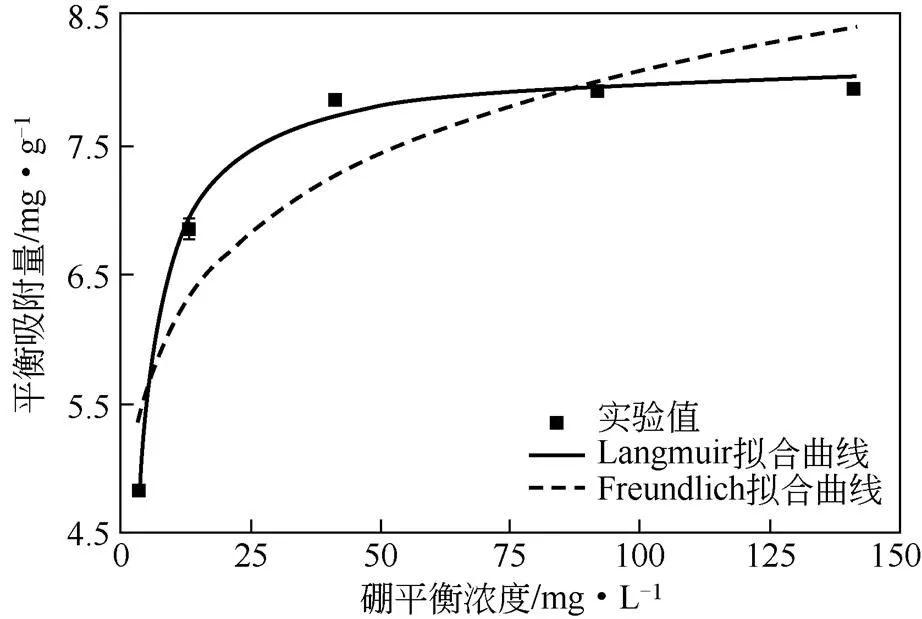
图9 硼的D564树脂吸附等温线及拟合结果
2.2.2 洗脱
对吸附后的D564树脂分别采用HCl和NaOH溶液进行洗脱。实验表明,0.5mol/L的HCl溶液对D564树脂的洗脱效果较理想。将不同体积的浓度为0.5mol/L的HCl溶液与1g吸附后的D564树脂置于烧杯中,于室温下搅拌30min后测量溶液中的硼浓度,得到洗脱剂体积对硼洗脱率的影响,结果如图10所示。从图10可以看出,随着HCl溶液体积的增加,洗脱率呈上升趋势,当HCl的体积为50mL时,洗脱已接近完全。作为对比,使用50mL 0.5mol/L的NaOH溶液对1g吸附后D564树脂进行洗脱,发现其洗脱率仅为14.43%。
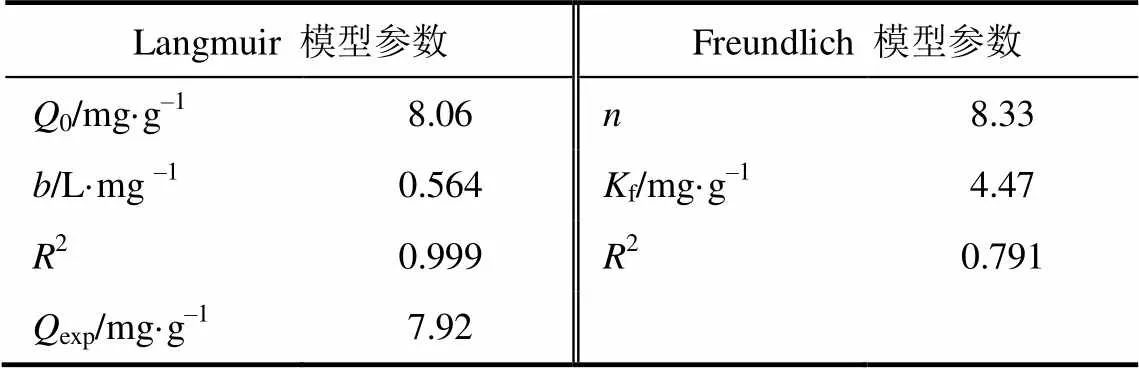
表3 硼的D564树脂吸附等温线方程参数
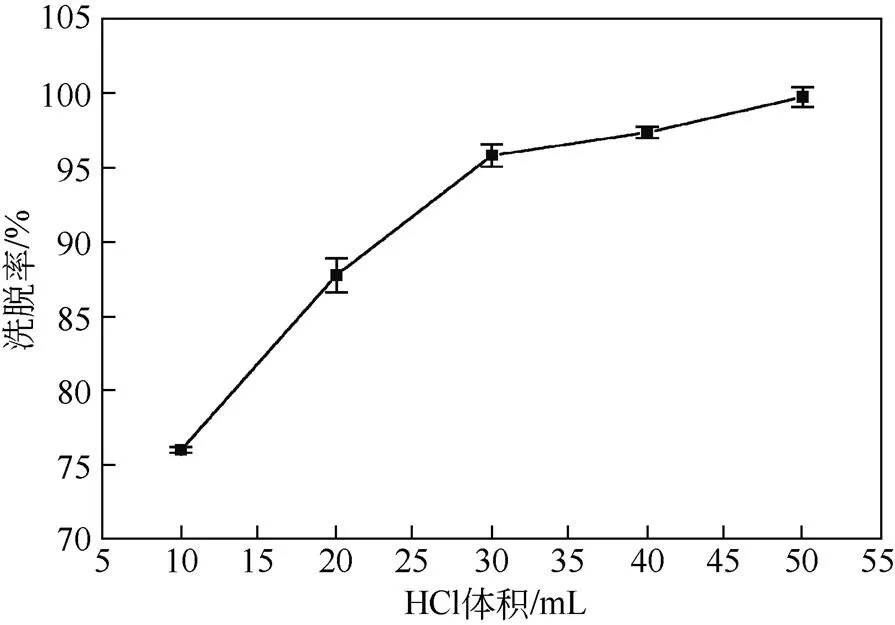
图10 浓度为0.5mol/L HCl溶液体积对D564树脂中硼的洗脱率影响
3 结论
(1)卤水pH、相比、萃取级数对萃取过程影响的研究表明,pH为2时萃取剂对硼的萃取效果最好,单级萃取率为98.38%,当卤水中硼浓度较低时,继续增加相比和萃取级数对降低硼浓度的效果不明显。一级萃取造成的萃取剂溶解损失为0.8%,卤水中锂的损失为3.5%。NaOH溶液可作为反萃剂对萃取相进行反萃,NaOH的适宜浓度为0.1mol/L,经三级反萃硼的反萃率接近100%。
(2)D564树脂对卤水中硼的吸附性能较好,吸附量随着卤水pH的增加而增加。吸附动力学及吸附等温线符合准二级动力学模型和Langmuir等温吸附模型。D564树脂的洗脱性能良好,吸附后树脂经浓度为0.5mol/L的HCl溶液洗脱后,洗脱率可达99.8%。
(3)采用溶剂萃取-树脂吸附联合新工艺,对单级溶剂萃取后的卤水中的硼采用D564树脂吸附,当卤水pH为7,树脂用量为6g/(100mL卤水)时,可将卤水中的硼含量降低到1mg/L以下,有利于提高后续碳酸锂等产品的生产质量。
需要指出的是,对于降低萃取剂在萃取过程中的溶解损失以及萃取-吸附联合方法的连续操作的设计和优化等,有待进一步深入研究。
符号说明

A——吸附率,% Ba——吸附后卤水中硼浓度,mg·L–1 Bb——卤水中硼的初始浓度,mg·L–1 Be——洗脱剂中硼浓度,mg·L–1 Bo——萃取相中硼的浓度,mg·L–1 Bs——反萃剂中硼的浓度,mg·L–1 Bw——萃余相中硼的浓度,mg·L–1 b——Langmuir平衡常数 Ce——平衡时溶液中硼浓度,mg·L–1 D——分配系数 E——萃取率,% Kf——相对吸附能力,mg·g–1 k1——准一级速率常数,h–1 k2——准二级速率常数,g·mg-1·h–1 m——吸附的硼质量,mg n——吸附过程强度 Q0——最大吸附容量,mg·g–1 qe——平衡吸附量,mg·g–1 qt——t时刻吸附量,mg·g–1 R——洗脱率,% S——反萃率,% t——时间,h Vb——卤水体积,L Ve——洗脱剂体积,L Vo——萃取相体积,L Vs——反萃剂体积,L
下角标

b——原始卤水 o——萃取相 s——反萃剂 w——萃余相
致谢:感谢青海中信国安科技发展有限公司对本研究工作的大力支持,感谢谢云荣等对论文提出的宝贵意见和建议。
[1] OZTURK N,KOSE T.Boron removal from aqueous solutions by ion-exchange resin:batch studies[J].Desalination,2008,227(1/2/3):233-240.
[2] YAN C Y,YI W T,MA P H,et al.Removal of boron from refined brine by using selective ion exchange resins[J].Journal of Hazardous Materials,2008,154(1/2/3):564-571.
[3] 杨鑫,徐徽,陈白珍,等.盐湖卤水硫酸法提取硼酸的工艺研究[J].湖南师范大学自然科学学报,2008,31(1):72-77.
YANG X,XU H,CHEN B Z,et al.Study on the extraction of boric acid from salt lake brine by vitriol method[J].Journal of Natural Science of Hunan Normal University,2008,31(1):72-77.
[4] 熊妍,鲍宗必,邢华斌,等.盐湖卤水提硼萃取剂的研究进展[J].化工进展,2012,31(8):1647-1655.
XIONG Y,BAO Z B,XING H B,et al.Progress in extractants for boron recovery from salt-lake brine[J].Chemical Industry and Engineering Progress,2012,31(8):1647-1655.
[5] 赵先银,郭志栋,唐平洋.异辛醇从油田卤水中萃取提硼[J].化工矿物与加工,2015,44(6):16-19.
ZHAO X Y,GUO Z D,TANG P Y.Extraction of boron in oilfield brine by iso-octyl alcohol[J].Industrial Minerals & Processing,2015,44(6):16-19.
[6] 熊妍,鲍宗必,邢华斌,等.1,3-二元脂肪醇萃取硼酸的平衡特性[J].化工学报,2012,63(11):3546-3552.
XIONG Y,BAO Z B,XING H B,et al.Equilibrium behavior of boric acid extracted by aliphatic 1,3-diols[J].CIESC Journal,2012,63(11):3546-3552.
[7] KARAKAPLAN M,TURAL S,TURAL B,et al.The solvent extraction of boron with synthesized aliphatic 1,3-diols:stripping and extraction behavior of boron by 2,2,5-trimethyl-1,3-hexanediol [J].Solvent Extraction and Ion Exchange,2004,22(6):897-911.
[8] 肖美玲,曾英,蒋云江,等.混合醇萃取剂从盐湖老卤中提硼实验研究[J].化工矿物与加工,2013,42(11):9-13.
XIAO M L,ZENG Y,JIANG Y J,et al.Boron extraction from salt lake brine by mixed alcohols[J].Industrial Minerals & Processing,2013,42(11):9-13.
[9] GOLDBERG S,LESCH S M,SUAREZ D L.Predicting boron adsorption by soils using soil chemical parameters in the constant capacitance model[J].Soil Science Society of America Journal,2000,4(64):1356-1363.
[10] WANG L,QI T,ZHANG Y.Novel organic-inorganic hybrid mesoporous materials for boron adsorption[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2006,275(1/2/3):73-78.
[11] LIU H,YE X,LI Q,et al.Boron adsorption using a new boron- selective hybrid gel and the commercial resin D564[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2009,341(1/2/3):118-126.
[12] 肖湘,陈白珍,石西昌.D564树脂对盐湖卤水中硼的吸附[J].中南大学学报(自然科学版),2013,44(3):885-891.
XIAO X,CHEN B Z,SHI X C.Adsorption of boron from brine by D564 resin[J].Journal of Central South University(Science and Technology),2013,44(3):885-891.
[13] 张利珍,赵恒勤,谭秀民,等.D564树脂提硼试验研究[J].化工矿物与加工,2013,42(1):9-12.
ZHANG L Z,ZHAO H Q,TAN X M,et al.Experimental study on extracting boron by D564 resin[J].Industrial Minerals & Processing,2013,42(1):9-12.
[14] 何天明,陈白珍,石西昌,等.XSC-700树脂对盐湖卤水中硼的吸附[J].中南大学学报(自然科学版),2011,42(6):1538- 1542.
HE T M,CHEN B Z,SHI X C,et al.Boron adsorption from salt lake brine on XSC-700 resin[J].Journal of Central South University(Science and Technology),2011,42(6):1538-1542.
[15] SAHIN S.A mathematical relationship for the explanation of ion exchange for boron adsorption[J].Desalination,2002,143(1): 35-43.
[16] 刘明言,宋军超,徐杨书涵.采用溶剂萃取-离子交换吸附联合的提硼的方法:104445242 B[P].2016-08-24.
LIU M Y,SONG J C,XU Y S H.Method for extracting boron with combination of solvent extraction-ion exchange adsorption:104445242 B[P].2016-08-24.
[17] 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.离子交换树脂预处理方法:GB/T 5476—2013[S].北京:中国标准出版社,2013.
General Administration of Quality Supervision,Inspection and Quarantine of the People’s Republic of China,Standardization Administration of the People’s Republic of China.Methods of pretreating ion exchange resins:GB/T 5476—2013[S].Beijing:Standards Press of China,2013.
[18] HO Y S,MCKAY G.The sorption of lead (Ⅱ) ions on peat [J].Water Research,1999,33(2):578-584.
[19] HO Y S,MCKAY G.Pseudo-second order model for sorption processes [J].Process Biochemistry,1999,34(5):451-465.
[20] WANG L P,HUANG Z C,ZHANG M Y,et al.Adsorption of methylene blue from aqueous solution on modified ACFs by chemical vapor deposition[J].Chemical Engineering Journal,2012,189/190:168-174.
[21] MONAZAM E R,SHADLE L J,MILLER D C,et al.Equilibrium and kinetics analysis of carbon dioxide capture using immobilized amine on a mesoporous silica[J].AIChE Journal,2013,59(3):923-935.
[22] 中国科学院青海盐湖研究所.卤水和盐的分析方法[M].北京:科学出版社,1973:302.
Qinghai Institute of Salt Lakes,Chinese Academy of Sciences. Analytical methods of brine and salts[M].Beijing:Science Press,1973:302.
[23] COTTON F,GEOFFREY W,CARLOS M,MANFRED B.Advanced inorganic chemistry[M].6th ed.New York:John Wiley & Sons Inc.,1999:1376.
[24] FORTUNY A,COLL M T,KEDARI C S,et al.Effect of phase modifiers on boron removal by solvent extraction using 1,3 diolic compounds[J].Journal of Chemical Technology & Biotechnology,2014,89(6):858-865.
[25] GUAN Z M,LV J F,BAI P,et al.Boron removal from aqueous solutions by adsorption:a review[J].Desalination,2016,383: 29-37.
[26] CENGELOGLU Y,ARSLAN G,TOR A,et al.Removal of boron from water by using reverse osmosis[J].Separation and Purification Technology,2008,64(2):141-146.
Removal of micro-amount boron from salt lake brine by solvent extraction-resin adsorption combined method
WANG Xiong1,LIU Mingyan1,2,SONG Junchao1
(1Collaborative Innovation Center of Chemical Science and Engineering(Tianjin),School of Chemical Engineering and Technology,Tianjin University,Tianjin 300072,China;2China State Key Laboratory of Chemical Engineering(Tianjin University),Tianjin 300072,China)
A solvent extraction-resin adsorption combined method was developed to recover and remove micro-amount boron from brine of salt lake in Qinghai. The effects of pH,phase ratio, extraction stages on extraction process, and the effect of pH of brine after first stage extraction, resin dosage on boron adsorption were investigated. The adsorption isotherm and kinetics were studied. The stripping and elution process were also optimized. The results showed that best extraction result could be obtained when pH was 2. The reduction of boron concentration was not obvious when the phase ratio and extraction stage value were above 3. The best pH for boron adsorption from brine was 7. The adsorption kinetics and adsorption isotherm data were fitted well with pseudo-second-order rate model and Langmuir model,respectively. The concentration of boron could be reduced to 1.0mg/L or less when resin dosage is 6g/(100mL brine) using the extraction-adsorption combined method. The proper stripping agent and eluent were 0.1mol/L NaOH and 0.5mol/L HCl, respectively.
solvent extraction;adsorption;boric acid;salt lake brine
TQ128+.54
A
1000–6613(2017)10–3625–08
10.16085/j.issn.1000-6613.2017-0106
2017-01-17;
2017-04-26。
王雄(1991—),硕士研究生。E-mail:wangxiong105 @126.com。
刘明言,教授,主要研究方向为多相流及传递过程强化。E-mail:myliu@tju.edu.cn。
