HPLC法测定甲苯磺酸依度沙班有关物质
2017-10-19李志伟张任飞刘颖娜禹叶广谢英花仇燕
李志伟,张任飞,刘颖娜,禹叶广,谢英花,仇燕
(1.河北科技大学 化学与制药工程学院,河北 石家庄 050018;2.河北科技大学 生物科学与工程学院,河北 石家庄 050018)
HPLC法测定甲苯磺酸依度沙班有关物质
李志伟1,张任飞1,刘颖娜1,禹叶广1,谢英花1,仇燕2
(1.河北科技大学 化学与制药工程学院,河北 石家庄 050018;2.河北科技大学 生物科学与工程学院,河北 石家庄 050018)
建立了一种高效液相色谱(HPLC)法,用于检测甲苯磺酸依度沙班有关物质.该法采用SunFire C8(250 mm×4.6 mm,5 μm)色谱柱,以20 mmol/L磷酸氢二钾(pH 4.0)-乙腈(体积比为90∶10)为流动相A,20 mmol/L磷酸氢二钾(pH 4.0)-乙腈(体积比为30∶70)为流动相B,按梯度洗脱程序洗脱.该方法的检测波长为290 nm,流速为1.0 mL/min,柱温为30 ℃,进样量为10 μL.结果表明,甲苯磺酸依度沙班及各杂质均能有效分离;在相应的浓度范围内,各物质的线性关系良好;各杂质的回收率均在98.0%~102.0%,RSD(n=9)均小于2.0%;在色谱条件有微小变化时,各物质均能有效分离且杂质含量的差异在可接受范围内.经方法学验证,该方法专属性好、灵敏度高、准确度高、耐用性好,可用于甲苯磺酸依度沙班的质量控制.
甲苯磺酸依度沙班;有关物质;高效液相色谱法;质量控制
甲苯磺酸依度沙班(edoxaban tosilate hydrate)是由日本第一三共株式会社研制的一种口服小分子抗凝血药物,可用于治疗静脉血栓和全髋关节置换[1-3].甲苯磺酸依度沙班通过高选择性直接抑制凝血因子Xa的表达,起到抗凝血作用,其对Xa的选择性较对凝血酶高10 000倍,对其他丝氨酸蛋白酶无作用[4].甲苯磺酸依度沙班片于2011年在日本上市,2015年先后在美国和欧洲上市[5-7],目前还未在国内上市.
为了保证药物的安全性、可靠性,需对甲苯磺酸依度沙班的杂质进行研究.目前,有诸多文献报道甲苯磺酸依度沙班的合成、药理学、药效学和药动学[8-11],但甲苯磺酸依度沙班有关物质的检测方法未见报道.本文根据甲苯磺酸依度沙班的合成路线,建立了一种液相色谱测定甲苯磺酸依度沙班及其杂质的方法.按加校正因子的主成分对照法计算杂质含量,其中杂质A、杂质B和杂质E分别为甲苯磺酸依度沙班的起始原料1、起始原料2和起始原料3;杂质C和杂质D分别为甲苯磺酸依度沙班中间体1和中间体2;杂质F为合成中间体1中的副产物;杂质G、杂质H和杂质I为甲苯磺酸依度沙班的非对映异构体,即SRR-依度沙班,RRR-依度沙班和SSR-依度沙班.甲苯磺酸依度沙班和各杂质的结构式分别见图1和图2.

图1 甲苯磺酸依度沙班-水合物结构式Fig.1 Structure of edoxaban tosilate hydrate

图2 甲苯磺酸依度沙班杂质结构式Fig.2 Structure of impurities of edoxaban tosilate hydrate
1 实验部分
1.1 仪器与试剂
SHIMADZU高效液相色谱仪(包括SCL-10Avp控制器,DGU-14A脱气机,LC-10ADvp泵,SIL-10ADvp进样器,CTO-10ACvp柱温箱,SPD-10AV检测器及LC solution工作站);Waters高效液相色谱仪(包括Waters 2695 Separations Module和Waters 2996 Photodiode Array Detector);AUW120D电子天平(SHIMADZU);pH计,pHS-3C,上海精科;乙腈,色谱纯,霍尼韦尔贸易(上海)有限公司;磷酸氢二钾,分析纯,天津市永大化学试剂有限公司;磷酸,分析纯,天津市永大化学试剂有限公司.甲苯磺酸依度沙班、杂质A、B、C、D、E、F、G、H、I(自制,石家庄佰锐生物科技有限公司),甲苯磺酸依度沙班(石家庄佰锐生物科技有限公司,批号:20141101、20141102、20141103).
1.2 色谱条件
色谱柱:SunFire C8(250 mm×4.6 mm,5 μm),流动相A为20 mmol/L磷酸氢二钾(pH 4.0)-乙腈(体积比为90∶10),流动相B为20 mmol/L磷酸氢二钾(pH 4.0)-乙腈(体积比为30∶70),梯度洗脱,梯度洗脱程序见表1,流速为1.0 mL/min,柱温为30 ℃,检测波长为290 nm,进样量为10 μL.

表1 梯度洗脱程序Tab.1 Gradient elution procedure
1.3 溶液配制
杂质F储备液:取杂质F适量,精密称定,用乙腈溶解并稀释制成每1 mL含0.05 mg的杂质F储备液.
其他杂质储备液:分别取杂质A、E、C、D、G、H、I、甲苯磺酸依度沙班对照品各适量,精密称定,分别加甲醇溶解并稀释制成1 mL中约含0.5 mg的各杂质一级储备液.取上述杂质的一级储备液2.5 mL,置50 mL量瓶中,用甲醇稀释至刻度,摇匀,得对照品储备液.
标准溶液:分别精密量取杂质A、E、C、D、G、I、H储备液各5 mL,杂质F储备液2.5 mL以及甲苯磺酸依度沙班对照品适量(约含依度沙班25 mg),置于同一50 mL容量瓶中,用甲醇稀释定容至刻度,制成每1 mL中约含2.5 μg的各杂质对照品和每1 mL中约含0.5 mg依度沙班对照品的标准溶液.
供试品溶液:取本品适量(含依度沙班约25 mg),精密称定,置50 mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,作为供试品溶液.
对照溶液:精密量取供试品溶液1 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀;再精密量取溶液1 mL,置10 mL量瓶中,用甲醇稀释至刻度,摇匀,作为对照溶液.
2 结果与讨论
2.1 色谱条件选择
2.1.1 检测波长的选择
取甲苯磺酸依度沙班、杂质A、B、C、D、E、F、G、H、I适量,用甲醇稀释至适当浓度,于190~400 nm波长内扫描,甲苯磺酸依度沙班和大部分杂质在290 nm附近有强吸收,因此选择290 nm作为检测波长.杂质B的最大吸收波长在206 nm,在290 nm处无吸收,该杂质在中间体1的过程中严格控制,因此不作为本文考察的杂质.
2.1.2 色谱柱的选择
在梯度洗脱程序确定前,首先对色谱柱进行筛选,包括:Agela Venusil ASD C18(250 mm×4.6 mm,5 μm)色谱柱,phenomenex Luna (250 mm×4.6 mm,5 μm)色谱柱,SHIMADZU HRC-C8(150 mm×4.6 mm,5 μm)色谱柱,Waters SunFire C8(250 mm×4.6 mm,5 μm)色谱柱.在相同的分析条件下,4根不同品牌的色谱柱都不能将主峰与其后的杂质分离,但Waters SunFire C8 (250 mm×4.6 mm,5 μm)色谱柱对杂质的分离优于其他色谱柱,因此最终确定选用Waters SunFire C8 (250 mm×4.6 mm,5 μm)色谱柱作为甲苯磺酸依度沙班有关物质的分析色谱柱.
2.1.3 pH值的选择
在梯度洗脱程序确定后,本文考察了pH值对杂质分离度的影响.将磷酸盐缓冲液的pH值调整为7.0、5.5、4.0、3.0对杂质进行分析.实验结果表明,随着pH值的减小,杂质的分离度增强,当pH值为7.0和5.5时,该梯度洗脱程序不能将杂质全部分离,当pH值为4.0和3.0时,各物质均能有效分离,但考虑到色谱柱pH值的耐用范围,确定磷酸盐缓冲液的pH值为4.0.
2.2 方法学验证
2.2.1 专属性
取空白溶剂(甲醇)、标准溶液、供试品溶液和各杂质定位溶液,按“1.2”节色谱条件进行测定,标准溶液的出峰顺序杂质E、杂质D、对甲苯磺酸、依度沙班、杂质G、杂质H、杂质I、杂质A、杂质C、杂质F,且空白溶剂不干扰甲苯磺酸依度沙班和各杂质的检测,且各杂质间最小的分离度为1.775,达到分离要求,实验结果表明该法专属性良好.实验结果见图3.

图3 专属性实验对比Fig.3 Chromatograms comparison of methanol and standard solution
2.2.2 系统精密度
按“1.3”节配制标准溶液,于“1.2”节的分析方法下连续进样6次,杂质E峰面积的相对标准偏差为10.55%,其他各物质峰面积的相对标准偏差均小于2.0%,保留时间的相对标准偏差均小于1.0%.实验结果表明,杂质E不稳定,就其他物质而言,该方法系统适用性良好.
2.2.3 降解实验
酸降解实验:取甲苯磺酸依度沙班约25 mg,精密称定,置50 mL量瓶中,加0.1 mol/L盐酸2 mL,于室温下放置24 h后,加2 mL 0.1 mol/L氢氧化钠溶液中和,用甲醇稀释至刻度,摇匀,测定.另取同法配制酸空白溶剂做空白实验.
碱降解实验:取甲苯磺酸依度沙班约25 mg,精密称定,置50 mL量瓶中,加0.1 mol/L氢氧化钠2 mL,于室温下放置5 min后,加2 mL 0.1 mol/L盐酸溶液中和,用甲醇稀释至刻度,摇匀,测定.另取同法配制碱空白溶剂做空白实验.
氧化降解实验:取甲苯磺酸依度沙班约25 mg,精密称定,置50 mL量瓶中,加2 mL质量分数 30%双氧水,于室温下放置24 h后,用甲醇溶解定容并稀释至刻度,摇匀,测定.另取同法配制氧化空白溶剂做空白实验.
高温固体降解实验:取甲苯磺酸依度沙班约25 mg,精密称定,置50 mL量瓶中,于80 ℃烘箱中放置24 h后,用甲醇溶解并稀释至刻度,摇匀,测定.
光照降解实验:取甲苯磺酸依度沙班约25 mg,精密称定,置50 mL量瓶中,于照度为 4 500 lx下放置24 h后,用甲醇溶解并稀释至刻度,摇匀,测定.
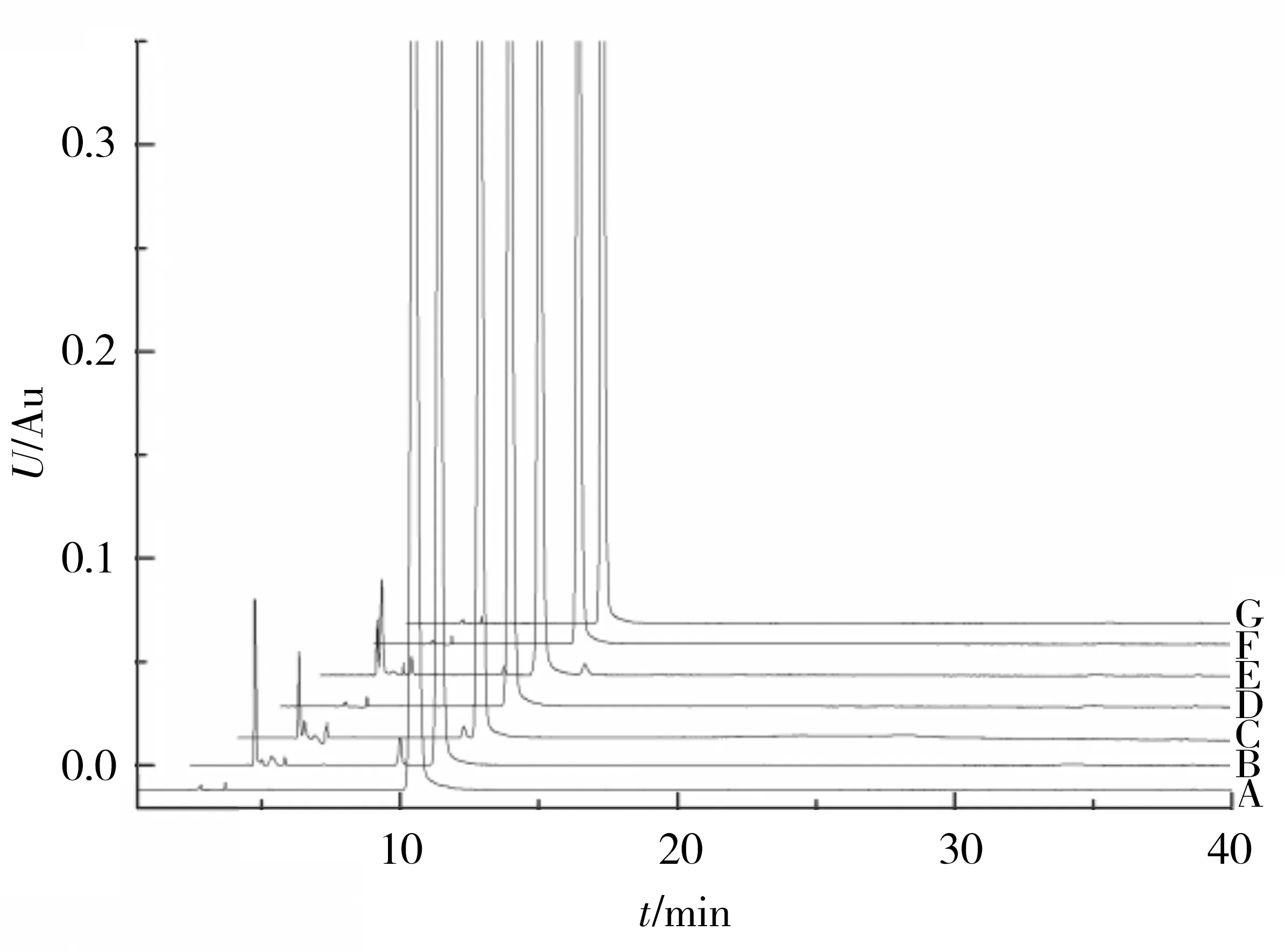
A.未破坏;B.酸破坏;C.碱破坏;D.光照液体;E.氧化破坏;F.高温固体破坏;G.光照固体破坏.图4 降解实验色谱Fig.4 Chromatograms of forced degradation test
光照液体降解实验:取甲苯磺酸依度沙班约25 mg,精密称定,置50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,于4 500 lx下放置24 h后进行测定.
照上述分析方法测定,各条件下降解实验的物料守恒值均在90%~110%,遵循物料守恒原则,且主峰的纯度角度值均小于阈值,表明峰纯度符合要求.本品在酸、碱、氧化条件下有杂质产生,酸降解实验产生了杂质E和2个未知杂质;碱降解实验产生了杂质E和1个未知杂质;氧化降解实验产生了杂质E和3个未知杂质.各条件下杂质均能达到有效分离,表明该方法专属性强.实验结果见图4.
2.2.4 检测限与定量限
以信噪比S/N=3时的浓度作为检测限,S/N=10时的浓度作为定量限,并取定量限溶液进行重复性实验,定量限重复性实验峰面积的相对标准偏差均小于5.0%,保留时间的相对标准偏差均小于1.0%,实验结果见表2和图5.

表2 检测限、定量限实验结果Tab.2 Results of LOD and LOQ

图5 定量限图谱Fig.5 Chromatogram at the limit of quantitation of edoxaban tosilate hydrate and its impurities
2.2.5 线性与范围
取甲苯磺酸依度沙班和各杂质储备液适量,用甲醇稀释成6个不同质量浓度的混合溶液,按“1.2” 节色谱条件进样分析,以各物质的线性质量浓度为横坐标,峰面积为纵坐标,进行线性回归.实验结果表明,各物质在相应的质量浓度范围内,线性关系良好.线性实验结果见表3.

表3 线性实验结果Tab.3 Results of linearity test
2.2.6 重复性
按“1.3”节的溶液配制方法配制6份供试品溶液和自身对照溶液,分别进行色谱分析,6份供试品溶液中均未检测出已知杂质,均检测到同一未知杂质,未知杂质的质量分数均值为0.044%,RSD为3.81%,小于4.0%,符合要求.实验结果表明,该方法重复性良好.
2.2.7 中间精密度
由不同人员于不同时间按“重复性”项下操作,进行样品测定,6份供试品溶液中均未检测出已知杂质,均检测到同一未知杂质,未知杂质的质量分数均值为0.047%,RSD为4.32%,小于5.0%.与重复性结果共计,12份样品未知杂质含量的RSD为5.20%,小于6.0%.实验结果表明,该方法中间精密度良好.
2.2.8 溶液稳定性
按“1.3”节配制供试品溶液和标准溶液,在室温下放置,分别于0、2、4、6、8 h进样分析,考察其稳定性.经测定,杂质E峰面积的RSD为13.83%,其余各物质峰面积的RSD均小于2.5%,则说明杂质E不稳定,需临用现配,其他各杂质在室温下放置8 h稳定.供试品溶液的杂质质量分数均值为0.042%,RSD为3.94%,小于4.0%,说明甲苯磺酸依度沙班溶液在室温下放置8 h稳定.
2.2.9 回收率
分别向甲苯磺酸依度沙班中加入80%、100%、120% 3种质量分数的杂质溶液,每个质量浓度平行配制3份溶液,按“1.2”节测定,按外标法计算各杂质的回收率,各杂质的回收率均在98%~102%,RSD均小于2.0%.实验结果表明,该方法准确度高.实验结果见表4.

表4 回收率实验结果Tab.4 Results of recovery test
2.2.10 耐用性
本实验主要考察了在流速改变±0.1 mL/min,流动相乙腈体积分数改变±2%,柱温变化±5 ℃,pH调节±0.1条件下各杂质的分离情况和供试品的杂质含量.在上述条件下,各杂质的分离度均大于1.5,符合分离要求;供试品总杂质在各个条件下的RSD最大为5.92%.实验结果表明,该方法在适量改变(流速±0.1 mL/min,流动相乙腈比例±2%,柱温± 5℃,pH±0.1)范围内耐用性良好.
2.3 样品测定结果
取中试3批(批号为:20141101、20141102、20141103)样品,按照上述方法进行测定, 3批样品均未检测出已知杂质,未知杂质质量分数分别为0.049%、0.053%、0.051%.
3 结论
本文建立了一种高效液相色谱分析方法,用于检测甲苯磺酸依度沙班的有关物质,采用加校正因子的自身对照法计算杂质含量.实验结果表明,方法专属性好,灵敏度高,准确度高,耐用性好,可用于甲苯磺酸依度沙班有关物质的检测.
[1] 王利华,赵丽嘉,李文利,等.直接抑制凝血因子Xa的口服抗凝药物Edoxaban Tosilate Hydrate [J].药物评价研究,2011,34(6):478-481.
[2] BROWN K S,WICKREMASINGHA P,PARASRAMPURIA D A,et al.The impact of a three-factor prothrombin complex concentrate on the anticoagulatory effects of the factor Xa inhibitor edoxaban [J].Thrombosis Research,2015,136(4): 825-831.DOI:10.1016/j.thromres.2015.07.012.
[3] MORISHIMA Y,KAMISATO C,HONDA Y.Treatment of venous thrombosis with an oral direct factor Xa inhibitor edoxaban by single and multiple administrations in rats [J].European Journal of Pharmacology,2014,742: 15-21.DOI:10.1016/j.ejphar.2014.08.020.
[4] 康银花.国外新型抗凝药物的临床研发动态[J].中国新药杂志,2013,22(1):53-58.
KANG Y H.Advance in clinical study of new anticoagulants in foreign countries [J].Chinese Journal of New Drugs,2013,22(1): 53-58.
[5] DAIICHI SANKYO COMPANY LIMITED.Daiichi Sankyo submits edoxaban marketing authorization application to the EMA for once daily use for stroke prevention in atrial fibrillation and for the treatment and prevention of recurrence of venous thromboembolism.http://www.daiichisankyo.com/media_investors/media_relations/press_releases/detail/006062.html.
[6] DAIICHI SANKYO COMPANY LIMITED.Daiichi Sankyo’s once-daily Lixiana (edoxaban)receives positive CHMP opinion for the prevention of stroke and systemic embolism in non-valvular atrial fibrillation and for the treatment and prevention of recurrent venous thromboembolism in Europe.http://www.daiichisankyo.com/media_investors/media_relations/press_releases/detail/006278/20150427_571_ E.pdf.
[7] DAIICHI SANKYO COMPANY LIMITED.SAVAYSATM (edoxaban)now available in U.S.pharmacies.http://www.daiichisankyo.com/media_investors/media_relations/press_releases/detail/006247.html.
[8] 潘林玉,梁斌,张福利.依度沙班合成路线图解[J].中国医药工业杂志,2013,44(11):1170-1173.DOI:10.16522/j.cnki.cjph.2013.11.016
PAN L Y,ZHANG B,ZHONG F L.Graphical synthetic routes of edoxaban [J].Chinese Journal of Pharmaceuticals,2013,44(11): 1170-1173.DOI:10.16522/j.cnki.cjph.2013.11.016.
[9] 解静蕾,胡春.依度沙班对甲苯磺酸盐一水合物[J].中国药物化学杂志,2015,25(4):330.DOI:10.14142/j.cnki.cn21-1313/r.2015.04.018
XIE J L,HU C.Edoxaban tosylate monohydrate [J].Chinese Journal of Medicinal Chemistry,2015,25(4): 330.DOI:10.14142/j.cnki.cn21-1313/r.2015.04.018.
[10] HONDA Y,KAMISATO C,MORISHIMA Y,et al.Prevention of arterial thrombosis by edoxaban,an oral factor Xa inhibitor in rats: monotherapy and in combination with antiplatelet agents [J].European Journal of Pharmacology,2016,786: 246-252.DOI:10.1016/j.ejphar.2016.06.011.
[11] SHIRASAKI Y,MORISHIMA Y,SHIBANO T,et al.Comparison of the effect of edoxaban,a direct factor Xa inhibitor,with a direct thrombin inhibitor,melagatran,and heparin on intracerebral hemorrhage induced by collagenase in rats [J].Thrombosis Research,2014,113(4): 622-628.
(责任编辑:梁俊红)
DeterminationofrelatedsubstancesinedoxabantosilatehydratebyHPLC
LIZhiwei1,ZHANGRenfei1,LIUYingna1,YUYeguang1,XIEYinghua1,QIUYan2
(1.College of Chemical &Pharmaceutical Engineering,Hebei University of Science and Technology,Shijiazhuang 050018,China;2.College of Bioscience &Bioengineering,Hebei University of Science and Technology,Shijiazhuang 050018,China)
A HPLC method was established to separate edoxaban tosilate hydrate and its related substances.SunFire C8 (250 mm×4.6 mm,5 μm)column was adopted in the analysis method and its temperature was kept at 30 ℃.The mobile phase A consisted of 20 mmol/L K2HPO4(pH 4.0)-acetonitrile (90∶10,V/V)and the mobile phase of B consisted of 20 mmol/L K2HPO4(pH 4.0)-acetonitrile (30∶70,V/V).A gradient elution at flow of 1.0 mL/min was used.The detection wavelength was 290 nm and the injection volume was 10 μL.The calibration curve of all substances were linear in appropriate concentration range,and the average recovery of all compounds were among 98.0%~102.0%,RSD (n=9)values were less than 2.0%.Each impurity was separated when the parameters had small changes and the assay variation of impurities was accepted.Methodology validation results proved that the method had good selectivity,high sensitivity,high accuracy and good robustness and it can be used for quality control of edoxaban tosilate hydrate.
edoxaban tosilate hydrate;related substances;HPLC;quality control
O29
A
1000-1565(2017)05-0489-08
10.3969/j.issn.1000-1565.2017.05.008
2016-12-25
河北省自然科学基金资助项目(C2014208084)
李志伟(1977—),男,河北唐县人,河北科技大学副教授,主要从事药物分析和分离材料方面的研究.E-mail:lizhiwei@hebust.edu.cn
