纳米K-OMS-5电极材料的制备与电化学性能
2017-10-13王君熠朱杨军索晓燕温祖标
王君熠,朱杨军,代 芳,索晓燕,余 敏,章 磊,温祖标
(1. 江西师范大学 化学化工学院, 南昌 330022;2. 南昌工程学院, 南昌 330099)
纳米K-OMS-5电极材料的制备与电化学性能
王君熠1,朱杨军1,代 芳2,索晓燕1,余 敏1,章 磊1,温祖标1
(1. 江西师范大学 化学化工学院, 南昌 330022;2. 南昌工程学院, 南昌 330099)
在25℃下,以KMnO4、KOH和MnCl2为反应物,利用液相氧化还原法制备δ-MnO2,然后以所制备的δ-MnO2和KOH为前驱体,在180℃水热下反应2d,合成纳米K-OMS-5(钾-八面体分子筛);分别采用X射线衍射光谱、扫描电镜和热重分析等物理方法对晶体结构、表面形貌及其热稳定性进行表征;用循环伏安、恒流充放电和交流阻抗等电化学方法研究其电化学性能.结果表明,纳米K-OMS-5材料在相同的扫描速率或电流密度下比电容的大小关系为K2SO4>Na2SO4>Li2SO4,且在0.5molL-1K2SO4电解液中的2000次循环充放电中展现出了良好的循环稳定性,这或许为K-OMS-5材料在电化学电容器中的应用提供了一种有前景.
电化学电容器; 电极材料; 嵌入化合物; K-OMS-5
电化学电容器是介于电池和传统电容器之间的一种新型能量储存器件,具有环境友好、比电容大、功率密度高、充电时间短、可靠性高、循环寿命长、稳定性高等优点而引起研究者的广泛关注,而在汽车工业、电子、通讯、电气设备、航空航天和军工等领域广泛应用并迅猛发展[1].与此同时,美国能源部将电化学电容器提升到与二次电池同样重要的战略地位,作为未来储能设备之一[2].
电极材料是影响电化学电容器性能的核心因素,因此开发高性能、低成本的电极材料一直是电化学电容器研究的重要课题.电化学电容器的电极材料主要有碳材料、导电聚合物和过渡金属氧化物等[3].在过渡金属氧化物中,二氧化锰(MnO2)是电化学电容器的重要电极材料,有较高的电极电势和大的理论比容量以及突出的离子存储性能,较其他金属氧化物如氧化钌、氧化镍、氧化钴和氧化钒等,其具有易得、价廉、无毒、环境友好、存在多种价态和β-、γ-、α-、δ-、λ-MnO2与OMS-5等多晶型[4].但是,二氧化锰作为电极材料存在两个不足: 一是电导率较低(0.1S·cm-1),是一种半导体材料;二是在电化学反应中,隧道结构的不稳定和锰的部分溶解,严重影响了电极中活性物质的利用率和循环稳定性[5].为了改善MnO2的电化学性能,通常制备其纳米结构材料或者在结构中嵌入离子.因为纳米结构可缩短电子和电解质离子的扩散路径,增强MnO2的电子电导率和通道中离子电导率,而提高其化学活性[6];嵌入离子可消除Mn的d2sp3杂化轨道的简并性,降低锰原子的姜-泰勒(John-Teller)效应,使得其晶格不易变形,可在一定程度上解决长期困扰着MnO2电极材料循环稳定性的问题[7].
本文以一种具有0.46nm×0.92nm大通道结构的OMS-5型MnO2作为宿主,制备了一种纳米K-OMS-5化合物,利用X射线衍射光谱、扫描电镜和热重分析等物理方法分别表征其晶体结构、形貌特征和热稳定性;采用循环伏安(Cyclic Voltammetry, CV)、恒流充放电(Galvanostatic Charge-Discharg, GC)和交流阻抗(Electrochemical Impedance Spectroscopy, EIS)等电化学方法测试其在0.5molL-1Li2SO4、Na2SO4和K2SO4电解液中的电化学性能,探讨了通道结构与金属离子N(N=Li+、Na+、K+)种类的匹配关系,进而探索材料的储能机理.
1 实 验
1.1纳米K-OMS-5电极材料的制备
将0.112mol MnCl2溶解在400mL蒸馏水中作为溶液A,0.3mol KOH和0.01mol KMnO4混合溶解在100mL蒸馏水中作为溶液B.在冰水浴条件下,将溶液A逐滴入到搅拌的溶液B中使之反应,完后在25℃下静置老化一天,抽滤,用去离子水和无水乙醇洗涤样品至中性,在70℃条件下干燥24h即可得到δ-MnO2;称取所制备的δ-MnO21.0g均匀分散在200mL的0.1molL-1KOH溶液中,将混合溶液放在密封的高压反应釜中180℃加热2d,然后抽滤,用去离子水和无水乙醇洗涤样品至中性,然后在80℃条件下干燥48h即可得到纳米K-OMS-5.
1.2材料的物理表征
用XRD(Cu靶,D8 ADVANCE,Bruker,德国)对材料的晶相结构进行分析,扫描范围为5°~90°,管压为40kV,扫描速度10°/min;采用扫描电子显微镜(S-3400N型,日本日立公司)观察材料颗粒大小和表面形貌;在空气氛下用高温热重-差热同步分析仪(Diamond TG/DTA型,美国PE公司)对材料进行热重分析,升温速率为5℃/min.
1.3电极片制备与电化学性能测试
依次称取所制备的纳米K-OMS-5、导电石墨和粘结剂(Polytetrafluoroethylene, PTFE)各0.8g、0.1g和0.1g,用无水乙醇均匀混合分散,在称量纸上用玻璃棒压成薄片,用打孔器在薄片上截取圆形电极片,80℃真空干燥,烘干后于8MPa压力下压在集流体镍网上,将压制好的电极片分别浸渍在0.5molL-1Li2SO4、Na2SO4和K2SO4中10h.在三电极体系中,以制备的电极片为工作电极、空白镍网为对电极、饱和甘汞电极(Saturated Calomel Electrode, SCE)为参比电极,在电化学工作站(CHI660E,上海辰华仪器公司)上测试电极的电化学性能.
2 结果与讨论
2.1纳米K-OMS-5电极材料的物理表征
2.1.1 材料的结构和元素分析
图1(a)、(b)分别为所制备样品的XRD图谱和EDS图谱.由图1(a)可以得出,该样品最高峰在2θ=12.22°处,各衍射峰晶面指标如图示,表明该样品为OMS-5,这与Shen等[8]研究的结果是一致的;并且晶胞参数为a=14.22nm、b=2.853nm、c=24.28nm和β=91.32°,属于单斜晶系中C2/m空间群.由图1(b)可知,样品出现了明显的K、Mn和O的特征峰,由此可进一步论证所制样品含有K元素,是K-OMS-5化合物,嵌入离子K+可适当消除Mn的d2sp3杂化轨道的简并性,降低锰原子的John-Teller效应,而提高材料循环稳定性.
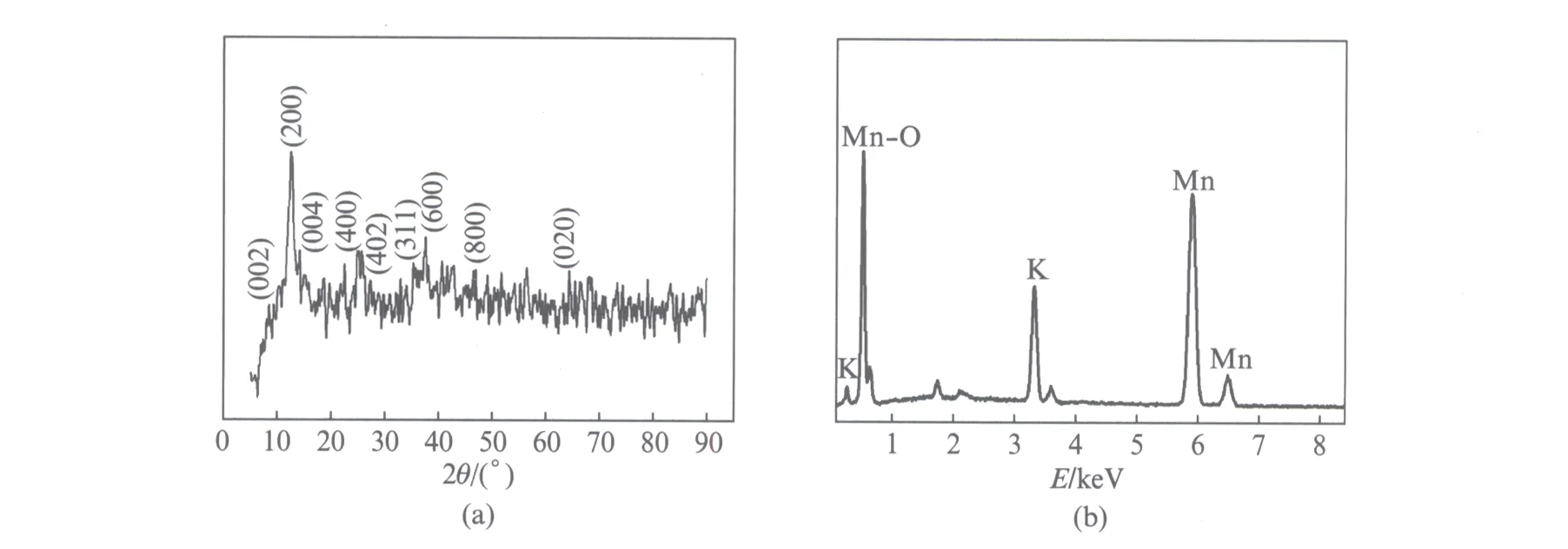
图1 (a) K-OMS-5的XRD图;(b) K-OMS-5的EDS图Fig.1 (a) XRD patterns of K-OMS-5; (b) EDS patterns of K-OMS-5
2.1.2 纳米K-OMS-5材料的形貌表征
图2(a)、(b)分别是K-OMS-5不同放大倍数的SEM图.从图2可看出,所制备的K-OMS-5是纳米线状结构,且尺寸较均匀.由此可推测,所制备的K-OMS-5化合物的纳米结构将有利于电子和电解质离子的吸附/脱附运动,而可能表现出良好的电化学活性.

图2 K-OMS-5的SEM图Fig.2 The SEM images of K-OMS-5
2.1.3 热失重分析
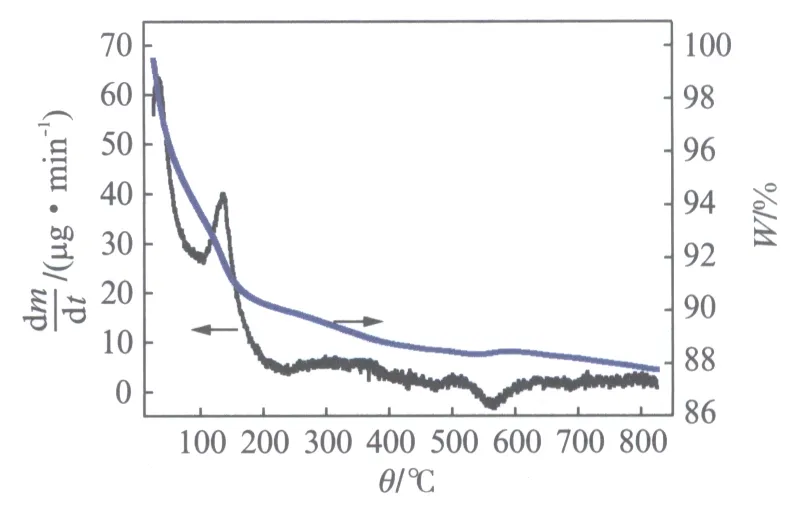
图3 K-OMS-5样品的TG/DTG图谱Fig.3 TG/DTG plots of the K-OMS-5 sample
图3是K-OMS-5样品的TG/DTG曲线.由图3可知,该样品的热失重过程大致经历了两个阶段: 在温度低于200℃时,失重量约为8%左右,主要是样品失去表面吸附水和结晶水;温度在200~800℃间时,失重量约为3%,可能是样品失去了其隧道结构中极少量的K+和水分子.这预示着所制样品K-OMS-5化合物结构稳定,有着良好的热稳定性,这有利于提高材料的电化学循环稳定性能.
2.2纳米K-OMS-5电极材料的电化学性能
2.2.1 循环伏安特性
图4(a)、(b)和(c)是纳米K-OMS-5化合物分别在0.5molL-1Li2SO4、Na2SO4和K2SO4电解液中在不同扫描速率下的循环伏安曲线图.由图4可知,K-OMS-5在Li2SO4电解液中的CV曲线严重扭曲而成近似叶形,这表明样品在Li2SO4电解液中的电容特性较差;样品K-OMS-5电极在Na2SO4和K2SO4电解液中的CV曲线接近矩形,并且在低扫速下可观察到发生氧化还原反应的驼峰,这表明样品K-OMS-5不仅具有双电层电容性能,而且还有赝电容性能[9].这主要是因为锂离子Li+水合离子半径较大,而Na+、K+水合离子半径较小,纳米K-OMS-5表面吸附的Na+、K+水合离子较Li+水合离子多.业内知道,在相同扫描速率下,电极材料的比电容(Cp)与CV曲线围成的面积大小成正比;由图4(a)、(b)和(c)可知,K-OMS-5电极在Na2SO4和K2SO4电解液中的Cp近似相等,且大于在Li2SO4电解液中的Cp.为了定量评价K-OMS-5电极在3种电解液中的电容性能,我们计算了不同扫描速率下的Cp,并得到了扫描速率与Cp的曲线图(如图4(d)所示).由图可知,随着扫描速率的增大,电极在3种电解液中的Cp均不同程度的降低.这是因为扫描速率较低时,电解质离子有足够的时间发生吸附/脱附反应;当扫描速率较高时,电解质离子受到迁移时弛豫时间和电解液电阻等电极过程的影响,使得Cp降低.其次,在相同扫描速率下,在K2SO4中的Cp最大,在Li2SO4中的Cp最小.一方面,是由于离子的水合半径大小顺序为Li+(3.82Å)>Na+(3.58Å)>K+(3.31Å),Li+和Na+在电极反应中更容易破坏了活性物质的晶体结构,使得K+比Li+、Na+发生电极反应时更稳定[10];另一方面,由于K-OMS-5材料是一种纳米材料,因在其表面吸附/脱附K+,使得电极在K2SO4电解液中的K+在电极反应过程中缩短了传输的时间,提高了电极中活性物质的利用率[11].
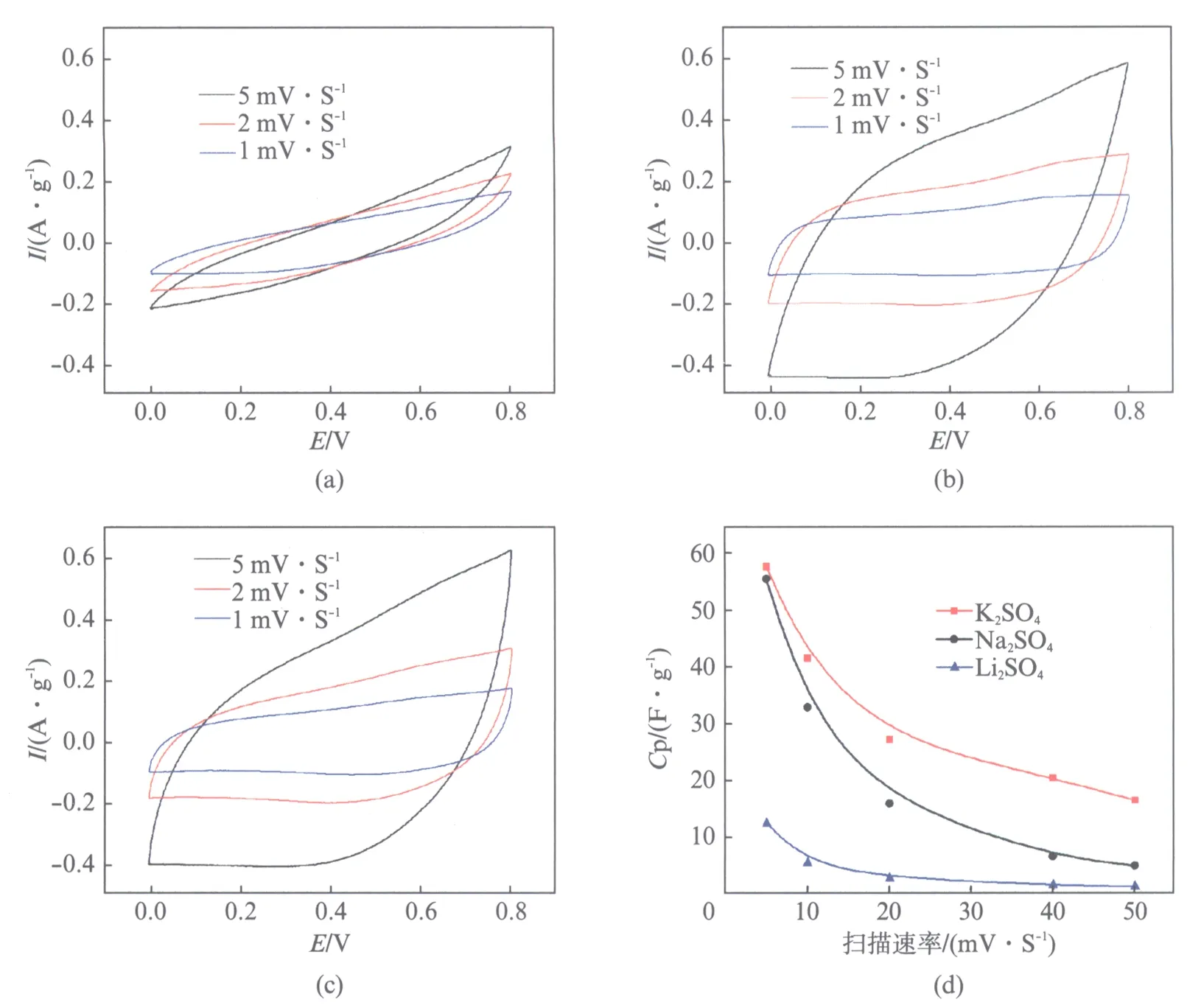
图4 K-OMS-5电极在0.5molL-1 Li2SO4(a)、Na2SO4(b)和K2SO4(c)电解液中不同扫描速率下的循环伏安图和扫描速率与Cp的关系曲线图(d)Fig.4 CV curves of K-OMS-5 electrode in 0.5molL-1 Li2SO4(a), Na2SO4(b) and K2SO4(c) aqueous solution at different scan rates respectively; (d) evolution of the scan rates versus specific capacitance
2.2.2 恒流充放电曲线
图5(a)、(b)和图5(c)(见第318页)分别是K-OMS-5电极在0.5molL-1Li2SO4、Na2SO4和K2SO4溶液中不同电流密度的恒流充放电曲线.由图可见,K-OMS-5电极在3种电解液中并没有出现明显的充放电平台,并且在Na2SO4和K2SO4呈现比较对称的三角形,这意味着该电极材料在3种电解液中的比电容主要是由双电层电容组成;还可以看出随着电流密度的增大放电时间不同程度的减小,这主要是由于随着电流的增大,电解质离子在电极过程中受到迁移速率和电导率等因素的影响,导致电极极化变大,电极反应受到限制[12].此外,对比图5中的(a)、(b)和(c),我们不难发现,在相同的电流密度下,电极在Na2SO4和K2SO4电解液中的放电时间明显大于在Li2SO4中的放电时间,这可能是由于离子电导率K+>Na+>Li+所导致的[13],与循环伏安所得出的结论是一致的.图5(d)(见第318页)是K-OMS-5电极在0.5molL-1K2SO4溶液中0.1A·g-1的恒流充放电曲线,可以看出经过多次循环后,曲线依然保持着良好的等腰三角形且放电瞬间没有明显的电压降,具有良好的重现性,表明电极充放电性能稳定、循环可逆性好和库仑效率高[14].下面就K-OMS-5电极在K2SO4电解液中作进一步研究.

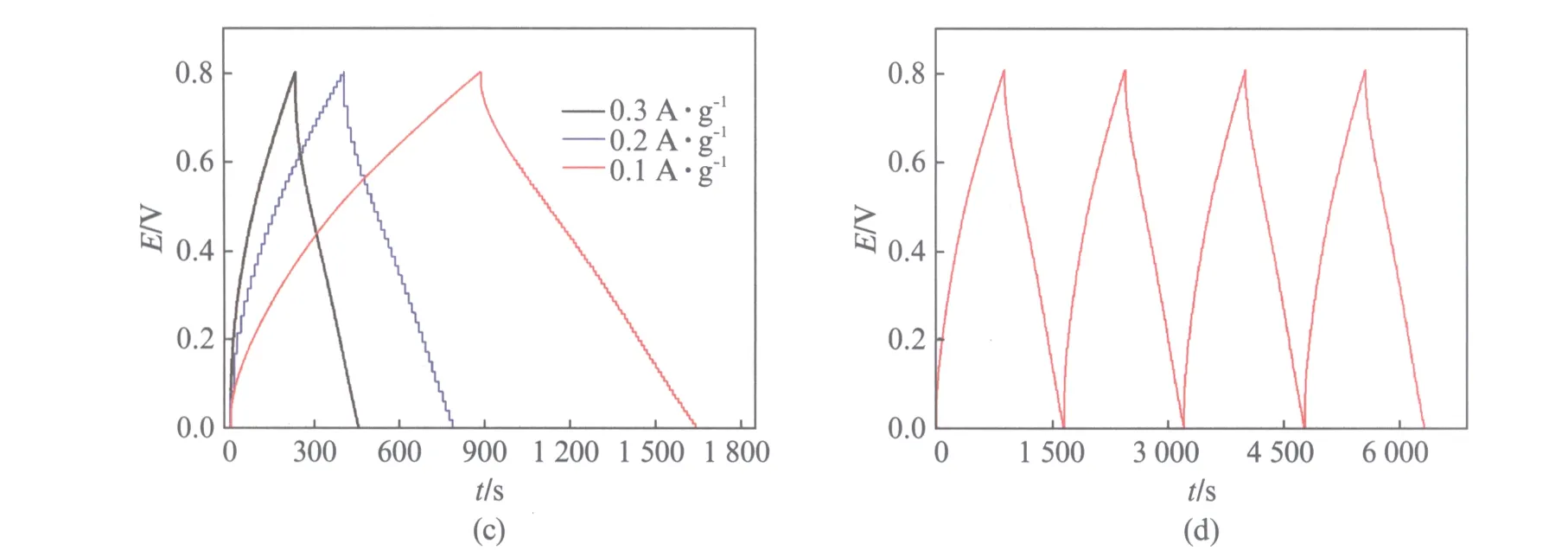
图5 K-OMS-5电极在0.5molL-1 Li2SO4(a)、Na2SO4(b)和K2SO4(c)溶液中不同电流密度的恒流充放电曲线和K-OMS-5电极在0.5molL-1 K2SO4溶液中0.1A·g-1的恒流充放电循环曲线(d).Fig.5 GC curves of K-OMS-5 electrode in 0.5 molL-1 Li2SO4(a), Na2SO4(b) and K2SO4(c) aqueous solution at different current density respectively and GC curves of K-OMS-5 electrode in 0.5 molL-1 K2SO4aqueous solution at 0.1 A·g-1(d)
2.2.3 交流阻抗性能
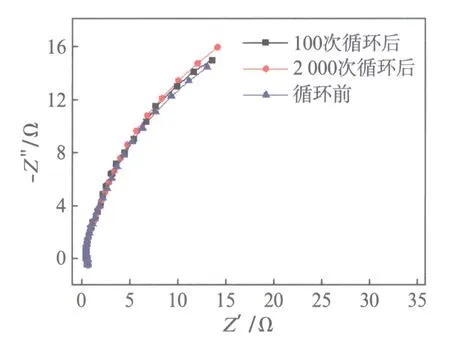
图6 K-OMS-5电极在0.5molL-1 K2SO4中100和2000次循环前后的交流阻抗图谱Fig.6 Nyquist impedance spectra of K-OMS-5 electrode after 100 and 2000 cycles in 0.5molL-1 K2SO4 respectively
交流阻抗是研究电极反应和电化学反应界面的一种重要的测试技术.图6是K-OMS-5电极在0.5molL-1K2SO4电解液中100和2000次循环前后的交流阻抗图谱,采用的交流信号振幅为5mV,频率范围为0.01~100kHz,对K-OMS-5电极的交流阻抗特征进行测试.由图6可得,在100和2000次循环前后的高频端Z′轴上的截距即等效串联电阻均为0.5Ω,该等效串联电阻主要包括电极材料的电阻、电解液电阻、电极材料与电解液的接触电阻等[15];在高频端没有明显的容抗弧,意味者转移电阻很小;在低频端倾斜直线的角度大于45°,表明了Warburg阻抗的存在和典型的电容特性[16].另外,在100和2000次循环前后的交流阻抗图谱基本重合,意味着K-OMS-5电极的在K2SO4中得循环稳定性较好[17],这与恒流充放电所得结论是一致的.
2.2.4 漏电流和循环性能
漏电流是衡量电极材料的一个重要参数[18],漏电流主要来源于电解液的不可逆分解和电极材料表面官能团的反应[19].图7(a)是K-OMS-5电极的漏电流曲线,在一定电压下,充电电流随着时间的增加不断降低,在200s后趋于稳定,稳定后的电流即漏电流为0.008mA,表明该电极材料具有良好的电化学性能.循环性能是衡量电极材料的性能的另一重要参数,图7(b)是K-OMS-5电极在100mV·s-1时循环2000次的CV曲线,由图7(b)可知2000次循环前后CV曲线重现性较好,意味着该电极材料在K2SO4中具有良好的循环稳定性[20],这与交流阻抗所得结论是一致的.
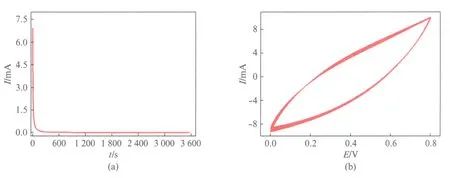
图7 (a) K-OMS-5电极在0.5molL-1 K2SO4中的漏电流曲线;(b) K-OMS-5电极在0.5molL-1 K2SO4中的循环性能曲线Fig.7 (a) Leakage current curve of K-OMS-5 electrode in 0.5molL-1 K2SO4; (b) Cycle life curve of K-OMS-5 electrode in 0.5molL-1 K2SO4
本论文以δ-MnO2为前驱体,KOH为嵌入离子源,采用水热沉积法制备了具有隧道结构的纳米K-OMS-5电极材料,研究了其在0.5molL-1Li2SO4、Na2SO4和K2SO4电解液中的电化学性能.研究结果表明,K-OMS-5材料在3种电解液中比电容的大小顺序依次为K2SO4>Na2SO4>Li2SO4,并且在0.5molL-1K2SO4电解液中具有良好的循环稳定性和可逆性.以上研究结果可能为后续更优性能的MnO2电极材料在电化学电容器的应用中提供帮助.
[1] 于峰,朱杨军,李莉,等.δ-MnO2的制备和电化学性能研究 [J].复旦学报(自然科学版),2015,54(4): 522-528.
[2] SIMON P, GOGOTSI Y. Materials for electrochemical capacitors [J].NatMater, 2008,7(11): 845-854.
[3] WANG G P, ZHANG L, ZHANG J J. A review of electrode materials for electrochemical supercapacitors [J].ChemSocRev, 2012,41(2): 797-828.
[4] THACKERAY M M. Manganese oxides for lithium batteries [J].ProgSolidStateChem, 1997,25(1): 1-71.
[5] 万厚钊,缪灵,徐葵,等.MnO2基超级电容器电极材料 [J].化工学报,2013,64(3): 801-813.
[6] GHODBANE O, PASCALJ L, FAVIER F. Microstructural effects on charge-storage properties in MnO2-based electrochemical supercapacitors [J].ACSAppl.Mater&Interfaces, 2009,1(5): 1130-1139.
[7] QU Q T, LI L, TIAN S,etal. A cheap asymmetric supercapacitor with high energy at high power: Activated carbon//K0.27MnO2·0.6H2O [J].JPowerSources, 2010,195,2789-2794.
[8] SHEN X F, DING Y S, LIU J,etal. Control of nanometer-scale tunnel sizes of porous manganese oxide octahedral molecular sieve nanomaterials [J].AdvMater, 2005,17(7): 805-809.
[9] 朱杨军,代芳,于峰,等.硝酸改性活性炭电极材料的电化学性能研究 [J].复旦学报(自然科学版),2014,53(1): 93-98.
[10] REDDY R N, REDDY R G. Sol-gel MnO2as an electrode material for capacitors [J].JPowerSource, 2003,124,330-337.
[11] QU Q T, ZHANG P, WANG B,etal. Electrochemical performance of MnO2nanorods in neutral aqueous electrolytes as a cathode for asymmetric supercapacitors [J].JPhysChemC, 2009,113(31): 14020-14027.
[12] BORGOHAIN R, LI J, SELEGUE J P,etal. Electrochemical study of functionalized carbon nano-onions for high-performance supercapacitor electrodes [J].JPhysChemC, 2012,116(28): 15068-15075.
[13] QU Q T, WANG B, YANG L C,etal. Study on electrochemical performance of activated carbon in aqueous Li2SO4, Na2SO4and K2SO4electrolytes [J].ElectrochemCommun, 2008,10(10): 1652-1655.
[14] 孙现众,张熊,张大成,等.活性炭基Li2SO4水系电解液超级电容器 [J].物理化学学报,2012,28(2): 367-372.
[15] 温祖标,刘亚菲,胡中华,等.薄层晶状α-MnO2/活性炭复合电极材料的制备和电化学性质 [J].化学学报,2010,68(15): 1473-1480.
[16] 闻斌,魏双,施展,等.稻壳多孔碳材料的电容性能及模型计算 [J].高等学校化学学报,2013,34(3): 674-678.
[17] FRACKOWIAK E, BEGUIN F. Carbon materials for the electrochemical storage of energy in capacitors [J].Carbon, 2001,39(6); 937-950.
[18] 李晶,赖延清,金旭东,等.超级电容器的制造工艺优化与性能研究 [J].电池工业,2010,15(10): 131-135.
[19] HSIEH C T, TENG H. Influence of oxygen treatment on electric double-layer capacitance of activated carbon fabrics [J].Carbon, 2002,40(5): 667-674.
[20] 朱杨军,代芳,谭军艳,等.OMS-5型纳米MnO2电极材料的制备与电化学性能研究 [J].兵器材料科学与工程,2016,39(2): 33-37.
Abstract: In this paper, δ-MnO2was synthesized with liquid oxidation-reduction method by using KMnO4, KOH and MnCl2at 25℃, and nanostructural K-OMS-5 was prepared by hydrothermal method treated the mixture of δ-MnO2and KOH at 180℃ for 2 day. X-ray diffraction, scanning electron microscopy, thermogravimetric analysis would be used to characterize the crystal structure, morphology, thermal stability of nanostructural K-OMS-5, respectively. The electrochemical performances were investigated by cyclic voltammetry, galvanostatic charge-discharge and electrochemical impedance spectroscopies, etc. The results show that the specific capacitance of K-OMS-5 is in the order of K2SO4>Na2SO4>Li2SO4at same scan rates or current density. K-OMS-5 as the electrode material both exhibits excellent cycling behavior in 2000 cycles of charge-discharge in 0.5 molL-1K2SO4electrolyte, which maybe have a promising prospect for application in electrochemical capacitors.
Keywords: electrochemical capacitors; electrode material; intercalation compounds; K-OMS-5
PreparationandElectrochemicalPerformancesofNanostructuredK-OMS-5IntercalationCompounds
WANG Junyi1, ZHU Yangjun1, DAI Fang2, SUO Xiaoyan1, YU Min1, ZHANG Lei1, WEN Zubiao1
(1.CollegeofChemistryandChemicalEngineering,JiangxiNormalUniversity,Nanchang330022,China; 2.NanchangInstituteofTechnology,Nanchang330099,China)
O646.54
A
0427-7104(2017)03-0314-07
2016-06-24
国家自然科学基金(21463013);江西省教育厅科技项目(GJJ160290);江西师范大学研究生创新基金(YJS2016080)
王君熠(1994—),女,硕士研究生;章 磊,女,副教授,通信联系人,E-mail: lzhang@jxnu.edu.cn;温祖标,男,副教授,E-mail: zbwen@jxnu.edu.cn.
