喹诺酮类先导化合物14a在大鼠体内的组织分布
2017-10-12孙文霞
樊 静, 孙文霞
(成都大学 四川抗菌素工业研究所, 四川 成都 610052)
喹诺酮类先导化合物14a在大鼠体内的组织分布
樊 静, 孙文霞
(成都大学 四川抗菌素工业研究所, 四川 成都 610052)
采用RP-HPLC法测定喹诺酮类先导化合物14a在大鼠体内各组织中的浓度及分布.将18只SD大鼠随机分成3组,分别按剂量85 mg/kg灌胃给药,在1 h、2 h和24 h时处死并迅速取出各组织,制成匀浆样品,测定各组织中的药物浓度.结果显示,大鼠灌胃给药14a后迅速分布在各组织中,且在肝、肾、肺中浓度高于其他组织.实验表明,14a吸收较快,在组织中分布广且无蓄积.
喹诺酮类先导化合物14a;组织分布;反相高效液相法
0 引 言
喹诺酮类先导化合物14a(1-环丙基-6-氟-1,4-二氢-8-甲氧基-7-(3-氨基-4-烷氧亚胺基-1-哌啶基)-4-氧代-3-喹啉羧酸)为喹诺酮类化合物巴罗沙星C-7位的3-甲氨基哌啶基引入甲氧亚胺基结构得到的一种新的先导化合物[1].相关的体内和体外实验表明,14a与已上市的喹诺酮类药物相比,表现出更优的抗菌活性[2-4].对此,本研究采用RP-HPLC法测定大鼠灌胃14a后在不同时间点各组织中14a的浓度,分析了14a在大鼠各组织中的分布,拟为14a的药物代谢动力学分析提供进一步的实验依据.
1 实 验
1.1 仪器与试药
1)实验所用仪器.LC-10AT型高效液相色谱仪(岛津公司),N-2000型双通道数据工作站(浙江大学智能信息工程有限公司),XW-80A型涡流混合仪、匀浆机(海门其林贝雨仪器制造有限公司),80-2型离心沉淀器(上海仪器厂),Sartorius BS 224S型电子天平、FE20型pH计(梅特勒—托利多仪器有限公司).
2)实验所用试药.14a对照品(含量,99.94%)、内标莫西沙星对照品(含量,99.31%),由四川抗菌素工业研究所提供;色谱级二氯甲烷(批号,20140213),由国药集团化学试剂有限公司提供;乙腈为色谱纯;水为双蒸水,其他试剂为分析纯.
1.2 方法与结果
1.2.1 色谱条件.
实验色谱条件:色谱柱为Sinochrom C18ODS-AP(4.6 mm×200 mm,5 μm,大连依利特科学仪器有限公司);流动相为乙腈—水(21∶79,加0.2%三乙胺后用磷酸调pH至2.80);检测波长为307 nm;流速为1 mL/min;柱温为40 ℃;进样量为20 μL.
1.2.2 溶液的配制.
精密称取14a对照品25.0 mg,置25 mL量瓶中,以蒸馏水配制成浓度为1 mg/mL溶液,作为对照品储备液;精密称取莫西沙星对照品2.5 mg,置于25 mL容量瓶中,加蒸馏水配制成0.1 mg/mL溶液,作为内标储备液.
1.2.3 实验动物.
健康SD大鼠18只,购自达硕生物科技有限公司(SCXK(川)70B-24),雌雄各半,体重200~220 g,实验前适应性圈养一周.
1.2.4 生物样品的采集.
18只SD大鼠,随机均分成3组,每组6只,雌雄各半.实验前禁食12 h,自由饮水,按85 mg/kg灌胃给药,分别于1 h、2 h和24 h时断颈处死,迅速取出心、肝、脾、肺、肾、肠、胃、骨骼肌、睾丸、子宫、大脑和脂肪等组织,用蒸馏水洗净,滤纸吸干,称重,加生理盐水均浆制成匀浆样品,于-20 ℃保存备用.
1.2.5 样品前处理.
精密量取组织匀浆样品200 μL,加入5 μL内标溶液,混匀, 加入二氯甲烷1 mL, 涡流提取1 min,3 000 r/min离心10 min,吸取下层有机相600 μL,37 ℃水浴氮气吹干,残渣加200 μL流动相复溶,过滤,取20 μL进样,以内标法按标准曲线计算14a浓度.
1.2.6 方法的专属性.
按“1.2.1”项条件下测得的色谱图中(见图1),化合物14a和内标物的峰形良好,分离度为5.186,分离完全,内源性杂质峰无干扰,理论塔板数以14a计大于9 000.
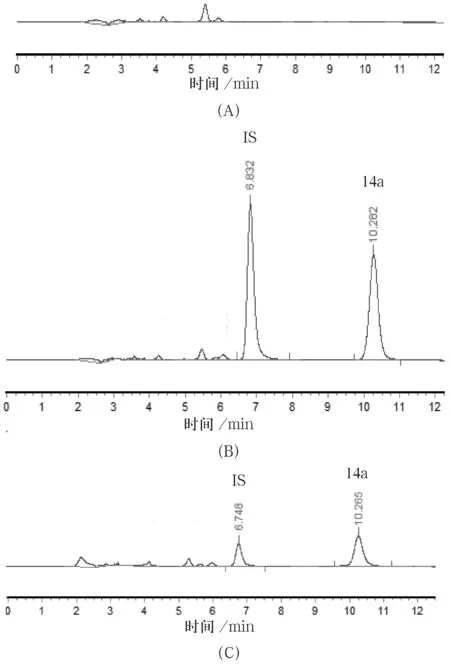
图1心空白组织匀浆(A)、心空白组织匀浆加入14a和莫西沙星内标(B)和心匀浆样品加入莫西沙星内标(C)的色谱图
1.2.7 标准曲线及定量限.
精密量取空白组织匀浆200 μL,分别加入14a对照品溶液10 μL和内标溶液5 μL,配制成14a浓度分别为0.25、0.50、2.50、5.00、7.50、15.00 μg/mL的组织匀浆样品和血浆样品,按“1.2.5"项下方法处理后测定,以14a峰面积(A14a)与内标峰面积(AIS)的比值对14a浓度(C)进行线性回归,得到回归方程及线性范围,具体如表1所示.
结果表明,各组织样品在0.25~10.00 μg/mL浓度范围内14a与内标峰面积比值的线性关系良好,定量限为0.25 μg/mL.
1.2.8 回收率及精密度.
取空白组织匀浆,按“1.2.7"项下方法,配制成含14a浓度为0.50、5.00、7.50 μg/mL的QC样品各5份,按“1.2.5"项下方法处理后测定,测得14a峰面积为A1;另取14a对照品溶液适量,以流动相配制成14a浓度为0.50、5.00、7.50 μg/mL的标准液,取20 μL进样分析,测得14a峰面积为A2.

表1 14a在大鼠各组织样品的线性
计算14a在各组织中的提取回收率(%)(A1/A2×100%).将QC样品测得的峰面积比(A14a/AIS)代入标准曲线求出各组织的14a药物浓度C1,并与QC样品的已知浓度C2相比,从而求得各种组织中14a的方法回收率,计算结果见表2.

表2 14a在各组织中的精密度和回收率(n=5)
1.2.9 14a的组织分布.
将采集的组织样品匀浆,按“1.2.5”项下方法测定,得到不同时间点各组织的药物浓度,结果见表3和图2.结果表明,14a在各组织中均有分布,其中在肝、肺、肾中浓度较高.

表3 大鼠各组织中14a的分布
注:“nd”为未检出.

图2 14a在大鼠各组织中的分布(n=6)
2 讨 论
实验发现,使用Sinochrom C18ODS-AP色谱柱分离测定时,内标和14a分离较好,但内标和14a均有一定程度的拖尾,尤其是14a拖尾明显.经实验,加入一定量的扫尾剂三乙胺可以改善峰形,三乙胺的加入量以0.2%为佳.14a的最大吸收峰在波长273 nm处,在波长307 nm和362 nm处有次要吸收峰.由于在波长273 nm处溶剂与组织匀浆中引入的杂质干扰了测定,很难达到基线分离.经实验,将测定波长定为307 nm.
前期,本研究对14a在大鼠体内的药动学进行了初步分析,发现14a在大鼠体内的Tmax为1.5~2 h,因而组织分布的采集时间点确定为1 h,2 h和24 h:大鼠灌胃给药后,1 h时各组织中14a的浓度最高,2 h次之,24 h时几乎检测不到,此说明14a在组织中无蓄积.此外,在大鼠各组织中,14a分布较广但浓度有差异,其中在胃、肠、肺、肝、肾中浓度较高,心、脾、生殖腺、肌肉、脂肪、脑中浓度较低,给药后1 h时,胃、肠分布较多,此与文献报道的其他喹诺酮类药物的组织分布相似[5-9].另外,给药1 h后,大鼠脑组织中均能检测出少量的14a,说明14a具有一定的脂溶性,可少量地通过血脑屏障进入大脑.
[1]卞其龙,程强,孙文霞,等.RP-HPLC测定犬血浆中的喹诺酮类先导化合物14a[J].中国抗生素杂志,2015,30(1):59-61.
[2]蒋晓磊,催玉彬,曹胜华,等.喹诺酮类抗菌药物研究新进展[J].中国抗生素杂志,2011,36(4):255-263.
[3]夏蕊蕊,国宪虎,张玉臻,等.喹诺酮类药物及细菌对其耐药性机制研究进展[J].中国抗生素杂志,2010,35(4):255-261.
[4]王秀云,郭强,王玉成,等.7-(3-氨基-4-烷氧亚胺基-1-哌啶基)喹诺酮类化合物的合成与抗菌作用[J].药学学报,2008,43(8):819-827.
[5]Turnpenny P,Padfield A,Barton P,et al.BioanalysisofpseudomonasaeruginosaalkylquinolonesignallingmoleculesininfectedmousetissueusingLC-MS/MS;anditsapplicationtoapharmacodynamicevaluationofMvfRinhibition[J].J Pharm Biomed Anal,2017,139:44-53.
[6]Ren L P,Zhao H Y,Chen Z L.Studyonpharmacokineticandtissuedistributionoflycorineinmiceplasmaandtissuesbyliquidchromatography-massspectrometry[J].Talanta,2014,119:401-406.
[7]黄伟.加替沙星在大鼠体内的组织分布[J].儿科医学杂志,2006,12(2):3-5.
[8]Vishwanathan K,Bartlett M G,Stewart J T.Determinationofmoxifloxacininhumanplsmabyliquidchromatographyelectrosprayionizationtandemmassspectrometry[J].J Pharm Biomed Anal,2002,30(4):961-968.
[9]宋坤改,孙涛,林赴田,等.甲磺酸左氧氟沙星大鼠体内分布和血清蛋白结合率[J].中国抗生素杂志,1999,24(3):208-210.
Abstract:The paper adopts the RP-HPLC method to detect the concentration and distribution of 14a in different tissues in rats.18 SD rats are randomly divided into 3 groups,intragastric administration of 85 mg/kg are done on these rats respectively.Take out tissues from the rats quickly and make the homogenate samples the minute the rats are dead in 1 h,2 h and 24 h.HPLC is used for the determination of drug concentration in various tissues.The results show that after the intragastric administration is done on rats,14a is rapidly distributed to all tissues,and the amount of 14a in liver,kidney,and lung is higher than that in other tissles.The conclusion drawn from the paper is that 14a is quickly absorbed and extensively distributed without accumulation.
Keywords:Quinolones leading compounds 14a;tissues distribution;RP-HPLC
TissuesDistributionofQuinolonesLeadingCompound14ainRats
FANJing,SUNWenxia
(Sichuan Industrial Institute of Antibiotics, Chengdu University, Chengdu 610052, China)
R969.1;TQ460.7+2
A
2017-05-17.
成都大学校青年基金(2015XJZ07)资助项目.
樊 静(1983 — ), 女, 研究实习员, 从事药物代谢动力学研究.
