pDNA-巯基壳聚糖纳米粒的制备及Box-Behnken效应面法工艺优化
2017-10-11曾皓月王之方美娟王立强
曾皓月, 王之, 方美娟, 王立强
(1. 华侨大学 生物医学学院, 福建 泉州 362021;2. 兰州军区总医院 临床药学科, 甘肃 兰州 730000;3. 厦门大学 药学院, 福建 厦门 361000)

pDNA-巯基壳聚糖纳米粒的制备及Box-Behnken效应面法工艺优化
曾皓月1, 王之2, 方美娟3, 王立强1
(1. 华侨大学 生物医学学院, 福建 泉州 362021;2. 兰州军区总医院 临床药学科, 甘肃 兰州 730000;3. 厦门大学 药学院, 福建 厦门 361000)
以巯基壳聚糖(TCS)为基因载体,采用离子交联法制备能用于基因口服研究的质粒DNA-巯基壳聚糖纳米粒(pDNA-TCS-NPs).分别以TCS质量浓度、三聚磷酸钠(TPP)质量浓度、pH值和转速为考察对象,以pDNA-TCS-NPs粒径和Zeta电位为评价指标,采用4因素3水平Box-Behnken 效应面法筛选最佳制备工艺,并对其外观形态,包封率等体外性质进行考察.结果表明:TCS质量浓度为0.80 mg·mL-1,TPP质量浓度为0.65 mg·mL-1,pH=5.3,转速为2 000 r·min-1是最优制备工艺,可制得粒径为(134.21±1.34) nm,Zeta电位为(24.36±0.29) mV,包封率在(80.26±0.56)%,形状规则且分散良好的pDNA-巯基壳聚糖纳米粒;Box-Behnken 实验设计可用于预测和优化pDNA-TCS-NP制备工艺优化筛选.
巯基壳聚糖; 质粒DNA; 纳米粒; Box-Behnken效应面法; 离子交联法; 工艺优化
Abstract: Preliminary exploration to prepare plasmid DNA-loaded thiolated chitosan nanoparticles (pDNA-TCS-NPs) which can be used for gene oral administration was investigated. Using TCS as gene carriers, the pDNA-TCS-NPs were prepared by the ionic cross-linking method. The effects of the concentrations of TCS and TPP, pH value and stirring speed were investigated on the particle diameter and zeta potential of the pDNA-TCS-NPs. In addition, the formula was optimized by Box-Behnken design and response surface method with four factors and three levels, and the physic-chemical properties such as the shape and encapsulation efficiency were also studied. The results showed that the optimal formula was as follows: TCS concentration 0.80 mg·mL-1, TPP concentration 0.65 mg·mL-1, pH 5.3, and stirring speed 2 000 r·min-1. Particle diameter was (134.21±1.34) nm, zeta potential was (24.36±0.29) mV, and efficiency was (80.26±0.56)%.under the optimal conditions. The pDNA-TCS-NPs showed uniform spherical solid particles with regular shape and ideal uniformly dispersion. It′s also confirmed that the Box-Behnken experimental design and response surface method could be used to predict and optimize the pDNA-loaded TCS nanoparticles.
Keywords: thiolated chitosan; plasmid DNA; nanoparticle; Box-Behnken design and response surface method; ionic cross-linking method; formula optimization
如何用药学技术手段提高口服基因药物在体内外的稳定性,从而提高口服基因转染效率,是当前口服基因治疗的首要问题[1-2].通过采用高分子材料制备出直径1 000 nm以内的纳米粒.以此构建出非病毒口服基因药物递送系统,因其具有提高基因药物稳定性,促进生物膜的转运和吸收,且靶向性、顺应性好等诸多优点已成为一大研究热点[3].与使用其他非病毒纳米粒制备的载体相比,以巯基壳聚糖为基础的口服纳米递送系统,具有以下3个主要特点:1) 巯基壳聚糖中游离的巯基经氧化可形成二硫键,其结合力远强于静电效应可提高载体的胞外稳定性[4];2) 巯基壳聚糖上的巯基通过与肠黏膜和肠上皮细胞表面富含半胱氨酸残基的粘蛋白形成二硫键,发挥黏附作用延长所载药物滞留时间,促进药物吸收;3) 当其入胞后,在细胞内谷胱甘肽的参与下,破坏其二硫键,将基因药物与载体解离令目的基因得以释放[5-6].响应曲面法(RSM)是通过对实验设计的因素进行考察,对其相关关系进行分析,从而确定出最佳实验方案,并利用计算机技术进行数据分析的优化方法.目前,最常用有星点设计法(CCD),Box-Behnken Design(BBD)法等[7].本文通过采用 Box-Behnken效应面法,对质粒DNA-巯基壳聚糖纳米粒(pDNA-TCS-NPs)的制备工艺进行优化.
1 材料与方法
1.1仪器与试剂
微量紫外分光光度计(美国Thermo公司);集热式磁力搅拌器(河南省巩义市华仪仪器有限公司);台式高速离心机(美国Thermo公司);Malvern ZEN-3600型粒径测试仪(英国马尔文公司);LGJ-18S型冷冻干燥机(北京松源华兴科技有限公司);透射电镜(日本Nikon公司).
巯基壳聚糖(华侨大学实验室提供);三聚磷酸钠(分析纯,上海国药集团化学试剂有限公司);增强型绿色荧光蛋白质粒基因(pDNA,5.3 kb,华侨大学实验室扩增和提纯);其余常规试剂(上海国药集团化学试剂有限公司).
1.2pDNA-TCS-NPs的制备
采用离子交联法制备质粒DNA-巯基壳聚糖纳米粒(pDNA-TCS-NPs).取适量巯基壳聚糖,缓慢加入0.1 mol·L-1的醋酸溶液,在37 ℃下搅拌溶解,并调节其pH值,制备出巯基壳聚糖溶液;然后,向溶液中缓慢加入1 μg的pDNA,另取适量的TPP溶于去离子水中,将TPP溶液以15 滴·min-1的速度缓慢加入到巯基壳聚糖溶液中,搅拌30 min,于超纯水中透析36 h(截留相对分子质量为3.5 u),冻干可得pDNA-TCS-NPs.
1.3pDNA-TCS-NPs体外性质初步评价
1.3.1 形态测定 采用复染法对其形态进行测定,吸取适量浓缩pDNA-TCS-NPs溶液置于铜网中,使用磷钼酸铵溶液进行负染,待其风干后,采用透射电镜拍摄纳米粒的形态.
1.3.2 粒径与Zeta电位的测定 使用去离子水对经过透析浓缩的pDNA-TCS-NPs悬液进行稀释,采用马尔文粒径测试仪测量其粒径(d)和Zeta电位(E).
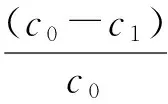
1.4Box-Behnken效应面法优化
选取对pDNA-TCS-NPs粒径和电位影响较为显著的4个因素,即TCS质量浓度(A),TPP质量浓度(B),pH值(C),转速(D),在3个水平上进行优化研究.效应面因素水平,如表1所示.

表1 效应面因素水平表Tab.1 Factors and levels of response surface method
2 实验结果与分析
2.1Box-Behnken效应面法设计结果
2.1.1 拟合方程 以Y1(粒径,d)和Y2(电位,E)为相应指标,进行29个实验点的优化实验,结果如表2所示.

表2 Box-Behnken 实验设计及响应值Tab.2 Box-Behnken experimental design and response values
利用Design-Expert 8.0软件,对设计实验结果(表2)进行分析.以粒径Y1作为因变量,通过拟合,得出的方程为
以电位Y2作为因变量,通过拟合,得出的方程为
2.1.2 效应面优化与预测 根据拟合方程的相关系数可知,该模型拟合度良好,可以用来作为TCS-NP的分析和预测,结果如表3所示.
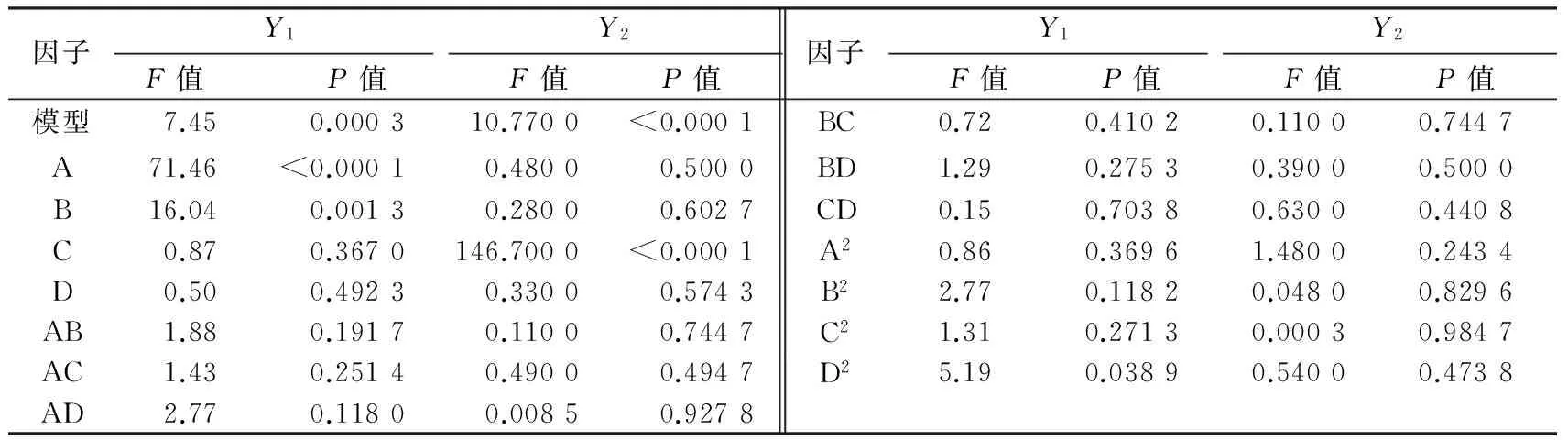
表3 检测回归方程中系数的显著性Tab.3 Significance test of coefficient in regressionequation
根据拟合方程(1),(2),运用Design-Expert 8.0软件,绘制因素A(ρ(TCS)),B(ρ(TPP)),C(pH),D(n)对Y1(d),Y2(E)的响应面图[7],如图1所示.
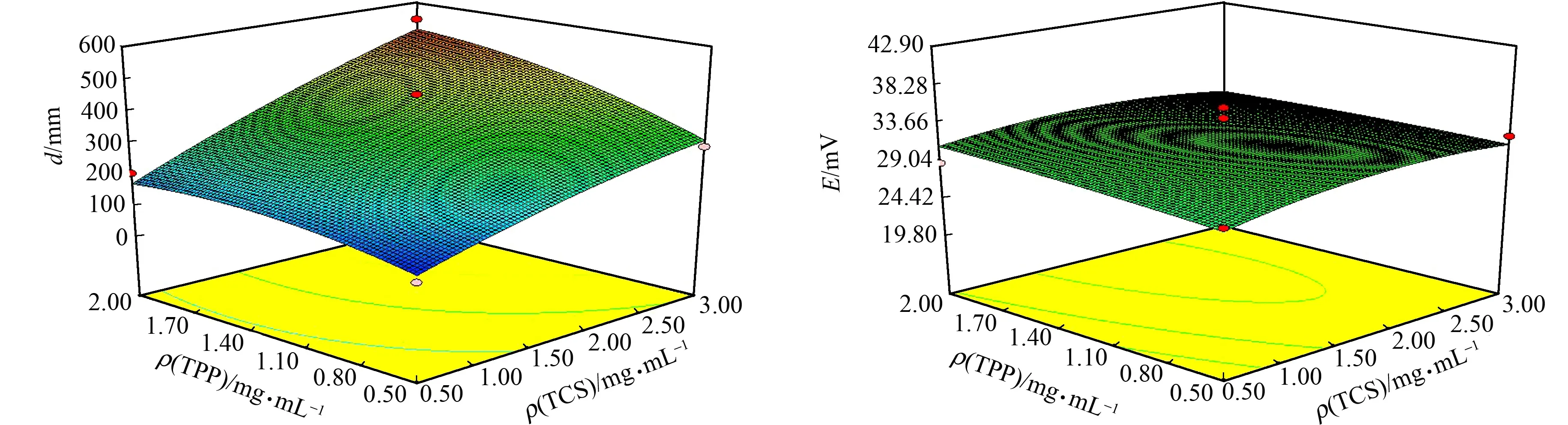
(a) A-B-Y1 (b) A-B-Y2

(c) A-C-Y1 (d) A-C-Y2

(e) A-D-Y1 (f) A-D-Y2
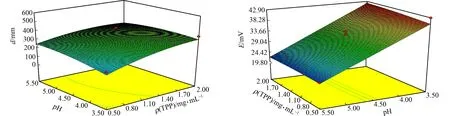
(g) B-C-Y1 (h) B-C-Y2
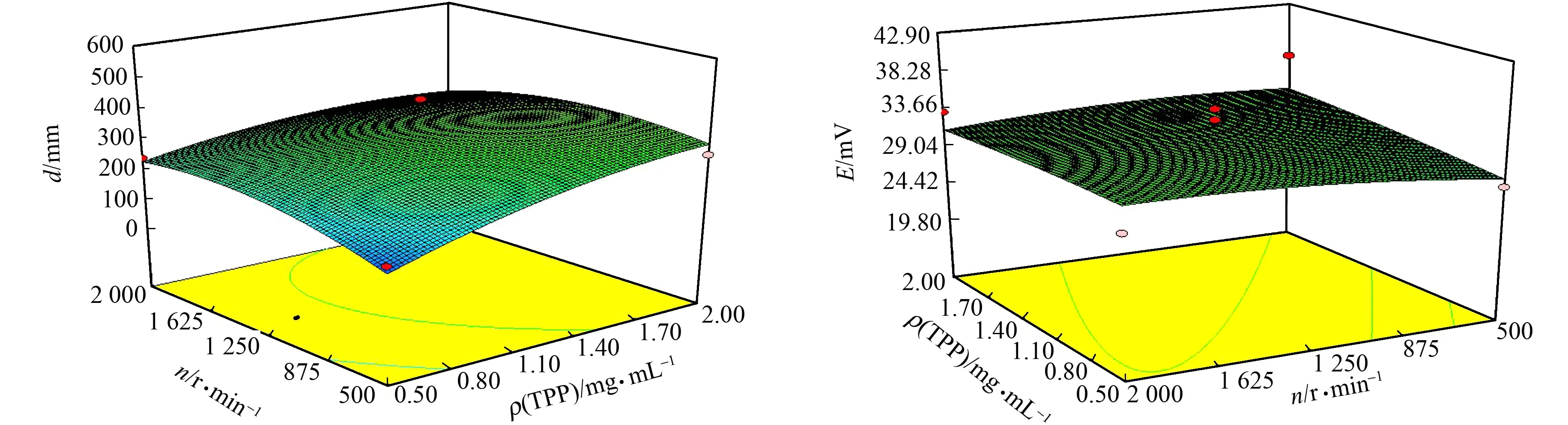
(i) B-D-Y1 (j) B-D-Y2

(k) C-D-Y1 (l) C-D-Y2图1 各因素与响应值的三维图Fig.1 Three-dimensional plot of independent factors and response values
根据实验结果选定适当的评价指标范围,可以得到最优制备工艺,即TCS质量浓度为0.82 mg·mL-1,TPP质量浓度为0.67 mg·mL-1,pH值为5.27,转速为1 992.23 r·min-1,则由此可预测粒径为130.215 nm,电位为25 mV.

图2 pDNA-TCS-NPs纳米粒透射电镜照片Fig.2 SEM photograph of plasmid DNA-loaded thiolated chitosan nanoparticles
2.1.3 优化工艺验证 为验证最优制备工艺及模型的准确性,并考虑实际操作的可行性,将各个处方因素进行细微调整,即TCS质量浓度为0.80 mg·mL-1,TPP质量浓度为0.65 mg·mL-1,pH值为5.3,转速为2 000 r·min-1.按照上述工艺制备出3批pDNA-TCS-NPs,并对其粒径、电位、包封率进行测试,可得粒径为(134.21±1.34) nm,电位为(24.36±0.29) mV,包封率为(80.26±0.56)%.通过透射电镜观察pDNA-TCS-NPs,发现其外观为较规则的圆形,如图2所示.
3 讨论
对壳聚糖进行化学修饰,能够进一步改善壳聚糖基因药物运输载体的稳定性、运输效率及转染效率等性能.Jiang等[8]通过对聚乙二醇壳聚糖接枝聚乙烯亚胺,制备出可用于肝细胞的基因药物运输载体.Kwon等[9]采用叶酸修饰壳聚糖,制备出能够在叶酸阳性受体细胞表达的基因药物载体.研究采用经巯基修饰的壳聚糖,制备出可用于口服的纳米药物运输载体.
在进行多变量多水平的实验设计时,采用Box-Behnken 效应面法,可以考察各变量间交互作用.该方法与中心复合设计法相比,具有试验次数少、节约成本的特点,还避免了由于正交设计和均匀设计试验所引起的无法精确得到最佳点的问题[10].
选择pDNA-TCS-NPs粒径和Zeta电位作为评价标准,对其制备工艺进行改善.结果表明:在一定范围内,pDNA-TCS-NPs粒粒径大小与巯基壳聚糖质量浓度关系呈正相关,TCS质量浓度高,高分子数目增多,增强了分子间凝聚作用,所以pDNA-TCS-NPs粒粒径变大.在低质量浓度TCS下,TPP质量浓度变化对粒径的影响不大;但在高质量浓度下,纳米粒粒径随着TPP质量浓度呈现出正相关关系.因为在合适的质量浓度下,微粒间的接触增加利于发生交联,从而可通过调节TCS与TPP的质量浓度来改变纳米粒的粒径.
TCS纳米粒的电位则主要与溶液pH值有关.纳米粒电位随着pH值的降低而增大,pH值较低时,聚合物电离程度高,便于其与TPP反应,形成小粒径纳米粒.文中所制备的纳米粒呈较为规则的球形,包封率良好,用于细胞和动物模型均得到理想的实验预期,保证了体内外的稳定性.说明该纳米粒在口服基因领域的独特优势,后期可研究其胞内转运的相关机制.
[1] MENZEL C,BONENGEL S,De SOUSA I P,etal.Preactivated thiolated nanoparticles: A novel mucoadhesive dosage form[J].International Journal of Pharmaceutics,2015,497(1/2):123-128.DOI:10.1016/j.ijpharm.2015.11.037.
[2] HE Chunbai,YIN Lichen,TANG Cui,etal.Multifunctional polymeric nanoparticles for oral delivery of TNF-α siRNA to macrophages[J].Biomaterials,2013,34(11):2843-2854.DOI:10.1016/j.biomaterials.2013.01.033.
[3] HAMIDI M,AZADI A,RAFIEI P.Hydrogel nanoparticles in drug delivery[J].Advanced Drug Delivery Reviews,2008,60(15):1638-1649.DOI:10.1016/j.addr.2008.08.002.
[4] Jr DUBENSK T W,LIU M A,ULMER J B.Delivery systems for gene-based vaccines[J].Molecular Medicine,2000,6(9):723-732.
[5] BERNKOP-SCHNÜRCH A,GUGGI D,PINTER Y.Thiolated chitosans: Development andinvitroevaluation of a mucoadhesive, permeation enhancing oral drug delivery system[J].Journal of Controlled Release,2004,94(1):177-186.DOI:10.1016/j.jconrel.2003.10.005.
[6] FÖGER F,SCHMITZ T,BERNKOPSCHNÜRCH A.Invivoevaluation of an oral delivery system for P-gp substrates based on thiolated chitosan[J].Biomaterials,2006,27(23):4250-4255.DOI:10.1016/j.biomaterials.2006.03.033.
[7] 张南生,孙卫军,郭虹,等.Box-Behnken Design效应面法在制剂处方优化中的应用[J].中国医药导报,2015,12(23):34-37.
[8] JIANG H L,KWON J T,KIM E M,etal.Galactosylated poly (ethylene glycol)-chitosan-graft-polyethylenimine as a gene carrier for hepatocyte-targeting[J].Journal of the Controlled Release Society,2008,131(2):150-157.DOI:10.1016/j.jconrel.2008.07.029.
[9] KWON O J,KANG E,CHOI J W,etal.Therapeutic targeting of chitosan-PEG-folate-complexed oncolytic adenovirus for active and systemic cancer gene therapy[J]. Journal of the Controlled Release Society,2013,169(3):257-265.DOI:10.1016/j.jconrel.2013.03.030.
[10] 王芳,翟文婷,李艳丽,等.Box-Behnken效应面法优化穿心莲内酯-PLGA微球处方研究[J].中草药,2013,44(13):1743-1747.DOI:10.7501/j.issn.0253-2670.2013.13.009.
(责任编辑: 陈志贤英文审校: 刘源岗)
PreparationofpDNA-LoadedThiolatedChitosanNanoparticlesandOptimizationbyUsingBox-BehnkenDesignandResponseSurfaceMethod
ZENG Haoyue1, WANG Zhi2, FANG Meijuan3, WANG Liqiang1
(1. School of Biomedical Sciences, Huaqiao University, Quanzhou 362021, China; 2. Department of Clinical Pharmacy, General Hospital of Lanzhou Military Command, Lanzhou 730000, China;3. School of Pharmaceutical Sciences, Xiamen University, Xianmen 361000, China)
10.11830/ISSN.1000-5013.201703054
2017-03-17
王立强(1970-),男,教授,博士,主要从事药剂学和药物开发的研究.E-mail:wlq1599@163.com.
国家自然科学基金资助项目(81302652); 福建省自然科学基金资助项目(2015J01342)
R 944
A
1000-5013(2017)05-0676-06
