抗CD20单抗在致敏受者异基因造血干细胞移植中的应用
2017-10-09杨金慧
李 丹,王 易,杨金慧
(1.山西省太钢总医院,山西太原030003; 2.苏州大学附属儿童医院,江苏苏州215003)
抗CD20单抗在致敏受者异基因造血干细胞移植中的应用
李 丹1,王 易2,杨金慧1
(1.山西省太钢总医院,山西太原030003; 2.苏州大学附属儿童医院,江苏苏州215003)
目的:探讨抗CD20单抗(美罗华)在致敏受者造血干细胞移植预处理中应用后的脱敏效果。方法:5例致敏患儿中3例在造血干细胞移植预处理前应用美罗华。对比观察脐血移植后造血重建、供受体DNA短串联重复序列多态性分析嵌合度及有无移植物抗宿主病(GVHD)发生。结果:5例患儿造血干细胞移植后造血完全重建,编号2(未用美罗华)造血重建时间(造血干细胞移植后65 d)明显晚于预处理前使用美罗华患儿(编号3、4、5);其中2例出现血小板植入延迟,编号1(未用美罗华)血小板植入时间较编号4(经美罗华处理患儿)明显延长;5例供受体稳定嵌合;编号1(未用美罗华)出现极重度aGVHD,造血干细胞移植前应用美罗华患儿未出现或仅出现轻至中度aGVHD,编号4出现轻度cGVHD,累及胃肠道,经FK506调整后已明显好转。目前随访中位时间7.5个月,病情稳定。结论:美罗华在致敏受者异基因造血干细胞移植前应用对降低敏感性有一定疗效。
异基因造血干细胞移植;致敏受者;抗CD20单抗
某些血液系统性疾病如再生障碍性贫血、地中海贫血等均依赖长期输血,造血干细胞移植是根治此类疾病的有效方法[1-2]。部分患者由于多次输血,致使体内预存抗HLA抗体及MICA抗体,此类抗体的存在可导致造血干细胞移植术后造血系统重建失败或各种难以逆转的移植物抗宿主病,所以有学者认为输血致敏是引起移植失败的重要因素之一[3]。随着对抗体介导排斥反应发生机制研究的进展,近年来针对B细胞表面抗原的新型药物不断出现,使高致敏患者成功接受造血干细胞移植成为可能。美罗华是一种对B细胞上特有的CD20抗原具有高亲合力的单克隆抗体,本文探讨该抗体对致敏患儿脱敏的疗效。
1 资料与方法
1.1 一般资料
接受造血干细胞移植术者5例(按造血干细胞回输时间先后编号为1~5)。男2例,女3例;中位年龄11岁。原发病急性白血病(M2)1例(编号1),再生障碍性贫血4例。其中编号2患儿骨髓涂片诊断再生障碍性贫血,骨髓活组织检查提示骨髓增生异常综合征可能,环孢素正规治疗后仍三系血细胞(红细胞、白细胞、血小板)减少;编号3系阵发性睡眠性血红蛋白尿-再生障碍性贫血综合症,经保守治疗效果不佳;编号4系重型再生障碍性贫血,经丙种球蛋白、环孢霉素及两次抗淋巴细胞免疫球蛋白治疗均无效,移植前有铁过载并行祛铁治疗;编号5系极重型再生障碍性贫血,经环孢霉素及一次抗淋巴细胞免疫球蛋白治疗效果不理想。供、受者在移植前均进行HLA和MICA基因分型、HLA和MICA混合抗体及特异性抗体检测。所有受者均在移植后接受随访。
1.2 方 法
1.2.1 致敏预存抗体检测 由江苏省血研所(美国ASHI认证实验室)采用序列特异寡核苷酸探针(PCR—SSOP)法进行HLA和MICA基因分型、免疫磁珠液相芯片技术检测抗HLA抗体和MICA抗体。HLA-I类和HLA-Ⅱ类混合抗体阳性的标准是阳性与阴性抗原磁珠的比值>1.5,MICA混合抗体阳性标准是阳性与阴性抗原磁珠的比值>2.5。 HLA-I类特异性抗体检测包括 HLA-A、HLA-B、HLA-Cw,HLA-Ⅱ特异性抗体检测包括HIA-DRBl、HLA-DQBl,特异性抗体百分率≥10%为阳性。
1.2.2 造血干细胞移植情况 造血干细胞移植受者1例输注同胞全相合外周造血干细胞,1例输注同胞全相合骨髓,2例输注双份无血缘全相合脐血,1例输注双份无血缘4/6相合脐血。具体情况见表1。脐血均来自于上海脐带血造血干细胞库,且均经细胞培养、脐血本身及母亲血传染病检测,冻存干细胞复温后于当天回输。2例HLA抗体和MICA抗体阳性受者患儿(编号3、4)于造血干细胞移植预处理第1天单次应用美罗华,编号5用美罗华后因HLA-A抗体滴度下降不理想加用1次,并行血浆置换。美罗华应用方法:美罗华375 mg/m2,静脉点滴 6~8 h,滴速为 50 mg/h,以每30 min增加25 mg/h的幅度逐步加量,直至最大滴速400 mg/h。输注美罗华前给予异丙嗪及甲泼尼龙,甲泼尼龙与美罗华同步维持静脉点滴,在移植预处理第一天使用。在静脉滴注美罗华过程中密切观察有无不良反应,如发生不良反应,暂时减慢或停止输注。
1.2.3 移植后造血重建的监测 定期评估造血重建及供受体嵌合DNA短串联重复序列(STR)。评估造血重建标准:中性粒细胞连续3 d≥0.5×109/L为粒细胞植入;血小板连续7 d≥20×109/L为血小板植入;血小板植入时间延长:血小板植入时间晚于移植后30 d;继发性血小板植入失败:在血小板原发植入后,出现血小板水平再次下降至植入标准以下(低于20×109/L)并再次依赖血小板输注。供受体嵌合度评估:根据供者来源的造血细胞植入状态,一般将造血嵌合体分为3种类型:当供者细胞占据受者的骨髓或外周血百分比>95%时,即供者细胞完全植入时,称为完全嵌合;若移植后受者细胞仍出现在骨髓或外周血中,可以同时检测到供者和受者两种细胞成分,供者细胞占5%~95%,称为混合嵌合;微嵌合则是指供者细胞<5%。
1.2.4 移植后并发症评估 造血干细胞移植后并发症主要包括移植物抗宿主病、植入综合症等。按照西雅图Glucksberg分级系统与国际骨髓移植登记处(IBMTR)积分法判断aGVHD严重程度。
2 结果
2.1 造血干细胞移植前输血量及预存HLA抗体和MICA抗体情况
患儿造血干细胞移植前输注成分血的情况见表2。移植前HLA抗体阴性1例(编号2);HLA混合抗体阳性,但HLA特异性抗体未能分离1例(编号3);HLA混合抗体及特异性抗体均阳性2例(编号1、5);仅HLA-Ⅱ类特异性抗体阳性1例(编号 4);MICA 抗体阳性 2例(编号 2、4),具体致敏抗体种类及见表3。

表1 5例患儿基本情况

表2 患儿造血干细胞移植前输血情况
2.2 不良反应
3例患儿应用美罗华过程顺利,输注前后均无过敏反应及低热、低血压、心动过速等不良反应。
2.3 造血干细胞移植后造血重建时间
5例患儿造血功能均成功重建,2例患儿出现血小板植入延迟(编号1、4),编号1患儿血小板植入时间较编号4明显延长,编号2造血重建时间(造血干细胞移植后65 d)明显晚于预处理前使用美罗华患儿(编号3、4、5)。结果见表4。
2.4 移植后并发症评估结果
编号4和编号5于造血干细胞移植后1 w左右出现植入综合症,经糖皮质激素处理后好转。由表5可以看出,编号1出现极重度aGVHD,造血干细胞移植前应用美罗华患儿(编号3、4、5)未出现或仅出现轻至中度aGVHD。截止2012年10月20日,随访中位时间为7.5个月,100 d内均无aGVHD复发,病例4出现轻度cGVHD,累及胃肠道,经FK506调整后已明显好转,余4例均未出现cGVHD。5例患儿均在免疫抑制剂减量阶段。结果见表5。
3 讨论
1958年Dausset等发现多次接受输血的患者存在不同特异性的白细胞抗体,用这些抗体所鉴定出的不同特异性白细胞抗原,称为人类白细胞抗原(human leucocyte antigen,HLA)。HLA 分子的主要生理作用是将抗原递呈给T细胞,对诱导体液及细胞免疫反应起重要作用。由于红细胞、淋巴细胞和血小板表面存在HLA抗原,人可因妊娠或多次输血等原因使受血者体内产生HLA抗体。MICA基因属于非经典HLA-I类样分子,其组成、表达和产物与HLA-I类基因不同。由MICA介导的排斥反应常表现为血管内皮细胞的破坏和重塑,出现血管特征性的结构改变,最终可能导致血管的完全闭塞[4],这种表现多在慢性排斥中发现。HLA抗体与MICA抗体的存在不仅直接导致造血干细胞移植后出现移植物抗宿主病,也会引起造血重建不良,进而影响患者的总体预后。
19世纪七十年代,国外有学者对再生障碍性贫血进行骨髓移植中发现,移植前受者体内存有致敏抗体组比无致敏抗体组易于发生骨髓移植后排斥反应,并认为此致敏抗体可作为预测造血干细胞移植排斥的一项指标[5]。同时也有研究表明,致敏与急、慢性排斥反应、供者干细胞植入及长期存活率均有密切关系[6]。本研究中编号1脐血移植后血小板植入显著延迟,发生Ⅳ级GVHD可能与移植前预存混合性及特异性HLA-I、Ⅱ抗体且未予干预治疗和行双份4/6相合脐血移植均有关系;编号4、5患儿在脐血移植前筛查示致敏抗体阳性,尽管输注双份全相合脐血,但仍出现血小板植入延迟及轻~中度移植物抗宿主病,这可能与多方面因素有关,如脐血移植本身较骨髓移植造血重建晚;输注双份脐血可能出现双份脐血干细胞植入竞争;患儿体内的HLA-Ⅱ类抗体和MICA抗体滴度偏高。但该2例患儿出现急性移植物抗宿主病,药物可以控制,而且造血系统成功重建,均可能与移植前预处理中应用的美罗华脱敏等干预治疗有关,移植后期是否会出现慢性移植物抗宿主病,需继续密切观察随访。
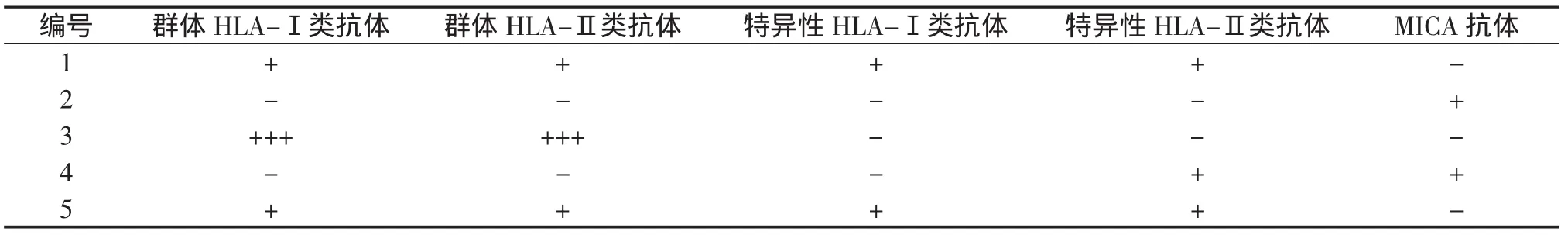
表3 患儿预存致敏抗体情况
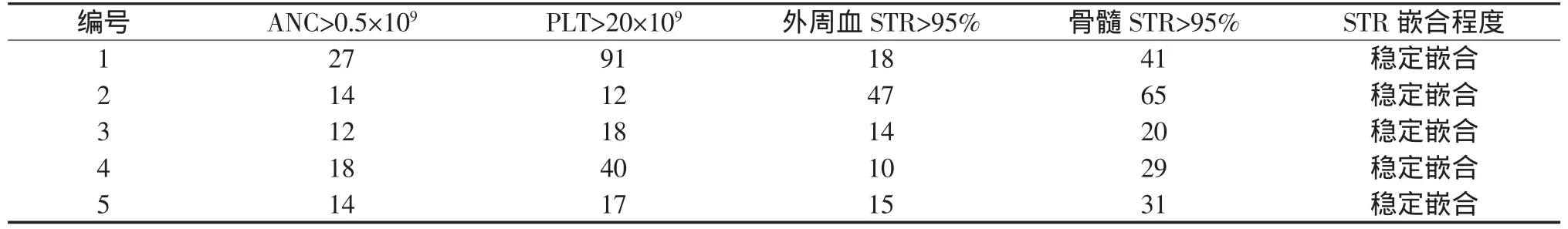
表4 造血系统重建时间(d)
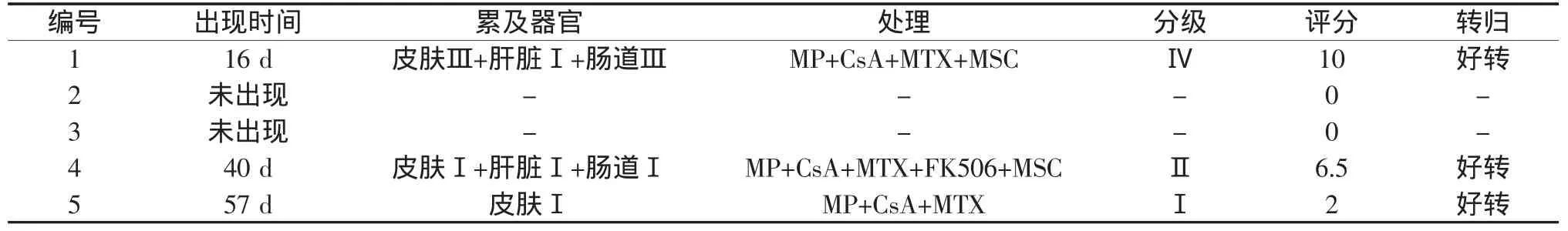
表5 异基因造血干细胞移植后aGVHD
美罗华是一种对B细胞特有CD20抗原具有高亲合力的单克隆抗体,最早于1997年应用于治疗复发及难治性非霍奇金淋巴瘤,近年来在高致敏移植受者的脱敏治疗、抗体介导的排斥反应、移植后淋巴细胞增生性疾病(PTLD)、及ABO血型不符患者的移植中起着重要的作用。在联合血浆置换、免疫球蛋白治疗的同时,对高致敏患者应用美罗华已成为一种脱敏治疗的重要方法。它清除B细胞可能以三种方式起作用:补体依赖细胞介导的细胞毒反应(CDC);药物诱导B细胞凋亡;抗体依赖的细胞毒反应(ADCC)。有国外学者应用CD20单抗美罗华及血浆置换等方法干预处理4例致敏受者,发现有2例患者血清抗体滴度明显下降,异基因骨髓细胞在致敏受者体内植入获得成功,而另外2例血清滴度仍保持高滴度水平的患者,移植后均出现造血干细胞移植排斥[7]。Genberg H等[8]对49例患者术前使用单次剂量美罗华(375 mg/m2)后,发现患者外周血 CDl9、CD20 B淋巴细胞计数从术后24 h开始减少,3~6 w时外周血CDl9、CD20 B淋巴细胞耗竭,并可维持14~16个月,说明该方法不仅起效快,且维持时间长。同时有临床报道联合应用美罗华与血小板输注,可成功促进造血干细胞在致敏受者的植入[9],提示应用美罗华有望成为解决血小板植入延迟的新策略。本研究前期由于监测水平限制,虽除编号5患儿外,其余4例患儿HLA-Ⅱ类抗体及MICA抗体滴度于造血干细胞移植前后均未予评估,但患儿造血干细胞移植后的造血植入时间和排异程度也间接地反应美罗华具有一定的疗效。
近年来已有美罗华造成迟发性中性粒细胞减少的报道,但并无感染增加的情况出现[10],本研究中5例患儿在移植后出现巨细胞病毒波动性感染是否与美罗华或其他免疫抑制药物有关尚需进一步研究。
总之,本研究中使用了美罗华联合丙种球蛋白及血浆置换,使高致敏患者成功接受异基因造血干细胞移植3例,避免了移植相关死亡的发生,移植术后近期结果显示是有效、安全的,但致敏患者接受此种联合治疗的远期预后仍需进一步观察。抗CD20单抗在体液免疫中发挥重要调节作用,而如何在致敏受者合理应用抗CD20单抗以促进异基因造血干细胞的植入还有待进一步研究。本研究的病例数仅5例,研究的结论还需扩大病例数并监测致敏抗体水平得以证实。
[1]Walters M C,Sullivan K M.Stem-cell transplantation for sickle cell disease[J].N Engl J Med,2010,362(10):955-956.
[2]Isgrò A,Gaziev J,Sodani P,et a1.Progress in hematopoietic stem cell transplantation as allogeneic cellular gene therapy in thalassemia[J].Ann N Y Acad Sci,2010,1202:149-154.
[3]Kobayashi T,Maruya E,Niwa M,et al.Significant association between chronic antibody-mediated rejection and donor-specific antibodies against HLA-DRB rather than DQB in renal transplantation[J].Hum Immunol,2011,72(1):11-17.
[4]姚站馨,解金辉.MICA:一种重要的移植免疫抗原[J].现代中西医结合杂志,2009,18(16):1 952-1 954.
[5]Glckman E.Pretransplant lymphocytotoxins and bone-marrow graft rejection[J].Lancet,1978,1(8 061):443.
[6]Locatellli F.Reduced-intensity regimens in allogeneic hematopoietic stem cell transplantation for hemoglobinopathies[J].Hematology Am Soc Hematol Educ Program,2006,260(103):398-401.
[7]Ciurea S O,de Lima M,Cano P,et al.High risk of graft failure in patients with anti-HLA antibodies undergoing haploidentical stem-cell transplantation[J].Transplantation,2009,88(8):1 019-1 024.
[8]Genberg H,Hansson A,Wernerson A,et al.Pharmacodynamics of rituximab in kidney allotransplantation[J].Am J Transplant,2006,6(10):2 418-2 428. [9]Narimatsu H,Wake A,Miura Y,et al.Successful engraftment in crossmatch-positive HLA-mismatched peripheral blood stem cell transplantation after depletion of antidonor cytotoxic HLA antibodies with rituximab and donor platelet infusion[J].Bone Marrow Transplant,2005,36(6):555-556.
[10]Mitsuhata N,Fujita R,Ito S,et al.Delayed-onset neutropenia in a patient receiving rituximab as treatment for refractory kidney transplantation[J].Transplantation,2005,80(9):1 355.
(编辑:张世霞)
Application of anti-CD20 monoclonal antibody in sensitized receptor who will be treated with umbilical cord blood transplantation
Li Dan1,Wang Yi2,Yang Jinhui1
(1.General Hospital of TISCO,Taiyuan Shanxi 030003;2.Children′s Hospital of Soochow University,Suzhou Jiangsu 215003)
Objective:To evaluate the effect of anti-CD20 monoclonal(RTX)antibody in sensitized recipients of hematopoietic stem cells transplantation.Methods:Three of five children
RTX before allo-geneic hematopoietic stem cells transplantation (HSCT).Hematopoietic reconstitution,chimerism level of genetic polymorphisms of short tandem repeats between donator and recipients,graft-versus-host disease were observed after implantation.Results:5 cases had hematological recovered after transplantation successfully.Two of them had delayed platelet engraftment.Number 1 case developed severe acute graft-versus-host disease(aGVHD),but other 3 cases who received RTX before transplantation did not appear or only appeared light to moderate aGVHD.Number 4 case who appeared mild cGVHD,involving the gastrointestinal,has improved significantly after the FK506 adjustment.Now they are all in stable condition.Conclusion:RTX has certain curative effect on allogeneic hematopoietic stem cell transplantation in sensitized receptor.
allogeneic hematopoietic stem cell transplantation;sensitized receptor;anti-CD20 monoclonal antibody
R733
:A
:1671-0258(2017)03-0035-05
李丹,硕士,E-mail:lidanxu912113r@163.com
杨金慧,主任医师
