利奈唑胺万古霉素治疗耐甲氧西林金黄色葡萄球菌感染的疗效及安全性分析
2017-10-09高永民
高永民
(青海省西宁市第一人民医院药品调配站, 青海 西宁 810000)
利奈唑胺万古霉素治疗耐甲氧西林金黄色葡萄球菌感染的疗效及安全性分析
高永民
(青海省西宁市第一人民医院药品调配站, 青海 西宁810000)
目的探讨利奈唑胺与万古霉素治疗耐甲氧西林金黄色葡萄球菌(MRSA)肺炎的疗效以及安全性。方法收集2016年1月至2017年3月入院的60例耐甲氧西林金黄色葡萄球菌(MRSA)肺炎的患者采用随机数字表法分为两组,对照组患者给予万古霉素进行治疗,实验组患者则给予利奈唑胺进行治疗,比较两组患者总体治疗有效率、治疗前以及治疗后血白细胞浓度、血液C反应蛋白浓度以及两组患者不良反应(率)发生情况比较。结果不同治疗方法:经过卡方检验,实验组较对照组患者临床总有效率比较,实验组显著升高,差异显著,具有显著统计学意义(P<0.01);不同治疗方法:经过t检验,治疗前两组WBC以及CRP比较,差异不具有统计学意义(P>0.05);治疗后两组WBC以及CRP指标均较治疗前明显降低,差异具有统计学意义(P<0.05),且治疗后观察组WBC以及CRP指标均明显低于对照组,差异具有统计学意义(P<0.05);实验组与对照组患者不良反应比较,总不良反应率差异不具有统计学意义(P>0.05),而实验组患者主要以腹泻、恶心等胃肠道不良反应为主,对照组患者主要以皮肤反应、肾功能障碍不良反应为主。结论利奈唑胺治疗MRSA肺炎患者的效果较万古霉素而言,利奈唑胺降低炎症细胞、控制炎症反应效果都更好,治疗总有效率更高,利奈唑胺治疗主要以腹泻、恶心等胃肠道不良反应为主,而万古霉素治疗患者主要以皮肤反应、肾功能障碍不良反应为主,两组不良反应较少,安全性较高,值得临床推广,具有借鉴性。
利奈唑胺; 万古霉素; 耐甲氧西林金黄色葡萄球菌; 疗 效; 安全性
金黄色葡萄球菌肺炎是呼吸内科乃至整个内科系统中十分常见病症之一,近年来我国有多项文献报道院内感染以及社区感染发生多为革兰阳性球菌,感染性疾病患者中发生革兰阳性菌为主要病原菌,其中凝固酶阴性葡萄球菌是临床上最为常见的病原菌,并且由于过去广谱抗生素滥用,细菌多重耐药现象十分严重,但是万古霉素和利奈唑胺的耐药菌株目前还暂时没有发现,这就使得万古霉素和利奈唑胺这两种药物成为了耐甲氧西林金黄色葡萄球菌(MRSA)肺炎的有效治疗手段[1,2],有研究指出[3],万古霉素和利奈唑胺不易和其他抑制细菌蛋白合成的抗菌药物产生交叉耐药,所以在多重耐药革兰阳性球菌的感染患者中效果十分显著,特别是在MRSA感染所致肺炎患者的治疗中,十分突出。但是治疗严重感染患者病死率仍然高达25%左右,远期观察发现万古霉素具有肾毒性作用[4],如果应用在患者中可能会加重患者的肾损害危险,故将我院60例研究对象进行临床研究,现报道如下:
1 资料与方法
1.1一般资料:收集2016年1月至2017年3月入院的60例耐甲氧西林金黄色葡萄球菌(MRSA)肺炎的患者采用随机数字表法分为两组,每组30例。所有患者均满足人卫第八版《内科学》[5]中关于耐甲氧西林金黄色葡萄球菌(MRSA)肺炎之诊断,并经实验室检查与临床症状确诊,痰培养MRSA均呈阳性,表现为咳嗽、咳痰、湿啰音,并且经喹诺酮类、三四代头孢等抗菌药物治疗无效。且未使用过利奈唑胺和万古霉素,不合并严重心肝肾功能障碍的患者。其中,实验组患者男14例,体重57~66kg,平均体重(58.2±4.5)kg,女16例,体重47~62kg,平均体重(51.2±8.5)kg,年龄为54~70岁,平均年龄为(64.6±3.9)岁;对照组患者男11例,体重53~66kg,平均体重(59.1±3.8)kg,女19例,体重41~61kg,平均体重(49.7±7.8)kg,年龄为51~73岁,平均年龄为(62.7±5.5)岁。两组患者的性别、年龄、体重等一般情况的差异无统计学意义,具有可比性(P>0.05)。
1.2方法:基础治疗相同,对照组:建立静脉通道,通过静脉滴注注射用盐酸万古霉素(浙江海正药业股份有限公司,0.5g/瓶),剂量选择0.5g/6h,控制输入速度适宜,不宜过快,每次滴注时间维持在1h以上,均维持治疗2周;观察组静脉滴注利奈唑胺注射液(美国辉瑞制药有限公司,600mg/300mL)600mg,静脉滴注方式,2次/d。均维持治疗2周。所有患者基础治疗均相同,均给予止咳、祛痰、补液及营养支持等常规治疗
1.3检测方法[6,7]:疗效评价:按原国家卫生部颁发的《抗菌药物临床使用路径》,抗菌药物疗效分级为:痊愈、有效和无效3级。痊愈:治疗后体温、白细胞等恢复正常,胸片明显改善或恢复正常,肺部症状完全消退;显效:治疗后体温、白细胞均有一定恢复,胸片明显改善,肺部症状有所改善;无效:体温、白细胞不降低,胸片未见改善,肺部症状未消退总。有效率=(治愈例数+有效例数)/总例数×100%
观察指标:记录两组患者不良反应发生的情况;治疗前后,采用速率比浊法检测C反应蛋白(CRP),实验室检测外周血WBC。

2 结 果
2.1两组患者临床总有效率比较:实验组患者临床总有效率较对照组高,差异有统计学意义(χ2=8.366,P<0.01)。
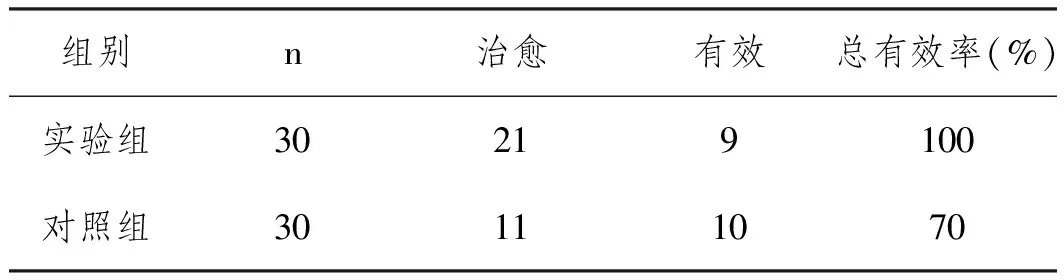
表1 两组患者疗效比较n(%)
2.2两组患者治疗前以及治疗后血白细胞浓度、血液C反应蛋白浓度比较:治疗前两组WBC以及CRP比较,差异不具有统计学意义(P>0.05);治疗后两组WBC以及CRP指标均较治疗前明显降低,差异具有统计学意义(P<0.05),且治疗后观察组WBC以及CRP指标均明显低于对照组,差异具有统计学意义(P<0.05)。
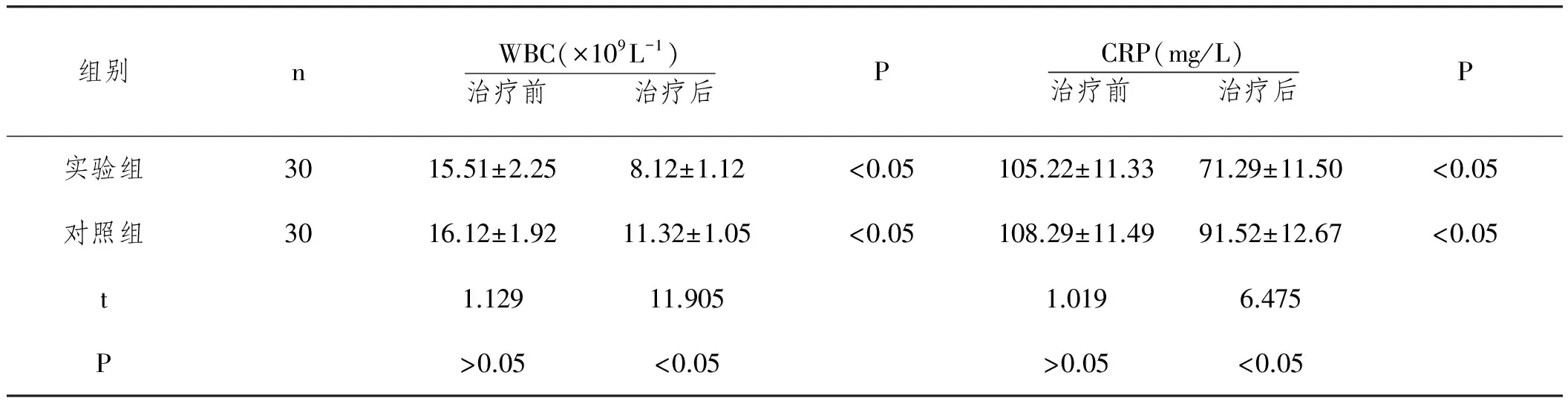
表2 两组患者治疗前以及治疗后血白细胞浓度血液C反应蛋白浓度比较
2.3两组患者不良反应发生率比较:实验组与对照组患者总不良反应发生率差异不具有统计学意义(P>0.05),而实验组患者以腹泻、恶心等胃肠道不良反应发生相对较多,对照组患者以皮肤反应、肾功能障碍不良反应发生相对较多。
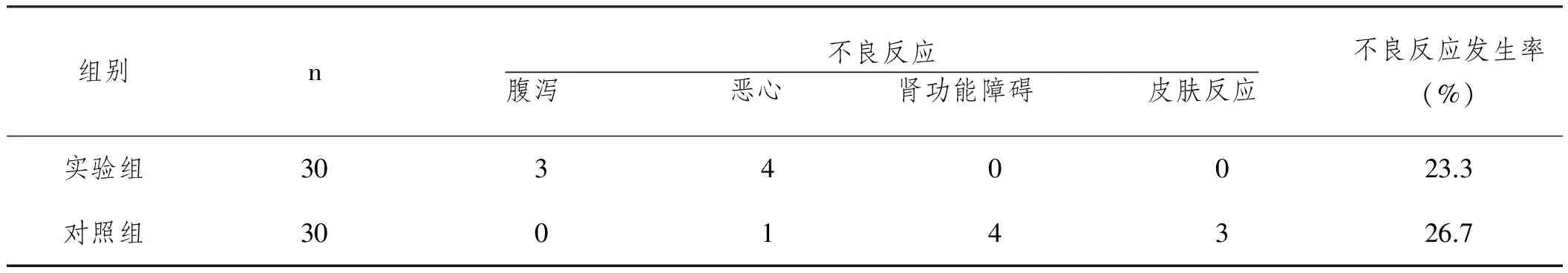
表3 两组患者不良反应发生率比较
3 讨 论
由于长期抗生素的广泛过量使用,导致了耐甲氧西林金黄色葡萄球菌(MRSA)成为了院内和社区感染的重要病原菌之一,特别是身体机能较差的老年患者,老年患者肺部感染后可致急性肺炎,并发化脓性感染,导致重症肺炎,致死率较高[8,9]。细菌多重耐药现象十分严重,但是万古霉素和利奈唑胺的耐药菌株目前还暂时没有发现,而以万古霉素为代表的糖肽类抗菌药是治疗MRSA感染的一线用药,但用药后的各类不良反应临床都有所报道[10,11],所以对于体弱或老年患者的应用应该较为谨慎。相比较于万古霉素,利奈唑胺是恶唑烷酮类当中比较新型的抗菌药,其代谢过程对肝、肾功能影响较小,且对各类耐药革兰阳性球菌杀伤效果显著,对金黄色葡萄球菌敏感性十分高[12,13]。万古霉素是传统临床常用肺炎治疗药物,该药属于治疗耐甲氧西林金葡菌(MRSA)感染所致肺炎的一线用药选择,但从临床文献报道中我们发现,治疗严重感染患者病死率交稿,可能因为是万古霉素有很强的肾毒性,应用在老年患者中存在潜在肾损害危险,这届大大局限了万古霉素的使用[14,15]。利奈唑胺属于新型恶唑烷酮类广谱抗革兰阳性球菌药物,其发挥作用是通过抑制细菌蛋白合成酶的活性,阻断细菌蛋白质的合成过程,相比其他药物有所不同,通过选择性地与50S亚单位核糖体结合,而对其他肽基转移酶的干扰则可以忽略不计,于编码翻译起始阶段对细菌合成蛋白产生抑制,临床效果更优秀[16,17]。
本研究发现不同治疗方法:经过卡方检验,实验组较对照组患者临床总有效率比较,实验组显著升高,差异显著,具有显著统计学意义(P<0.01),可见利奈唑胺治疗效果更为显著;不同治疗方法:经过t检验,治疗前两组WBC以及CRP比较,差异不具有统计学意义(P>0.05);治疗后两组WBC以及CRP指标均较治疗前明显降低,差异具有统计学意义(P<0.05),且治疗后观察组WBC以及CRP指标均明显低于对照组,差异具有统计学意义(P<0.05),说明利奈唑胺对炎症的控制更为显著,炎症所致的免疫反应损伤更低;实验组与对照组患者不良反应比较,总不良反应率差异不具有统计学意义(P>0.05),而实验组患者主要以腹泻、恶心等胃肠道不良反应为主,对照组患者主要以皮肤反应、肾功能障碍不良反应为主。
综上所述利奈唑胺治疗MRSA肺炎患者的效果较万古霉素而言,利奈唑胺降低炎症细胞、控制炎症反应效果都更好,治疗总有效率更高,利奈唑胺治疗主要以腹泻、恶心等胃肠道不良反应为主,而万古霉素治疗患者主要以皮肤反应、肾功能障碍不良反应为主,两组不良反应较少,安全性较高,值得临床推广,具有借鉴性。
[1] 林志青,黄延玲.利奈唑胺和万古霉素治疗耐甲氧西林金黄色葡萄球菌感染疗效的Meta分析[J].中华传染病杂志,2011,39(6):361~365.
[2] 郭伟.重症监护病房中利奈唑胺耐药的金黄色葡萄球菌感染的暴发流行[J].中华结核和呼吸杂志,2011,34(2):103.
[3] Hiroaki Takada,Toru Hifumi,Naoki Nishimoto,et al. Linezolid versus vancomycin for nosocomial pneumonia due to methicillin-resistant staphylococcus aureus in the elderly: a retrospective cohort analysis[J].American Journal of Emergency Medicine,2016, 35(2):245~248.
[4] 朱林.利奈唑胺治疗老年人院内耐甲氧西林金黄色葡萄球菌感染的效果分析[J].中国当代医药,2013,20(32):94~95.
[5] 葛均波,徐永健,主编.内科学[M].第8版.北京.人民卫生出版社,2013:297~368.
[6] Equils Ozlem,da Costa Christopher,Wible Michele,et al. The effect of diabetes mellitus on outcomes of patients with nosocomial pneumonia caused by methicillin-resistant staphylococcus aureus: data from a prospective double-blind clinical trial comparing treatment with linezolid versus vancomycin[J].BMC infectious diseases,2016,16: 476.
[7] Caffrey AR,Quilliam BJ,Laplante KL,et al.利奈唑胺和万古霉素治疗甲氧西林耐药金黄色葡萄球菌感染的疗效比较[J].中国感染与化疗杂志,2011,11(4):255.
[8] An MM 吴娜(译).利奈唑胺和万古霉素治疗耐甲氧西林金黄色葡萄球菌感染的比较:随机对照试验的荟萃分析[J].中国医药工业杂志,2013,44(10):1053.
[9] Laura A,Puzniak,Kimbal D,et al.The prevalence of methicillin-resistant staphylococcus aureus colonization in patients with complicated skin and skin structure infections after treatment with linezolid or vancomycin[J].Advances in Infectious Diseases,2014,04(04): 186~193.
[10] 徐丹,吴春荣,崔宇慧.利奈唑胺对耐甲氧西林葡萄球菌感染患者降钙素原水平的影响[J].中国生化药物杂志,2016,36(11):88~90.
[11] 秦红梅.利奈唑胺治疗耐甲氧西林金黄色葡萄球菌感染重症肺炎的疗效观察[J].中国老年学杂志,2014,34(20):5869~5870.
[12] Tong ManShan C,Wisniewski Christopher S,et al.Comparison of Linezolid and Vancomycin for methicillin-resistant staphylococcus aureus pneumonia: institutional implications[J].Pharmacotherapy,2016,36(7): 731~739.
[13] 李娉,李庆林.利奈唑胺和万古霉素对耐甲氧西林金黄色葡萄球菌感染疗效的Meta分析[J].安徽医药,2015,19(5):969~973.
[14] 庞昶,朴成浩,林树无.利奈唑胺治疗耐甲氧西林金黄色葡萄球菌感染肺炎并发肝功能损伤的危险因素分析[J].医药导报,2015,34(1):43~46.
[15] 范大平,张一梅,尚建欣.利奈唑胺治疗耐甲氧西林金黄色葡萄球菌感染的疗效及安全性分析[J].临床肺科杂志,2011,16(10):1520~1521.
[16] Alaniz Cesar,Pogue Jason M. Vancomycin versus linezolid in the treatment of methicillin-resistant Staphylococcus aureus nosocomial pneumonia: implications of the ZEPHyR trial[J].The Annals of Pharmacotherapy,2012,46(10): 1432~1435.
[17] 薛晓燕,周曙俊,王大明.治疗耐甲氧西林金黄色葡萄球菌感染的5种抗菌药物的应用评价[J].药学与临床研究,2015,23(5):497~500.
TheEffectandSafetyofLinezolidandVancomycinonMethicillin-resistantStaphylococcusAureusInfection
GAOYongmin
(DrugDispensingStationofXiningFirstPeople'sHospital,QinghaiXining810000,China)
Objective:To investigate the efficacy and safety of linezolid and vancomycin in the treatment of methicillin-resistant Staphylococcus aureus (MRSA) pneumonia.Methods60 patients with methicillin-resistant Staphylococcus aureus (MRSA) pneumonia were enrolled from January 2016 to March 2017 were randomly divided into two groups according to the random number table. The patients in the control group were treated with vancomycin, The patients in the experimental group were treated with linezolid, and the overall treatment efficiency, the white blood cell concentration before treatment and the concentration of C-reactive protein and the incidence of adverse reactions were compared between the two groups.ResultsCompared with the control group, the total effective rate of the experimental group was significantly higher than that of the control group (P <0.01). After treatment, WBC and CRP were significantly lower than those before treatment, the difference was significant, and there was no significant difference between the two groups before and after treatment.WBC and CRP were significantly lower than those in the control group (P <0.05). There was no significant difference in the adverse reaction rate between the experimental group and the control group, (P> 0.05), while the experimental group of patients mainly diarrhea, nausea and other gastrointestinal adverse reactions, the control group of patients mainly to skin reactions, renal dysfunction adverse reactions.ConclusionThe efficacy of linezolid in the treatment of MRSA pneumonia is lower than that of vancomycin, and it is better to control inflammatory response, and the total effective rate of treatment is higher. The treatment of linezolid is mainly caused by diarrhea, nausea and so on. Gastrointestinal adverse reactions, and vancomycin treatment of patients mainly to skin reactions, renal dysfunction adverse reactions, two groups of less adverse reactions, higher safety, worthy of clinical promotion, with reference.
Linezolid; Vancomycin; Methicillin-resistant staphylococcus aureus; Efficacy; Safety
1006-6233(2017)09-1448-05
A
10.3969/j.issn.1006-6233.2017.09.012
青海省自然科学基金项目,(编号:20060112)
