某肿瘤专科医院抗肿瘤药致不良反应报告309例分析Δ
2017-10-09潘文李豫黄天文雷宇梁琳琳广西医科大学附属肿瘤医院临床药学科南宁5300广西医科大学药学院南宁5300
潘文,李豫,黄天文,雷宇,梁琳琳(.广西医科大学附属肿瘤医院临床药学科,南宁5300;.广西医科大学药学院,南宁 5300)
某肿瘤专科医院抗肿瘤药致不良反应报告309例分析Δ
潘文1*,李豫1,黄天文1,雷宇1,梁琳琳2(1.广西医科大学附属肿瘤医院临床药学科,南宁530021;2.广西医科大学药学院,南宁 530021)
目的:了解抗肿瘤药致药品不良反应(ADR)的特点和发生规律,为临床安全使用抗肿瘤药提供参考。方法:采用回顾性研究方法,对某肿瘤专科医院2015年1-12月收集的309例抗肿瘤药致ADR报告进行统计、分析。结果:309例ADR患者中,女性(58.25%)多于男性(41.75%);40岁以上患者所占比例较高(78.64%);引发ADR的给药途径以静脉滴注为主(94.82%);严重的ADR 225例(72.82%);经停药或治疗后好转的有268例(86.73%)。309例ADR共涉及24种抗肿瘤药物,引发ADR最多的药品依次为多西他赛、顺铂和环磷酰胺;ADR累及器官/系统以造血系统最常见(64.24%),临床表现主要为骨髓抑制。结论:临床应加强抗肿瘤药的ADR监测,及时预防、发现和诊治抗肿瘤药引发的ADR,以减少对患者造成的伤害,保证药物治疗的安全、有效。
抗肿瘤药;药品不良反应;回顾性分析
随着肿瘤发病率逐年升高,肿瘤患者也随之增多。抗肿瘤药近年发展较快,但绝大多数都具有细胞毒性作用,不可避免地对正常组织、器官产生损害,导致出现不同程度的药品不良反应(ADR)。我院作为肿瘤专科医院,住院患者大多数是肿瘤患者,抗肿瘤药的使用量较大,引发的ADR也较多,但常出现漏报、瞒报现象。近年,随着临床药师工作的开展,通过监控临床检验危急值的改变,主动收集到抗肿瘤药引发的ADR,极大地提高了上报率,减少了临床漏报、瞒报现象。现对我院2015年上报的309例抗肿瘤药致ADR报告进行回顾性分析,了解该类药物致ADR发生的特征和规律,为临床安全用药提供参考。
1 资料与方法
收集2015年1月1日-12月31日我院上报至国家ADR监测网数据库,与抗肿瘤药有因果关系的ADR报告共309例,按患者的一般信息、给药途径、用药剂型、ADR涉及药品种类、累及器官/系统及临床表现等进行统计,分析其特征。ADR类型分级参照《药品不良反应报告和监测工作手册》[1]。
2 结果
2.1 患者年龄与性别
309例ADR患者中,男性129例(41.75%),女性180例(58.25%);年龄4~86岁,40岁以上患者243例(78.64%),详见表1。
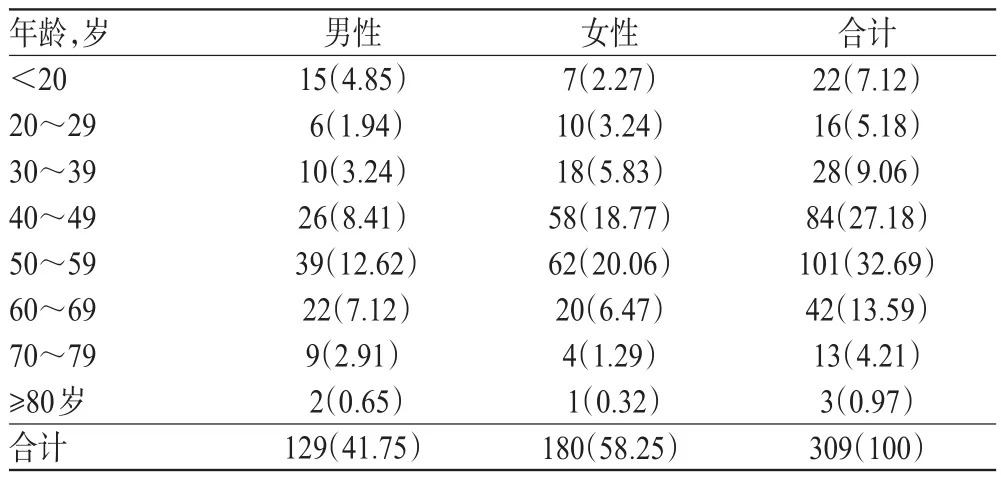
表1 发生ADR患者的年龄与性别分布[例(%%)]Tab 1 Distribution of patient's age and gender in ADR cases[case(%%)]
2.2 ADR的药物剂型与给药途径分布
引发ADR的抗肿瘤药剂型以注射剂为主,共299例,占96.76%;其他剂型有片剂/胶囊剂10例,占3.24%。我院309例ADR报告中,有298例由静脉给药所引发,占96.44%,其中静脉给药又以静脉滴注为主,共293例;其余途径(包括口服和腹膜腔内给药)共11例,占3.56%。
2.3 ADR类型分级及转归情况
309例ADR中,一般的ADR 84例(27.18%),严重的ADR 225例(72.82%);经停药或治疗后好转的有268例(86.73%),未好转的有13例(4.21%),结果不详的有27例(8.74%),痊愈的有1例(0.32%),没有死亡病例。
2.4 药品种类
本次统计的309例ADR报告中共有533条用药记录,涉及24种抗肿瘤药,详见表2。
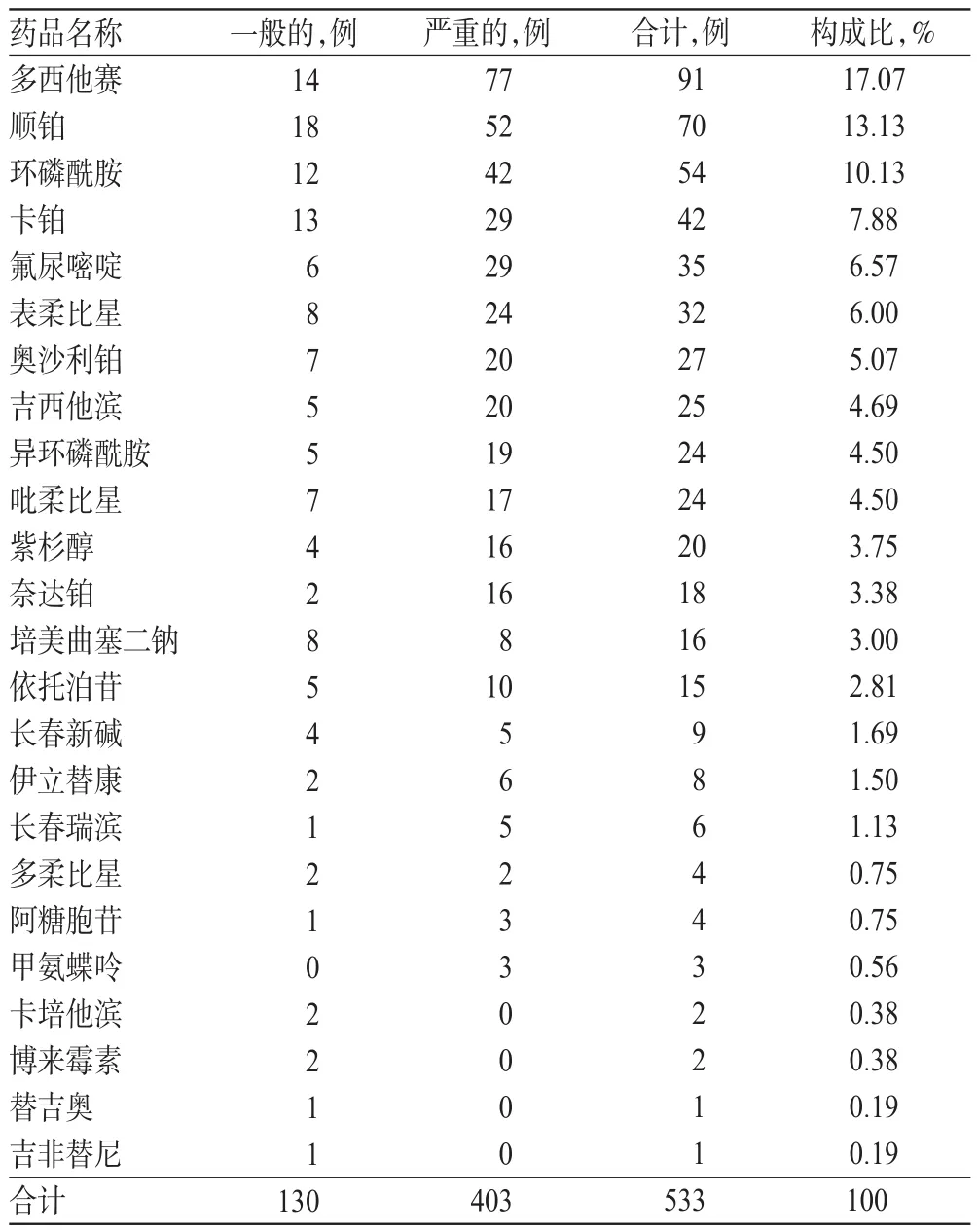
表2 引发ADR的抗肿瘤药及构成比Tab 2 ADR-inducing antineoplastics and constitution ratio
2.5 累及器官/系统及临床表现
ADR累及器官/系统主要为造血系统,其次为心血管系统、消化系统和全身性损害等,共计332例次,详见表3(注:1例ADR可能累及多个器官/系统,故合计例次>309)。
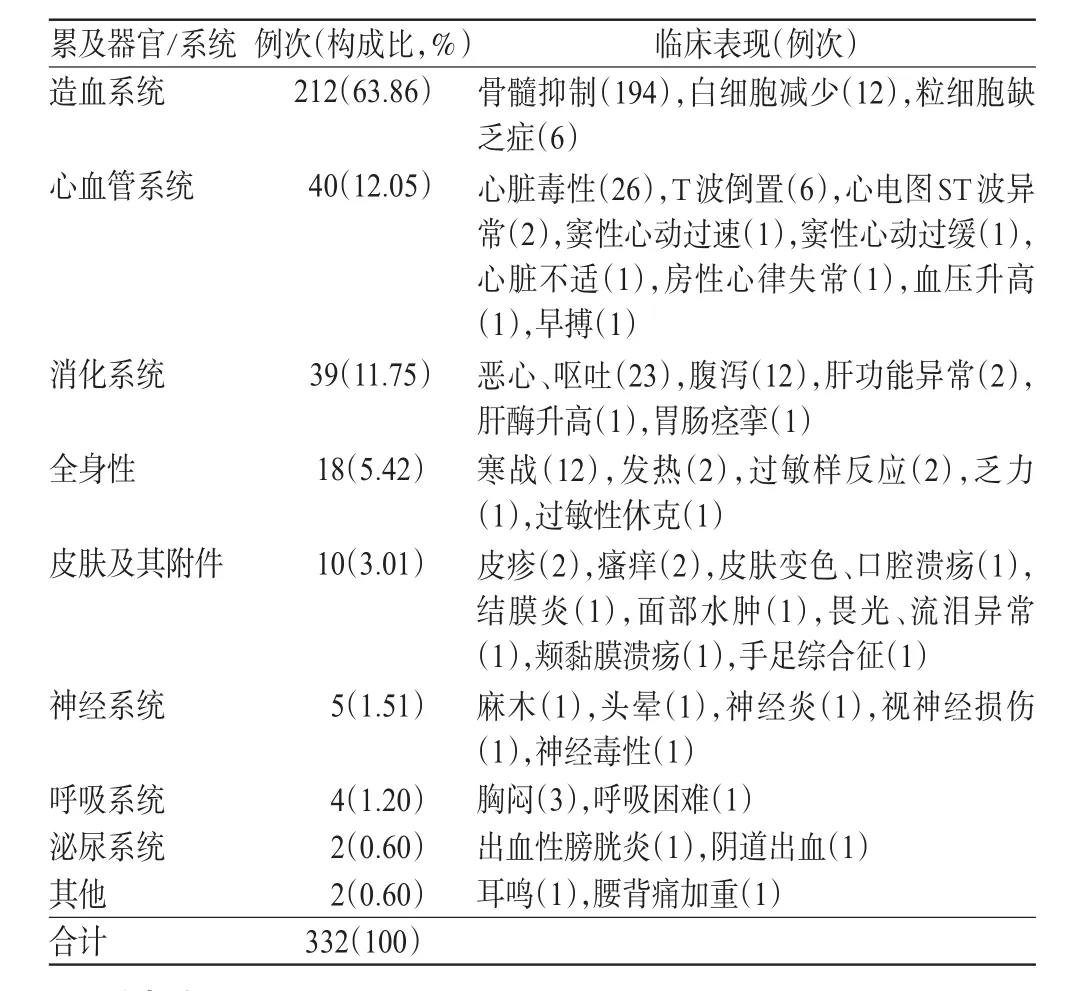
表3 ADR累及器官/系统及其临床表现Tab 3 Organs/systems involved in ADR and clinical manifestations
3 讨论
3.1 报告主体
国内大多数医疗机构都是采用自愿呈报方式上报ADR报告,报告主体是医师和护士。但存在效率低下、漏报率高的问题。目前,利用日益完善的数字化医院平台,自动全面地监测ADR,能够提高效率和减少漏报率[2]。我院临床药师利用抗肿瘤药ADR网络监控体系,结合检验危急值对患者进行主动筛查,共收集309例抗肿瘤药ADR报告,其中大部分来源于药师,仅少数为医师和护士通过自愿呈报方式上报,这也与国外文献报道[3]的呈报主体一致。为患者提供用药安全信息是药师的职责,同时药师也负责医院ADR信息操作平台的维护,在发现和收集ADR方面较医护人员更有优势,其可将收集到的ADR信息及时反馈给临床医护人员,从而保障临床用药安全。
3.2ADR个体差异
本研究结果显示,发生ADR的患者在性别分布上女性高于男性,可能与女性体内药动学特点、生理因素等有关;另外,也可能与女性患者对药物毒性较男性更为敏感有关[4]。因此,在对女性肿瘤患者临床用药时,应充分考虑生理期、绝经期等与女性激素水平影响因素相关的各类特殊情况。
3.3 年龄因素
从年龄分布看,ADR可能发生于任何年龄组的患者,大部分患者集中在40岁以上,且50~59岁年龄段占最高。40岁以后,人的生理上开始退行性改变,组织器官功能开始逐渐衰退,肝药酶活性减弱而致其解毒能力下降,机体代谢和排泄速度减慢,血液中血浆蛋白含量降低,导致血药浓度增加,容易出现药物蓄积,从而导致ADR发生率增高[5]。多数抗肿瘤药药理学特性复杂,治疗窗窄,中毒剂量与治疗剂量接近,因此临床上使用抗肿瘤药治疗过程中应注意个体化给药,并根据患者生理、病理情况适当调整药物的剂量,按照相关癌症指南使用辅助用药进行预处理,从而减少ADR的发生[6]。
3.4 给药途径
本研究结果显示,静脉给药途径发生的ADR占96.44%。大多数抗肿瘤药均以静脉给药为主,而静脉给药的特点是药物直接迅速地进入人体循环,避开肝脏的首关效应,因此对人体的刺激也随着增强。此外,输液的配伍、操作过程及输注速度也可能成为ADR的诱因。而口服给药后经胃肠道吸收,再经肝脏的首关效应,因此安全性相对静脉给药高。所以,在临床应用中,应坚持能口服不静脉给药的原则,并根据患者病情尽量选择口服给药。本次统计的309例ADR报告中,有11例为口服给药所引起,多为严重的ADR。提示临床不仅应该关注以静脉给药方式引起的ADR,也应该对口服抗肿瘤药引起的ADR进行重点监测,以防止严重的ADR发生。
3.5 ADR类型分级与转归
本研究309例ADR中,225例严重的ADR临床多表现为显著骨髓抑制、胃肠道损害和心血管损害等,均会危及患者生命或延长患者住院时间。此类反应大多数是迟发性的,应积极采取应急预案进行对症处理,尽早使患者ADR好转。经处理后此类反应均可好转或治愈,未出现致死致残病例。尽管抗肿瘤药致严重的ADR发生率较高,但只要加强预防措施,在发生后严格按照抗肿瘤药致ADR发生后的处理流程及时对症治疗,仍可以使ADR的转归趋于好转甚至治愈。
3.6 药物种类
本研究结果还显示,309例ADR报告中,以多西他赛和顺铂所致的ADR最多,其次为环磷酰胺。多西他赛是一种新型植物碱类抗肿瘤药,相比其他紫杉醇类,多西他赛有较好的生物利用度、更高的细胞内浓度及优异的抗癌广谱性,且低剂量诱导细胞凋亡效应显著,因此细胞毒性也较大。铂类是一类细胞周期非特异性抗肿瘤药,毒性大、抗瘤谱广,是临床多种实体肿瘤治疗的主要药物,使用量大,导致临床出现ADR更为常见。随着临床应用顺铂前加强水化预处理及通过结构改造后的其他铂类肾毒性和神经毒性的降低,临床应用铂类出现肾毒性和神经毒性较前明显减少。目前主要表现为恶心、呕吐、腹泻等胃肠道反应,其次为骨髓抑制[7],严重骨髓抑制可危及患者生命或延长住院时间。因此,临床用药中,应特别注意对使用铂类抗肿瘤药的患者进行必要的用药教育,做好预防措施,高度警惕ADR的发生。
本研究中的ADR多为联合用药所致,化疗方案大多数是联合用药,很多具有细胞毒性作用,容易出现毒性的累积,更加容易出现ADR,并且出现较多严重的ADR。在住院期间所用的药物种类越多,则其ADR发生的次数也越多[8]。挪威的一项研究显示,在住院的癌症死亡患者中,约有4%是由严重的不良药物相互作用引起的[9],而对于非住院癌症患者,目前尚无相关流行病学研究。因此,在联合用药提高疗效的同时,也应尽量减少合并用药种数,以保证患者用药安全。
3.7 ADR累及器官/系统
国内文献报道,抗肿瘤药的ADR以胃肠道反应最为常见[10-11]。但本研究结果显示,骨髓抑制等造血系统损害所占比例较高(64.05%),这与我院以药师作为报告主体,通过医院ADR监控系统主动收集上报有关。出现骨髓抑制最严重时期一般在化疗结束后7~10 d,主要表现为白细胞、粒细胞、血小板、血红蛋白的同时降低,常影响下一周期的化疗[12]。严重骨髓抑制可导致粒细胞缺乏,常常伴有不明原因的发热,从而导致严重感染,甚至感染性休克,危及患者生命,因此对于抗肿瘤药引起的骨髓抑制,需要加强肿瘤患者化疗前后的血液学监测,密切监控患者血常规指标,注意按照粒细胞缺乏伴发热的治疗指南,及时给予抗菌药物、细胞刺激因子等加强抗感染对症支持治疗。对既往有过重度骨髓抑制的患者,因为具有在下一周期化疗后重复出现重度骨髓抑制的高危因素,应在下一周期化疗结束后24 h立即预防性使用升白细胞药物,以降低骨髓抑制发生风险。
4 结语
抗肿瘤药是肿瘤专科医院最重要的一类治疗性药物,用量较其他综合性医院多,由于其药理活性特点,出现ADR的概率较大。目前很难从根本上消除抗肿瘤药的ADR,除了通过相关的预防措施降低ADR的严重程度之外,通过了解其ADR发生的规律和特点也有助于保障临床用药安全,切实减少抗肿瘤药致ADR的发生,有效保证化疗方案的顺利实施,提高患者生存质量。因此,临床医师则应按照相关癌症治疗指南,规范肿瘤治疗,对细胞毒性较大的药物做好ADR防治工作,保障化疗顺利进行;而临床药师应对现有抗肿瘤药物出现的ADR进行研究,寻找其中的规律,作出安全性评价,指导临床合理用药,为患者的化疗提供安全保障。
[1]国家食品药品监督管理局安全监管司,国家药品不良反应监测中心.药品不良反应报告和监测工作手册[S].2005-09.
[2]李春荣,邱吉苗,徐立,等.药品不良反应自动化监测系统的开发与应用[J].中国数字医学,2016,11(4):48-49.
[3]Kofoed S,Breen S,Gough K,et al.Benefits of remote real-time side-effect monitoring systems for patients receiving cancer treatment[J].Oncology Reviews,2012,16(1):129-132.
[4]钱之玉.药物不良反应及其对策[M].北京:化学工业出版社,2005:6.
[5]熊秋菊.红花注射液致寒战3例报道[J].中国药师,2008,11(9):10-11.
[6]郑冬雁,翟淑越,崔冉,等.4 120例抗肿瘤药品不良反应分析[J].中国药物警戒,2014,11(5):291-294.
[7]郭佳栋,张雪梅,刘影,等.8种治疗胃癌常用抗肿瘤药物致不良反应病例报告分析[J].中国药房,2016,27(33):4627-4630.
[8]孙定人,齐平,靳颖华.药物不良反应[M].3版.北京:人民卫生出版社,2003:22-28.
[9]Buajordet I,Ebbesen J,Erikssen J,et al.Fatal adverse drug events:the paradox of drug treatment[J].J Intern Med,2001,250(4):327-341.
[10]蒙光义,韦银,庞家莲,等.我院215例抗肿瘤药致不良反应报告分析[J].中国药房,2014,25(34):3233-3235.
[11]张红银,吴映蓉.我院420例抗肿瘤药品不良反应报告分析[J].中国药业,2013,22(21):52.
[12]谢嵩,魏长生.肿瘤化疗患者骨髓抑制发生情况调查与分析[J].中国现代应用药学,2010,27(13):1219-1220.
Analysis of 309 Antineoplastics-induced ADR Reports in a Tumor Hospital
PAN Wen1,LI Yu1,HUANG Tianwen1,LEI Yu1,LIANG Linlin2(1.Dept.of Clinical Pharmacy,the Affiliated Tumor Hospital of Guangxi Medical University,Nanning 530021,China;2.College of Pharmacy,Guangxi Medical University,Nanning 530021,China)
Antineoplastics;ADR;Retrospective analysis
R978.1;R969.3
A
1001-0408(2017)26-3646-04
2017-01-19
2017-03-10)
(编辑:晏 妮)
DOI 10.6039/j.issn.1001-0408.2017.26.13
广西壮族自治区卫生厅课题项目(No.Z2014256)
*副主任药师。研究方向:临床药学、药事管理。电话:0771-5332630。E-mail:Pw.0771@163.com
ABSTRACTOBJECTIVE:To investigate the characteristic and regularity of antineoplastics-induced ADR,and to provide reference for safety use of antineoplastics in clinic.METHODS:In retrospective study,309 cases of antineoplastics-induced ADR collected from a special hospital during Jan.-Dec.2015 were summarized and analyzed statistically.RESULTS:Among 309 ADR cases,female(58.25%)was more than male(41.75%).The patients aged more than 40 years old occupied the highest proportion(78.64%).Main route of administration was intravenous dripping(94.82%).There were 225 cases of severe ADR(72.82%).Total 268 cases were improved after drug withdrawal or treatment(86.73%).A total of 24 kinds of antineoplastics were involved in 309 ADR cases;most of ADR were induced by docetaxel,followed by cisplatin,cyclophosphamide.Most common organs/system involved in ADR was hemopoietic system(64.24%),main clinical manifestation was myelosuppression.CONCLUSIONS:It is necessary to strengthen ADR monitoring,prevent,discover and treat antineoplastics-induced ADR timely,in order to reduce the harm to the patients and ensure the safety and effectiveness of drug treatment.
