2010-2015年美国FDA批准上市的孤儿药研究
2017-10-09王丽皮婷刘艳秋古曦赵方允昆明市延安医院药学部昆明650051
王丽,皮婷,刘艳秋,古曦,赵方允(昆明市延安医院药学部,昆明650051)
2010-2015年美国FDA批准上市的孤儿药研究
王丽*,皮婷,刘艳秋,古曦,赵方允#(昆明市延安医院药学部,昆明650051)
目的:了解2010-2015年美国FDA批准的孤儿药的情况,为我国孤儿药的相关立法和新药研发提供参考。方法:查阅近年来国内外相关文献,对2010-2015年美国FDA批准的孤儿药进行统计和分析。结果与结论:2010-2015年美国FDA批准上市的孤儿药共77种,仅2015年就有21种,占该年获批新药的46.67%。获批孤儿药主要是治疗肿瘤、内分泌及代谢系统疾病、心血管疾病、感染性疾病、神经及精神疾病和血液系统疾病等全球高发疾病的药物,其中以抗肿瘤药物为主(38种,占49.35%),主要用于治疗黑色素瘤、非小细胞肺癌和白血病。美国FDA批准的孤儿药的研发企业以美国为主。我国尚无明确的罕见病和孤儿药的定义及相关立法,亟需加快相关立法进程,结合国情开展孤儿药的研发与审批。
孤儿药;罕见药;罕见病;美国食品药品监督管理局
孤儿药又称罕见药,是用于有效预防、治疗和诊断罕见病的药物,由于罕见病患病人数少(仅占总人口数的0.65‰~1‰),其治疗药物市场需求小、研发难度和成本高,制药企业较少关注其相关治疗药物的研发,因此这类药被形象地称为“孤儿药”[1-4]。药物创新是全球医药行业和医药市场快速发展的推动力,带来了巨大的社会效益和经济效益[5-8]。美国FDA是世界公认的食品、药品、化妆品和医疗器械等产品品质和效果的最高标准证明机构[9-11]。为了解孤儿药的发展情况及重点研发领域,笔者查阅近年来国内外相关文献,对2010-2015年美国FDA批准上市的孤儿药进行统计和分析,以期为我国孤儿药的相关立法和新药研发提供参考。
1 孤儿药的批准上市情况
自1983年美国国会通过《孤儿药法案》以来,美国FDA已经批准了近400种孤儿药上市[12-15]。其中,2010-2015年美国FDA批准上市的新药共203种,孤儿药77种,占新药种类的37.93%,该占比整体呈增长趋势,于2015年达到46.67%[16],详见表1。
2 获批孤儿药的治疗领域
2010-2015年美国FDA批准上市的孤儿药以抗肿瘤药物为主,共38种(占49.35%),其次为内分泌及代谢系统紊乱药物(8种,占10.39%)、心血管系统疾病药物(5种,占6.49%)、抗感染药物(4种,占5.19%)、神经及精神系统疾病药物(4种,占5.19%)和呼吸系统疾病药物(4种,占5.19%)等,详见表2。

表1 2010-2015年美国FDA批准上市的孤儿药分布
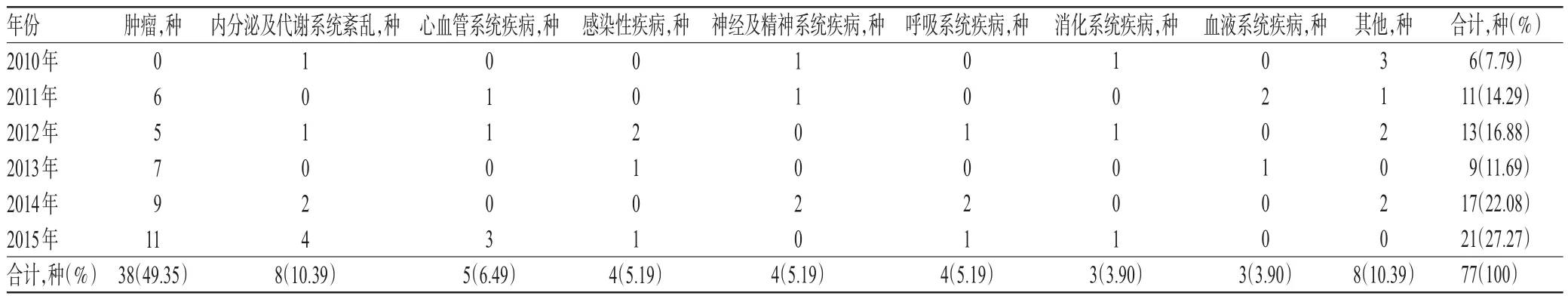
表2 2010-2015年美国FDA批准上市孤儿药的治疗领域分布情况
3 孤儿药的研发领域
3.1 肿瘤
肿瘤是严重威胁人类生命健康的常见病和多发病,化疗是肿瘤患者重要的治疗方法[17-21]。据统计,2007-2010年全球销量排名前20位的药品中,抗肿瘤药物稳居首位[22]。2010-2015年获美国FDA批准上市的孤儿药以抗肿瘤药物为主(38种),涉及的疾病种类主要为黑色素瘤、非小细胞肺癌(NSCLC)和白血病。2013年,获批的达拉非尼和曲美替尼均用于治疗检测有鼠类肉瘤滤过性毒菌致癌同源体B(BRAF)基因突变的黑色素瘤的治疗,代表着靶向转移性黑色素瘤的个体化治疗和非侵入性肿瘤监测的最新进展[23]。2014年,获批的布利莫单抗是一种基于双特异性T细胞衔接系统(BiTE)开发的免疫疗法,双特异性指向CD19/CD3的T细胞衔接器,适用于费城染色体阴性复发性或难治性B细胞前体急性淋巴细胞白血病的治疗[24]。BiTE主要由2条单链抗体连接而成,其分子量较小(55 000~60 000),易渗透至肿瘤组织,但BiTE缺乏Fc段导致免疫源性较低[25]。布利莫单抗也是全球首个获美国FDA批准的CD19药物[26]。新型、高效的化疗药物研发是治疗NSCLC药物的主要研究方向,阿法替尼是全球首个上市的不可逆性原癌基因ErbB抑制剂,用于治疗伴有表皮生长因子受体(EGFR)突变的局部晚期或转移性NSCLC[27-32]。阿法替尼在EGFR突变患者中的总生存期表现出显著延长的优势,患者生存质量改善率达11%[33-35]。2010-2015年美国FDA批准上市的抗肿瘤孤儿药药研发企业有25家(占65.79%)为美国企业,其次为英国企业6家、瑞士企业4家、日本企业2家、德国企业1家,详见表3。
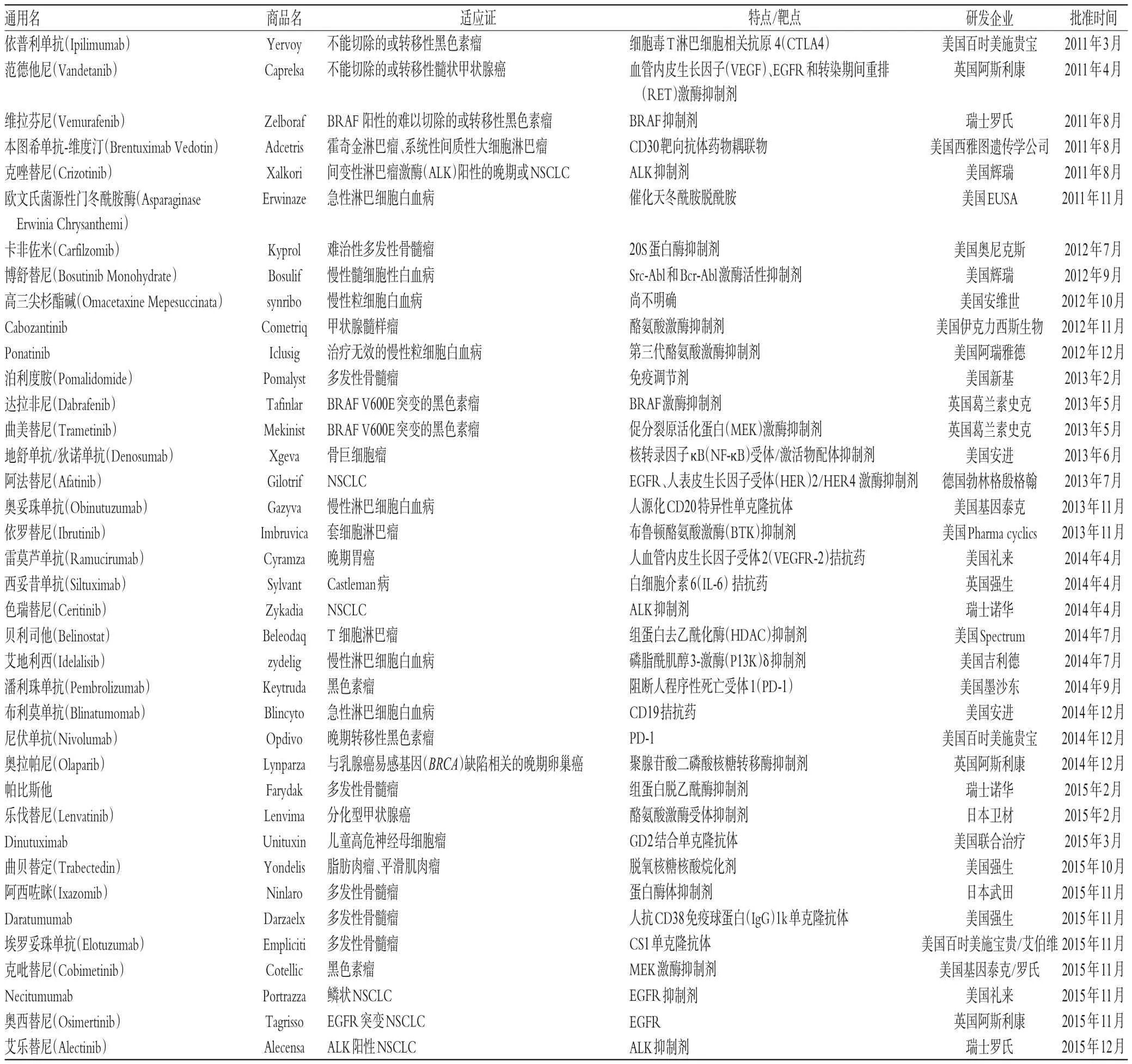
表3 2010-2015年美国FDA批准上市的抗肿瘤孤儿药
3.2 内分泌及代谢系统
2010-2015年获美国FDA批准上市的内分泌及代谢系统药物的数量仅次于抗肿瘤药,共8种。其中,由美国百时美施贵宝研制的美曲普汀是首个适用于先天性/获得性全身性脂肪代谢障碍合并症的药物,通过结合或/激活瘦素发挥作用[36]。尿苷三乙酸酯是获美国FDA批准的第一个治疗遗传性乳清酸尿症的药物,为尿苷的乙酰酯化前体药,口服吸收后经酯酶水解,释放尿苷至体循环[37]。2010-2015年美国FDA批准上市的内分泌及代谢系统孤儿药有7种由美国企业研发,另1种由瑞士企业研发,详见表4。

表4 2010-2015年美国FDA批准上市的内分泌及代谢系统孤儿药
3.3 心血管系统
心血管系统疾病已成为全球居民死亡和残疾的主要原因[38-40]。2010-2015年美国FDA批准上市的心血管系统孤儿药共5种。其中,于2015年获美国FDA批准的Evolocumab是一种用于原发性高胆固醇血症的新一代前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂类降脂药。PCSK9抑制剂是一种人单克隆抗体,能产生降低肝从血液中清除低密度脂蛋白(LDL-C)的能力。Evolocumab用于杂合子型家族性高胆固醇血症、纯合子型家族性高胆固醇血症、动脉粥样硬化性心血管疾病,以及在他汀类药物最大耐受剂量基础上,需额外降低LDL-C水平的成年患者[41-43]。对Evolocumab药物安全性进行的一项Meta分析显示,Evolocumab具有较强的降脂效果[41,44-46]。2010-2015年美国FDA批准上市的心血管系统孤儿药有2种由美国企业研发,其余分别来自爱尔兰、德国和瑞士企业,详见表5。
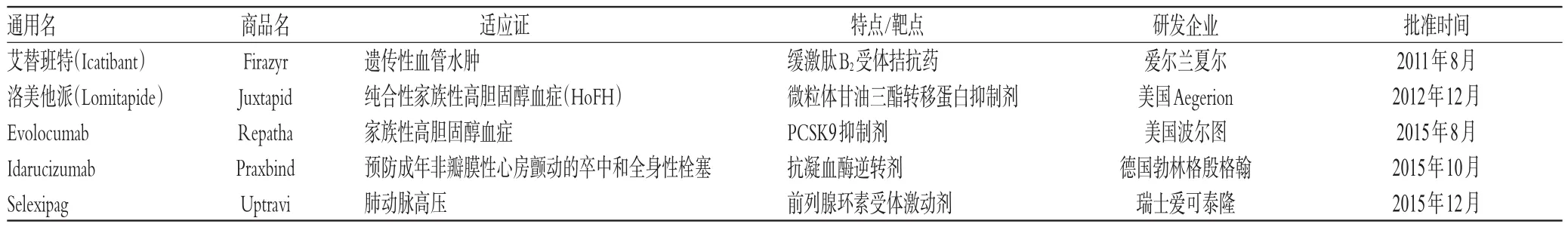
表5 2010-2015年美国FDA批准上市的心血管系统孤儿药
4 结语
随着近年来欧美各国对孤儿药审批给予的支持和鼓励,获批上市的孤儿药逐渐增多。2010-2015年美国FDA批准上市的孤儿药共77种,仅2015年就有21种,占该年度获批新药的46.67%。获批孤儿药主要是治疗肿瘤、内分泌及代谢系统疾病、心血管疾病、感染性疾病、神经及精神疾病和血液系统疾病等全球高发疾病的药物,其研发企业以美国为主。目前,我国尚无明确的罕见病和孤儿药的定义及相关立法,对罕见病的防治和救助方面进展缓慢,孤儿药的研发尚处于空白阶段,亟需加快相关立法进程,结合国情开展孤儿药研发与审批,摆脱罕见病“无药可治”和“无药可用”的窘境。
[1]易八贤,王广平,霍艳飞,等.基于药物可负担性的罕见病用药定义探讨[J].中国医药工业杂志,2015,46(6):658-664.
[2]Lavandeira A.Orphan drugs:legal aspects,current situation[J].Haemophilia,2002,8(3):194-198.
[3]Schieppati A,enter JI,Daina E,et al.Why rare diseases are an important medical and social issue[J].Lancet,2008,371(9629):2039-2041.
[4]孙赛男,董江萍.国外孤儿药现状分析及对我国的启示[J].中国医药工业杂志,2015,46(10):1146-1150.
[5]邹栩,顾凯.世界新药研发动向[J].中国新药杂志,2007,16(22):1821-1825.
[6]孟光兴.基于市场导向的新药研发决策模型研究[J].中国新药杂志,2016,25(2):121-124.
[7]田月,赵志刚.全球重要领域的新药研发与进展[J].药品评价,2015,12(18):6-11.
[8]高婧,杨悦.全球创新药物研发趋势分析[J].中国新药杂志,2015,24(24):2764-2769.
[9]王帅,罗欣,陈玉文.近5年获美国FDA批准的新药及其治疗领域分析[J].中国药房,2014,25(13):1156-1158.
[10]袁林,邵明立.美国FDA加快新药审评策略以及对我国的启示[J].中国新药杂志,2015,24(21):2401-2404.
[11]高敏洁.美国FDA对新药临床试验申办者和合同研究组织的监管模式[J].中国新药与临床杂志,2016,35(2):109-113.
[12]张延军,王静波,郭剑非.美国孤儿药法案及其对新药研发的影响[J].中国药物经济学,2010,5(1):27-34.
[13]Reaves ND.A model of effective health policy:the 1983 orphan drug act[J].J Health Soc Policy,2003,17(4):61-71.
[14]李认书,李鸿彬.美国与欧盟孤儿药研发上市管理制度及对我国的启示[J].中国药事,2014,28(10):1109-1113.
[15]谢冰洁,宋高广.美国生物制品中孤儿药的研发现状及对中国孤儿药研发策略的思考[J].药学进展,2016,40(6):404-410.
[16]陈玲,刘艳红,邹栩,等.2015年全球重要治疗领域新药研究的最新进展[J].中国新药杂志,2016,25(6):601-621.
[17]朱斌,余波,翟青.影响肿瘤患者化疗疗效的医源性因素分析[J].中国药房,2012,23(14):1327-1329.
[18]何明珠,姜玲,王静,等.肿瘤化疗患者心理韧性及其影响因素的研究[J].护理学杂志,2015,30(1):60-62.
[19]陈万青,郑荣寿,张思维,等.2012年中国恶性肿瘤发病和死亡分析[J].中国肿瘤,2015,24(1):1-10.
[20]陈万青,郑荣寿,张思维.中国恶性肿瘤的动态变化[J].科技导报,2014,32(26):65-71.
[21]中国临床肿瘤学会抗肿瘤药物安全管理专家委员会.肿瘤治疗相关呕吐防治指南:2014版[J].临床肿瘤学杂志,2014,19(3):263-273.
[22]IMS.Top20global therapeutic classes,2010,total audit-ed markets[EB/OL].[2014-03-01].http://www.ims.com.
[23]汤仲明.2013年上半年美国FDA批准药物简介[J].国际药学研究杂志,2013,40(4):501-509.
[24]汤仲明.2014年下半年美国FDA批准药物简介[J].国际药学研究杂志,2015,42(1):115-126.
[25]NaqorsenD ,Kufer P,Baeuerle PA,et al.Blinatumomab:a historical perspective[J].Pharmacol Ther,2012,136(3):334-342.
[26]陈玲,赵天笑,邹栩,等.2014年美国FDA批准上市新药回顾及重点药物分析[J].中国新药杂志,2015,24(4):361-369.
[27]王淋丽,李娜,廖玉芳,等.非小细胞肺癌一线化疗药物的研究进展[J].中国药房,2016,27(5):717-720.
[28]李莹,田驰,王磊,等.小分子表皮生长因子受体酪氨酸激酶抑制剂的研究进展[J].肿瘤药学,2016,6(2):81-88.
[29]刘静毅,张俊萍.阿法替尼在NSCLC治疗中的研究进展[J].实用肿瘤杂志,2016,31(2):111-115.
[30]李静,武新虎,刘志冰,等.阿法替尼联合西妥昔单抗治疗非小细胞肺癌EGFR T790M突变所致的吉非替尼耐药[J].肿瘤,2013,33(7):619-623.
[31]魏瑜,张莉.阿法替尼治疗晚期非小细胞肺癌的Meta分析[J].现代肿瘤医学,2017,25(12):1894-1898.
[32]鞠娜,史美祺,寇莹莹,等.阿法替尼在克服一代EGFRTKI耐药方面的研究进展[J].中南药学,2016,14(5):511-515.
[33]Miller VA,Hirsh V,Cadranel J,et al.Afatinib versus placebo for patients with advanced,metastatic non-smallcell lung cancer after failure of erlotinib,gefitinib,or both,and one or two lines of chemotherapy(LUX-Lung 1):a phase 2b/3 randomised trial[J].Lancet Oncol,2012,13(5):528-538.
[34]潘燚,谭佩欣.一线阿法替尼与化疗对EGFR突变伴有脑转移的非小细胞肺癌患者的疗效评价[J].循证医学,2016,16(4):230-232.
[35]张丽,汤依群,史美祺,等.阿法替尼治疗晚期非小细胞肺癌的疗效和安全性观察[J].安徽医药,2015,19(7):1375-1378.
[36]汤仲明.2014年上半年美国FDA批准药物简介[J].国际药学研究杂志,2014,41(4):493-502.
[37]马帅,温颖玲,周伟澄.2015年美国FDA批准上市的新药简介[J].中国医药工业杂志,2016,47(1):79-105.
[38]赵鸿萍,蒋宏民,相秉仁.近5年全球在研心血管药物研发热点靶标及趋势分析[J].中国药科大学学报,2012,43(6):573-576.
[39]成承,李文婷,裴常伯,等.焦虑抑郁与心血管系统疾病的研究[J].中华保健医学杂志,2016,18(1):24-26.
[40]李静静,赵建力.窖蛋白与心血管系统疾病关系的研究进展[J].中西医结合心脑血管病杂志,2014,12(9):1124-1126.
[41]郑少微,巩付华,展淑琴,等.Evolocumab治疗高胆固醇血症患者的Meta分析[J].中国临床药理学与治疗学,2016,21(5):520-525.
[42]孙树森,韩容,赵志刚.2015年上半年美国FDA批准的新分子实体与评价:心血管系统疾病和癌症治疗用药[J].药品评价,2015,12(16):6-12.
[43]朴元林.心血管系统疾病中西药物合用的研究进展[J].中国临床医生杂志,2014,42(6):12-15.
[44]刘兴兰.Evolocumab降低LDL-C有效性及安全性的Meta分析[D].重庆:重庆医科大学,2015.
[45]苏婷.Evolocumab调脂治疗的有效性与安全性Meta分析[D].兰州:兰州大学,2016.
[46]钟小燕,杨旭平,余彬,等.Evolocumab治疗血脂异常的疗效与安全性的系统评价[J].临床心血管病杂志,2016,32(1):19-24.
(编辑:陶婷婷)
R951
A
1001-0408(2017)26-3733-05
2016-10-19
2017-02-24)
DOI 10.6039/j.issn.1001-0408.2017.26.38
*主管药师。研究方向:医院药学与临床药学。电话:0871-63211154。E-mail:wangli530520@126.com
#通信作者:主管药师,硕士。研究方向:药理学,医院药学。电话:0871-63211205。E-mail:zhaofangyun@126.com
