示差折光-HPLC法测定舒血宁注射液中山梨醇的含量
2017-09-28周永妍孙胜斌姜国志武晓媛王文鹏
高 亮,周永妍,孙胜斌,,姜国志,武晓媛,王文鹏
(1.神威药业集团有限公司,河北石家庄 051430;2.中药注射剂新药技术开发国家地方联合工程实验室,河北石家庄 051430)
示差折光-HPLC法测定舒血宁注射液中山梨醇的含量
高 亮1,周永妍1,孙胜斌1,2,姜国志2,武晓媛1,王文鹏1
(1.神威药业集团有限公司,河北石家庄 051430;2.中药注射剂新药技术开发国家地方联合工程实验室,河北石家庄 051430)
现有检测方法在测定舒血宁注射液中的山梨醇含量时,存在着专属性不强、操作复杂等弊端。针对此问题,建立了示差折光-HPLC测定舒血宁注射液中山梨醇含量的方法。色谱柱为Carbomix Ca-NP 10:8%(7.8 mm×300 mm),以水为流动相,流速为0.5 mL/min,柱温为80 ℃。结果表明:山梨醇在0.2~2.0 mg/mL(r2=0.999 5)质量浓度范围内与峰面积具有良好的线性关系,平均回收率(n=9)为99.9%。该方法简便,专属、重复性好,可作为舒血宁注射液中山梨醇含量的测定方法。
色谱分析;山梨醇;舒血宁注射液;HPLC;示差折光
舒血宁注射液具有扩张血管、改善微循环的功效,用于治疗缺血性心脑血管疾病、冠心病、心绞痛、脑栓塞、脑血管痉挛等[1-2],属于国家中药保护品种[3]。舒血宁注射液具有独特的治疗优势,临床应用广泛[4]。然而,中药注射剂的成分比较复杂,使用过程中会存在一定的风险[5-7],其辅料的合理使用可增加制剂的稳定性并降低毒副作用,但若使用不当又会增加药物不良反应的发生率[8]。舒血宁注射液中的辅料山梨醇(sorbitol)是一种糖醇,为等渗调节剂和助溶剂[9]。现有山梨醇含量的检测方法虽然很多,但应用在测定舒血宁注射液中的山梨醇含量时,存在着专属性不强、操作复杂等问题。例如:2015年版《中华人民共和国药典》中山梨醇含量的测定方法为高碘酸钠氧化-硫代硫酸钠滴定法[10],用于检测山梨醇纯品;而舒血宁注射液的成分比较复杂,应用此法检测专属性不强。梁振明[11]采用分光光度法测定山梨醇的含量,山梨醇与氢氧化铜在碱性溶液中生成蓝色络合物,在665 nm波长处存在最大吸收,但此方法操作复杂。罗清波[12]采用糖分析柱,用示差折光检测器测定山梨醇的含量,但糖分析柱价格贵,使用娇气,普及性低。通过参考相关文献方法[13-14]及实验研究,发现采用Carbomix Ca-NP10:8%(7.8 mm×300 mm)色谱柱、示差折光检测器测定山梨醇含量的方法不受舒血宁复杂成分的干扰,检测过程中无有毒废液产生,检测方法快速、高效、准确。
1 主要仪器与试药
DIONEX Ultimate 3000高效液相色谱仪,美国赛默飞世尔公司提供;CPA225D型电子分析天平,德国赛多利斯公司提供。
山梨醇对照品,批号为101109-201402,购自中国食品药品检定研究院;舒血宁注射液,神威药业集团有限公司生产,批号为17011611,17011711,17011811,17011911,17012011,17012111,17012211及17012311;水为超纯水。
2 方法与结果
2.1色谱条件与系统适用性试验
以Carbomix Ca-NP 10:8%(7.8 mm×300 mm)柱为色谱柱,采用示差折光-HPLC法,以水为流动相A,流速为0.5 mL/min,柱温为80 ℃,进样量为20 μL,理论塔板数按山梨醇峰计算,应不低于1 450,分离度按山梨醇与相邻溶剂峰计算,应大于1.5[15]。
2.2对照品溶液的制备
精密称取山梨醇对照品适量,加水制成每1 mL含山梨醇对照品1 mg的溶液。
2.3供试品溶液的制备
精密量取舒血宁注射液2 mL,放入100 mL容量瓶中,加水稀释至刻度,摇匀即得。
2.4阴性对照溶液的制备
按舒血宁注射液处方制备不含山梨醇的阴性样品,精密量取阴性样品2 mL,放入100 mL容量瓶中,加水稀释至刻度,摇匀即得。
2.5专属性试验
分别精密吸取对照品溶液、供试品溶液和阴性对照溶液各20 μL,注入液相色谱仪进行测定。结果表明:阴性样品在与供试品中山梨醇相同的保留时间处无干扰峰,供试品和对照品的山梨醇峰与溶剂峰之间的分离度达3.8以上,理论塔板数按山梨醇峰计算达1 480以上。色谱图见图1。

图1 山梨醇高效液相色谱图Fig.1 High performance liquid chromatogram of sorbitol
2.6线性关系考察
精密称取山梨醇对照品10 mg,置于50 mL量瓶中,用水溶解并稀释至刻度,摇匀,作为标准储备液。精密量取标准储备液1.0,3.0,5.0,7.0,9.0,10.0 mL,分别加水定容至10 mL,得到标准液。精密吸取标准液各20 μL,注入液相色谱仪进行测定。山梨醇峰面积与质量浓度线性关系的结果见表1。以峰面积为纵坐标,以质量浓度为横坐标进行线性回归,得到回归方程为y=5.963x-0.180 5,相关系数r2=0.999 7(n=6)。结果表明,山梨醇在0.2~2.0 mg/mL范围内线性关系良好[16],详见图2。

表1 峰面积与质量浓度线性关系结果
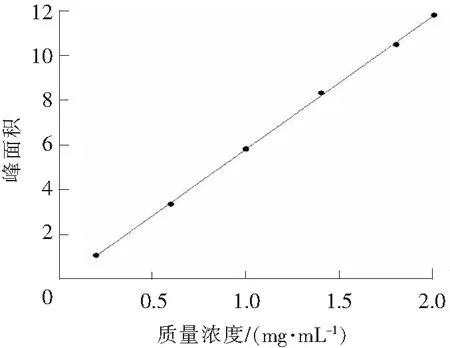
图2 线性关系图Fig.2 Linear relation
2.7精密度试验
将批号为17011611的舒血宁注射液制备成供试品溶液。分别精密吸取对照品溶液和供试品溶液20 μL,注入液相色谱仪进行测定。对供试品溶液连续进样测定5次,按式(1)计算供试品山梨醇的含量:
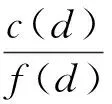
(1)
式中:c为浓度;f为峰面积;d代表对照品;y代表供试品。
精密度结果见表2。结果表明,山梨醇的相对标准偏差(RSD)为1.4%,精密度良好。

表2 精密度结果
2.8稳定性试验
将批号为17011611的舒血宁注射液制备成供试品溶液。分别精密吸取对照品溶液和供试品溶液各20 μL,注入液相色谱仪进行测定。对供试品溶液分别于0,1,2,4,8,12,24 h进样测定,稳定性结果见表3。结果表明:山梨醇含量的相对标准偏差(RSD)为1.6%,表明样品在24 h内稳定。
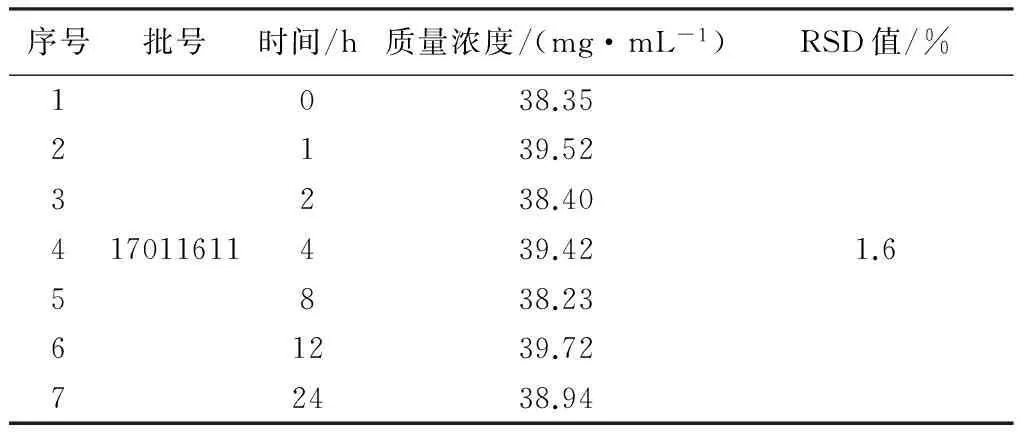
表3 稳定性结果
2.9重复性试验
向9个100 mL的容量瓶中分别精密量取批号为17011611的样品1,1,1,2,2,2,3,3,3 mL,加水稀释至刻度,摇匀即得。以Carbomix Ca-NP 10:8%(7.8 mm×300 mm)柱为色谱柱,水为流动相A,流速为0.5 mL/min,柱温为80 ℃,进样量为20 μL,采用示差折光检测器检测。按含量计算:山梨醇的相对标准偏差(RSD)为1.7%。结果表明本方法的重复性良好。
2.10加样回收率试验
向9个100 mL的容量瓶中分别精密量取已知含量批号为17011611的舒血宁注射液1 mL。将每3个容量瓶定为一组,再向每组分别精密加入相当于样品中所含山梨醇量50%,100%,150%的对照品溶液,加水稀释至刻度,摇匀。以Carbomix Ca-NP 10:8%(7.8 mm×300 mm)柱为色谱柱,水为流动相A,流速为0.5 mL/min,柱温为80 ℃,进样量为20 μL,采用示差折光检测器进行检测,计算加样回收率,结果见表4。

表4 加样回收率试验结果(n=9)
结果显示,平均回收率为99.90%,相对标准偏差为1.3%,表明系统误差非常小。
2.11样品含量测定
取8批样品,每批制备供试品溶液2份,作为平行样。分别精密吸取对照品溶液和供试品溶液20 μL,注入液相色谱仪进行测定,计算各批样品的山梨醇含量,结果见表5。结果表明,该方法可作为舒血宁注射液中山梨醇含量的测定方法,具有简便快捷、置信度和准确性高等优点。

表5 样品测定结果(n=2)
3 结 语
第一支中药注射剂发展至今已有60多年了。历史证明,作为现代中药的新剂型,中药注射剂在治疗疾病、保障人民健康的事业中做出了很大贡献,丰富和推动了中药事业的发展与壮大。然而,不良反应问题又是制约中药注射剂发展的瓶颈,其多由原材料质量的可控性低、复方成分复杂、生产工艺及质量标准方面的技术不足、临床配伍不规范等原因造成的[17]。在质量标准方面,应通过不断进行基础研究,使物质所含成分更加明确。采用更高质量控制把关产品质量,可以保证产品质量合格、稳定、均一。
采用示差折光-HPLC法测定舒血宁注射液中山梨醇的含量,具有简便快捷、置信度和准确性高等优点,检测过程中无有毒废液产生,检测方法快速、高效、准确。未来中药注射液达到“689”质控标准要求是大势所趋。今后,还将对舒血宁注射液其他辅料及银杏叶提取物进行更为深入的研究。
/
:
[1] WS3-B-3707-98-2004—2012,国家药品标准[S].
[2] 郭玉东.舒血宁注射液药效学再评价及生物活性测定法用于其质量控制的研究[D].北京:北京中医药大学,2011. GUO Yudong. Pharmaco Dynamic Evaluation of Shuxuening Injection and Study on the Quality Control of Biological Acti-vity Assay[D]. Beijing:Beijing University of Chinese Medicine, 2011.
[3] 杨扬,周斌,赵文杰.银杏叶史话:中药/植物药研究开发的典范[J].中草药,2016,47(15):2579-2591. YANG Yang, ZHOU Bin, ZHAO Wenjie. Ginkgo biloba leaves history: A model of research and development for Chinese materia medica/phytomedicine[J]. Chinese Medicinal Herb, 2016, 47(15): 2579-2591.
[4] 高颖,郭鹏,张静泽.中药注射剂的研究进展[J].武警医学院学报,2009,18(3):249-251. GAO Ying, GUO Peng, ZHANG Jingze. The research progress of traditional Chinese medicine injection[J], Academy of Armed Police Medical Journal, 2009,18(3):249-251.
[5] 吴秀玲,李世玲,刘兴来,等.浅谈现代中药注射剂的合理应用[J].中国保健营养,2012(9):577-578. WU Xiuling, LI Shiling, LIU Xinglai,et al. Rational application of modern TCM injection[J].China Health Care Nutrition, 2012(9):577-578.
[6] 陆云霞,潘星燕,姚军.HPLC测定奥贝胆酸片含量[J].河北科技大学学报,2017,38(2):158-162. LU Yunxia,PAN Xingyan,YAO Jun.Content determination of obeticholic acid tablets by HPLC[J]. Journal of Hebei University of Science and Technology, 2017,38(2):158-162.
[7] 杨林.中药注射剂的安全性探讨[J].现代养生,2015(1):224.
[8] 王华锋.注射剂药用辅料安全性值得关注[N].中国医药报,2016-08-09(7).
[9] 秦美蓉,王平,陈润桦.药用辅料山梨醇(供注射用)的细菌内毒素检查法[J].中国现代应用药学,2014,31(2): 207-209. QIN Meirong, WANG Ping, CHEN Runhua. Bacterial endotoxin test for excipients sorbitol for injection preparations[J]. Chinese Journal of Modern Applied Pharmacy,2014,31(2): 207-209.
[10] 国家药典委员会.中华人民共和国药典[M]. 北京:中国医药科技出版社,2015.
[11] 梁振明.分光光度法测定山梨醇含量[J].中国食品添加剂,2007(1):184-187. LIANG Zhenming. Determination of sorbitol content by spectrophotometry[J]. China Food Additives,2007(1):184-187.
[12] 罗清波.HPLC测定山梨醇水溶液中山梨醇和甘露醇的含量[J].分析测试学报,1993,12(4):73-75. LUO Qingbo. HPLC determination of sorbitol and mannitol insorbitol aqueous solution[J].Journal of Instrumental Analysis,1993,12(4):73-75.
[13] 李太平.高效液相色谱法的基本理论浅述[J].丹东医药,2002(3):53-57.
[14] 熊素玉,杨丽.高效液相色谱法及其应用[J].食品安全导刊, 2017(3):120.
[15] 王树全,郑金琪.示差折光-HPLC法测定复方氨基酸注射液(18AA)中山梨醇的含量[J].中国卫生检验杂志, 2013,23(18):3558-3560. WANG Shuquan, ZHENG Jinqi. Determination of sorbitol in compound amino acid injection (18AA) by HPLC with refractive index detector[J]. Chinese Journal of Health Laboratory Technology, 2013,23(18):3558-3560.
[16] 朱凤梅.山梨醇含量快速检测法[J].木薯精细化工,2001(3):18-21. ZHU Fengmei. The quick method to examine’s content[J]. Cassava Fine Chemical Industry, 2001(3):18-21.
[17] 高旺,张骥鹏,楚金.浅谈中药注射剂存在的问题与未来[J].实用药物与临床,2009, 12(6):460-462.
Determination of sorbitol in Shuxuening injection by HPLC with refractive index detector
GAO Liang1, ZHOU Yongyan1, SUN Shengbin1,2, JIANG Guozhi2, WU Xiaoyuan1, WANG Wenpeng1
(1.Shineway Pharmaceutical Group Limited Company,Shijiazhuang,Hebei 051430, China;2.State-Local Joint Engineering Laboratory of New Drugs Development Technology for TCM Injection, Shijiazhuang,Hebei 051430,China)
The existing sorbitol content detection method in the determination of the sorbitol content in Shuxuening injection has some problems such as that the specificity is not strong, the operation is complicate and so on. Aiming at the problems, the refractive index-HPLC method for the determination of sorbitol content in Shuxuening injection is established. The content of sorbitol in Shuxuening injection is determined on a Carbomix Ca-NP10:8%(7.8 mm×300 mm) with a mobile phase of water at a flow rate of 0.5 mL/min. Column temperature is 80 ℃ and refractive index detector of HPLCis used. The results show that a nice linearity is obtained between the sorbitol mass concentration of 0.2~2.0 mg/mL (r2=0.999 5) and peak area, and the average recovery (n=9) is of 99.9%.The method is convenient, selective and reproducible, and can be used for quality control of Shuxuening capsules.
chromatographic analysis; sorbitol; Shuxuening injection; HPLC; refractive index detector
1008-1534(2017)05-0324-04
2017-06-07;
2017-08-26;责任编辑:张士莹
国家“重大新药创制”科技重大专项(2014ZX09201022-004)
高 亮(1988—),男,吉林九台人,助理工程师,主要从事药品工艺技术、质量及产业化方面的研究。
王文鹏工程师。E-mail:449119178@qq.com
R917
:Adoi: 10.7535/hbgykj.2017yx05003
高 亮,周永妍,孙胜斌,等.示差折光-HPLC法测定舒血宁注射液中山梨醇的含量[J].河北工业科技,2017,34(5):324-327. GAO Liang, ZHOU Yongyan, SUN Shengbin,et al.Determination of sorbitol in Shuxuening injection by HPLC with refractive index detector [J].Hebei Journal of Industrial Science and Technology,2017,34(5):324-327.
